铜合金中铅测定的探讨
2011-11-07李正权
李正权
(贵州航天精工制造有限公司,贵州 遵义 563100)
铜合金中铅测定的探讨
李正权
(贵州航天精工制造有限公司,贵州 遵义 563100)
对铬酸铅沉淀-硫酸亚铁铵滴定法测定铜合金中铅的试验方法进行探讨,改善原来的滴定分析方法,提高了方法的稳定性和准确度。
铅;沉淀;硝酸银;pH
铜合金中铅的测定方法有电解法、火焰-原子吸收光谱法、发射光谱法等,这些方法属于仪器检测法,有些操作麻烦,分析耗时长;有些仪器昂贵。从分析成本和试验时间上综合考虑,容量分析是较适宜的。采用铬酸铅沉淀-硫酸亚铁铵滴定法进行测定,存在滴定终点不很明显(有时甚至不出现终点),稳定性差,重复性差等问题。对此方法进行改进,加入硝酸银形成氯化银对铬酸铅沉淀吸附,改用醋酸钠缓冲溶液代替醋酸铵溶液,严格控制溶液的pH值,使得测定准确度和稳定性提高,达到标准要求。
1 试验部分
1.1 仪器与试剂
PHS-3B精密pH计。
重铬酸钾标准溶液 c (1/6K2Cr2O7)=0.0500 mol·L-1:称取2.4515 g基准重铬酸钾,用水溶解后,稀释至1000 mL。
乙酸钠溶液:称取乙酸钠8 g,加入36%的醋酸134 mL,用水稀释至500 mL,摇匀,用氢氧化钠(40 g·L-1)或盐酸(1+5)调节 pH 到 3.5。
氢氧化钠溶液 100g·L-1,硝酸锶溶液 100g·L-1,硝酸银溶液 2 g·L-1,氯化钠溶液 10 g·L-1。
邻苯氨基苯甲酸指示剂2 g·L-1:称取邻苯氨基苯甲酸0.2g,溶于2g·L-1的碳酸钠溶液100mL中,溶液贮存于棕色瓶中。
硫酸、磷酸混合酸:于600 mL水中加入硫酸150 mL及磷酸150 mL,冷却,加水稀至1000 mL。
硫酸亚铁铵标准溶液 c(Fe2+)=0.020 mol·L-1:称取硫酸亚铁铵[Fe(NH4)2(SO4)2·6H2O] 7.9 g,溶于硫酸(5+95)1000 mL中,为保证二价铁稳定加几小颗纯铝。
重铬酸钾标准溶液与硫酸亚铁铵标准溶液的比值 K 的求法:用移液管移取 c(1/6K2Cr2O7)=0.0500 mol·L-1的重铬酸钾标准溶液 V0(10 mL 或20 mL),置于 250 mL锥形瓶中,加水 80 mL,加入硫酸、磷酸混合酸20 mL,邻苯氨基苯甲酸指示剂 3 滴,用 c(Fe2+)=0.020 mol·L-1硫酸亚铁铵标准溶液滴定至亮绿色为终点。

式中:V0——吸取c(1/6K2Cr2O7)=0.0500mol·L-1的重铬酸钾标准溶液的的体积,mL;
V1——消耗硫酸亚铁铵标准溶液的体积,mL。
1.2 试验方法
1.2.1 试验步骤
称取试料 m(1.0000 g或 0.5000 g),置于300 mL 锥形瓶中,加入硝酸(1+3)15 mL,加热溶解,取下冷却,加少量水,用PHS-3B精密pH计测定 pH 值,用氢氧化钠(100 g·L-1)或盐酸(1+5)调节溶液的 pH 到 3~4。加入硝酸锶溶液(100 g·L-1)4 mL、氯化钠溶液(10 g·L-1)2 mL,加入乙酸钠缓冲溶溶液(pH3.5)25 mL 及 c(1/6K2Cr2O7)=0.0500 mol·L-1的重铬酸钾标准溶液 V0mL,加入适量硝酸银溶液(2g·L-1)。将锥形瓶放在电热板上加热,煮沸2~3min,冷却。加水 50 mL 及硫酸、磷酸混合 酸 20 mL,用 c(Fe2+)=0.020 mol·L-1硫酸亚铁铵标准溶液滴定数mL后,加入邻苯氨基苯甲酸指示剂3滴,继续滴定溶液由紫红色转变为亮绿色为终点。按以下公式计算铅含量:
w(Pb)/%= ( V0-KV2) c0×6.907/m
式中:V0—加入重铬酸钾标准溶液的体积,mL;
V2—滴定消耗硫酸亚铁铵标准溶液的体积,mL;
c0—重铬酸钾标准溶液浓度 c(1 /6K2Cr2O7),mol·L-1;
m—试料质量,g。1.2.2 试验内容
控制溶液pH=3.5,试验加入不同量的硝酸银2 g·L-1溶液,测定铜合金中铅的含量;控制溶液中加入相同量硝酸银 2 g·L-1溶液(10 mL),在不同的pH值下测定铜合金中铅的含量。
2 结果与讨论
2.1 测定结果
2.1.1 硝酸银加入量的影响
对加入不同量硝酸银2 g·L-1溶液的试样进行测定,结果见表1。
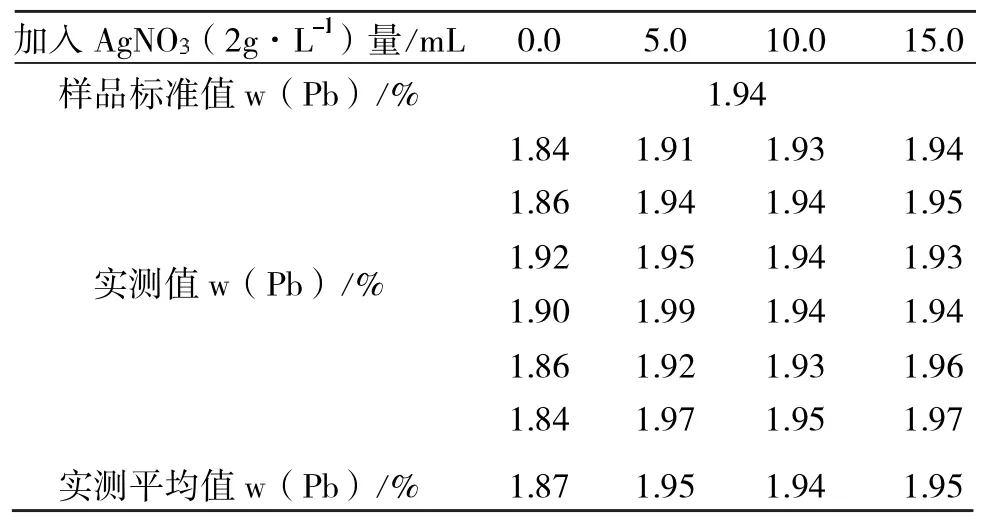
表1 硝酸银加入量对测定结果的影响
从试验结果得知,不加硝酸银时,测定铅含量与标准值相差大,重复性差;当加入AgNO3(2g·L-1)量为10.0mL时,测定结果与标准值最接近,且稳定性好;当加入 AgNO3(2 g·L-1)量≥15.0 mL时,测定结果有大于标准值的趋势。说明当加入 AgNO3(2 g·L-1)量为 10.0 mL 左右较适宜。
2.1.2 pH值控制的试验
对溶液在不同pH值下,进行铅的含量测定,试验结果见表2。

表2 pH值对测定结果的影响
从试验数据中看出,随着pH的增加,测定结果有升高的现象,pH在3~4之间稳定性较好,pH=3.5时,测定结果与稳定性最佳。
2.2 测定原理
用定量的硝酸溶解试样,加入过量的重铬酸钾标准溶液,在pH 3~4的醋酸介质中使铅定量地生成铬酸铅沉淀,过量的重铬酸钾,在不分离铬酸铅沉淀的情况下,提高溶液酸度后用硫酸亚铁铵标准溶液滴定,用邻苯氨基苯甲酸作指示剂。
用硫酸亚铁铵标准溶液滴定重铬酸钾,必须在较高的酸度条件下进行,而在低酸度下生成的铬酸铅沉淀在高酸度的溶液中会逐渐溶解,因此有的方法要求将铬酸铅沉淀分离后再进行滴定。本实验采用加入硝酸锶作为凝聚剂,使铬酸铅沉淀在较高的酸度条件下也不溶解。
加入适量氯化钠,使溶液中有少量氯化银沉淀,凝聚析出的铬酸铅小颗粒沉淀被氯化银吸附,煮沸陈化后生成较大的颗粒,从而减少对其它离子的吸附,使测定结果稳定。氯化银沉淀量太少,吸附作用不大;过多,可能对Fe2+离子有影响,导致测定结果偏高。实验表明,加入AgNO3(2 g·L-1)量为 10.0 mL 时,较适宜。
沉淀铬酸铅时pH的影响,由于铜、锶的铬酸盐都微溶于水,酸度较低时,铜、锶离子作为抗衡离子被铬酸铅吸附的量较大,加入硫酸、磷酸混合酸后,部分被吸附于沉淀上的铜、锶铬酸盐来不及溶解或转化即被瞬间形成的硫酸锶沉淀所包围。故加入重铬酸钾沉淀铅时,溶液的pH值有一定的影响。pH值小时,测定结果偏低。pH值大时,测定结果偏高。实验表明,pH为3.5左右时,测定结果准确。
试验中之所以采用醋酸钠缓冲溶液代替醋酸铵缓冲溶液,是由于溶液中有大量的铵离子存在时,析出的硫酸锶疏松,对铬酸铅沉淀的保护作用差,滴定终点不稳定。而钠离子可使硫酸锶致密,滴定终点能稳定25 min左右。
2.2 结论及其它
在形成铬酸铅沉淀时,加入硝酸银形成氯化银对铬酸铅沉淀吸附,用醋酸钠-醋酸作缓冲溶液,控制溶液的pH值3.5左右,采用铬酸铅沉淀-硫酸亚铁铵滴定法进行铜合合金中铅的测定结果准确。操作过程简化,分析的时间缩短,分析成本降低。铜合金中常见的含量元素均不干扰铅的定量沉淀,硝酸溶解后试样中的锡以偏锡酸沉淀析出,故不干扰铅的沉淀。
重铬酸钾标准溶液[c(1/6K2Cr2O7)=0.0500mol·L-1]10 mL可沉淀铅24 mg,故对一般的铅黄铜称取试料质量1 g即可。对其它牌号的铜可调整试料称样量或增加重铬酸钾标准溶液的加入量。例如铅含量w (Pb)% 为2.5~3.5时,称取试料质量0.5 g,或者增加重铬酸钾标准溶液为20 mL即可。方法对比结果见表3。
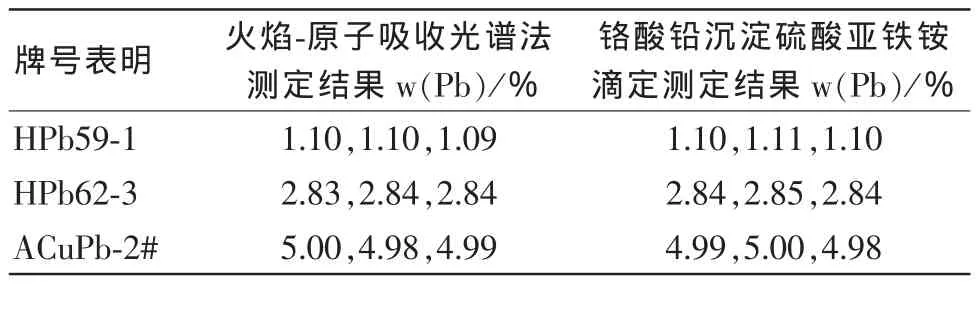
表3 方法对比结果
[1] 赵巍.铬酸铅沉淀-亚铁滴定法测定铜合金中铅的研究[J]. 辽宁化工,2001,(11):509-510.
[2] 上海材料研究所.金属材料化学分析方法(第二分册)[M].北京:机械工业出版社,1982.
[3] 沈含熙,等.2-(2-噻唑偶氮)-5-二乙氨基苯甲酸分光光度法测定微量钯[J]. 冶金分析,1988,(6):1-4.
[4] 王辄.铬酸铅沉淀-亚铁滴定法测定铜含金中铅的方法讨论[J]. 理化检验-化学分册,1989, 25(1):56.
Determination of Lead in Copper Alloy
LI Zheng-quan
(Test Center of Guizhou Aerospace Seiko Manufacturing Co.Ltd., Zunyi 563100,China)
The determination method of lead in copper alloy by lead chromate precipitated-ammonium ferrous sulphate titration was improved and the stability and accuracy was increased.
lead; precipitation;silver nitrate; pH
O 655
A
1671-9905(2011)04-0033-03
李正权(1962-),男,工程师,从事化学分析检测工作
2010-12-20
