己二酸的绿色合成探究—绿色化学实验在基础有机化学实验中的应用
2011-10-23王继业冯玉玲
王继业 张 轩 冯玉玲
河北师范大学化学与材料科学学院 河北石家庄 050016
己二酸的绿色合成探究—绿色化学实验在基础有机化学实验中的应用
王继业 张 轩 冯玉玲
河北师范大学化学与材料科学学院 河北石家庄 050016
以30%过氧化氢为氧化剂,用钨磷酸催化氧化环己醇合成己二酸,考察了催化剂用量,反应物配比和反应时间对己二酸产率的影响。当反应物物质的量比为钨磷酸:环己醇:过氧化氢=1:250:1125,在一定温度下回流反应4~6h,产率可达到50%;且催化剂可以重复使用。结果表明:本方法操作简单,无污染,符合绿色化学发展的要求,可用于基础有机合成实验。
己二酸;钨磷酸;催化氧化;绿色化学
Abstract: Adipic acid is synthesized by tungstophosphoric acid catalyzed oxidation cyclohexanol with 30 percent hydrogen peroxide.The effects of catalyst amount and reactants’proportion and reaction time on the yield of adipic acid are investigated.The results show when the mole ratio of tungstophosphoric acid: cyclohexanol: hydrogen peroxide equals 1 : 250 :1125, the isolated yield of adipic acid can reach 50% under such temperature in 4-6 h.The catalyst can be used repeatedly. It also shows that this process has many advantages such as simple operation, no pollution and meeting to the requirement of green synthesis.
Key words: adipic acid; tungstophosphoric acid; catalytic oxidation; green chemistry
己二酸是重要的化工原料和合成中间体,己二酸的合成是高校有机化学实验教学的一个重要的基础实验。目前国内外有机实验和工业生产中大多采用浓硝酸或高锰酸钾直接氧化环己醇或环己酮制备己二酸。但这些方法存在着明显的不足:硝酸氧化法由于剧烈反应会产生戊二酸,丁二酸等副产物,并且释放出大量的NO2等有毒气体,给环境带来严重污染,在实际的实验教学中很少采用;高锰酸钾做氧化剂虽然无有害气体放出,反应条件比较优化,产物收率也很高,但采用该方法合成己二酸,温度难以控制,操作不当即会造成冲料而导致实验失败。
针对以上己二酸合成方法的缺点,从根本上解决实验中的污染危害,把绿色化学的思想渗透到有机化学实验中,绿色合成己二酸已成为国内外研究的重要课题。近年来,杂多酸作为一种环境友好的新型催化剂,在有机合成反应中的应用迅速发展。我们以钨磷酸做催化剂、30%的H2O2作为氧化剂,催化氧化环己醇来合成己二酸。该反应条件温和,易控制,反应过程中无毒害物质产生,且反应后产物易分离,用于实验教学中能得到满意的效果。
1 实验部分
1.1 实验试剂和仪器
RY-1熔点仪;傅里叶红外光谱仪(FTIR-8900)。
所用试剂均为分析纯试剂,没有做特别的处理。
1.2 催化剂制备
钨磷酸按照文献[8]制备。称取30g钨酸钠和12g六偏磷酸钠,磁力搅拌下溶于120mL热水(70~75℃)中,边搅拌边滴加30mL浓盐酸。滴加完毕后溶液略呈淡黄色。将反应混合物冷却到室温,并将其转移至分液漏斗中,分别加入30mL乙醚和15mL浓度为6mol/L的盐酸, 充分振荡, 静置。分出下层油状物于蒸发皿中,在水浴上慢慢蒸出其中的乙醚,然后放在空气中自然干燥。再将蒸发皿置于70℃烘箱中干燥2h,得到白色的钨磷酸固体9.8g。产率45.3%。
1.3 己二酸的合成
在100ml三颈瓶上装上温度计,球型冷凝管及恒压滴液漏斗,依次加入0.2mmol (0.6g) 钨磷酸,一定量的30%H2O2,室温下磁力搅拌搅拌15min后,用恒压滴液漏斗缓慢加入50mmol(5ml)环己醇。高速搅拌,加热回流。将反应液冷却至室温后再用冰水浴冷却,大量己二酸从水相中结晶出来,催化剂溶在母液中。用布氏漏斗抽滤,并用少量冰水洗涤,得到己二酸白色晶体。在室温下干燥,称重,计算产率。
1.4 产物分析
在大多数情况下,所得己二酸无需重结晶即可得到很高的纯度。对白色晶体产物进行熔点、IR测定。产物的IR谱图与标准谱图非常吻合,1695cm-1出现了特征羧基上O-H的伸缩振动;多数情况下产物的熔点为149~152℃与文献值(152℃)非常接近,证明是己二酸。
2 结果与讨论
在该反应体系中,H2O2是绿色的氧化剂,其还原产物仅为水,不会给合成带来任何有害物质,也不会腐蚀设备;钨磷酸是环境友好的催化剂,其催化效率高。我们分别从催化剂的用量,反应物的摩尔配比,反应时间的选择几个方面来研究最佳的反应条件,并且验证了催化剂的重复使用性。
2.1 钨磷酸的用量对反应产率的影响
固定30%H2O223ml(220mmol) 及环己醇5ml(50 mmol),考察了钨磷酸的用量对反应产率的影响,反应结果见表1。

表 1 钨磷酸用量的影响
由表1可以看出,在钨磷酸的用量仅为0.07mmol时,己二酸的收率可达38.4%,当钨磷酸的用量在0.07~0.21mmol之间变化时,产品的产率随着钨磷酸用量的增加逐渐增大;当钨磷酸用量为0.21mmol时,己二酸收率达最大值。但当钨磷酸用量大于0.21mmol时,产品己二酸的产率反而呈下降趋势。这是因为催化剂钨磷酸既具有酸性又具有氧化性,当催化剂用量为0.21mmol时,催化活性中心最好,己二酸收率最高;催化剂的加入量少时,不能提供足够的活性中心,己二酸收率较低;催化剂加入量太多,H2O2分解加剧,利用率低,同时产生的副产物增多,己二酸的收率反而下降。因此我们确定钨磷酸在0.21mmol时为该反应催化剂的最佳用量
从表1的结果表明,在该反应条件下,当钨从熔点值可以看出此时产品纯度很高。
2.2 反应物配比对反应产率的影响
我们是通过固定催化剂钨磷酸0.6g(0.2mmol)和环己醇5ml(50mmol)的用量,改变30%H2O2用量来探究反应物配比对产率的影响,结果见表2。

表 2 反应物配比的影响
由表2可知,当H2O2用量为11.5ml时,由于供氧不足,环己醇未能全部被氧化,仅得到少量的己二酸(副产物较多,产品难以分离)。随着H2O2用量的增大,产品的产率也逐渐增大,当用23ml H2O2参与反应时,产率达到最大值,此时的产品纯度也很高。当H2O2用量继续增大时,产品的产率变化不明显,并呈现下降的趋势,这可能是生成的己二酸又进一步被氧化。因此我们可以选择H2O2的用量为23ml(即钨磷酸、环己醇与H2O2物质的量比为1∶250∶1125),为最佳反应用量。
2.3 反应时间的影响
以30% H2O223ml,环己醇5ml(50mmol),钨磷酸0.6g(0.2mmol)为反应体系,在一定温度下考察了反应时间对反应的影响,表3列出了不同反应时间下己二酸的产率。
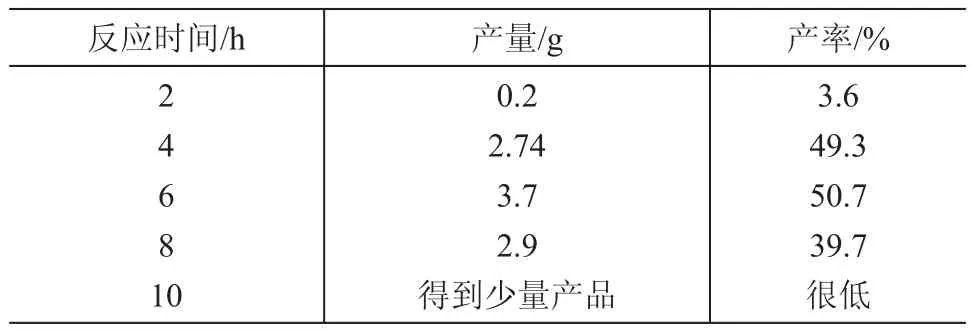
表3 反应时间的影响
由表中的结果表明随着反应时间的增加,己二酸的产率增大。当反应时间为2h时,收率仅为2.74%,这说明反应时间太短,反应不完全,产物处于中间状态,如二醇或其他环氧化合物。当反应时间为4h,己二酸的产率明显增大,到6h己二酸产率达到最大值(但与4h相比变化不明显)。当反应时间增大到8h时,产品的产率又有所降低,这可能是因为反应时间过长,过氧化氢已经消耗完,己二酸又转化为其他的副产物而影响到己二酸的收率。反应进行到10h,主要生成了副产物,仅得到少量己二酸且难以分离。因此实验的最佳的反应时间为4~6h,此时己二酸的产率可达到50%左右。
2.4 催化剂可否重复使用
在最佳反应条件下,我们还考察了催化剂的重复使用性。我们将反应后的母液加热浓缩至5ml,再加入30%过氧化氢23ml,环己醇5ml,在回流温度下反应6h。结果也得到了己二酸产品,这说明钨磷酸作为催化剂可以重复利用。但本次实验产品产率较低,还有待进一步实验研究。
3 结论
(1)通过本次实验可知,合成己二酸的最佳反应条件为:钨磷酸:环己醇:H2O2物质的量比为1∶250∶1125,加热回流反应4~6小时,平均产率可达到50%左右。
(2)本实验采用钨磷酸作为催化剂,该催化剂制备比较简单,用量较少,得到的产品的纯度较高,并且可以重复使用,是一种绿色的催化剂。
(3)钨磷酸可由学生自己合成,可用于综合设计实验。能和重结晶练习、熔点的测定组成系列实验,不仅可以节省试剂,减少污染,又可以缩短试验时间,从而取得更好的效果。
(4)改进后的实验反应条件温和,操作简单,易于控制,得到产品的纯度高,反应无污染,符合绿色化学实验的发展。
通过本次实验,不仅能让学生掌握一些常用的合成技术和表征方法,而且能让学生了解并深刻体会绿色化学研究的意义。
[1] 曾昭琼.有机化学实验(第三版)[M].北京:高等教育出版社,2000
[2] 谷珉珉,贾韵仪,姚子鹏.有机化学实验[M].上海:复旦大学出版社,1991
[3] 宫红,杨中华,姜恒.己二酸合成实验的改进[J].大学化学,2003,18(2):53~56
[4] 曹小华,徐常龙,赵新萍,等.磷钨钼杂多酸催化氧化环己醇清洁合成己二酸[J].化工进展,2008,27(8):1258~1261
[5] 张金辉,宫红.杂多酸清洁催化氧化环己烯制备己二酸[J].石油化工高等学校学报,2003,16(2):25~28
[6] 徐常龙,柳闽生,曹小华,等.己二酸合成实验的绿色化探究[J].化工时刊,2006,20(5):7~8,11
[7] 章文伟,薛强,张晖,等.己二酸的绿色合成[J].实验室研究与探索,2009,28(11):22~24
[8] 陈志敏,李江.12-钨磷酸催化合成甲基叔丁基醚[J].燃料化学学报,2008,36(1):115~117
[9] 胡玉华,单胜艳.杂多酸催化剂在有机合成中的应用[J].化工进展,2006,25(5):520~523
[10] 张敏,刘星明.己二酸的绿色化学合成研究进展[J].湖南科技学院学报,2008,29(12):38~41
Preparation of adipic acid—The application of green chemistry in organic chemistry experiment
Wang Jiye, Zhang Xuan, Feng Yuling
Hebei normal university, Shijiazhuang, 050016, China
2011-01-04 稿件编号:1101006
王继业,硕士,高级实验师。张轩,河北师范大学2010届毕业生。
河北省教育厅自然科学基金资助项目(编号:Z2006436);河北师范大学设备处基金资助项目。
