ABn型α-环糊精单体及其超支化聚合物的合成及表征
2011-10-18火跃芳卞庆亚蒋立英
王 宁,火跃芳,卞庆亚,仇 凡,蒋立英
(盐城卫生职业技术学院,江苏 盐城 224006)
研究开发
ABn型α-环糊精单体及其超支化聚合物的合成及表征
王 宁,火跃芳,卞庆亚,仇 凡,蒋立英
(盐城卫生职业技术学院,江苏 盐城 224006)
为了得到结构确定的α-环糊精(α-CD)单体并用于聚合,通过对由单取代十一烯酸酯化的α-CD上羟基的酯化,得到 ABn型功能化α-CD类单体,并利用 Hoveyda-Grubbs第二代催化剂引发该单体在水/有机溶剂[D2O/(CD3)2CO]中的非环二烯烃易位聚合,一步法得到新型超支化聚(α-CD)。采用1H NMR、FTIR、飞行时间质谱(MALDI-TOF MS)和元素分析对ABn型α-CD单体及其超支化聚合物的结构进行表征。结果表明,单体和聚合物的结构与所设计的分子结构相符合。多角度激光光散射/凝胶渗透色谱(MALLS–GPC)联用仪测得超支化聚(α-CD)的数均分子量为13200~56300,分子量分布在2.78~2.63。利用1H NMR图谱计算出该聚合物支化度在0.41~0.52。
ABn型α-环糊精单体;超支化聚合物;Hoveyda-Grubbs第二代催化剂;非环二烯烃易位聚合
超支化聚合物(HBP)作为一类新型的高分子材料,由于具有新颖的化学结构、独特的使用性能和潜在的应用前景,而受到科学界和工业界的普遍关注[1-3]。超支化的概念最初由 Flory在 1952年提出[4],只要单体为ABn型(n≥2)的,且A、B均为具有反应活性的官能团,就可以产生超支化结构。因此,ABn类单体的设计与合成在制备HBP的过程中占有很重要的地位,能否合成出一种合适的ABn类单体至关重要。此外,这类聚合物具有近似球形或椭球形的三维结构、大量的末端活性官能团、较高的溶解性、较低的黏度等许多线型聚合物所不具有的独特的物理和化学性质[5-7]。虽然没有树枝状聚合物的高度结构规整性和单分散性,但其合成方法简单,易于纯化与分离[8-9]。目前,许多活性聚合方法常用来制备HBP[10-12]。
环糊精(CD)是一个中空环状低聚糖化合物,分子形状略呈锥形,锥腔具有内疏水、外亲水的特点,正是因为CD分子这种独特的双亲性结构和在生物医学领域重要的应用,使其具有识别多种客体化合物并与之形成超分子包合物的特性[13-14]。然而,由于其复杂的合成过程,CD并没有经常被考虑作为单体来制备 HBP。但实际上,通过使用改性的CD作为单体,成功设计并获得的CD基HBP将拥有一些特殊的结构和性质。这些HBP结合了支化结构和CD分子链段两种不同的分子空腔,大大提高了客体小分子的包覆和识别能力,并在复合药物传递系统方面赋予重要的作用。
目前,以功能化的环糊精为单体直接合成超支化聚合物的研究仅有少量报道。但单体的合成路线都较繁琐,HBP的制备条件也较苛刻[15]。烯烃易位聚合作为一种有效合成高度官能化聚烯烃的方法,对聚合物化学,尤其是活性聚合领域有着很重要的影响。然而,利用烯烃易位聚合的方法制备 HBP还没有受到广泛的关注[16-19]。本文通过两步简单的酯化反应得到功能化的ABn型环糊精单体,首次在均相的 D2O/(CD3)2CO中通过非环二烯烃易位(ADMET)聚合一步得到超支化聚(α-CD),这种新型的 HBP有望在药物控制释放领域得到广泛的应用,具体见图1。
1 实验部分
1.1 试剂与仪器
1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDCI·HCl),4-二甲氨基吡啶(DMAP),丙烯酸,上海国药集团化学试剂有限公司,AR;α-环糊精,Alfa Aesar;十一烯酸,Alfa Aesar;第二代Hoveyda-Grubbs催化剂,Aldrich。二甲亚砜(DMSO)经氢化钙干燥,使用前蒸馏。Bruker DPX 500 MHz型核磁共振波谱仪,内标 TMS,溶剂(CD3)2SO;Nicolet Nexus 670型傅里叶红外光谱(FTIR)仪,采用溴化钾压片法;Bruker Biflex III型飞行时间质谱(MALDI–TOF MS)仪;多角度激光光散射-凝胶渗透色谱(MALLS-GPC)联用检测仪,以DMF/LiCl为流动相,40 ℃下测定分子量及其分布,溶剂流出速度0.5 mL/min。
1.2 单取代十一烯酸酯化α-CD的合成
将α-CD(4.86 g,5.0 mmol)、十一烯酸(0.92 g,5.0 mmol)和 DMAP(60 mg,0.6 mmol)溶于60 mL无水的DMSO中,搅拌,冰水浴下冷却15 min,加入EDCI(1.12 g,6 mmol),待溶液温度升至室温后继续搅拌2 d,体系浓缩至近10 mL后沉淀到大量的CH2Cl2中,抽滤,重复3次操作后,80 ℃下真空干燥24 h得到目标产物,收率87%。从图 2(a)中可以看到,目标产物的1H NMR(DMSO-d6,δ):5.79~5.73[m,13H,OH(2,3)+ CH2=CHCH2],5.00~4.92(m,2H,CH2=CHCH2),4.82[s,6H,CH(1)],4.45[s,5H,OH(6)],4.27~4.22(m,2H,OOCCH2),3.75~3.55[m,6H,CH(3)+ 6H,CH(5)+ 12H,CH2(6)],3.36~3.32[m,6H,CH(2)+ 6H,CH(4)],2.01~1.99(d,2H,CH2=CHCH2),1.69~1.41(m,2H,CH2OOCCH2CH2),1.38~1.15(m,10H,CH2CH2CH2CH2CH2)。C47H79O31元素分析实验值(计算值%):C 49.49(49.52),H 6.95(6.93),O 43.56(43.55)。

图1 超支化聚(α-环糊精)的合成路线
1.3 ABn型α-CD单体的合成
将上述合成的改性单取代α-CD(3.42 g,3 mmol)、丙烯酸(7.2 g,100 mmol)和 DMAP(0.75 g,6 mmol)溶于80 mL无水的DMSO中,搅拌,冰水浴下冷却15 min,加入EDCI(11.5 g,60 mmol),待溶液升至室温后继续搅拌7 d,体系浓缩至近15 mL后沉淀到大量的CH2Cl2中,抽滤,重复3次操作后,80 ℃下真空干燥24 h得到目标产物,收率85%。从图2(b)中可以看到,目标产物的1H NMR(DMSO-d6,δ):6.45~6.31(d,17H,OCOCH=CH),6.27~6.13(m,17H,OCOCH=CH),5.96~5.92(d,17H,OCOCH=CH),5.77~5.71(m,1H,CH2=CHCH2),5.01~4.95(m,2H,CH2=CHCH2),4.83[s,6H,CH(1)],4.25~4.23(m,2H,OOCCH2),3.75~3.55[m,24H,CH(3)+ CH(5)+ CH2(6)],3.39~3.32[m,12H,CH(2)+ CH(4)],2.18~2.11(d,CH2=CHCH2),1.72~1.56(m,2H,CH2OOCCH2CH2),1.37~1.26(m,12H,CH2CH2CH2CH2CH2CH2)。MALLS-GPC:Mn=2060,Mw/Mn=1.06。MALDI-TOF MS(m/z):2057.982。理论计算值:Mn,th=2059.522。C98H113O48元素分析实验值(计算值,%):C 57.19(57.17),H 5.46(5.49),O 37.35(37.34)。
1.4 超支化聚α-环糊精的合成

图2 α-CD单体及其超支化聚合物的核磁氢谱图* DMSO-d6;** H2O
10 mL Schlenk 反应管中加入ABn型α-CD单体(411.4 mg,0.2 mmol),加0.6 mL D2O使其完全溶解。另一支 10 mL Schlenk 管中加入第二代Hoveyda-Grubbs催化剂(单体摩尔质量的0.5%)和(CD3)2CO(0.4 mL),两管经液氮冷冻,抽真空,充氮气,解冻循环3次,在通氮气的条件下用注射器将催化剂溶液加入到单体中,50 ℃油浴中搅拌反应,到预定时间后,加入少量终止剂乙烯基乙醚,再室温搅拌0.5 h后停止。反应生成的聚合物溶液搅拌下加入到大量的甲醇中沉淀(反复进行2次),真空烘箱干燥至恒重。从图2(c)中可以看到,超支化聚(α-CD)的1H NMR(DMSO-d6,δ):6.98~6.91(m,OCOCH=CH),6.49~6.37(d,OCOCH=CH),6.23~6.15(m,OCOCH=CH),5.91~5.76(d,OCOCH=CH),5.73~5.58(m,CH2=CHCH2),5.07~4.91(m,CH2=CHCH2),4.87[s,CH(1)],4.29~4.21(m,OOCCH2),3.82~3.65[m,CH(3)+ CH(5)+ CH2(6)],3.34~3.29[m,CH(2)+ CH(4)],3.25~3.21(m,CH2OCH2),2.03~1.99(d,2H,CH=CHCH2),1.79~1.68(m,CH2OOCCH2CH2),1.47~1.23(m,CH2CH2CH2CH2CH2CH2)。MALLS-GPC:反应 24 h,Mn= 13200,Mw/Mn= 2.78;反应 48 h,Mn= 29800,Mw/Mn= 2.72;反应96 h,Mn= 56300,Mw/Mn= 2.63。
2 结果与讨论
2.1 ABn型α-CD单体的分子设计与合成
首先将α-CD分子中一个羟基进行功能化,即利用酯化反应将A官能团——富电子烷基烯烃引入到α-CD母体中,随后再通过与丙烯酸的酯化反应将B官能团——负电子的烯烃接入α-CD母体上,从而得到可用于合成超支化聚合物的功能化环糊精单体(图2)。
从其1H NMR图谱[图2(a)]的分析可知,在δ= 5.00~4.92出现一个新的烯烃质子峰(Ha),在δ= 4.27~4.22(He)、δ= 2.01~1.99(Hc)、δ=1.69~1.41(Hj)和δ= 1.38~1.15(Hd)处代表十一烯酸中亚甲基上质子的出峰。对图 2(a)中各羟基上质子的峰面积进行积分可知仅有一个羟基发生了酯化反应,得到了单取代烯烃改性的α-CD。此外,FTIR 谱图[图 3(a)]显示了在 3420 cm-1、2856~2918 cm-1和 2721 cm-1处 O—H、不饱和C=C—H以及C=O的特征吸收峰,这也表明酯化反应的进行。

图3 单取代十一烯酸酯化α-CD(a),ABn型α-CD单体(b)和超支化聚α-环糊精(c)的红外谱图
ABn型α-CD单体则是通过大量的丙烯酸与上述改性的α-CD中其余的羟基发生酯化反应获得。图2(b)中δ= 5.79~5.73和δ= 4.45处O—H中质子峰的消失及δ= 6.45~6.31、δ= 6.27~6.13和δ=5.96~5.92处CH2=CH—中质子峰的形成,证明制备了ABn型单体。通过对图2(b)中丙烯酸双键上质子峰面积进行积分可知酯化度为16.92,即α-CD中剩余的17个羟基几乎全部转化为丙烯酸酯,并计算出该 ABn型α-CD大单体的数均分子量为2059.522;飞行时间质谱(图 4)测得的单体为2057.982;MALLS-GPC测试(图5)结果可知Mn=2060,Mw/Mn= 1.06。由此可见三者的结果较为接近,说明B官能团的平均个数为16~17,几乎消耗了α-CD中所有的羟基。因此该α-CD大单体为混合型单体,故称为 ABn型,其中n的个数可能为16或17。从[图3(b)]可以看出,波数在3420 cm-1处O—H键的消失也进一步说明α-CD中所有羟基都酯化完全,成功制得了 ABn型α-CD单体。
2.2 超支化聚α-CD的合成与表征
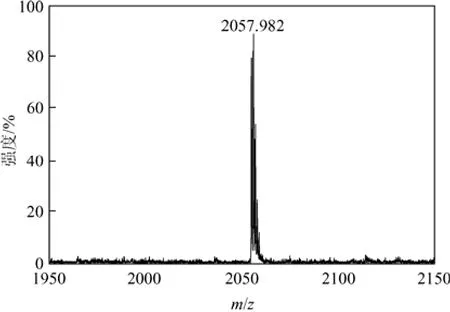
图4 ABn型α-CD单体的飞行时间质谱图

图5 典型的ABn型α-CD单体和超支化聚α-环糊精的多角度激光光散射-凝胶渗透色谱
通过ADMET聚合,在D2O/(CD3)2CO溶剂(体积比为 3∶2)中,以 ABn型α-CD 单体为原料,Hoveyda-Grubbs第二代为催化剂,50 ℃油浴下反应24~96 h,得到超支化聚α-CD(图1)。由于催化剂在溶液中的寿命只能保持36~48 h,因此,在聚合 48 h后向体系中又补加等量的催化剂。从1H NMR图谱[图2(c)]可以看出,与单体相比,聚合物在δ= 6.98~6.91(Hm)处产生了新的质子峰,归属于交叉易位反应后新生成的内部丙烯酸酯中不饱和双键上的质子峰,而其它的化学位移并没有明显变化,由此说明该HBP是由单体经ADMET聚合获得。从FTIR谱图[图3(c)]中可以看出,单体与HBP有着相似的吸收峰,表明它们具有相同的结构组成。综合1H NMR和FTIR谱图分析可知,超支化聚(α-CD)已成功制得。
为了更好地了解聚合的过程,MALLS-GPC联用检测仪被用来跟踪单体的聚合。从MALLS-GPC图(图5)以及表1中的数据可以看出,曲线呈多峰分布,分子量分布指数也较宽,这与HBP的组成和性质是一致的[4]。随着聚合反应的进行,低分子量处的峰面积逐渐减小,24 h后,分子量明显增加(Mn= 13200,Mw/Mn= 2.78),48 h后,单体几乎聚合完全,HBP的洗脱曲线移到了更高分子量的位置(Mn= 29800,Mw/Mn= 2.72)。随后,向体系中补加新的催化剂,分子量有了进一步的提高,分子量分布指数也相应变窄(Mn= 56300,Mw/Mn=2.63),这些都说明延长聚合时间会产生高分子量和低分子量分布指数的 HBP。此外,这种新型的HBP能溶于水、DMF和DMSO等强极性溶剂中,但不溶于非极性溶剂。
支化度(DB)是表征HBP的另一重要参数。根据 Frechet等的报道[20],DB可用公式计算,即DB= (D + T)/(D + L + T)。其中,D、L、T分别代表HBP中的树枝状单元、线形单元和端基单元的数量。利用Frechet方法,由图2(c)可以得到这三个单元的化学位移δ分别为 5.67、5.64和 5.61(Hb),并对其所对应的峰面积积分,代入上述公式可计算出HBP的DB(表1)。这与文献报道的HBP的理论DB值较为接近。
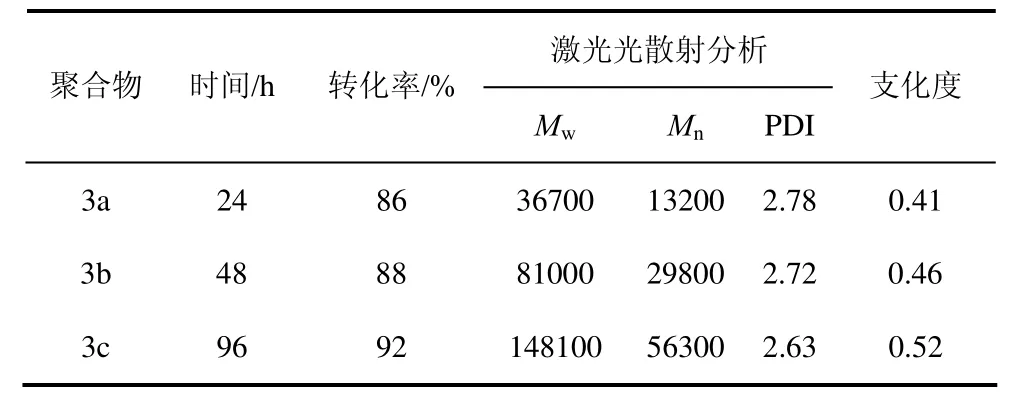
表1 超支化聚(α-环糊精)的结构表征参数
3 结 论
通过对α-CD上羟基的两步酯化改性得到同时含有一个富电子的烷基烯烃和许多负电子的丙烯酸酯烯烃的ABn型α-CD单体,在Hoveyda-Grubbs第二代催化剂作用下,首次在水/有机溶剂的均相体系中进行ADMET聚合,制备出一种新型的水溶性超支化聚α-CD。利用MALLS-GPC联用检测仪测得该聚合物拥有相对较高的分子量(2600~51300)和中等的分子量分布(2710~2590)。
超支化聚合物拥有一些特殊的性能,因此,受到许多科研工作者的关注,这种新型的超支化聚合物能溶于水等强极性溶剂,环糊精大量的空腔以及超支化聚合物的球形结构使得这类聚合物有望在药物控制释放等领域获得广泛应用。
[1]Mori H,Seng D,Lechner H,et al. Synthesis and characterization of branched polyelectrolytes. 1. Preparation of hyperbranched poly(acrylic acid)viaself-condensing atom transfer radical copolymerization[J].Macromolecules,2002,35:9270-9281.
[2]Hu Q,Liu D,Zeng S M,et al. Preparation and properties of highly branched waterborne poly(urethane-urea)viaA2+ B3approach[J].J.Applied Polym. Sci.,2010,116:817-824.
[3]Zhou Y F,Huang W,Liu J Y,et al. Self-assembly of hyperbranched polymers and its biomedical applications[J].Adv. Mater.,2010,22:4567-4590.
[4]Flory P J. Molecular size distribution in three dimensional polymers.VI. Branched polymers containing A—R—Bf-1 type units[J].J. Am.Chem. Soc.,1952,74:2718-2723.
[5]Kim Y,Webster O. Hyperbranched polyphenylenes[J].Macromolecules,1992,25:5561-5572.
[6]Hong C,Pan C Y. Synthesis and characterization of hyperbranched polyacrylates in the presence of a tetrafunctional initiator with higher reactivity than monomer by self-condensing vinyl polymerization[J].Polymer,2001,42:9385-9391.
[7]Gao C,Yan D. Hyperbranched polymers:From synthesis to applications[J].Prog. Polym. Sci.,2004,29:183-275.
[8]Voit B,Lederer A. Hyperbranched and highly branched polymer architectures-synthetic strategies and major characterization aspects[J].Chem. Rev.,2009,109:5924-5973.
[9]Voit B. Hyperbranched polymers—All problems solved after 15 years of research?[J].J. Polym. Sci. Part A:Polym. Chem.,2005,43:2679-2699.
[10]Koh M L,Konkolewicz D,Perrier S. A simple route to functional highly branched structures:RAFT homopolymerization of divinylbenzene[J].Macromolecules,2011,44:2715-2724.
[11]Xu J T,Tao L,Boyer C,et al. Combining thio-bromo “click”chemistry and RAFT polymerization:A powerful tool for preparing functionalized multiblock and hyperbranched polymers[J].Macromolecules,2010,43:20-24.
[12]Kong L Z,Sun M,Qiao H M,et al. Synthesis and characterization of hyperbranched polystyreneviaclick reaction of AB2macromonomer[J].J. Polym. Sci. Part A:Polym. Chem.,2010,48:454-462.
[13]靖波,陈晓,柴永存. 环糊精与大分子组装(准)聚轮烷[J]. 化学进展,2006,18:1361-1368.
[14]Kato K,Komatsu H,Ito K. A versatile synthesis of diverse polyrotaxanes with a dual role of cyclodextrin as both the cyclic and capping components[J].Macromolecules,2010,43:8799-8804.
[15]Tian W,Fan X,Kong J,et al. Cyclodextrin-based hyperbranched polymers:Molecule design,synthesis,and characterization[J].Macromolecules,2009,42:640-651.
[16]Gorodetskaya I A,Choi T L,Grubbs R H. Hyperbranched macromoleculesviaolefin metathesis [J].J. Am. Chem. Soc.,2007,129:12672-12673.
[17]Fokou P A,Meier M A R. Acyclic triene metathesis polymerization with chain-stoppers:Molecular weight control in the synthesis of branched polymers [J].Macromol. Rapid Commun.,2008,29:1620-1625.
[18]Mathers R T,Damodaran K,Rendos M G,et al. Functional hyperbranched polymers using ring-opening metathesis polymerization of dicyclopentadiene with monoterpenes[J].Macromolecules,2009,42:1512-1518.
[19]Ding L,Zhang L Y,Xie M R,et al. Hyperbranched azo-polymers synthesized by acyclic diene metathesis polymerization of an AB2monomer[J].Macromolecules,2009,42:5036-5042.
[20]Hawker C J,Lee R,Frechet J M J. One-step synthesis of hyperbranched dendritic polyesters [J].J. Am. Chem. Soc.,1991,113:4583-4588.
Synthesis and characterization of ABn-typeα-cyclodextrin monomer and its hyperbranched polymer
WANG Ning,HUO Yuefang,BIAN Qingya,QIU Fan,JIANG Liying
(Yancheng Health Vocational and Technical College,Yancheng 224006,Jiangsu,China)
To obtain well-defined structures ofα-cyclodextrin (α-CD) based monomer and its hyperbranehed polymer (HBP), a modifiedα-CD molecule with one electron-rich alkene and many electron-poor acrylates was first prepared through the esterification reaction between mono-ester undecylenic acid-α-CD and acrylic acid. It was then utilized as an ABn-type monomer for subsequent ADMET polymerization between alkene and acrylate using the second generation Hoveyda-Grubbs catalyst in homogeneous water/organic [D2O/(CD3)2CO]mixturesviaacyclic diene metathesis(ADMET) polymerization. A novel cyclodextrin-based HBP was obtained in prolonged reaction time.The monomer and HBP were characterized by NMR, elemental analysis, FTIR, and MALDI-TOF MS measurements. It was found that the actual molecular structures of both monomer and polymer were identical with the designed structures. The produced polymers have molecular weights within 13.2 and 56.3 kDa, and their polydispersity indices range from 2.78 to 2.63 by multiangle laser light scattering-gel permeation chromatography. The degree of branching was determined by1H NMR spectroscopy and the values ranges from 0.41 to 0.52.
ABn-typeα-cyclodextrin monomer;hyperbranched polymer;second generation Horeyda-Grubbs catalyst;diene metathesis polymerization
TQ 314.2
A
1000–6613(2011)12–2679–06
2011-08-25。
盐城卫生职业技术学院立项项目。
王宁(1960—),男,副教授,硕士,研究方向为有机合成和计算化学。E-mail jsywwn@163.com。联系人:卞庆亚,教授,硕士生导师,研究方向为有机结构分析,E-mail biangy1964@163.com。
