高效液相色谱法测定白芍药材中芍药苷和芍药内酯苷的含量
2011-10-09李伟张建军王卫茜陈振振王景霞欧丽娜
李伟,张建军,王卫茜,陈振振,王景霞,欧丽娜
白芍为毛茛科植物芍药Paeonia lactiflora Pall.的干燥根,味苦、酸,性微寒,归肝、脾经,功能平肝止痛,养血调经,敛阴止汗。白芍中主要含有单萜及其苷类化合物,称为白芍总苷(TGP),包含芍药苷、芍药内酯苷、氧化芍药苷(又名羟基芍药苷)、苯甲酰芍药苷、芍药新苷、芍药苷元酮和白芍苷R1等十余种成分[1~4]。目前,对芍药苷的活性研究较多,白芍药材及含白芍制剂的质量控制多以芍药苷为指标,采用高效液相色谱法测定,但对芍药内酯苷的研究较少,近年来对芍药内酯苷的活性和含量测定越来越引起重视[5~6]。为更好的控制白芍药材质量,指导其药学、药效毒理学研究,本研究建立了采用高效液相色谱法同时测定白芍药材中芍药苷、芍药内酯苷的方法。
1 仪器与试剂
Agilent1100型高效液相色谱仪(美国安捷伦公司),Kromasil C18(4.6×250 mm,5 μm)色谱柱(瑞典EKA Chemicals公司),超声波清洗器(功率250 W,频率50 kHz)(济宁天华超声电子仪器有限公司),甲醇(色谱纯,Merck公司),水为超纯水,磷酸、氢氧化钠为分析纯。芍药苷对照品购自:中国药品生物制品检定所(供含量测定用,批号:110736-200732);芍药内酯苷对照品购自:wako日本和光纯药公司(批号:016-22201)。本研究收集市售白芍药材样品8批,由北京中医药大学基础医学院方药系临床中药教研室张建军副研究员鉴定为毛茛科植物芍药Paeonia lactif l ora Pall.的干燥根。
2 方法与结果
2.1 对照品溶液的制备
精密称取芍药内酯苷对照品和芍药苷对照品适量,加甲醇制成每1 mL各含0.02 mg的溶液,即得。
2.2 供试品溶液的制备
取白芍药材粉末约0.1 g,精密称定,置50 mL量瓶中,加入稀乙醇45 mL,超声提取30分钟,放冷,加稀乙醇稀释至刻度,摇匀,滤过,取续滤液,即得。
2.3 色谱条件
以十八烷基硅烷键合硅胶为填充剂,以甲醇-0.1%磷酸溶液(用1%氢氧化钠溶液调节pH值至4.2)(34∶66)为流动相,检测波长为230 nm。进样量10 μL,理论板数按芍药苷峰计算应不低于2000。见图1。
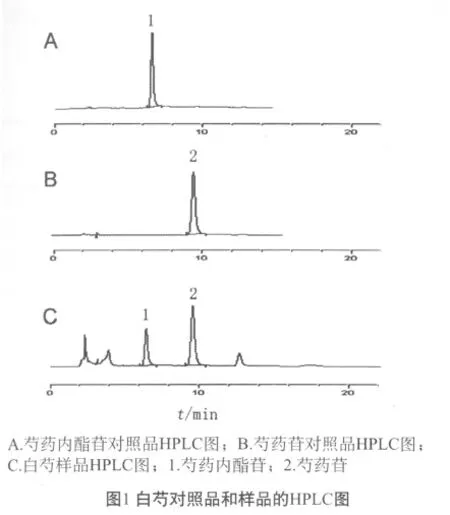
2.4 检测波长的确定
经紫外光谱扫描,确定检测波长为芍药内酯苷和芍药苷的最大吸收波长230 nm。
2.5 线性关系考察
精密称取芍药内酯苷对照品适量,加甲醇配制成每1 mL含芍药内酯苷0.0018 mg,0.0036 mg,0.0072 mg,0.0144 mg,0.0288 mg,0.0576 mg的溶液;精密称取芍药苷对照品适量,加甲醇配制成每1 mL含芍药苷0.0028 mg,0.0056 mg,0.0112 mg,0.0224 mg,0.0448 mg,0.0896 mg的溶液。分别吸取各对照品溶液10 μL,注入高效液相色谱仪,依法测定峰面积,绘制标准曲线。结果表明,芍药内酯苷在0.018~0.576 μg范围内呈线性关系,其回归方程为:Y=926.19X-0.9368,r=0.9999;芍药苷在0.028~0.896 μg范围内呈线性关系,其回归方程为:Y=1440X-0.3503,r=0.9999。
2.6 对照品纯度考察
分别精密称取芍药内酯苷和芍药苷对照品,用流动相溶解,制成每1 mL含量为2.58 mg和2.36 mg的对照品溶液,吸取20 μL注入高效液相色谱仪,按面积归一化法测定纯度。结果表明,芍药内酯苷对照品纯度为98.51%,RSD为0.22%;芍药苷对照品纯度为98.61%,RSD为0.18%。
2.7 仪器精密度实验
精密称取芍药内酯苷和芍药苷对照品,重复进样6次,测定峰面积,计算RSD分别为1.2%,0.94%。
2.8 稳定性实验
取芍药内酯苷和芍药苷对照品溶液及供试品依法制备成供试品溶液,在0、24、48小时内依法测定。结果表明,芍药内酯苷和芍药苷对照品溶液和供试品溶液在48小时内稳定,RSD分别为0.67%,0.95%;0.97%,0.61%。
2.9 样品重复性实验
精密称取同一批次白芍药材6份,按上述方法测定芍药内酯苷和芍药苷含量。测得芍药内酯苷、芍药苷的平均含量分别为0.75%、3.13%,RSD分别为1.27%,1.32%,表明方法重复性良好。
2.1 0 回收率实验
精密称取已知含量的同一批次白芍药材0.05 g,按样品重复性实验结果计算芍药内酯苷含量为7.48 gkg-1,分别精密加入芍药内酯苷对照品0.358 mg,按供试品溶液制备方法及上述高效液相色谱条件操作,测定含量,计算回收率。结果表明,芍药内酯苷平均回收率98.18%,RSD%为1.78%。结果见表1。
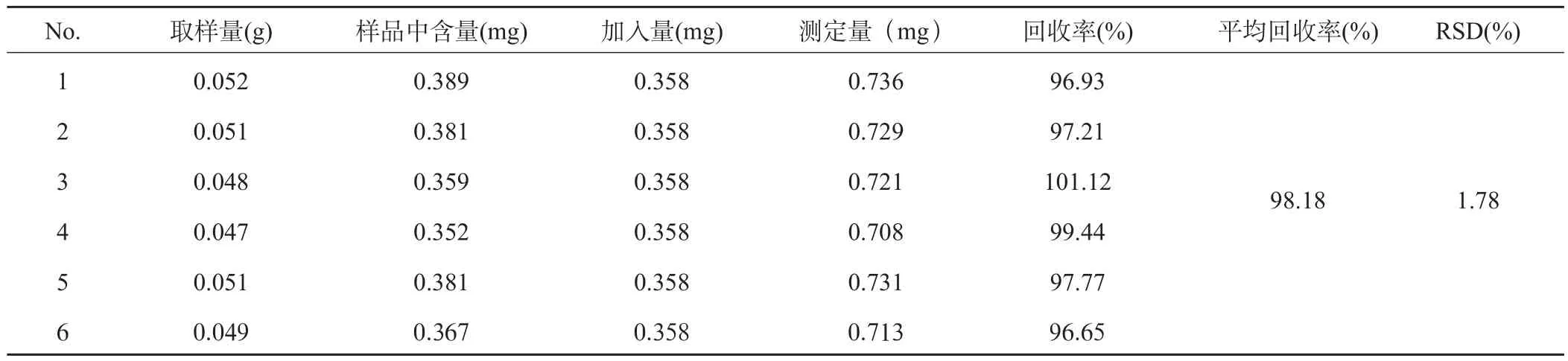
表1 芍药内酯苷回收率实验
精密称取已知含量的同一批次白芍药材0.05 g,按样品重复性实验结果计算芍药苷含量为31.30 gkg-1,分别精密加入芍药苷对照品1.502 mg,按供试品溶液制备方法及上述高效液相色谱条件操作,测定含量,计算回收率。结果表明,芍药苷平均回收率为98.26%,RSD%为1.25%。结果见表2。
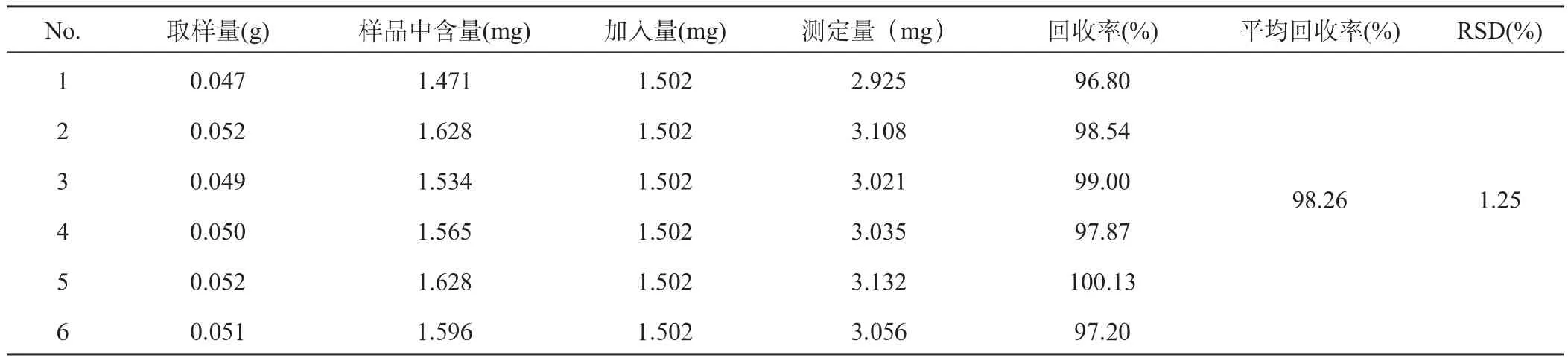
表2 芍药苷回收率实验
2.1 1 样品含量测定结果
从白芍药材的主要产地(浙江、安徽、四川)收集多批次未经硫磺熏制加工的白芍药材样品,按上述含量测定方法进行含量测定。结果表明芍药内酯苷和芍药苷含量分别不少于0.75%和2.71%,平均值分别为0.95%和2.93%。结果见表3。
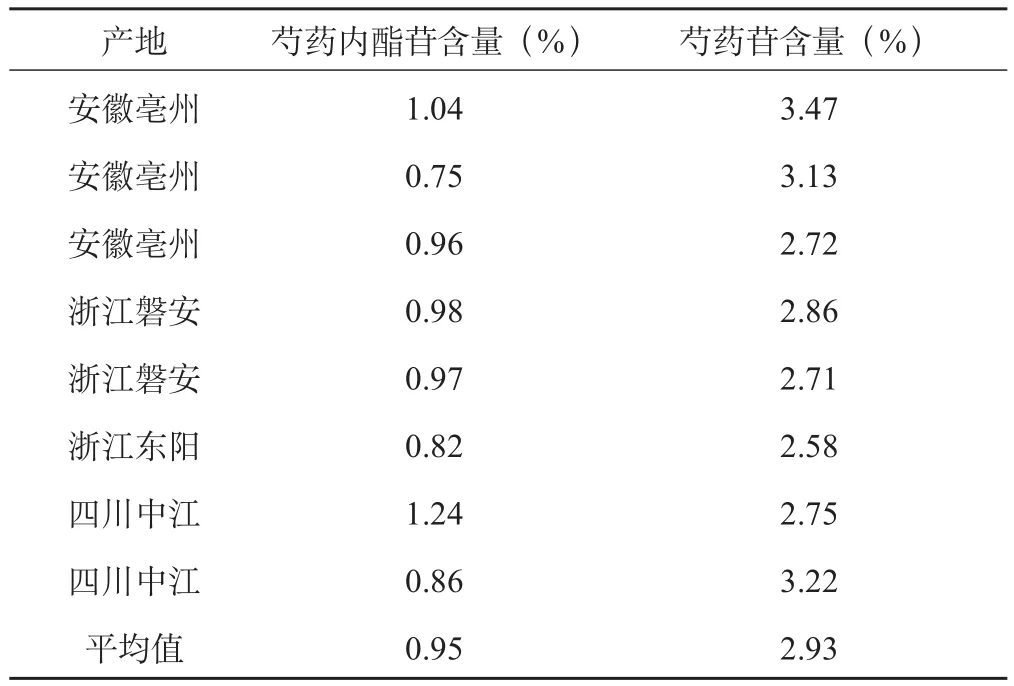
表3 白芍药材含量测定结果
3 讨论
3.1 氧化芍药苷干扰芍药内酯苷含量测定
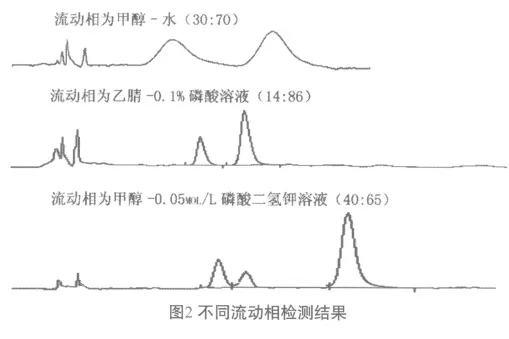
参考以往文献报道,采用下述3种流动相进行高效液相色谱法检测,方法①:采用中国药典2010版一部白芍药材芍药苷含量测定项下流动相乙腈-0.1%磷酸溶液(14:86);方法[7]②:采用甲醇-水(30:70)为流动相[8];方法③:采用中国药典2010版一部赤芍药材芍药苷含量测定项下的流动相甲醇-0.05molL-1磷酸二氢钾溶液(40:65)[9]。结果见图2。方法①和②的色谱图均为两个峰,但芍药内酯苷加样回收率不符合规定,说明可能该方法不能准确测定芍药内酯苷;方法③色谱图为三个峰,芍药内酯苷芍药苷之间有一个色谱峰且和芍药内酯苷不能完全分离,调整流动相中有机相和水相的比例亦无法分离;同一样品,在芍药苷峰面积近似的情况下,方法③芍药内酯苷和该未知成分的色谱峰面积之和与方法①和②芍药内酯苷面积基本相等。结果表明在以上条件下,白芍药材中含有对芍药内酯苷检测有干扰的成分。经与氧化芍药苷对照品进行对照,确定此干扰成分为氧化芍药苷。
3.2 采用甲醇与适宜pH的盐溶液组成的流动相可以同时测定芍药苷、芍药内酯苷
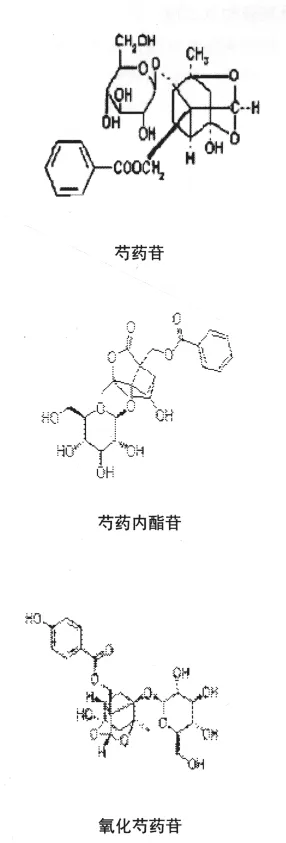
对芍药苷、芍药内酯苷和氧化芍药苷的化学结构进行比较,芍药内酯苷和芍药苷是同分异构体,但芍药内酯苷具有内酯结构,极性比芍药苷大;氧化芍药苷比芍药苷多一个酚羟基,极性也比芍药苷大。而氧化芍药苷色谱行为易受pH影响,可利用酸碱性使其与芍药内酯苷分离。
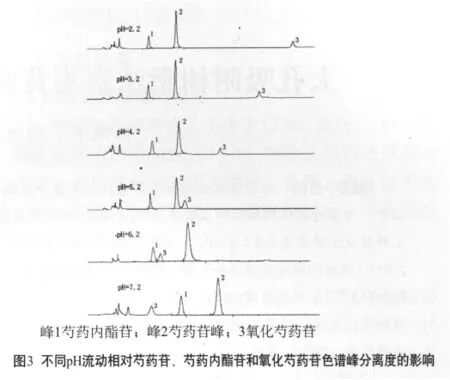
流动相采用甲醇-不同pH的磷酸-磷酸盐溶液,配制含有芍药苷、芍药内酯苷和氧化芍药苷的对照品溶液,以3个色谱峰的分离度为指标,对流动相的pH进行考察。结果见图3。结果表明,改变流动相pH,芍药内酯苷和芍药苷的分离度没有明显改变,而氧化芍药苷随流动相pH升高,保留时间缩短;反之,pH降低,保留时间延长。确定选用pH为4.2的流动相,可使3个色谱峰完全分离,并可节省检测时间。
芍药内酯苷和芍药苷均为白芍中含量相对较高的单萜类成分,目前2010年版《中国药典》只规定了白芍药材和饮片中的芍药苷的含量,未规定芍药内酯苷的含量。本研究为确定白芍药材中芍药苷和芍药内酯苷的含量提供了方法,对于白芍药材、饮片或制剂生产的质量控制具有指导意义。
[1] Kaneda M,Iitaka Y,Shibata S.The absolute structure of paeoniflorin, albiflorin, oxypaeoniflorin and benzoylpaeoniflorin isolated from Chinese paeony root[J].Tetrahedron, 1972,28:4309.
[2] Yu J,Elix J,Iskander M.Lactiflorin,a monoterpene glycoside from paeony root[J].Phytochemistry,1990,29(12):3859.
[3] Mineo S,Toshimitsu H,Naokata M,et al.The structure of paeonif l origenone,a new monoterpene isolated from Paeoniae Radix[J].Chem Pharm Bull,1983,31(2):577.
[4] 张晓燕,高崇凯,王金辉,等.白芍中的一种新的单萜苷[J].药学学报,2002,37(9):705.
[5] Sugaya A,Suzuki T,Sugaya E,et al.Inhibitory effect of peony root extract on pentylenetetrazol-induced EEG power spectrum changes and extracellular calcium concentration changes in rat cerebral cortex[J].Ethnopharmacol,1991,33(1-2):159.
[6] Jeon MH,Kwon HJ,Jeong JS,et al.Detection of albiflorin and paeoniflorin in Paeoniae radix by reversed-phase highperformance liquid chromatography with pulsed amperometric detection[J].J Chromatogr A,2009,1216(21):4568.
[7] 中华人民共和国药典委员会《中华人民共和国药典》一部[S].北京:中国医药科技出版社,2010:96.
[8] 姜晓燕,罗琳,窦志华,等.HPLC法测定赤芍饮片中芍药内酯苷及芍药苷的含量[J].齐鲁药事,2008,27(3):147.
[9] 中华人民共和国药典委员会《中华人民共和国药典》一部[S].北京:中国医药科技出版社,2010:147.
