基于分子内电荷转移的阴离子比率荧光分子探针
2011-09-29刘阁邵杰
刘 阁 邵 杰
(1赤峰学院化学系,赤峰 024000)(2南京林业大学化学与材料科学系,南京 210037)
基于分子内电荷转移的阴离子比率荧光分子探针
刘 阁*,1邵 杰2
(1赤峰学院化学系,赤峰 024000)(2南京林业大学化学与材料科学系,南京 210037)
设计合成了一种基于4-甲基-1-羟基二苯甲酮对硝基苯腙的比色和比率荧光阴离子受体1。此类受体以羟基和腙单元为识别位点,以硝基苯基为信号报告基团。向受体1的DMSO溶液中加入AcO-、H2PO4-、F-后,溶液颜色由黄色变为紫红色,而加入所研究的其它阴离子则无变化,从而实现对AcO-、H2PO4-、F-这三种离子的裸眼识别。利用紫外-可见吸收光谱、荧光光谱考察了其与AcO-,H2PO4-,F-,Cl-,Br-,I-等阴离子的识别作用。1H NMR滴定为受体分子与阴离子之间氢键作用本质提供了有力证据。
阴离子传感器;分子内电荷转移;比率;荧光;比色
0 引 言
阴离子在生物体系中无处不在,在广泛的生化过程中扮演着重要的角色,阴离子在环境污染方面的效应现在也被人们意识到[1]。因此,近年来,设计合成在生物或环境领域中具有重要作用的阴离子的化学传感器引起了诸多科研工作者的关注[2]。特别是在近20年内,这个发展尤其明显,人们投入了大量的精力去发展阴离子物种的非生物受体,进而设计出了一些能够识别与检测各种各样重要阴离子的探针。由于氢键的指向性和饱和性,所以在众多结合阴离子的作用力中,氢键作用是最常被采用的一种作用力。 许多氢键供体如酰胺[3-4]、硫脲[5-6]、酚羟基[7-8]及吡咯大环[9-10]化合物等已成功应用于阴离子识别研究中,而含酚羟基的希夫碱类化合物常被用于阳离子识别体系中[11-13],以其作为阴离子识别位点的研究相对较少。
一般地,比色和/或荧光阴离子探针至少要有两部分组成:阴离子受体和信号团部分。通常,这两部分是以共价键和非共价键两种结合方式连接起来。最常采用的信号团为荧光团,因为荧光探针在较低浓度的分析物下具有潜在的高灵敏度[14-15]。荧光探针主要是基于光诱导电子/能量转移(PET),光诱导电荷转移(PCT),单体激基缔合物/复合物的形成,刚性效应等。在这些发光机理中,光诱导电荷转移受到研究者的广泛青睐。基于该机理(PCT)的荧光探针在识别过程中表现出荧光光谱的比率变化。与在单一波长范围产生荧光强度的变化探针[16-18]相比,这类比率荧光探针具有更高的灵敏度和准确度。对仅仅荧光增强或减弱型的探针而言,在实际应用中会受到探针自身浓度、光源强度波动及仪器敏感性等因素的影响,降低了测定的准确度。而比率荧光探针的优点则是通过两个不同波长下荧光的比值变化,把这些影响测定准确性的因素消除掉,这样就扩大了这类探针的应用范围。令人遗憾的是,目前对于比率荧光阴离子探针的报道却非常少。
在本文中我们采用信号体受体直接耦合法设计合成了一个含酚羟基的Schiff碱型受体1,并详细研究了当加入AcO-、H2PO4-、F-后,探针分子的紫外可见光谱和荧光光谱的响应。通过受体1上的OH和NH作为阴离子结合点与吸电子基团(-NO2)共轭连接,吸电子基不仅能提高结合点酸性,增强其与阴离子的作用能力,而且增强分子内电荷转移的推-拉特征,增大分子内电荷转移程度。实验表明探针1对于无机生物阴离子能够作为便利的比色和比率荧光分子探针。

Scheme 1 Synthetic routes for the receptor 1
1 实验部分
1.1 仪器与试剂
所用仪器:TU-1810型紫外-可见分光光度计(北京普析通用仪器有限责任公司);F96荧光分光光度计(上海棱光技术有限公司);Mercury Vx300核磁共振仪(300MHz)。
所用阴离子均为四丁基铵盐,均购自Alfa Aesar公司;所用试剂均为分析纯试剂。
1.2 实验方法
除特别说明外,所有的实验均是在298.2±0.1 K下进行。 首先,配制化合物 1(0.5 mmol·L-1,DMSO)和各种阴离子(10 mmol·L-1,DMSO)的溶液并储存于干燥的气氛中。然后,取适当体积的所配溶液于比色皿中,适当稀释后用于所有光谱研究。1H NMR滴定实验:配制主体 1(10 mmol·L-1,DMSO-d6)的溶液,在不存在和存在不同量氟离子的情况下,测定其1H NMR谱图。
1.3 受体分子1的合成
称取4-甲基-1-羟基二苯甲酮[19]848 mg(4 mmol)置于50 mL圆底烧瓶中,加入15 mL无水甲醇,缓慢加热至全部溶解,得到透明溶液,向该溶液中加入4-硝基苯肼612 mg(4 mmol)的甲醇溶液,加热回流2 h,停止加热,冷却至室温,旋除有机溶剂,空气干燥。 过柱提纯(淋洗剂:二氯甲烷∶甲醇=100∶1,V/V),收集第二带,旋除有机溶剂,真空干燥,得产品受体1 为 805 mg,产率 58%。1H NMR(CDCl3,300 MHz)δ:11.52(s,1H,OH),8.18(s,1H,NH),8.15(s,1H,ArH),7.656(t,J=24.9 Hz,4H,ArH),7.36(d,J=7.8 Hz,2H,ArH),7.09(d,J=10.2 Hz,1H,ArH),6.97(d,J=8.4 Hz,1H,ArH),6.90(d,J=9.3 Hz,2H,ArH),6.51(s,1H,ArH),2.14(s,3H,CH3);ESI-mass:C20H17N3O3,m/z=346.16[M]-;EA(%):C20H17N3O3(%)Calc for:C,69.15; H,4.93,N,12.10; Found:C,69.50;H,4.69;N,12.48。
2 结果与讨论
2.1 主客体作用的裸眼分析
进行裸眼检验,一般来说,需要受体分子中含有生色基团(比如:-NO2),通过观察受体溶液的颜色变化来鉴定阴离子[20-23]。 向受体 1(50 μmol·L-1,DMSO)溶液中分别加入12倍量的不同阴离子,导致受体1的颜色变化情况见图1。很容易观察到,当加入相同量的 AcO-,H2PO4-或 F-后,受体 1(50 μmol·L-1,DMSO)溶液便立刻由淡黄色变成了紫红色。而加入大量的Cl-,Br-或I-等离子不会使受体1溶液的颜色发生明显变化,从而实现了对AcO-,H2PO4-,F-这三种阴离子的裸眼识别。

图1 加入12倍量的不同阴离子导致受体1(50 μmol·L-1,DMSO)溶液的颜色变化Fig.1 Color changes observed in receptor 1(50 μmol·L-1,DMSO)in the presence of 12 equiv.of different anions
2.2 主客体作用的紫外-可见光谱的分析
用紫外-可见滴定的方法研究了不同阴离子与受体 1的结合能力,在受体 1(20 μmol·L-1)的 DMSO溶液中分别慢慢加入F-、AcO-、H2PO4-的紫外吸收光谱变化曲线见图2,从图中可以明显地看出,受体1的最大吸收峰处于 423 nm,加入 F-、AcO-、H2PO4-(四丁基铵盐)后,该吸收峰逐渐减弱,同时在540 nm处出现了新的吸收峰,且吸光度随F-、AcO-、H2PO4-浓度的增大而增大。主体分子的吸收峰出现红移现象,主要是因为苯环上的硝基是很强的吸电子基团,羟基是较强的供电子基团,在主客体之间快速有效地转移电子,使得阴离子配合物的光谱向长波方向移动[24-25]。同时,在370 nm、454 nm处可以观察到两个明晰的等吸收点,表明受体1与F-、AcO-、形成了具有确定组成的阴离子配合物[26]。然而,向受体1(20 μmol·L-1)的 DMSO 溶液中分别慢慢加入 12倍量的其它被研究的卤素阴离子(Cl-、Br-、I-)的四丁基铵盐,对受体1的吸收光谱影响非常小,甚至可以忽略,显示出受体1对F-、AcO-、H2PO4-的较高的识别能力,受体1与各阴离子作用的吸收光谱图见图3。

图2 受体分子1(20 μmol·L-1)的DMSO溶液中加入F-(a)、AcO-(b)和H2PO4-(c)的紫外吸收光谱图及其在490nm处的吸光度值拟合曲线Fig.2 UV-Vis spectra and the plot of the UV-Vis absorbance at 490 nm of 1(20 μmol·L-1)in DMSO after the addition of F-(a),AcO-(b)and H2PO4-(c)
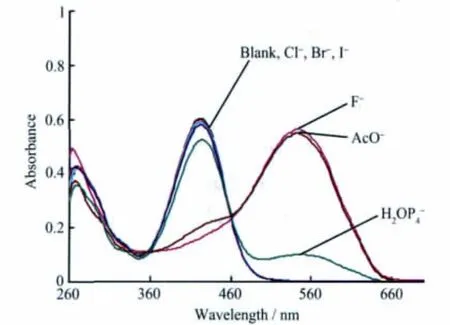
图3 受体 1(20 μmol·L-1)的 DMSO溶液中加入 60倍量的 F-、Cl-、Br-、I-、AcO-、H2PO4-的紫外吸收光谱图Fig.3 UV-Vis spectra of receptor 1(20 μmol·L-1)in DMSO in the presence of 60 equiv.of F-,Cl-,Br-,I-,AcO-and H2PO4-
2.3 主客体作用荧光光谱的分析
为了进一步探讨受体1与阴离子的相互作用,我们进行了荧光滴定实验。图4(a)中给出了向受体1(20 μmol·L-1)的 DMSO 溶液中慢慢滴加 F-后的荧光发射光谱的变化图。以波长为365 nm的光作为激发波长,自由的受体分子在波长540 nm处有一个弱的发射峰。当F-慢慢滴加后,在416 nm产生一个新的荧光发射带,且荧光强度随着F-浓度的增大而增强。与此同时,而受体1在540 nm的荧光发射峰的强度逐渐降低直至消失。像这种阴离子导致的主体荧光光谱的比率变化可以用光诱导的电荷转移发光机理来解释。在探针分子1中,羟基作为一个电子供体直接连接在荧光团(二苯甲酮)上,而该电子供体又同时作为阴离子受体的一部分。当接受体与阴离子作用后,对荧光团的推拉电子作用产生影响,从而导致荧光光谱的比率变化。有意思的是,加入阴离子后,紫外可见光谱发生了明显的红移变化而荧光光谱发生了蓝移变化。在已有的文献中,也很少见到像这种变化现象。一般来说,荧光光谱波长的移动应该和吸收光谱波长的移动方向是一致的,向长波长方向移动或者向短波长方向移动。可能的原因是荧光光谱的蓝移变化是由受体激发态的电荷转移性质变化引起的。 在基态和激发态下,阴离子对受体1的稳定性影响是不同的。所以受体1才呈现出了荧光光谱的蓝移变化,而紫外可见光谱的红移变化[27]。
图 4(b)表示的是受体 1(20 μmol·L-1)的 DMSO溶液中分别加入10倍量阴离子 (AcO-、H2PO4-、F-、Cl-、Br-、I-)的荧光光谱变化情况。从图中可以看出,AcO-和H2PO4-的引入产生了与F-相似的荧光光谱变化,而加入Cl-、Br-和I-对主体的发射光谱基本没有影响。
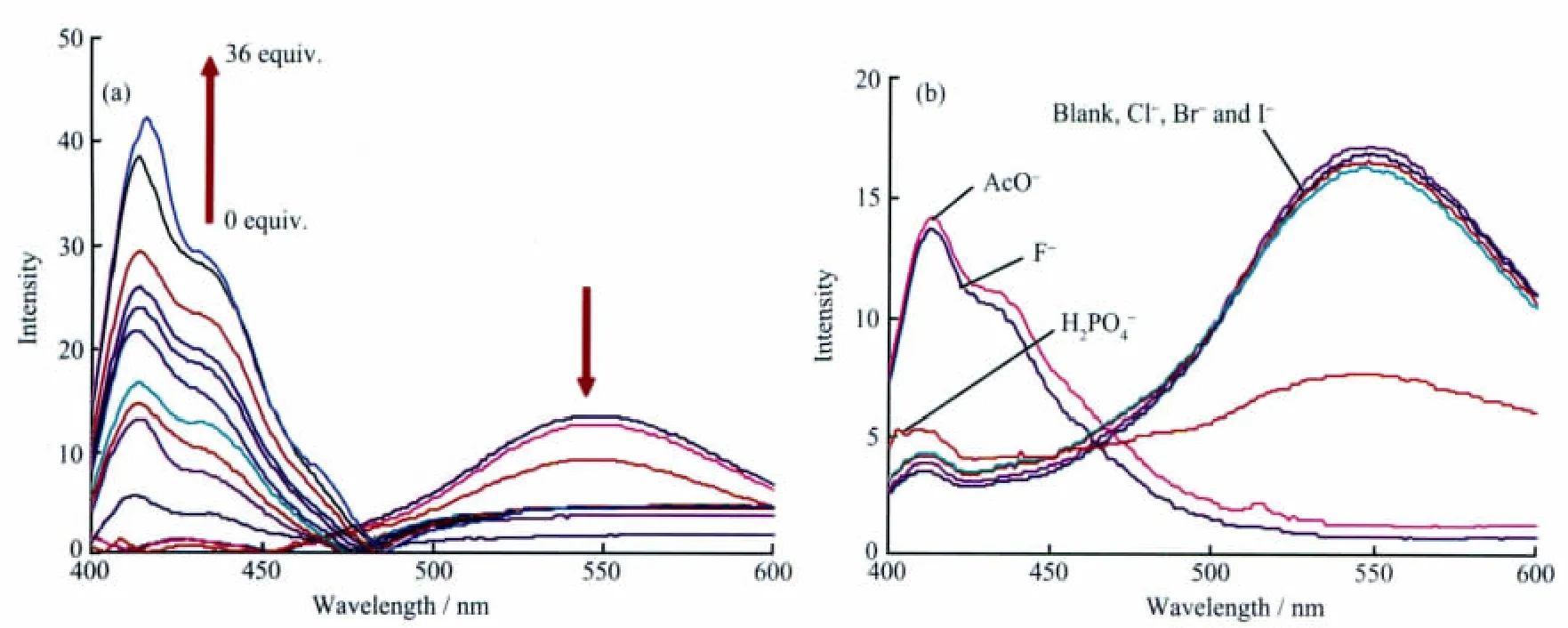
图4 (a)受体分子1的DMSO溶液中加入F-的荧光发射光谱图,(b)受体分子1的DMSO溶液中加入 10 倍量的 AcO-、H2PO4-、F-、Cl-、Br-and I-的荧光发射光谱图Fig.4 (a)Fluorescent spectra of 1(20 μmol·L-1)in DMSO after the addition of F-,(b)Fluorescent spectra of 1(20 μmol·L-1)in DMSO in the presence of 10 equiv.of AcO-,F-,H2PO4-,Cl-,Br-and I-
2.4 主客体结合常数的测定
在紫外-可见光谱滴定分析的基础上,我们对新产生的吸收峰的吸光度值进行了拟合,吸光度值对阴离子浓度的曲线呈‘S’型,这与主客体之间的计量比为2∶1的文献报道的结果一致[28]。Job′s曲线指示了一个受体1和F-的2∶1配合物的形成(见图5)。因此,本文采用如下主客体计量比为2∶1型的计算公式进行计算[29]。
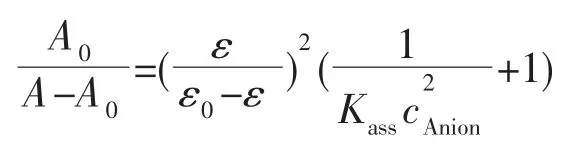
式中A0和A分别表示的是未与阴离子作用和作用时受体分子1的吸光度值;ε0和ε分别表示的是对应于A0和A时受体1的摩尔吸光率;Kass表示的是主客体之间的结合常数;canion表示的是阴离子的滴定浓度。以A0/(A-A0)对canion-2作图得到在540 nm处吸光度值的拟合曲线见图2中小图所示的拟合结果,并计算出受体1与阴离子之间的结合常数列于表1。拟合得到的较高的相关系数也表明受体1与阴离子之间的化学计量比的确为2∶1。从表1可知,受体1对阴离子识别能力的大小顺序为:AcO->F->受体 1 对 AcO-的选择性最高,主要与AcO-离子的碱性较强以及主客体之间的空间构型互补有关。
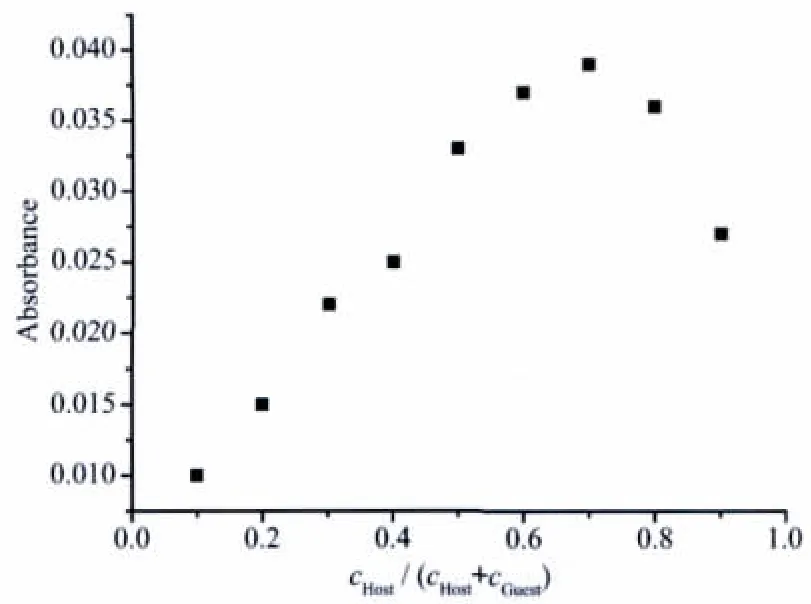
图5 540 nm处受体1与F-结合的Job′s曲线Fig.5 Job′s plot of receptor 1 and F-at 540nm
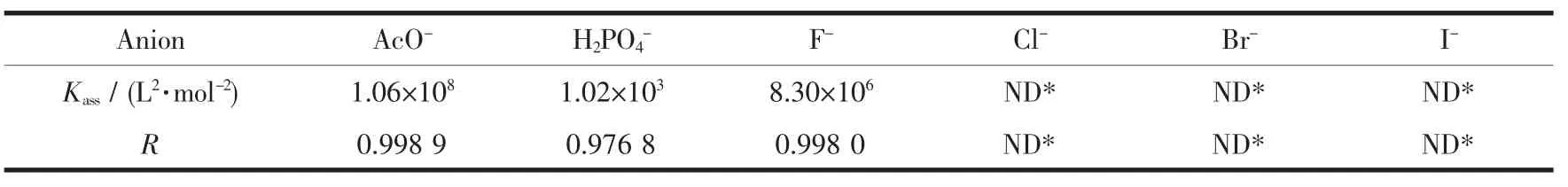
表1 受体1在DMSO溶液中与各阴离子之间的结合常数及相关系数Table 1 Association constants and correlation coefficient for various anions toward receptor 1 in DMSO,respectively
2.5 1H NMR滴定分析
为进一步阐明受体分子与阴离子间的氢键作用本质,进行了1H NMR滴定实验[30]。以CDCl3为溶剂,受体1的OH和NH质子化学位移分别为11.7 ppm和8.2 ppm。当加入不同浓度的F-的四丁基铵盐的CDCl3溶液时,OH质子峰位移向低场方向移动,并且峰形变宽,积分面积减小直至消失,这是因为具有强碱性的氟离子与受体分子作用后,识别位点上发生了去质子化。另外,NH质子峰积分面积明显地减小,这表明OH质子和NH质子均参与了与阴离子的作用。由于OH质子的酸性较强具有形成氢键的能力比NH质子强,在与氟离子作用过程中失去了质子发生了去质子化。另外,由于静电效应的影响,苯环上的电子密度增加,苯环上芳香质子的化学位移向高场发生了微小移动,见图6。Scheme 2给出了受体1与F-可能的结合方式。
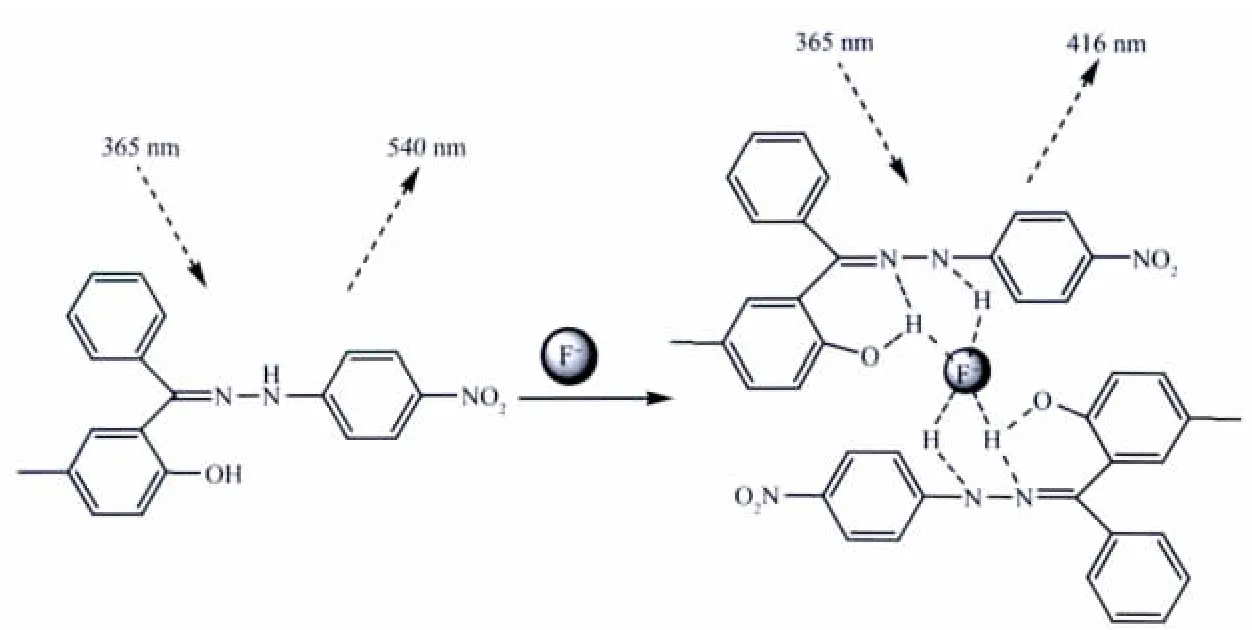
Scheme 2 Proposed binding mode of receptor 1 and F-
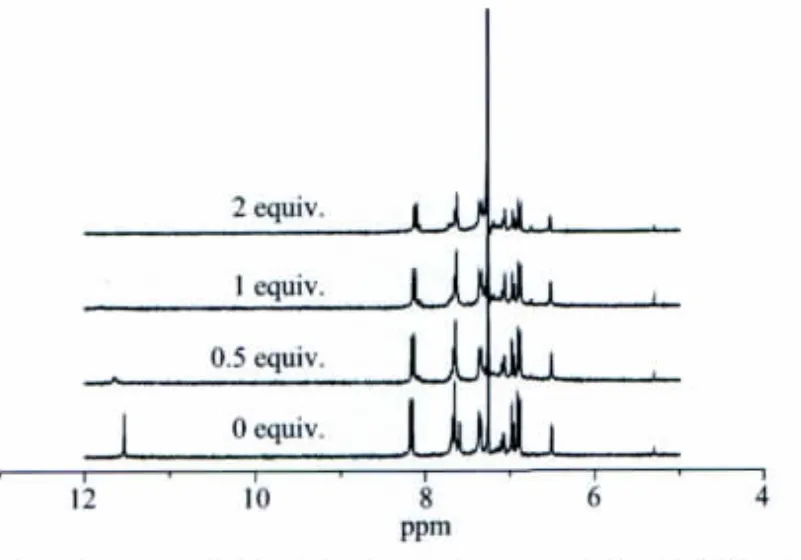
图 6 在 CDCl3溶液中受体 1(0.01 mol·L-1)在 F-存在时的1H NMR谱Fig.6 1H NMR spectra of receptor 1 in the absence and presence of F-in CDCl3
3 结 论
综上所述,我们成功地设计并合成了基于分子内电荷转移机制的阴离子传感器4-甲基-1-羟基二苯甲酮-4-硝基苯腙,考察了其对Cl-、Br-、I-等阴离子的识别作用, 发现F-的引入使受体溶液由黄色变为紫红色,实现了对这3种阴离子的裸眼识别, 受体 1的紫外光谱在540 nm处出现了新的吸收峰,于370 nm、454 nm处观察到明晰的等吸收点,以及拟合曲线均表明了受体1与形成了稳定的2∶1型阴离子配合物。荧光滴定进一步证实了受体1对具有较好的选择性,并通过1H NMR滴定实验验证了其与阴离子的配合机制。受体1这种特殊的比率荧光特性拓展了其在生命科学领域的应用价值。
[1]Beer P D,Gale P A.Angew.Chem.Int.Ed.,2001,40(3):486-516
[2]Martnez-Mez R,Sancenn F.Chem.Rev.,2003,103(11):4419-4476
[3]Gale P A.Acc.Chem.Res.,2006,39(7):465-475
[4]Kang S O,Begum R A,Bowman-James K.Angew.Chem.Int.Ed.,2006,45(47):7882-7894
[5]Gunnlaugsson T,Kruger P E,Jensen P,et al.J.Org.Chem.,2005,70:10875-10878
[6]Amendola V,Esteban-Gmez D,Fabbrizzi L,et al.Acc.Chem.Res.,2006,39(5):343-353
[7]Gong W T,Hiratani K,Lee S S.Tetrahedron,2008,64(49):11007-11011
[8]Jose D A,Kar P,Koley D,et al.Inorg.Chem.,2007,46(14):5576-5584
[9]Anzenbacher J P,Nishiyabu R,Palacios M A.Coord.Chem.Rev.,2006,250(23/24):2929-2938
[10]Chen C L,Chen Y H,Chen C Y,et al.Org.Lett.,2006,8(22):5053-5056
[11]Xiang Y,Tong A,Jin P,et al.Org.Lett.,2006,8:2863-2866
[12]Holbach M,Weck M.J.Org.Chem.,2006,71:1825-1836
[13]WU Fang-Ying(吴芳英),TAN Xiao-Fang(谭晓芳),CAI Hong-Hui(蔡红辉),et al.Acta Chim.Sin.(Huaxue Xuebao),2005,63:307-311
[14]Gunnlaugsson T,Glynn M,Tocci(née Hussey)G M,et al.Coord.Chem.Rev.,2006,250:3094-3117
[15]Martinez-Manez R,Sancenon F.Chem.Rev.,2003,103:4419-4476
[16]Ghosh Yang X K,Sarkar A R,Masanta G.Tetrahedron Lett.,2007,48:8725-8729
[17]Shen R,Pan X B,Wang H F,et al.Inorg.Chem.Commun.,2008,11:318-322
[18]Ye S J,Bai Q,Wang X Q.J.Fluoresc.,2007,17:81-87
[19]Atkins R,Brewer G,Kokot E,et al.Inorg.Chem.,1985,24:127-134
[20]Chawla H M,Shrivastava R,Sahu S N.New J.Chem.,2008,32:1999-2005
[21]Babu J N,Bhalla V,Kumar M,et al.New J.Chem.,2009,33:675-681
[22]Lowe A J,Dyson G A,Pfeffer F M.Eur.J.Org.Chem.,2008:1559-1567
[23]Hijji Y M,Bararea B,Kennedy A P,et al.Sens.Actuators,B,2009,136(2):297-302
[24]Christopher B B,Bruno A,Andrew C T.J.Am.Chem.Soc.,1999,121:10438-10439
[25]Santis G D,Fabbrizzi L,Licchelli M,Poggi A,et al.Angew.Chem.Int.Ed.,1996,35(2):202-204
[26]YU Ming(郁铭),LIN Hai(林海),LIN Hua-Kuan(林华宽).Chem.J.Chinese Universities(Gaodeng Xuexiao Huaxue Xuebao),2007,28(1):83-86
[27]Shao J,Lin H,Lin K.Talanta,2008,77:273-277
[28]Kubo Y,Kato M,Misawa Y,et al.Tetrahedron Lett.,2004,45:3769-3773
[29]Pérez-Casas C,Yatsimirsky A K.J.Org.Chem.,2008,7(6):2275-2284
[30]Bourson J,Pouget J,Valeur B J.Phys.Chem.,1993,97:4552-4556
A Colorimetric and Ratiometric Fluorescent Probes Based on Intramolecular Charge Transfer
LIU Ge*,1SHAO Jie2
(1Department of Chemistry,Chifeng University,Chifeng,Inner Mongolia 024000,China)(2Department of Chemistry and Materials Science,Nanjing Forestry University,Nanjing 210037,China)
A new colorimetric and ratiometric fluorescent anion receptor based on 4-methyl-1-hydroxybenzophenone p-nitrophenylhydrazone 1,was designed and synthesized.In the compound 1,the phenolic hydroxyl moiety and the hydrazone moiety are anion binding sites and the nitrobenzene moiety is a signaling group.Upon addition of AcO-,H2PO4-,F-,the color of receptor 1 in DMSO solutions changed from yellow to purple,while no obvious color changes were observed on addition of the other anions tested.Accordingly,the sensor 1 could sense visually AcO-,H2PO4-,F-without resorting to any spectroscopic instrumentation.The binding properties of the receptor 1 with anions such as AcO-,H2PO4-,F-,Cl-,Br-,I-were investigated by UV-Vis and Fluorescent titrations.The1H NMR titrations further looked into the nature of host-guest interactions.
anion sensor;intramolecular charge transfer;ratiometric;fluorescence;colorimetric
O654.2
:A
:1001-4861(2011)04-0731-06
2010-10-08。收修改稿日期:2010-11-27。
内蒙古自治区高等学校自然科学研究项目基金(No.NG09168)资助项目。
*通讯联系人。 E-mail:liu_ge2008@163.com
