CuCr2O4/ TiO2复合薄膜电极对染料敏化太阳能电池光电性能的影响
2011-09-26周红茹,胡志强,康姣
周 红 茹, 胡 志 强, 康 姣
( 大连工业大学 化工与材料学院, 辽宁 大连 116034 )
0 引 言
20世纪80年代以来,瑞士洛桑高等工业学院M. Grätzel教授的研究小组一直致力于纳米多孔TiO2薄膜电极电池的研究,这种电池被称为染料敏化太阳能电池(DSSC),并在1991年取得突破性进展,其光电转换效率可达7.1%[1];1993年,再次报道光电转换效率达到10%[2];1998年,进一步研究出全固态Grätzel电池[3],单色光转换效率达到33%;2001年,电池效率达到10.4%[4],其转换效率可与非晶硅太阳能电池相媲美。DSSC以其廉价的原材料、简单的制作工艺、性能稳定、衰减少等特点引起了全世界人们的关注。
DSSC的核心部分是由纳米TiO2多孔半导体薄膜组成的。TiO2是一种价格便宜、用途广泛、无毒、稳定且抗腐蚀性能好的物质。然而,TiO2的局限性是有一个很大的禁带宽度(锐钛矿,3.2 eV;金红石,3.0 eV),所以只能吸收紫外线(紫外线在可见光中的含量只有5%),因此为了加强二氧化钛对可见光的吸收,人们做了大量的研究。Kyung Hyun Ko等[5]报道了利用金属Al、W掺杂TiO2阳极,产生光谱红移来提高染料敏化太阳能电池光电转换效率[6]。考虑多元氧化物半导体的多样性和性质易调整的特点,本研究采用多元氧化物铬酸铜(CuCr2O4)掺杂到TiO2粉体中进行复合改性。CuCr2O4是一种尖晶石型结构,且禁带宽度较小的P型半导体[7],这种粉体具有稳定、耐高温和较好的光催化性等优点。由于两种半导体的导带、价带、禁带宽度不同而产生交叠,扩展了TiO2的光谱响应、提高TiO2薄膜电极的吸光度,因此,它对研究CuCr2O4/TiO2复合薄膜的光电转换具有重大的意义。
1 实 验
1.1 原料与试剂
Cu(NO3)2·3H2O(分析纯),Cr(NO3)3·9H2O(分析纯),氨水(NH4OH),无水乙醇(分析纯),PEG400(化学纯,平均相对分子质量400),TiO2粉体(P25)。
1.2 CuCr2O4/TiO2复合薄膜电极的制备[8]
将Cr(NO3)3·9H2O和Cu(NO3)2·3H2O按n(Cr3+)∶n(Cu2+)=1∶2比例溶于醇水中,完全溶解后加入聚乙二醇(400),在40 ℃水浴搅拌并加入适量氨水调节pH,制得复合氢氧化物沉淀。将前驱物沉淀经过水洗、乙醇中回流、抽滤、干燥并研磨,在1 000 ℃焙烧2 h制得试样。
分别取质量分数不同的CuCr2O4粉体加入到0.7 g TiO2粉体中,加入去离子水2 mL,乙酸0.5 mL,研磨10 min;加入去离子水1 mL,研磨5 min;加入OP乳化剂2滴,研磨10 min;最后加入去离子水0.5 mL,研磨15 min,得到印刷料浆。采用丝网印刷技术在镀有致密TiO2薄膜的掺杂氟的SnO2导电玻璃(FTO)上制备复合薄膜,薄膜先室温干燥后于80 ℃烘箱中干燥30 min,最后放入马弗炉中500 ℃下保温30 min,制得CuCr2O4掺杂的质量分数分别为0、1%、2%、3%、5% 的CuCr2O4/TiO2复合薄膜,待用。
1.3 染料敏化太阳能电池的组装
通过添加CuCr2O4粉体和丝网印刷的层数改变TiO2多孔膜的厚度,分别制得3~12层的复合薄膜电极,将制备的CuCr2O4/TiO2复合薄膜电极作为光阳极,浸泡在N719染料中8~12 h,与制备好的铂对电极进行组装并测试。
1.4 分析和测试
采用日本理学D/MAX-3B型X射线衍射仪(Cu Kα辐射,λ=0.154 0 nm,管压40.0 kV,管电流50 mA,连续扫描,扫描速度为6°/min)对复合薄膜进行物相和晶型分析;数显测厚指示表测试复合薄膜的厚度;用SOLAR SIMULATOR SS50 ABA型光电转换测定仪(AM 1.5,100 mW/cm2)测试电池的短路电流(Isc)、开路电压(Voc)、最大输出功率(Pm)、填充因子(FF)和光电转换效率(η)。
2 结果与讨论
2.1 X射线衍射分析
图1为500 ℃热处理后CuCr2O4/TiO2复合薄膜的XRD谱图。从图1可以看出,该衍射峰图谱与锐钛矿相TiO2标准卡片(PDF40-477)相符。图谱中观察到的A(101),A(103),A(200),A(105),A(211),A(004)等都为锐钛矿,其中R(110)为金红石。该衍射峰图谱对应TiO2三强线的d值分别为3.52,1.89和1.67。说明当CuCr2O4粉体掺杂到TiO2粉体后,复合薄膜的晶型没有发生改变,仍然为锐钛矿相结构。
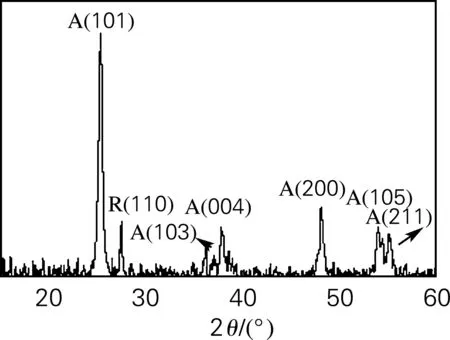
图1 500 ℃热处理后CuCr2O4/TiO2复合薄膜的XRD谱图
2.2 最佳膜厚的选择
图2(a)为薄膜厚度对电池的电流密度的影响。从图中可以看出,复合薄膜的厚度为5~25 μm时,电流密度随着薄膜厚度的增加先增大后减小。笔者认为光电流的增大是因为薄膜厚度增大时吸附更多的染料分子,从而产生更多的光生电子;然而,当膜厚增加到大于20 μm后,氧化还原电子在TiO2三维网络结构中的传递将变得困难。因此,只有一定数目的染料分子能被I-还原,同时光电流和效率也受到限制。制备CuCr2O4粉体时加入PEG,在烧结的过程中会产生孔洞,所以导致TiO2多孔膜的孔径和孔隙率也随之增大,单位面积膜内的TiO2质量减小,于是内表面积减小。因此,只有具有更大的膜厚才能增大TiO2薄膜的内比表面积。
图2(b)为薄膜厚度对电池的开路电压的影响。从图中可以看出,薄膜厚度从5 μm增加到20 μm时,电池的开路电压达到最高值,当厚度继续增大时,开路电压开始下降。这是因为电池的开路电压大小取决于电池的电流密度和内阻两个因素。总的来说。随着薄膜膜厚的增大,吸收的染料分子更多,光电流增大,但热处理后会产生更多的裂缝,影响了电子的传输,增大了注入电子在传输过程中与纳米粒子陷阱及表面态复合几率,造成内阻增大。电池的开路电压受电流密度增大的影响而增大,虽然内阻增大,但对开路电压的影响较小,所以整体来说,导致电池的开路电压增大。当薄膜厚度大于20 μm时,电池的开路电压主要取决于电池的内阻,所以整体来说,当薄膜太厚时,电池的开路电压下降。综上所述,实验中得出最佳膜厚为20 μm左右。

图2 薄膜对电流密度和开路电压的影响
2.3 电池性能的测试
在测试电池性能的过程中,当太阳光照射在CuCr2O4/TiO2复合薄膜电极时,液体电解质对失去电子的CuCr2O4提供电子使其还原,与此同时,电解质中失去电子将从外电路进入到对电极的电子得到补充,这样就是整个电池的一个循环过程。
从图3和表1可以看出CuCr2O4粉体的掺杂量对薄膜的光电性能产生很大的影响,光电性能会随着CuCr2O4的掺杂量的增加先增大后减小,说明CuCr2O4粉体是一种有效的窄禁带半导体光电材料。与纯TiO2薄膜电极(图3d)相比,当CuCr2O4的掺杂量为1%(图3b)时,复合薄膜的电流密度和光电转化效率分别提高了25%和16%。当掺杂量为2%时,电池电流密度和开路电压均有较大增加,分别为从5.42 到7.33 mA/cm2,从0.72到0.75 V。这种现象的原因是多方面的,首先单分子层染料的增大提高电极的光量子率,薄膜结构的改善促进光生电子的导出,提高光生电流。其次是两种半导体的导带、价带位置不一致而发生交叠,降低了电子-空穴的复合几率[9]。激发到TiO2价带的电子很容易注入CuCr2O4导带上,从而增加了电极传递的密度。激发后价带产生的空穴电极/溶液界面传递和电解质中的碘离子发生氧化反应,这样就提高了光生载流子的分离效率,促进了TiO2电子空穴分离,此时的光电转化效率为6.5%,比纯TiO2薄膜电极的光电转化效率提高了22.6%。说明此时的CuCr2O4粉体与TiO2粉体复合较好,形成良好的多孔结构。

图3 TiO2薄膜电极和CuCr2O4/TiO2复合薄膜电极的伏安特性曲线

表1 TiO2薄膜电极和CuCr2O4/TiO2复合薄膜电极的光电性能参数
根据填充因子计算公式FF=Pm/(Jsc·Voc)可知,填充因子的大小受电流密度和开路电压共同影响,虽然掺杂后对开路电压的增幅不大,但由于电流密度增大明显,因此填充因子也有较大的提高。
当CuCr2O4粉体掺杂量提高到3%(图3c)、5%(图3e)时,此时的光电转化效率与纯TiO2电极相比有一定提高,但是与掺杂2%的电池性能相比,各项性能开始下降,但均好于纯TiO2薄膜电极的光电转化效率。也就是说随着掺杂量的加大,会导致TiO2颗粒间的平均距离增大,阻碍了载流子的扩散,电流传输效率下降,电子-空穴几率变大,导致输出电流减小。因此要获得较高的电池性能,CuCr2O4粉体的掺杂量是非常重要的,当掺杂的质量分数为2%时,电池的光电性能最佳。
3 结 论
采用丝网印刷的方式制备CuCr2O4/TiO2复合薄膜电极,掺杂CuCr2O4粉体后对TiO2晶型没有影响,仍然为锐钛矿相结构。
与纯TiO2薄膜电极相比,CuCr2O4/TiO2复合薄膜电极可以有效提高电池性能。当CuCr2O4粉体的掺杂的质量分数为2%时,电池的电流密度为0.73 mA/cm2,开路电压为0.75 V,填充因子为0.53,光电转化效率达到了6.5%。
[1] O’REGAN B, GRATZEL M. A low-cost, high-effieiency solar cell based on dye-sensitized colloidal TiO2films[J]. Nature, 1991, 353:737-740.
[2] NAZEERUDDIN M K, KAY A, RODICIO R, et al. Conversion of light to electricity by cis-X-bis (2,2′-bipyridyl-4,4′-dicarboxyiate) ruthenium (Ⅱ) charge-transfer sensitizers (X=Cl-, Br-, I-, CN-, and SCN-) on nanocrystalline TiO2electrodes[J]. Journal of the American Chemical Society, 1993, 115(14):6382-6390.
[3] BACH U, LUPO D, COMTE P, et al. Solid-state dye-sensitized mesoporous TiO2solar cells with high photo-to-electron conversion efficiencies[J]. Nature, 1998, 395:583-585.
[4] GRATZEL M. Photoelectrochemical cells[J]. Nature, 2001, 414:338-344.
[5] KO K H, LEE Y C, JUNG Y J. Enhanced efficiency of dye-sensitized TiO2solar cells (DSSC) by doping of metal ions[J]. Journal of Colloid and Interface Science, 2005, 283(2):482-487.
[6] KITIYANAN A, YOSHIKAWA S. The use of ZrO2mixed TiO2nanostructures as efficient dye-sensitized solar cells electrodes[J]. Materials Letters, 2005, 59(29/30):4038-4040.
[7] YAN Jianhui, ZHANG Li, YANG Haihua, et al. CuCr2O4/TiO2heterojunction for photocatalytic H2evolution under simulated sunlight irradiation[J].Solar Energy, 2009, 83(9):1534-1539.
[8] 高岩,胡志强,李国,等. 温制备柔性染料敏化太阳电池TiO2薄膜电极[J]. 电子元件与材料, 2007, 26(7):4-6.
[9] 姜妍彦,李景刚,宁桂玲. 尖晶石型CuAl2O4纳米分体的制备及其可见光催化性能[J]. 硅酸盐学报, 2006, 34(9):1084-1087.
