唇裂防护膏微生物限度检查法研究
2011-09-17任安民杨晓莉周志云
任安民,杨晓莉,周志云
(陕西省食品药品检验所,陕西 西安 710061)
唇裂防护膏属于软膏剂类,是将药物均匀分散于蜂蜡、凡士林、固体石蜡、液体石蜡等油脂性基质中形成的油包水型制剂,供口唇涂抹以产生局部或全身性作用。唇裂防护膏是第四军医大学口腔医院自行研制的外用化妆品类软膏制剂,供边疆高原战士预防口唇干裂之用。根据2010年版《中国药典(二部)》[1]要求,软膏剂应进行微生物限度检查,规定细菌数不得过100/g、霉菌和酵母菌数不得过100/g;不得检出金黄色葡萄球菌、铜绿假单胞菌。但目前对化妆品类软膏剂尚无检查方法学验证与标准规定,为使检测结果科学、准确,检测前应进行方法学验证。对于软膏剂类的微生物限度检查,需要解决两个问题,一是制备供试液时对剂型的乳化[2],二是人为加入已知菌的检出回收率。笔者对此进行了研究,现报道如下。
1 实验材料
隔水式培养箱(重庆万达WGP-600.200.11382);真菌培养箱(上海一恒LRH-250-1786X);隔水式培养箱(重庆万达WGP-600.200.11381)。环境条件为洁净度10 000级下局部100级的单向流空气区域。试验菌种有枯草芽孢杆菌[CMCC(B)63501],金黄色葡萄球菌[CMCC(B)26003],大肠埃希菌[CMCC(B)44102],铜绿假单胞菌[CMCC(B)63501],黑曲霉[CMCC(F)98003]白色念珠菌[CMCC(F)98001],均由中国医学细菌保藏中心提供。试药试剂均由北京三药科技开发公司生产,营养琼脂培养基(批号为080922),改良马丁液体培养基(批号为0810203),营养肉汤培养基(批号为080624),玫瑰红钠琼脂培养基(批号为0810233),胆盐乳糖增菌液(批号为0805282),均按规定进行适应性检查;稀释液为pH=7.0的氯化钠-蛋白胨缓冲液[按2010年版《中国药典(二部)》方法配制];乳化剂(5 g司盘-80和5 g吐温-80研磨混匀,加稀释液至100 mL);乳化中和剂(取5 g司盘-80、5 g吐温-80混匀,加入3 g卵磷脂,充分研磨至乳白色乳膏状,少量多次研磨,加入蒸馏水稀释至100 mL)。
2 方法与结果
2.1 方法验证试验[3-4]
2.1.1 试验菌液制备
接种大肠埃希菌、金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌至营养肉汤培养基中,于(33±2)℃培养24 h;接种白色念珠菌至改良马丁培养基中,于(25±2)℃培养48 h;接种黑曲霉菌至改良马丁琼脂斜面,于(25±2)℃培养7 d(用0.9%无菌氯化钠溶液洗脱孢子,标准管比浊)。以上培养物均用0.9%无菌氯化钠溶液制成每1 mL含50~100 CFU的菌悬液备用。
2.1.2 供试液制备
取供试品5 g,加乳化剂100 mL,45℃水浴振摇,制备成1∶20的A供试液。取供试品5 g,加中和剂100 mL,45℃水浴振摇,制备成1∶20的B供试液。
2.1.3 预试验方法
试验组:取A供试液、B供试液加入大肠埃希菌、金黄色葡萄球菌50~100 CFU,采用平皿法进行细菌数测定。结果见表1。
对照组:按A供试液、B供试液制备方法,不加供试品,制备对照液,同时加入试验组试验菌50~100 CFU,采用平皿法测定乳化剂与中和剂对细菌回收率的影响。
供试品组:取A供试液、B供试液,不加试验菌,采用平皿法进行供试品本身细菌数测定。
菌液组:测定所加的试验菌数。
2.1.4 预试验结果
结果见表1。可见,A供试液、B供试液对照组回收率均大于70%,A供试液试验组大肠埃希菌与金黄色葡萄球菌的回收率均小于B供试液试验组。因此,可选择B供试液中和剂组进行方法学验证的细菌数测定。
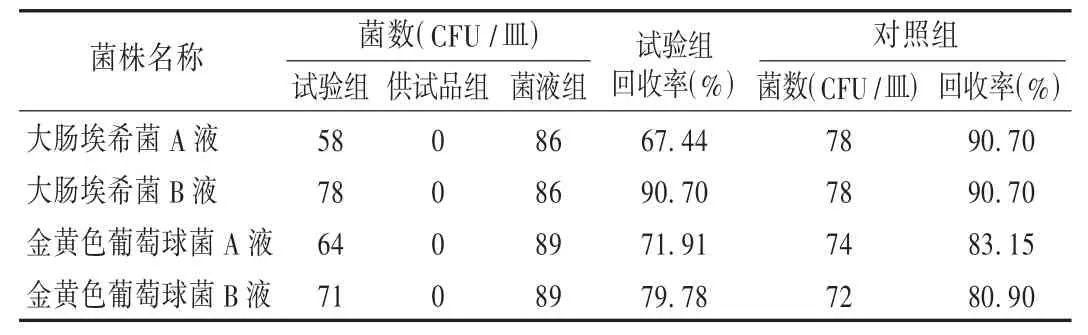
表1 方法预试验各组菌落均数测定结果
2.2 方法学验证
2.2.1 中和剂平皿法菌数回收率测定
取供试品5 g,加中和剂100 mL,45℃水浴振摇,制备成1∶20的供试液。分别加入各试验菌液,采用平皿法进行菌数回收率测定。试验组取1∶20的供试液1 mL和试验菌50~100 CFU,采用平皿法进行细菌、霉菌和酵母菌数测定。供试品组按试验组方法,不加试验菌,测定供试品的本底菌数。菌液组测定所加的试验菌数。对照组取中和剂1 mL和试验菌50~100 CFU,测定中和剂回收率。各组均进行重复试验3次。结果见表2。可见,试验组细菌、真菌的回收率均大于70%,中和剂对照组各菌的回收率均大于70%。因此,可采用中和剂平皿法进行细菌、霉菌和酵母菌数测定。

表2 细菌、霉菌和酵母菌回收率试验结果
2.2.2 控制菌检查方法验证
试验组:取2.2.1项下供试液20 mL和大肠埃希菌的试验菌液1 mL,加入到胆盐乳糖增菌液100 mL中,依据大肠埃希菌的检查法试验;取2.2.1项下供试液20 mL和金黄色葡萄球菌的试验菌液1 mL,加入到营养肉汤培养基100 mL中,依据金黄色葡萄球菌的检查法试验;取2.2.1项下供试液20 mL和铜绿假单胞菌的试验菌液1 mL,加入到胆盐乳糖增菌液100 mL中,依据铜绿假单胞菌的检查法试验。
阴性对照组:取2.2.1项下供试液20 mL和金黄色葡萄球菌的试验菌液1 mL,加入到胆盐乳糖增菌液100 mL中,依据大肠埃希菌的检查法试验;取2.2.1项下供试液20 mL和大肠埃希菌的试验菌液1 mL,加入到营养肉汤培养基100 mL中,依据金黄色葡萄球菌的检查法试验;取2.2.1项下供试液20 mL和大肠埃希菌的试验菌液1 mL,加入到胆盐乳糖增菌液100 mL中,依据铜绿假单胞菌的检查法试验。结果见表3。
可见,试验组检出大肠埃希菌、金黄色葡萄球菌、铜绿假单胞菌,阴性对照组未检出阴性对照菌。

表3 控制菌检查方法验证试验结果
3 讨论
软膏剂包括灭菌型与非灭菌型制剂,前者是指用灭菌的药物与基质在无菌环境条件下,按无菌操作规程进行配制的剂型,主要用于治疗眼黏膜或皮肤黏膜疾病以及手术、烧伤与严重创伤的局部给药[5],2010年版《中国药典(二部)》规定其应符合无菌检查法规定;后者指用适宜基质混合,容易涂抹皮肤、黏膜或创伤面的外用半固体剂型,主要用于对皮肤的保护与滑润[5],虽然对生产制剂环境未进行严格规定,但也应严格控制其微生物污染,2010年版《中国药典(二部)》对其微生物限度进行了明确的规定。第四军医大学口腔医院研制的唇裂防护膏,主要用于对高原部队官兵和高寒哨卡官兵在缺氧、寒冷、干燥气候条件下所出现的口唇干裂、冻裂的防护与保护,故要求对其按药典品种检查。本试验经对已知菌的回收率与控制菌的检测,结果表明,以上方法经验证符合2010年版《中国药典》规定,可以作为该产品的检测方法与质量标准。
本制剂按2010年版《中国药典(二部)》附录微生物限度检查法要求进行了方法学验证试验,结果表明,可采用中和剂平皿法进行细菌数、霉菌和酵母菌数检查;可采用中和剂常规法进行控制菌检查。为此,建议对化妆品类进行微生物限度检查法验证试验。若以每g为单位报告,建议限度标准可规定每g细菌数不得过100CFU,霉菌数不得过100 CFU,不得检出金黄色葡萄球菌和铜绿假单胞菌。
[1]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录114.
[2]马绪荣,苏德模.药品微生物检验手册[M].北京:科学出版社,2003:53-57.
[3]任安民,李秋菲,绳金房.注射剂无菌检查的方法学验证试验[J].西北药学杂志,2009,24(1):51 -52.
[4]应国红,邓 颖,冯丰凑.外用制剂微生物限度检查方法研究[J].中国药业,2008,17(21):32 -33.
[5]南京药学院.药剂学[M].北京:人民卫生出版社,1978:318,496.
