离子凝胶法制备壳聚糖纳米微粒的影响因素分析
2011-09-04赖克方马千里王长征
王 彦,赖克方*,张 巧,马千里,王长征
(1呼吸疾病国家重点实验室,广州医学院第一附属医院,广州呼吸疾病研究所,广州 510120;2第三军医大学新桥医院全军呼吸疾病研究所)
壳聚糖(CS)是天然多糖中惟一的阳离子碱性氨基多糖,生物相容性好,无毒,无抗原性,可生物降解,可包封带负电荷高聚物药物,是一种优良的药物载体,已成为医药领域的研究热点[1]。CS纳米粒的制备方法以离子凝胶法最常用,其原理是CS的氨基阳离子与三聚磷酸钠(TPP)的磷酸基阴离子通过静电吸引进行分子内或分子间交联,并进一步凝胶化而形成纳米颗粒,含有100 nm以上的纳米粒则可见乳光,因此制备成功的纳米微粒溶液呈乳光样,一般为泛蓝色,可作为评价CS 纳米粒制备成功与否的标准之一。2009年8月~2010年7月,我们观察了CS浓度、TPP浓度、CS/TPP质量比和CS溶液pH值对CS纳米粒乳光溶液制备,以及对CS纳米粒粒径和Zeta电位的影响。现报告并分析如下。
1 材料与方法
1.1 材料 CS(脱乙酰度95%,分子量40万,美国amerosco公司);TPP、冰醋酸(天津市大茂化学试剂厂);Zetasizer3000HS激光粒度仪及Zeta电位仪(英国Malvern公司);磁力搅拌器(德国IKA公司)。
1.2 实验方法
1.2.1 CS纳米粒制备 将CS溶解于1%醋酸溶液,调节pH值为4~6,TPP溶于超纯水,调节pH值为7.2 ~7.7,用0.45 μm 滤膜过滤。持续磁力搅拌下(200~400 r/min),取 CS溶液 8 ml,缓慢加入TPP溶液,保持搅拌20~30 min,以获得CS纳米粒。
1.2.2 CS纳米粒乳光液体制备的影响因素观察观察以下因素影响下的液体性状。①CS、TPP浓度:不同浓度CS溶液,调pH值为4.5,缓慢加入不同浓度TPP溶液。②CS溶液pH值:调节不同浓度CS溶液pH值分别为3.0~6.0,向不同pH值不同浓度CS溶液缓慢加入2.0 mg/ml TPP溶液。③CS/TPP质量比:调节CS溶液pH值为4.8,向不同浓度CS溶液中缓慢加入2.0 mg/ml TPP溶液达到不同CS/TPP质量比。
1.2.3 CS纳米粒的粒径和Zeta电位的影响因素观察 制备CS纳米粒的方法同1.2.1,观察以下因素对CS纳米粒粒径和Zeta电位的影响。①CS浓度:向pH值为4.8的不同浓度CS溶液中缓慢加入2.0 mg/ml TPP至CS/TPP质量比为6∶1。②CS溶液pH值:向不同pH值的1.0 mg/ml CS溶液中缓慢加入2.0 mg/ml TPP溶液使 CS/TPP质量比为6∶1。③CS/TPP质量比:调节 CS溶液 pH 值为4.8,向1.0 mg/ml CS溶液中缓慢加入2.0 mg/ml TPP溶液使CS与TPP达到不同质量比。采用激光粒度仪及Zeta电位仪测定以上条件下纳米粒粒径和Zeta电位。
2 结果
2.1 CS浓度和TPP浓度对液体性状的的影响 见表1。由表1 可见,CS 浓度在0.5 ~3.0 mg/ml、TPP浓度在0.8~3.0 mg/ml易获得CS纳米乳光溶液,且CS浓度较TPP浓度对反应结果影响更显著。当CS浓度≤0.2 mg/ml时,加入TPP即刻发生沉淀。CS浓度≥4.0 mg/ml,加入TPP不能产生乳光溶液。在合适 CS浓度(0.5~1.5 mg/ml)下,TPP浓度对CS纳米乳光溶液制备影响小。

表1 不同浓度的CS溶液(pH 4.5)与TPP溶液对液体性状的影响
2.2 CS溶液pH值对液体性状的影响 见表2。由表2可见,CS溶液pH值为6.0时加入TPP即刻发生沉淀。pH值≤3.0时,CS与TPP无法形成乳光溶液。CS溶液 pH 值为3.5~5.0、CS浓度为0.5~2.5 mg/ml时,易获得稳定的乳光溶液。

表2 CS溶液pH值对液体性状影响
2.3 CS/TPP质量比对液体性状的影响 见表3。由表3可见,CS/TPP质量比为4∶1~12∶1时易产生乳光溶液。随着 CS/TPP质量比增大,CS浓度降低,溶液乳光程度逐渐降低。CS/TPP质量比以6∶1~12∶1产生乳光溶液稳定,静置后不易产生沉淀。CS浓度≥1.5 mg/ml,CS/TPP 质量比为 3∶1 ~5∶1时乳光溶液静置后易产生沉淀,CS浓度越大沉淀越明显。
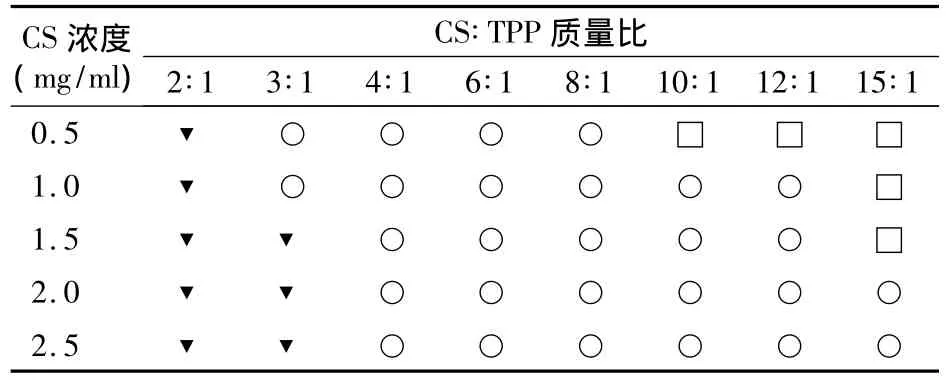
表3 CS/TPP质量比对液体性状的影响
2.4 CS浓度对纳米粒粒径和Zeta电位的影响 见表4。由表4可见,随着CS浓度的增加,CS纳米粒粒径和Zeta电位显著增大。
表4 CS浓度对纳米粒粒径和Zeta电位的影响()
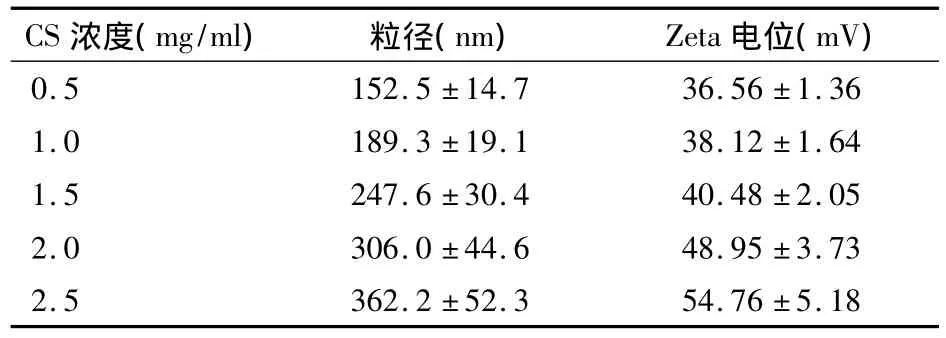
表4 CS浓度对纳米粒粒径和Zeta电位的影响()
CS浓度(mg/ml) 粒径(nm) Zeta电位(mV)0.5 152.5 ±14.7 36.56 ±1.361.0 189.3 ±19.1 38.12 ±1.641.5 247.6 ±30.4 40.48 ±2.052.0 306.0 ±44.6 48.95 ±3.732.5 362.2 ±52.3 54.76 ±5.18
2.5 CS溶液pH值对纳米粒粒径和Zeta电位的影响 见表5。由表5可见,pH值降低导致CS纳米粒Zeta电位增高。pH值对CS纳米粒粒径几乎无影响,但pH值为5.5时粒径突然显著增大。
2.6 CS/TPP质量比对纳米粒粒径及Zeta电位的影响 CS/TPP质量比增高引起CS纳米粒粒径逐渐变小,但对Zeta电位影响复杂(见表6)。CS/TPP质量比从6∶1降低至3∶1时,Zeta电位随之明显降低。
表5 CS溶液pH值对纳米粒粒径和Zeta电位的影响()
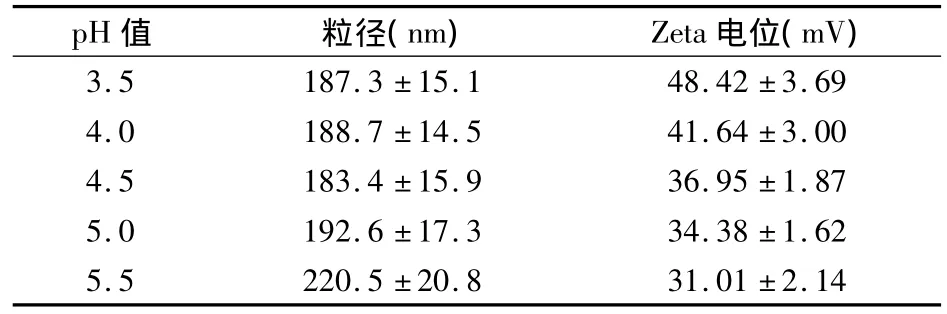
表5 CS溶液pH值对纳米粒粒径和Zeta电位的影响()
pH值 粒径(nm) Zeta电位(mV)3.5 187.3 ±15.1 48.42 ±3.694.0 188.7 ±14.5 41.64 ±3.004.5 183.4 ±15.9 36.95 ±1.875.0 192.6 ±17.3 34.38 ±1.625.5 220.5 ±20.8 31.01 ±2.14
表6 CS/TPP质量比对纳米粒粒径和Zeta电位的影响()
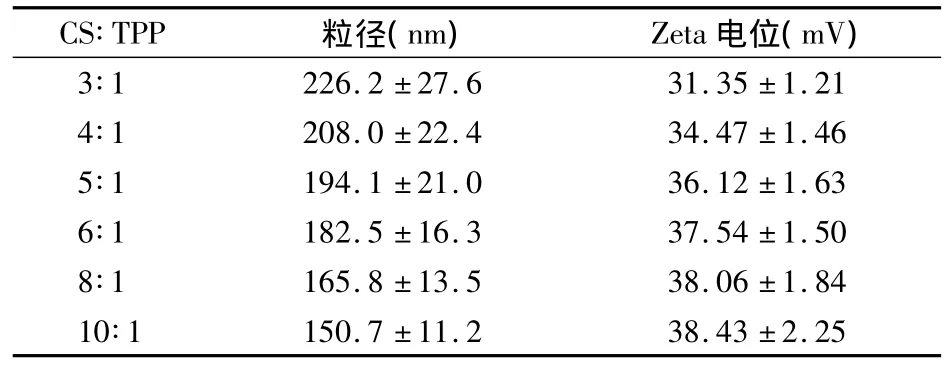
表6 CS/TPP质量比对纳米粒粒径和Zeta电位的影响()
CS∶TPP 粒径(nm) Zeta电位(mV)3∶1 226.2 ±27.6 31.35 ±1.214∶1 208.0 ±22.4 34.47 ±1.465∶1 194.1 ±21.0 36.12 ±1.636∶1 182.5 ±16.3 37.54 ±1.508∶1 165.8 ±13.5 38.06 ±1.8410∶1 150.7 ±11.2 38.43 ±2.25
3 讨论
离子凝胶法制备CS纳米粒简单易行,TPP无毒,无需使用有机溶剂,但是受多种因素的影响。CS为碱性多糖,在酸性溶液中发生氨基质子化是CS纳米形成的关键[2],因此CS-TPP反应结果与CS溶液pH值关系密切。本研究发现,CS溶液pH值以3.5 ~5.0为宜,这与吴振宇等[3]研究结果一致。CS溶液pH值为6.0时,加入TPP即刻发生沉淀,可能与CS溶解性降低和阳性电价发生改变有关,与CS浓度无关。而pH值≤3.0时,TPP的磷酸基团被氢离子占据,CS-TPP间的静电吸引受影响,而无法形成乳光溶液。
CS和TPP溶液的浓度、CS/TPP质量比对CS纳米粒的制备影响亦非常显著。CS浓度和TPP浓度过低导致离子强度太低,TPP的磷酸基与CS的氨基静电吸引力较小,分子内或分子间交联弱,无法使溶液凝胶化而形成纳米乳光溶液。CS和TPP浓度过高会因为离子强度太高无法得到CS纳米粒。研究发现,CS浓度过高时(CS≥4.0 mg/ml),CS溶液的离子强度高,CS氨基基团同性相斥促使CS分子弯曲聚集,加入TPP可促使CS进一步聚集而沉淀[4]。CS/TPP质量比过低或过高则会因为氨基和磷酸基搭配比例不均无法形成纳米粒。我们发现CS/TPP质量比<3∶1时出现沉淀,系磷酸基相对过多引起CS粒聚集所致。因此,CS浓度0.5~2.5 mg/ml,TPP 浓度为 0.8 ~ 3.0 mg/ml,CS/TPP 质量比为6∶1~12∶1,可得到稳定CS纳米粒乳光溶液。
本文还发现,CS浓度的增加导致CS纳米粒粒径和 Zeta 电位显著增大,与 Hu 等[5]、Grenha 等[6]研究结果一致。CS纳米溶液的Zeta电位与氨基被中和程度有关,CS浓度越高,未被中和的氨基越多,Zeta电位越高,而且未中和的氨基会导致更强的分子内交联,促使CS分子弯曲聚集,导致纳米粒粒径增大。我们发现pH值降低导致CS纳米粒Zeta电位增高,因为pH值越低,氨基越多。pH值对CS纳米粒径无显著影响,但pH值为5.5时粒径突然显著增大,可能因为微弱的CS-TPP相互作用诱发广泛的分子内交联导致粒径突然增大。CS/TPP质量比也是影响CS纳米粒特征的重要因素。我们发现,CS/TPP质量比降低,TPP相对量增多,剩余TPP促使单个纳米粒交联形成更大的纳米粒,导致CS纳米粒总体粒径增大,而且TPP相对量增多导致氨基总量相对减少,导致Zeta电位降低,此与国外研究结果一致[7]。
总之,离子凝胶法制备CS纳米粒的主要影响因素为CS浓度、CS/TPP质量比和CS溶液pH值,CS浓度和CS/TPP质量比对CS纳米粒粒径影响显著,CS浓度和CS溶液pH值对CS纳米粒Zeta电位影响显著。
[1]Rinaudo M.Chitin and chitosan:properties and applications[J].Prog Polym Sci,2006,31(7):603-632.
[2]Sun Y,Wan AJ.Preparation of nanoparticles composed of chitosan and its derivatives as delivery systems for macromoecules[J].J Appl Polym Sci,2007,105(2):552-561.
[3]吴振宇,陈钟,黄华,等.离子凝胶法制备壳聚糖纳米微粒[J].南通大学学报(医学版),2005,25(1):20-22.
[4]Tsai ML,Bai SW,Chen RH.Cavitation effects versus stretch effects resulted in different size and polydispersity of ionotropic gelation chitosan-sodium tripolyphosphate nanoparticle[J].Carbohydr Polym,2008,71(3):448-457.
[5]Hu B,Pan CL,Sun Y,et al.Optimization of fabrication parameters to produce chitosan-tripolyphosphate nanoparticles for delivery of tea catechins[J].J Agric Food Chem,2008,56(16):7451-7458.
[6]Grenha A,Seijo B,Remunán-López C.Microencapsulated chitosan nanoparticles for lung protein delivery[J].Eur J Pharm Sci,2005,25(4-5):427-437.
[7]Papadimitriou S,Bikiaris D,Avgoustakis K,et al.Chitosan nanoparticels loaded with dorzolamide and pramipexole[J].Carbohydr Polym,2008,73(1):44-54.
