采用P507(HEH/EHP)从废FCC催化剂中回收稀土
2011-08-04何捍卫孟佳
何捍卫,孟佳
(中南大学 粉末冶金国家重点实验室,湖南 长沙,410083)
石油催化裂化(Fluid catalytic cracking,简称FCC)催化剂,是石油炼制工业中一类非常重要的催化剂,具有催化活性高、选择性好、稳定性高以及抗毒能力强等特点。其中,稀土型催化剂在长时间使用后,由于渣油中含有较多重金属及残炭等有害物质,会导致催化剂的催化活性降低,催化效率下降,从而生成大量废催化剂。随着我国炼油工业的发展,FCC催化剂的消耗量不断增加,产生的废 FCC催化剂也不断增多。废FCC催化剂作为有毒固体废弃物,其稀土含量约为2%,其他有价金属含量约为1.5%,若将其作为废弃物处理,不但会造成环境污染,也会造成资源浪费。而有效合理地回收废FCC催化剂中的稀土元素,对它进行综合回收利用,可产生较高的经济效益和社会效益。目前,由于萃取法具有处理容量大、反应速度快、分离效果好的特点,它已成为国内外稀土工业生产中分离回收稀土元素的主要方法。我国稀土行业现行萃取分离工艺所普遍采用的萃取剂主要是环烷酸和 P507[1]。萃取剂 P507(2-乙基己基膦酸单 2-乙基己基酯,HEH/EHP)是一种酸性膦型萃取剂,具有良好的萃取分离性能,成为目前应用最为广泛的萃取剂[2]。关于用 P507等萃取剂萃取回收稀土元素的报道有很多。张玉良等[3]研究了用P507-煤油-HCl体系从YCl3溶液中萃取分离La3+和Ca2+,发现该萃取体系与以往的环烷酸萃取提纯钇工艺相比具有一定的优点。吴声等[4]研究 P507体系反萃取条件对平衡负载稀土量的影响,建立了引入平衡负载概念的反萃取工艺参数计算方法。黄小卫等[5]研究P204和P507组成的混合萃取体系在硫酸介质中萃取分离Nd和Sm,发现该二元萃取体系在硫酸介质中对Nd和Sm萃取时具有不同程度的正协同效应。付念新等[6]在非理想条件下,研究溶剂ShellsolD70中P507对硝酸溶液中钇和铕的萃取平衡。罗兴华等[7]研究P507和P204从硫酸介质中协同萃取 Ce(Ⅳ)的机制。还有一些文献和专利[8-17]报道了用P507为萃取剂或P507和其他萃取剂组成的协同萃取剂分离含有中重稀土的原料。而采用萃取法从废FCC催化剂中回收稀土元素的研究,尚未发现国内外相关文献报道。在此,本文作者对废FCC催化剂中稀土元素回收进行研究,对稀土元素的回收规律进行系统研究,探索用P507萃取剂从废FCC催化剂中萃取分离回收轻稀土元素La和Ce的工艺流程,并讨论萃取剂浓度、浸取液pH、相比、反萃酸度、平衡时间等对萃取稀土的影响,获得了实验室条件下的较优工艺条件和稀土回收的效果。
1 实验
1.1 仪器和试剂
仪器有:KS-2康氏振荡器、pHS-2c酸度计、梨形分液漏斗等。
试剂有:P507(2-乙基己基膦酸单-2-乙基己基酯,HEH/EHP),工业纯,洛阳市中达化工有限公司生产;煤油,分析纯,天津市大茂化学试剂厂生产;氨水、盐酸等,均为分析纯;废 FCC催化剂粉末(稀土氧化物含量2.24%),由中国石化催化剂长岭分公司提供。
1.2 实验方法
将废FCC催化剂粉末经盐酸浸取、过滤、澄清,得到含有稀土和其他非稀土杂质的浸取液。浸取液中主要含 La3+和 Ce4+等稀土元素,非稀土杂质主要有Al3+,Ca2+,Fe3+和Na+等。浸取液中各离子浓度分析结果见表1。

表1 浸取液中各离子浓度分析结果(质量浓度)Table 1 Analysis results of ion concentration of leaching solution g/L
再将不同体积分数的 P507与煤油以一定比例混合配制成有机相。将废FCC催化剂经过酸浸取处理所得的稀土浸取液调整至一定浓度,并用稀氨水调节其pH至一定范围。然后,在分液漏斗中按一定相比放入水相和有机相,置于振荡器上混合振荡一定时间,达到萃取平衡后,静置分层,得到萃余水相和负载有机相。将负载有机相用一定浓度盐酸反萃后,得到反萃水相。萃余水相和反萃水相中稀土和非稀土元素浓度用等离子体原子发射光谱法(ICP-AES)测定。负载有机相中各元素浓度根据物料平衡用差减法求得。
2 结果和讨论
2.1 P507从盐酸介质中分离稀土效果
在温度为 25 ℃,浸取液中稀土离子质量浓度为9.01 g/L,稀氨水调节浸取液pH为2.50,萃取相比为2:1条件下,用体积分数为60%的P507和煤油混合成的有机相对浸取液进行萃取,振荡30 min后,稀土和其他元素的分配比D及萃取率E见表2。
由表2可以看出:用P507在盐酸介质中进行萃取,稀土元素的萃取率较高,而非稀土元素的萃取率则较低。说明轻稀土元素La和Ce与萃取剂P507较易形成萃合物,从而易于被萃取。根据分配比,表示萃取体系达到平衡时,被萃溶质在有机相中的总浓度与水相中总浓度[A]之比。而萃取率(式中,R为相比)。由此式可以看出:当相比为定值时,萃取率取决于分配比。实验结果表明:在相比一定时,稀土的分配比越高,萃取率越高,也就是萃取越完全。

表2 P507 从盐酸介质中萃取稀土元素效果Table 2 Effect of extracting rare earth in hydrochloric acid system using P507
因此,利用这一规律,可以提高稀土萃入有机相的能力,使 P507从盐酸介质中能较好地将稀土元素La和Ce与Al,Ca,Fe和Na等贱金属分离。
2.2 萃取剂浓度对萃取稀土的影响
在温度为 25 ℃,浸取液中稀土离子质量浓度为9.01 g/L,相比为1:1,浸取液pH为2.50的条件下,振荡萃取30 min后,考察不同体积分数的P507对萃取稀土分配比的影响,结果见图1。

图1 P507体积分数对萃取稀土的影响Fig.1 Effect of volume fraction of P507 on extraction of rare earth
从图 1可以看出:有机相中萃取剂的浓度(P507的体积分数)对萃取稀土的分配比有影响。随着萃取剂浓度的增大,La和Ce这2种稀土元素的分配比逐渐增大,且P507体积分数在5%~70%之间变化时对Ce的分配比影响较为显著,当P507体积分数达到50%以上后,Ce的分配比增大较多。
由于 P507萃取剂在煤油等溶剂中以二聚体形式存在,其分子式可简写为(HL)2(0),低酸度下 P507萃取稀土RE3+按阳离子交换机理进行,其平衡反应[2]可表示为:

萃取平衡常数为:

当 pH恒定时,可知式(2)中[H+],此时稀土分配比:
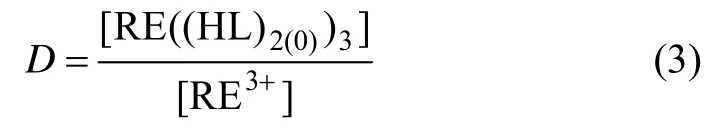
将式(3)代入式(2)可得到:

其中:K1为萃取平衡常数。将式(4)两边取对数得:
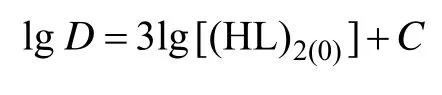
所以,图1中将2条曲线对应的点取对数作图将得到直线,直线斜率应在k=-3~-2之间,常数C为直线的截距。实际上斜率k即是被萃稀土离子形成萃合物所需萃取剂的分子数。将式(2)取对数后得到:

式(5)表明:当平衡pH恒定时,随着萃取剂浓度的增加,被萃取稀土的含量也随之增加。
虽然有机相中萃取剂浓度的提高可以有效地增大稀土的分配比,但在实际生产中,还需要考虑萃取剂浓度的升高可能会增大有机相的黏度,从而影响两相的充分混合和分相速度,在某些情况下,还可能影响萃取分离效果。实验中,随着萃取剂浓度的增加,被萃稀土的含量也随之增加,但是随着 P507体积分数达到60%以上后,水相和有机相分相速度较慢,分层时间延长,最后两相分层后有机相呈絮状泡沫,两相界面处有气泡存在;并且随同稀土共萃入有机相的杂质增多,萃取的分离效果变差。因此,在考虑上述因素后,选取P507体积分数在60%左右,更加有利于稀土的萃取。
2.3 浸取液pH的影响
在温度为 25 ℃,浸取液中稀土离子质量浓度为9.01 g/L,相比为1:1,P507体积分数为60%的条件下,用稀氨水调节浸取液至不同的pH,振荡萃取30 min后,考察浸取液不同 pH对萃取稀土的影响,分别得到了不同pH对稀土及其他元素的萃取率,结果如图2所示。

图2 不同pH下浸取液对稀土萃取率的影响Fig.2 Effect of pH of leaching solution on extraction rate of rare earth
从图2可以看出:浸取液在不同酸度下,稀土的萃取率较高,非稀土元素Al3+,Fe3+,Ca2+和Na+的萃取率较低;随着 pH的增加,稀土的萃取率先增加,然后逐渐下降;非稀土杂质中,Fe3+的萃取率随着pH的增大逐渐降低,Na+的萃取率随着pH的增大逐渐升高,而 Al3+的萃取率随 pH的增大变化不明显,Ca2+的萃取率则随pH的增大变化先降低然后增加。
稀土萃取率随pH变化的原因,可能是由于酸性萃取剂在萃取金属过程中都放出萃取的稀土越多,产生的氢离子越多,结果使体系的pH降低,从而降低了萃取效率。pH较低时,稀土萃取率低,这是由于萃取剂的质子化作用造成的(即萃取剂不能离解);pH过高,稀土的萃取率同样下降,这时稀土离子已发生水解,而这种水解产物是不能被萃取的。从而当浸取液pH在1.2~3.0范围内变化时,稀土的萃取率先增加然后减小,当浸取液pH在2.5左右时,稀土的萃取率可以达到最大值。当pH为2.5时,稀土与Al3+,Ca2+,Fe3+和Na+的分离系数分别为,,说明此时除 Fe3+外,稀土与其他非稀土杂质有较好的分离效果,且保证了稀土较高的萃取率。因此,浸取液pH调整至2.5左右较合适。
2.4 相比对萃取稀土的影响
在温度为 25 ℃,浸取液中稀土离子质量浓度为9.01 g/L,P507体积分数为60%的条件下,用稀氨水调节浸取液至pH为2.50,改变相比进行实验,振荡萃取30 min后,考察不同相比对萃取稀土的影响,结果见表3。
由表3可以看出:随着相比的增大,稀土萃取率升高,但稀土的萃取率在相比为 2:1~4:1范围内提高不明显;其他非稀土杂质的萃取率随着相比的增加也有所增加,Na+的萃取率变化则不大。分析萃取平衡后有机相和水相中稀土质量浓度的变化情况,可以得到萃取时相比(O/A)对稀土萃取影响的关系曲线,如图3所示。
由图3可以看出:随着相比的增加,稀土在两相中的分配比也是随之增加,这表明有机相和水相中的稀土浓度变化实际上也是稀土的萃取等温线。在保证稀土萃取率较高,且能与其他非稀土杂质有效分离的情况下,应尽可能最大程度地减少非稀土杂质随稀土一同萃入有机相的含量。因此,选择相比为2:1较为合适。

表3 不同相比对萃取稀土的影响Table 3 Effect of different volume ratio of organic phase to water phase on extraction of rare earth
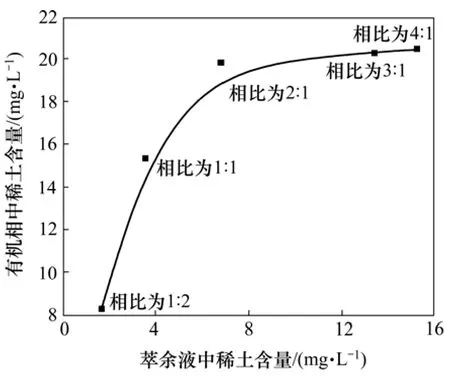
图3 相比对稀土萃取的影响Fig.3 Effect of volume ratio of organic phase to water phase on extraction of rare earth
2.5 反萃酸度对萃取稀土的影响
为得到除杂后的氯化稀土溶液,要对负载有机相进行反萃实验,反萃实验可以大量降低进入负载有机相中的非稀土杂质,对最终产品纯度的提高具有较大意义,所以进行反萃酸浓度实验是十分必要的。在温度为25 ℃,浸取液中稀土离子质量浓度为9.01 g/L,P507体积分数为60%的条件下,用稀氨水调节浸取液至pH为2.50,振荡萃取30 min,然后在温度为25℃,反萃相比为1:2的条件下,改变反萃酸度进行实验,反萃 60 min后,考察不同反萃酸度下稀土的反萃情况,结果见图4。

图4 不同反萃酸度对萃取稀土的影响Fig.4 Effect of different acidity of back extracting process on back extraction of rare earth
由图4可以看出:进行反萃实验可以降低反萃液中杂质离子的含量,稀土的反萃率先有所提高,但当反萃液酸度太高时,稀土反萃率反而下降;当反萃酸度c(H+)=2.0 mol/L时,稀土的反萃率最高。
根据简化的含酸体系萃取平衡模型[4],假定式(1)中各项的活度系数为常数,稀土组分为i,水相和有机相稀土浓度分别为xi和yi,水相中氢离子浓度为xH,有机相中萃取剂浓度为yH,代入式(2)可写为:

式中:平衡常数K1可由实验测出;有机相中萃取剂总浓度Y为自由萃取剂(HL)2(0)和负载萃取剂RE1/3(HL)2(0)的浓度之和,
水相阴离子总浓度为

式中:cx和cy分别为水相和有机相稀土浓度。单级萃取过程前后X和Y保持不变,cx和cy则将会根据萃取平衡关系发生变化。
可将式(6)可改写为:

将式(8)代入式(7),得:

若已知有机相萃取剂浓度yH和有机相稀土浓度yi,式(9)改写为关于xH三次函数,

而图4中其他非稀土元素的反萃率和稀土反萃率均较低,Ca2+的反萃率随着反萃酸度的提高而明显增加,即反萃出的钙越多;Fe3+和Na+进入反萃液的含量则是随着反萃液酸度的升高而有所下降;Al3+随着反萃酸度的变化则无明显规律。但是,在保证稀土反萃率最高的情况下,要尽量让其他非稀土杂质的含量都较低,以达到产品纯度要求。
2.6 平衡时间对萃取稀土的影响
在温度为 25 ℃,浸取液中稀土离子质量浓度为9.01 g/L,P507体积分数为60%的条件下,用稀氨水调节浸取液至pH为2.50,相比为2:1,改变振荡萃取时间,考察不同平衡时间对稀土La和Ce萃取效果的关系,结果见图5。

图5 平衡时间对稀土萃取率的影响Fig.5 Effect of equilibrium time on extraction rate of rare earth
由图5可以看出:该萃取过程速度较慢,随着有机相和水相接触时间的延长,稀土La和Ce的萃取率逐渐增加,当萃取时间达到30 min左右时,萃取才达到平衡。P507从HCl介质中萃取分离稀土元素的工艺已广泛用于工业生产中,但从动力学角度看,其萃取平衡时间在HCl介质中较长,这是影响萃取生产率和经济效益的因素之一[2]。因此,利用 P507从废 FCC催化剂中回收稀土的动力学还有待进一步研究。
3 结论
(1) 废FCC催化剂经过盐酸浸取的浸取液中主要含有稀土元素La和Ce,以及非稀土杂质Al,Ca,Fe和Na等。由P507和煤油组成的萃取体系可以从浸取液中有效地萃取出稀土元素,再经过反萃后除去非稀土杂质,使La和Ce得到回收。
(2) 采用P507作萃取剂回收废FCC催化剂中稀土元素,其最佳工艺条件是:萃取剂浓度(P507体积分数)为60%,浸取液pH为2.5,萃取相比为2:1,萃取平衡时间为30 min;负载有机相直接用盐酸进行反萃得到氯化稀土溶液,反萃盐酸浓度为2.0 mol/L,反萃平衡时间为60 min。
[1] 黄桂文. 我国稀土萃取分离技术的现状及发展趋势[J]. 江西冶金, 2003, 23(6): 62-68.HUANG Gui-wen. Development tendency and present situation of rare earth extraction separation technology in China[J].Jiangxi Metallurgy, 2003, 23(6): 62-68.
[2] 徐光宪. 稀土[M]. 北京: 冶金工业出版社, 2002: 526-540.XU Guang-xian. Rare earth[M]. Beijing: Metallurgical Industry Press, 2002: 526-540.
[3] 张玉良, 赵军. 用P507-煤油-HCl稀土从YCl3溶液中萃取分离La3+和Ca2+[J]. 湿法冶金, 2003, 22(3): 138-141.ZHANG Yu-liang, ZHAO Jun. Separating La3+and Ca2+from YCl3solution with P507-kerosene-HCl extraction system[J].Hydrometallurgy of China, 2003, 22(3): 138-141.
[4] 吴声, 廖春生, 贾江涛, 等. P507体系反萃取条件对平衡负载稀土量的研究[J]. 中国稀土学报, 2006, 24(2): 134-138.WU Sheng, LIAO Chun-sheng, JIA Jiang-tao, et al. Effect of cycling loaded Rare Earths on striping process in P507 extraction system[J]. Journal of the Chinese Rare Earths Society,2006, 24(2): 134-138.
[5] 黄小卫, 李建宁, 张永奇, 等. P204-P507在选型硫酸盐溶液中对 Nd3+和 Sm3+的协同萃取[J]. 中国有色金属学报, 2008,18(2): 366-371.HUANG Xiao-wei, LI Jian-ning, ZHANG Yong-qi, et al.Synergistic extraction of Nd3+and Sm3+from sulfuric acid medium with D2EHPA-HEHEHP in kerosene[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(2): 366-371.
[6] 付念新, 田中斡也. 非理想平衡条件下P507对硝酸溶液中钇和铕萃取平衡的分析模拟[J]. 稀土, 2007, 28(5): 56-63.FU Nian-xin, Tanaka M. Modeling analysis of extraction equilibrium of yttrium(Ⅲ) and europium(Ⅲ) from nitric acid with P507 under non-ideal conditions[J]. Chinese Rare Earths,2007, 28(5): 56-63.
[7] 罗兴华, 黄小卫, 朱兆武, 等. 2-乙基己基膦酸单 2-乙基己基酯和二(2-乙基己基)膦酸从硫酸介质中协同萃取 Ce(Ⅳ)的研究[J]. 中国稀土学报, 2008, 26(5): 566-569.LUO Xing-hua, HUANG Xiao-wei, ZHU Zhao-wu, et al.Synergistic extraction of cerium(Ⅳ) from sulphuric acid medium using mixture of 2-ethylhexyl phosphonic acid mono-ethyl hexyl ester and di-(2-ethyl hexyl) phosphoric acid as extractant [J].Journal of the Chinese Rare Earths Society, 2008, 26(5):566-569.
[8] Xiong Y, Wu D B, Li D Q, et al. Kinetics of Y(Ⅲ) stripping for the system Y/HCl/cyanex 272-P507/heptane with constant interfacial area cell with laminar flow[J]. Solvent Extr Ion Exch,2005, 23(6): 803-816.
[9] 黄小卫, 李建宁, 彭新林. 一种非皂化磷类混合萃取剂萃取分离稀土元素的工艺: 中国, 1804063A[P]. 2006-07-19.HUANG Xiao-wei, LI Jian-ning, PENG Xin-lin. A method about extraction and separation of rare earth with unsaponification mixed extractant: CN, 1804063A[P]. 2006-07-19.
[10] 李德谦, 王香兰, 孟淑兰, 等. 一种添加改良剂的萃取体系分离稀土元素的工艺: 中国, 1804063A[P]. 2005-09-21.LI De-qian, WANG Xiang-lan, MENG SHu –lan, et al. A method about separation of rare earth with extraction system of increasing improvers: CN, 1670228A[P]. 2005-09-21.
[11] 黄小卫, 李红卫, 龙志奇, 等. 一种非皂化有机相萃取稀土全分离工艺: 中国, 1824814A[P]. 2006-08-30.HUANG Xiao-wei, LI Hong-wei, LONG Zhi-qi, et al. A method about extraction and separation of rare earth with unsaponificated extractant: CN, 1824814A[P]. 2006-08-30.
[12] 廖春生. 一种萃取分离稀土元素的混合萃取方法及萃取剂:中国, 101230420A[P]. 2008-07-30.LIAO Chun-sheng. A mixed extract method and extractant of extraction and separation rare earth: CN, 101230420A[P].2008-07-30.
[13] Wang Z H, Ma G X, Lu J, et al. Separation of heavy rare earth elements with extraction resin containing 1-hexyl-4-ethyloctyl is opropylphosphonic acid[J]. Hydrometallurgy, 2002, 66(1/3):95-99.
[14] Buch A, Stambouli M, Pareau D. Solvent extraction of nickel(Ⅱ)by mixture of 2-ethyhexanal oxime and bis(2-ethyhexyl)phosphoric acid[J]. Solvent Extr Ion Exch, 2002, 20(1): 49-66.
[15] 廖春生. 重稀土的萃取分离[D]. 北京: 北京大学稀土材料化学及应用国家重点实验室, 1996: 1-20.LIAO Chun-sheng. Extraction and separation of heavy rare earth[D]. Beijing: Peking University. State Key Lab of Rare Earth Materials Chemistry and Applications, 1996: 1-20.
[16] Dhami P S, Chitnis R R, Gopalakrishnan V. Studies on the partitioning of actinides from high lever waste using a mixture of HDEHP and CMPO as extractant[J]. Sci Tech, 2001, 36(2):325-335.
[17] Jia J T, Wu S, Liao C S, et al. Research and application progress in countercurrent solvent extraction[J]. Journal of Rare Earths,2004, 22(1): 17.
[18] 杨佼庸, 刘大星. 萃取[M]. 北京: 冶金工业出版社, 1988:30-31.YANG Jiao-yong, LIU Da-xing. Extraction[M]. Beijing:Metallurgical Industry Press, 1988: 30-31.
