海洋来源真菌Fusarium sp.次级代谢产物的研究(Ⅱ)
2011-07-27李占林裴月湖华会明
刘 涛,李占林,王 宇,田 黎,裴月湖,华会明
(1.中国医科大学药学院,辽宁 沈阳 110001;2.沈阳药科大学 创新药物研究与设计教育部重点实验室,辽宁 沈阳 110016;3.国家海洋局第一海洋研究所,山东 青岛 266061;4.青岛科技大学,山东 青岛 266042)
近年来,海洋微生物次级代谢产物的相关研究日趋活跃,其中海洋真菌更是该领域研究的热点。海洋独特的生存环境使海洋真菌的次级代谢产物在结构类型及生物活性等方面都呈现出与陆生真菌不同的特点和多样性,其在抗肿瘤、抗微生物等方面巨大的开发与应用潜质,引起了人们的极大关注[1]。
作者在此对海洋来源真菌Fusariumsp.菌丝体的丙酮提取物进行了化学成分分离,通过波谱及理化性质分析确定了这些化合物的结构。
1 实验
1.1 材料、试剂和仪器
镰孢霉属真菌Fusariumsp.于2007年4月分离自南海潮间带红树植物正红树(Rhizophoraapiculata)根际泥,由国家海洋局第一海洋研究所、青岛科技大学田黎教授鉴定。菌株编号:HTTM-Z07006,存放于科技部资助的国家海洋局第一海洋研究所药用海洋微生物菌种资源库。
实验所用试剂为分析纯或色谱纯。
发酵培养基:马铃薯浸汁200 mL,蛋白胨2 g,酵母粉1 g,葡萄糖17 g,NaCl 15 g,MgCl2·6H2O 1 g,KCl 0.1 g,FePO40.01 g,水1000 mL。
开放ODS柱色谱填料(100 μm),日本YMC公司;Sephadex LH-20,GE Healthcare公司;柱色谱硅胶(200~300目)、薄层色谱硅胶,青岛海洋化工厂;Bruker ARX-300、AV-600型核磁共振仪;L2130型HPLC(检测器为HITACHI L 2400 型),日本HITACHI公司;YMC-Pack ODS-AM(10 mm×250 mm)。
1.2 方法
取菌种接种于发酵培养基,24 ℃、150 r·min-1振荡培养12 d,发酵量60 L。
发酵液经多层纱布过滤,分离得到滤液和菌丝体。菌丝体(湿重1906.5 g)经反复冷冻-融化处理后,用4 BV丙酮超声提取3次,每次提取1 h,合并提取液,减压浓缩得浸膏81.5 g。菌丝体丙酮提取物经硅胶柱色谱,用氯仿-甲醇[(100∶0)~(0∶100)]梯度洗脱,得到282个流分(500 mL/流分)。
第33~55流分合并,经Sephadex LH-20柱色谱,用氯仿-甲醇(1∶1)洗脱,第20~31亚流分经Sephadex LH-20柱进一步纯化,得到化合物1(2 mg)。
第73~84流分合并,经Sephadex LH-20柱色谱,用甲醇洗脱,第12亚流分经重结晶,得到化合物6(5 mg);第26~27亚流分合并得到化合物2(2 mg)。
第51~57流分合并,经Sephadex LH-20柱色谱,用氯仿-甲醇(1∶1)洗脱,第20~22亚流分合并,用甲醇-水(30%~100%)梯度洗脱及Sephadex LH-20柱色谱,得到化合物7(2 mg)和9(10 mg)。
第124~135流分合并,经Sephadex LH-20柱色谱,用氯仿-甲醇(1∶1)洗脱,第11亚流分得到化合物3(4 mg);第16~19亚流分合并,经纯化得到化合物8(5 mg)。
第136~149流分合并,经Sephadex LH-20柱色谱,用氯仿-甲醇(1∶1)洗脱,第14、15亚流分得到化合物10(30 mg)。
第180~188流分合并,经Sephadex LH-20柱色谱,用氯仿-甲醇(1∶1)洗脱,第19~25亚流分得到化合物4(6 mg)。
第195~210流分合并,经Sephadex LH-20柱色谱,用氯仿-甲醇(1∶1)洗脱,第26~43亚流分经开放ODS色谱柱,用甲醇-水(5%,10%)洗脱,得到化合物5(8 mg)。
2 结果与讨论
2.1 化合物结构表征
化合物1:桔黄色针晶(甲醇),UV 365 nm下有桔红色荧光,Bornträger′s反应阳性。IR(KBr),ν,cm-1:3424(OH),1628(缔合C=O);1HNMR(600 MHz,DMSO-d6),δ,ppm:12.12(1H,s,5-OH),12.07(1H,s,1-OH),11.40(1H,br s,3-OH),7.53(1H,d,J=1.2 Hz,H-8),7.20(1H,d,J=1.2 Hz,H-6),7.14(1H,d,J=2.1 Hz,H-4),6.60(1H,d,J=2.1 Hz,H-2),2.43(3H,s,7-CH3)。综合以上数据并结合文献[2],鉴定该化合物为1,3,5-三羟基-7-甲基蒽醌(1,3,5-Trihydroxyl-7-methylanthraquinone)。
化合物2:桔黄色无定形粉末,UV 365 nm下有桔红色荧光,Bornträger′s反应阳性。1HNMR(300 MHz,DMSO-d6),δ,ppm:12.16(2H,br s,1,8-OH),7.66(1H,br s,H-4),7.26(1H,br s,H-5),7.12(1H,br s,H-2),6.56(1H,br s,H-7),5.56(1H,br s,CH2OH),4.61(2H,d,J=4.7 Hz,CH2OH)。综合以上数据并结合文献[3],鉴定该化合物为6-羟基芦荟大黄素(Citreorosein)。
化合物3:白色无定形粉末,10% 硫酸乙醇显紫色,Molish反应阳性。1HNMR(600 MHz,C5D5N),δ,ppm:5.33(1H,br s,H-6),5.23(1H,q,J=6.6 Hz,H-28),5.07(1H,d,J=7.8 Hz,H-1′),4.58(1H,dd,J=12.0 Hz,2.4 Hz,H-6′a),4.43(1H,dd,J=12.0 Hz,5.4 Hz,H-6′b),4.32(1H,dd,J=9.0 Hz,8.0 Hz,H-4′),4.30(1H,dd,J=9.0 Hz,8.0 Hz,H-3′),4.08(1H,t,J=7.8 Hz,H-2′),4.01(1H,m,H-3),3.95(1H,m,H-5′),1.02(3H,d,J=7.2 Hz,H-21),0.89(3H,s,H-19)。13CNMR(150 MHz,C5D5N),δ,ppm:145.9(C-24),140.9(C-5),121.9(C-6),117.1(C-28),102.6(C-1′),78.7(C-3′),78.5(C-5′),78.1(C-3),75.4(C-2′),71.8(C-4′),62.9(C-6′),56.8(C-14),56.2(C-17),50.4(C-9),42.5(C-13),40.0(C-4),39.4(C-12),37.5(C-1),37.0(C-10),36.5(C-20),36.4(C-22),32.2(C-8),32.1(C-7),30.3(C-2),28.9(C-25),28.5(C-23),28.4(C-16),24.5(C-15),21.3(C-27),21.2(C-26),21.2(C-11),19.5(C-19),19.0(C-21),13.0(C-29),12.0(C-18)。综合以上数据并结合文献[4,5],鉴定该化合物为 3-O-β-D-吡喃葡萄糖基-豆甾-5,24(28)Z-二烯(3-O-β-D-Glucopyranosyl-stigmasta-5,24(28)Z-diene)。
化合物4:无色针晶(甲醇),UV 254 nm下有明显暗斑。1HNMR(300 MHz,DMSO-d6),δ,ppm:11.31(1H,s,NH),7.88(1H,d,J=8.1 Hz,H-6),5.77(1H,d,J=5.4 Hz,H-1′),5.62(1H,d,J=8.1 Hz,H-5),5.37(1H,d,J=5.7 Hz,OH),5.09(2H,m,OH),4.01(1H,m,H-3′),3.94(1H,m,H-2′),3.82(1H,m,H-4′),3.60(1H,m,H-5′a),3.53(1H,m,H-5′b)。与尿嘧啶核苷对照品共薄层,多种溶剂系统下Rf值一致,并结合文献[6],鉴定该化合物为尿嘧啶核苷(Uridine)。
化合物5:白色无定形粉末,UV 254 nm下有明显暗斑。1HNMR(300 MHz,DMSO-d6),δ,ppm:12.42(1H,br s,NH),8.35(1H,s,H-2),8.08(1H,br s,H-8),5.86(1H,d,J=6.0 Hz,H-1′),4.48(1H,m,H-3′),4.12(1H,m,H-2′),3.93(1H,m,H-4′),3.64(1H,m,H-5′a),3.55(1H,m,H-5′b)。13CNMR(75 MHz,DMSO-d6),δ,ppm:61.4(C-5′),70.4(C-3′),74.2(C-2′),85.7(C-4′),87.5(C-1′),124.5(C-5),138.8(C-2),146.0(C-8),148.3(C-4),156.6(C-6)。综合以上数据并结合文献[7],鉴定该化合物为次黄嘌呤核苷(Inosine)。
化合物6:无色针晶(甲醇),1HNMR(600 MHz,DMSO-d6),δ,ppm:8.09(1H,s,NH),4.12(1H,m,H-6),4.00(1H,d,J=16.8 Hz,H-3a),3.50(1H,dd,J=4.8 Hz,16.8 Hz,H-3b),3.37(2H,m,H-9),2.12(1H,m,H-7a),1.82(3H,m,H-7b,H-8)。13CNMR(150 MHz,DMSO-d6),δ,ppm:169.3(C-2),163.9(C-5),58.1(C-6),46.0(C-3),44.7(C-9),27.9(C-7),22.1(C-8)。综合以上数据并结合文献[8],鉴定该化合物为吡咯并哌嗪-2,5-二酮(Pyrrolopiperazine-2,5-dione)。
化合物7:无色针晶(甲醇),1HNMR(600 MHz,DMSO-d6),δ,ppm:7.95(1H,s,NH),4.12(1H,m,H-6),3.92(1H,br s,H-3),3.34(2H,m,H-9),2.34(1H,m,H-10),2.13(1H,m,H-7a),1.82(3H,m,H-7b,H-8),1.01(3H,d,J=7.2 Hz,H-11 or H-12),0.85(3H,d,J=6.6 Hz,H-12 or H-11)。综合以上数据并结合文献[9],鉴定该化合物为3-异丙基吡咯并哌嗪-2,5-二酮(3-Isopropylpyrrolopiperazine-2,5-dione)。
化合物8:白色无定形粉末,UV 254 nm下有明显暗斑。1HNMR(300 MHz,DMSO-d6),δ,ppm:10.94(1H,s,NH),10.75(1H,s,NH),7.37(1H,d,J=7.7 Hz,H-6),5.44(1H,d,J=7.7 Hz,H-5)。综合以上数据并结合文献[10],并与尿嘧啶对照品共薄层,Rf值一致,鉴定该化合物为尿嘧啶(Uracil)。
化合物10:无色针晶(甲醇),1HNMR(600 MHz,DMSO-d6),δ,ppm:4.41(2H,d,J=5.6 Hz,OH),4.33(2H,d,J=5.7 Hz,OH),4.13(2H,d,J=7.1 Hz,OH),3.59(2H,m,H-1a,H-6a),3.52(2H,t,J=7.7 Hz,H-1b,H-6b),3.43(2H,m,H-2,H-5),3.36(2H,m,H-3,H-4)。13CNMR(150 MHz,DMSO-d6),δ,ppm:63.7(C-1,C-6),69.6(C-3,C-4),71.2(C-2,C-5)。综合以上数据并结合文献[13],鉴定该化合物为甘露醇(Mannitol)。
2.2 化合物的结构式
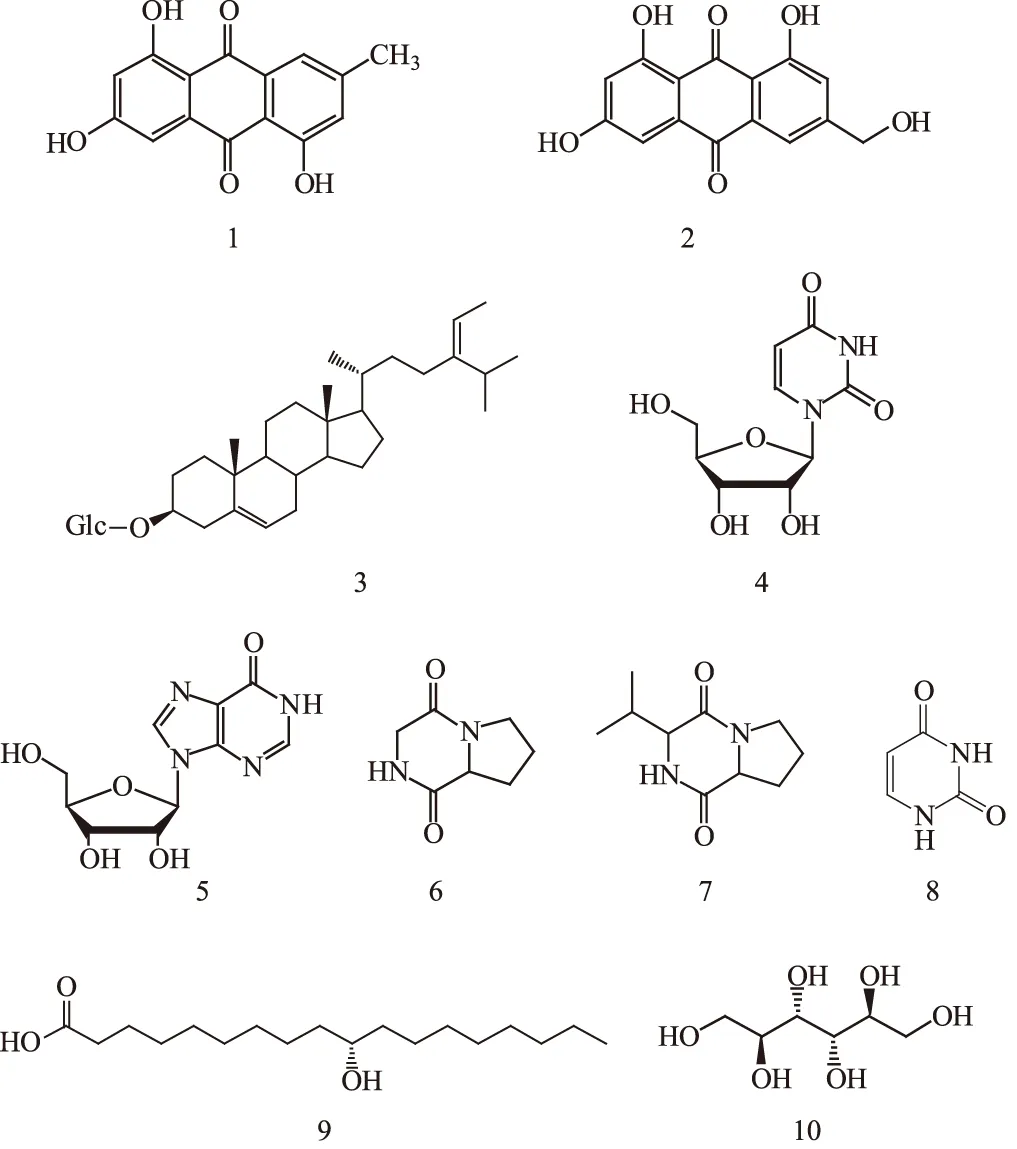
根据2.1分析结果,确定化合物1~10的结构式如下:
3 结论
从海洋来源真菌Fusariumsp.的菌丝体中分离得到10个化合物,通过波谱和理化性质分析,分别鉴定为1,3,5-三羟基-7-甲基蒽醌(1)、6-羟基芦荟大黄素(2)、3-O-β-D-吡喃葡萄糖基-豆甾-5,24(28)Z-二烯(3)、尿嘧啶核苷(4)、次黄嘌呤核苷(5)、吡咯并哌嗪-2,5-二酮(6)、3-异丙基吡咯并哌嗪-2,5-二酮(7)、尿嘧啶(8)、10S-羟基十八碳酸(9)、甘露醇(10)。其中化合物1、3和9均为首次从该属真菌中分离得到。
参考文献:
[1] 易杨华,焦炳华.现代海洋药物[M].北京:科学出版社,2006:4.
[2] 于明,李占林,李宁,等.头花蓼的化学成分[J].沈阳药科大学学报,2008,25(8):633-635.
[3] 刘晓秋,于黎明,吴立军.虎杖化学成分研究(I)[J].中国中药杂志,2003,28(1):47-49.
[4] Rosa S D,Giulio A D,Tommonaro G.Triterpenoids and sterol gl-ucoside from cell cultures ofLycopersiconesculentum[J].Phytochemistry,1997,44(5):861-864.
[5] 李占林.文冠果果壳化学成分及其生物活性研究[D].沈阳:沈阳药科大学,2006.
[6] 侯柏玲,李占林,李铣.苦马豆根和茎中一个新黄酮苷[J].药学学报,2005,40(6):533-535.
[7] 黄伟晖,宋纯清.当归化学成分研究[J].药学学报,2003,38(9):680-683.
[8] 刘海滨,高昊,王乃利,等.红树林真菌草酸青霉(092007)的环二肽类成分[J].沈阳药科大学学报,2007,24(8):474-478.
[9] Jayatilake G S,Thornton M P,Leonard A C,et al.Metabolites from an antarctic sponge-associated bacterium,Pseudomonasaeruginosa[J].Journal of Natural Products,1996,59(3):293-296.
[10] 陈光英,朱峰,林永成,等.南海红树内生真菌1947号次级代谢产物的研究[J].化学研究与应用,2007,19(1):98-99.
[11] 祝明松.质谱分析鉴定止血草药红棉藤-77(I)[J].药学学报,1981,16(6):471-473.
[12] Miller R W,Weisleder D,Kleiman R,et al.Oxygenated fatty ac-ids of isano oil[J].Phytochemistry,1977,16(7):947-951.
[13] 张海龙.海洋微生物次级代谢产物的研究[D].沈阳:沈阳药科大学,2004.
