碳还原氧化铜的探究
2011-07-17刘彬
刘 彬
(徐州市铜山中学 江苏 徐州 221100)
碳的还原性是中学化学教学中的一个重点,而碳还原氧化铜的演示实验又是教学中的一个难点。它是中学化学中首次接触的固相反应,而且是典型的高温固相反应。碳和氧化铜均为黑色物质,如果配比不当,其中任何一种物质的剩余都会影响实验结果的观察。再者,该反应活化能较高,800℃才开始反应,在此高温下较易生成铜镜,现象明显。但是这又会因试管局部受热而变形甚至损坏,造成了一定的经济损失,而且试剂的用量也较大,无论从实验教学效果的角度还是从经济与环保的角度看,该实验都需要改进。
为此,国内外有关学者作了大量的研究工作,对该实验从不同角度进行了改进,许多学者从实践和实用的角度提出了改进方案,例如通过颜色比较来判断生成物的化学成分,然后根据所生成的铜镜效果来确定最佳配比;有的是利用逐一验证法反复实验,然后选择最好的加热方式和最佳配比。究竟碳还原氧化铜的最佳反应条件是什么?到底应采用什么实验装置和方法呢?经过探索,我采用微型实验并利用正交试验这种数理统计方法来分析,同时分离并称量出反应生成的单质铜的质量。这样不仅实验效果明显,而且避免了不必要的重复。将反应物用量由常规用量的3g减少到0.050g,反应时间缩短到1min左右,这样更易于找到最佳的反应条件。
将常规试管改为Φ7×85mm的硬质玻璃管,微缩后的氧化铜很容易被还原为光亮的铜镜。采用微型实验能节省药品,减少废弃物的排放,显著提高了实验效果。微型实验仪器精致小巧,很适合学生分组实验。另外从环境保护和节约资源的角度出发,这样也有助于培养学生的环保意识。
一、实验仪器与试剂
Φ7×85mm硬质玻璃管,陶土塞,酒精喷灯,尖嘴半球型玻璃管[1],乳胶塞,322B微量分析天平,碳粉与氧化铜,新配制的澄清石灰水。
二、实验装置
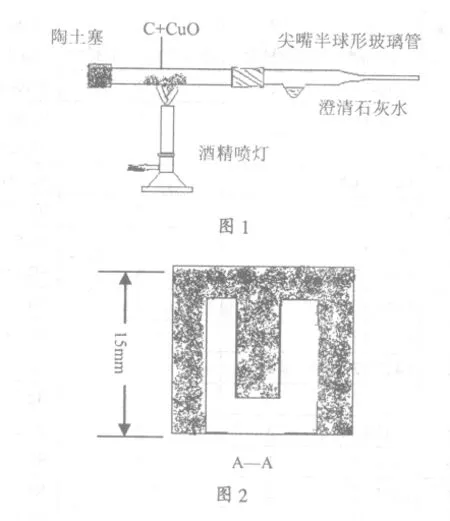
三、实验步骤
1.仪器制作
陶土塞:如图2所示,用陶土做成双层塞晾干后,1000℃焙烧即可。
2.实验方法
(1)将18支称量瓶洗涤,烘干。制备蔗糖脱水炭并研细,烘干活性炭和木炭,研细备用。
(2)按照 m(C)∶m(CuO)=1∶11 的比例分别称取三种碳和氧化铜的混合物研磨10到20 min后分别装入三个称量瓶中,贴上标签。 同样以 1∶11.5、1∶12、1∶12.5、1∶13、1∶13.5的比例分别按照步骤(2)称取研磨后装入称量瓶。将18只称量瓶放入干燥器中。
(3)设计正交试验表,按表格称量反应物进行实验。检测铜和氧化铜的含量。
四、实验数据
1.收率实验因素水平表

表1 收率实验因素水平表
2.收率实验方案表
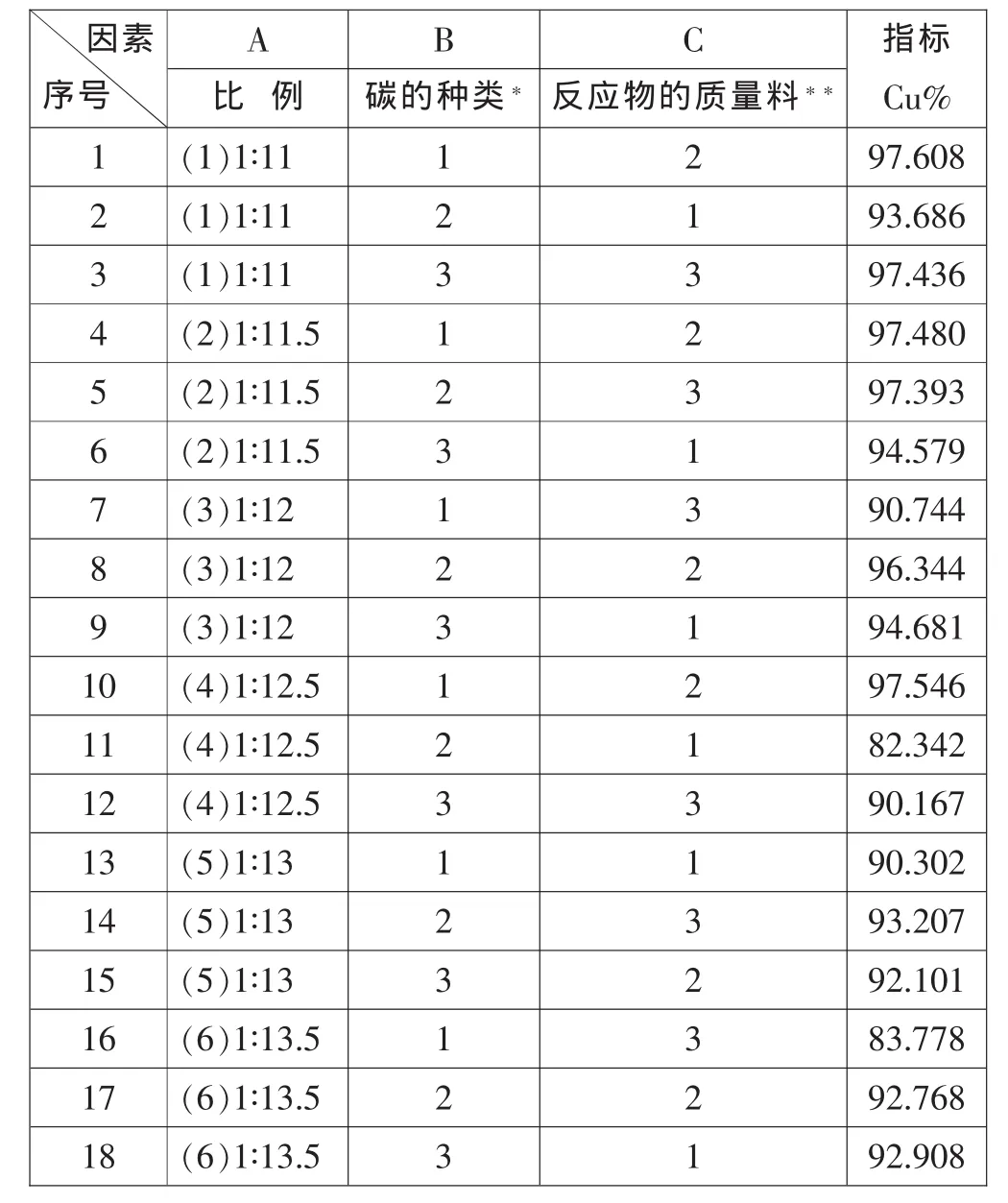
表2 收率实验方案表
3.铜的收率的计算
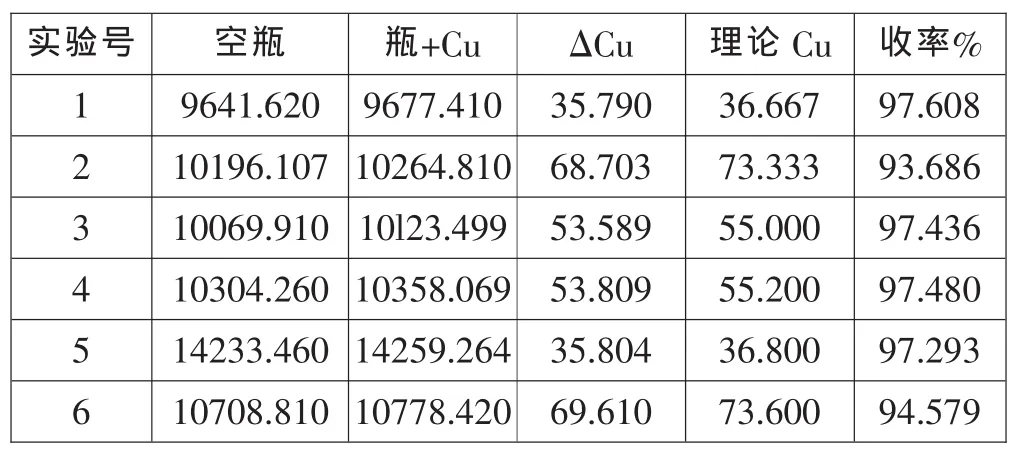
表3 铜的收率的计算

接上表
五、理论分析
在 C(s)+2CuO(s)=2Cu(s)+CO2(g)反应中,

由计算知,△Hθ298<0、△Sθ298>0、△Gθ298<0,从理论上分析,该反应在常温下为自发过程,但实际上该反应在常温下很难进行。在高温体系中,可能存在更多的物质:C、CuO、Cu2O、CO、CO2等,产物之一的二氧化碳与碳又存在如下平衡:CO2+C=2CO,高温下如在900℃,平衡气相组成中一氧化碳占34.0%,而二氧化碳只有0.2%[2],具体反应的热力学计算(数据来自文献[3])如下:

表4 相关反应的热力学数据
由表4知,四种反应均有可能发生,随温度升高,反应更易进行,由于△GθT(1)与△GθT(2)、△GθT(3)与△GθT(4)接近,反应物应含有氧化亚铜和铜,故要求强化还原气氛(即碳量稍多些),使生成的氧化亚铜进一步还原为铜。
六、正交实验的结果分析
1.因素主次的确定
比较三个因素的极差,可见A(即碳与氧化铜的质量比)的极差最大,其次是C(即混合物的总质量),而B(即碳的种类)的极差最小,极差越大,反映该因素水平变动时指标的变化越大,因此可以按照极差的大小顺序排出因素由主到次的顺序为:A→C→B。
2.反应条件的选择原则
将各个因素的好水平组合起来,一段会得到较好的反应条件,但是,我们还应同时考虑因素的主次,在同样满足指标要求的情况下,对一些比较次要的因素可以按照制取方便、价格便宜的原则来选取水平。
3.反应条件的确定
本例中因素A是主要因素,必须取它的好水平A2,因素C是第二重要的因素,取水平C2较好,因素B是次要因素,取水平B2时收率约为90.220%;取水平B1时收率约为89.587%,收率降低不多,但制取蔗糖脱水炭却很麻烦,可取活性炭代替蔗糖脱水炭,因此,A2B2C2或A5B1C2都可能是较好的反应条件,但从实验方便的角度考虑,A2B1C2为最佳的实验条件。
七、讨论
1.碳的选择
通过查阅资料,我发现碳还原氧化铜实验中的碳主要有以下五种:木屑、碳棒、活性炭、蔗糖脱水炭、木炭。经过反复定性实验,选择活性炭、脱水炭、木炭作为一个因素的三个水平。
2.确定比例
碳还原氧化铜实验中,理论值 m(C)∶m(CuO)=1∶13.3,但是按这种比例实验效果并不好,为此我在 1∶11~1∶13.5前后展开, 确定了六种配比进行实验:1∶11、1∶11.5、1∶12、1∶12.5、1∶13、1∶13.5。
3.反应物质量的选择
刚开始, 分别将反应物质量定为 0.003g、0.006g、0.009g,实验后发现效果并不好,实验的产物中几乎都有黑色物质存在,其中0.009g效果稍好。后来,将反应物质量增加到 0.009g、0.018g、0.027g,完成 18 个试验后,由结果看出 0.027g 效果更好, 最后, 选择了 0.050g、0.075g、0.100g作为一个因素的三个不同水平进行正交试验,效果明显。
4.反应装置的选择
由于微型试验中反应物用量少,反应温度高,故采用硬质玻璃管Ф7×85mm制作微型仪器,用酒精喷灯作热源,现象明显,而且不会破裂,玻璃管可以反复使用。
5.二氧化碳的检验
采用尖嘴半球型玻璃管检验二氧化碳,因为尖嘴可以使二氧化碳有较长的停留时间,体系与大气相通,而半球型玻璃管易于存放澄清石灰水,此装置检验现象明显,而且可以反复使用。
[1] 王锦化.微型无机化学实验仪器的设计[J].教学仪器与实验,1997,(4)
[2] 叶大论.实用无机物热力学数据手册[M].北京:冶金工业出版社,2002
[3] 陈达辉,龙光宇.碳还原氧化铜实验的改进[J].实验教学与仪器,1994,(Z1)
[4] 向庆华,李慈.用木炭和氧化铜做“铜热剂”实验[J].化学教学,1999,(12)
[5] 傅献彩,沈文霞,姚天扬.物理化学[M].北京:高等教育出版社,1990.5
[6] 董耀华.炭还原氧化铜的实验探讨与改进[J].教学仪器与实验,2000,(11)
