重视生成性问题 提高课堂实效
2011-07-17林亮
林 亮
(江苏省灌云高级中学 江苏 灌云 222200)
新课程标准认为,教学过程是开放的,不是封闭的;是生成的,不是预设的。是不可重复的激情和智慧的综合生成过程。一堂课,无论课前设计准备得多么充分,但是,在实施教学的过程中,都可能会有意见分歧,甚至出现一些意外或突发事件。如果为了完成教学任务,对此置之不理或极力掩饰,那只会扼杀学生的创新精神;而笔者认为突发生成性问题可能是课堂教学的催化剂和助推剂,如果因势利导处理得当,充分地用好课堂上生成性的问题,则可以使整个课堂充满生命活力,将使课堂教学更富有激情与智慧,必然能提高化学课堂教学的实效性。
所谓生成性问题教学是指教师在课堂上不机械地按原先确定的预设思路教学,而是重视师生生命活动的多样性和教学环境的复杂性,根据学生学习的情况,把教与学过程中的各种因素有机地组合起来,如在师生互动过程中产生的突发性的问题、新的情景,思维的碰撞、意见的分歧、情感的交融等,从而灵活地调整、生成新的超出原计划的教学流程。生成性的课堂教学中,教师虽然事先也有设计,但是随时准备修改自己的讲课内容与讲课思路,只以学生是否有所思、有所得为准,而不企求必须完成教学计划,更不把自己原来的设计强加于学生。
传统的教学过分强调预设,它反映的是僵化封闭的课程观和知识传递式的“填鸭式”教学观。从笔者近十几年的教学经验来看,这种课堂教学模式远远不能满足学生的学习“胃口”,它使学生的发展受到很多限制,使学生的生命力得不到充分发挥,教学效果大大降低,已不适应时代的要求。新课程理念要求重视课堂教学中生成性问题的教学,让课堂教学更富有激情与智慧,学生学习充满活力,真正提高化学课堂中教学的实效性。下面笔者就课堂教学中的体会谈谈如何重视生成性问题的教学来提高课堂教学的实效性。
一、鼓励提问,在学生质疑中重视生成性问题的教学
“学贵有疑”。疑是汲取知识的动力,有疑惑才有探求,才有积极主动的思维活动。课堂教学是千变万化的,再好的预设也不可能预见课堂上可能出现的所有情况。在具体实施教案时,课堂经常会被学生的一些意想不到的发现、疑问所打断。随着学生课堂主体性、自主性的增强,学生质疑、反驳、争论的机会大大增多,就会提出各种各样的问题,或对同一个知识多角度提出问题。这一切都需要教师学会倾听,成为学生的忠实“听众”,并在倾听过程中鼓励他们提出问题,并发现他们困惑的焦点、理解的偏差、观点的创意、批评的价值,这些“意外”或许会打乱教学的节奏,但许多不曾预约的精彩也会不期而至,从而使学生在不断的生成过程中得以发展。
例如:在必修1教材中讲到《几种重要的金属化合物》中过氧化钠的化学性质时,在推断Na2O2和H2O反应的产物,为了向学生证明有NaOH生成,做了如下实验:向Na2O2和H2O反应后的试管中滴加酚酞,振荡,预期的现象是出现红色来证明有NaOH生成。但是真正在实际操作中却出现了如下现象:溶液先变红,后褪色。学生困惑:溶液变红是因为反应中生成了NaOH,那为什么会褪色呢?对这个意外的现象,可以鼓励学生从不同的角度思考,查找原因:褪色可能的原因是什么?如何通过实验来证明你的假设是否成立呢?
引导猜测:可能的原因是什么?并为学生提供如下参考资料:Na2O2+2H2O=2NaOH+2H2O2
如:以下假设进行论证。
①温度过高;②被反应中生成的氧气氧化;③可能碱液浓度过大;④被反应过程中生成的H2O2氧化。
设计方案、实验论证、记录现象:
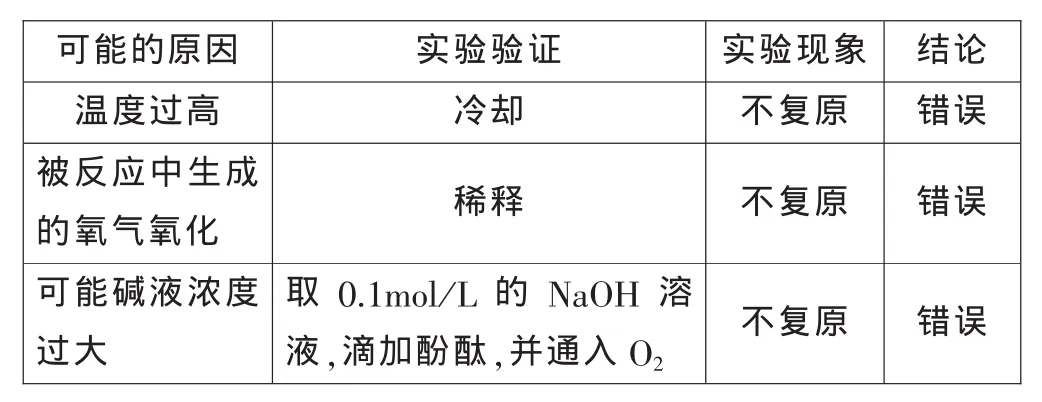
可能的原因 实验验证 实验现象 结论温度过高 冷却 不复原 错误被反应中生成的氧气氧化 稀释 不复原 错误可能碱液浓度过大取 0.1mol/L 的 NaOH 溶液,滴加酚酞,并通入O2不复原 错误

可能的原因 实验验证 实验现象 结论被反应过程中生成的H2O2氧化取 0.1mol/L 的 NaOH 溶液,滴加酚酞,并通入H2O2褪色 正确结论 溶液褪色是因为反应过程中生成的H2O2漂白的结果
学习过程中产生疑问是学生积极思维的表现,因此教师应该鼓励学生提出问题,并留给学生提出问题的空间,不能因为学生打断了教学进程而批评学生。不妨引导学生共同探究解决,这正是最生动的问题解决教学。
二、敢于放手,在学生的错误中实现的生成性教学
教学过程即是暴露学生各种错误、障碍和矛盾的过程,又是展示学生聪明才智、形成独特个性的过程。在课堂教学中教师要敢于放手,让课堂真正成为学生的表演的舞台,成为课堂中的主人。只有这样,学生的主体作用才真正发挥出来。在这样开放性的动态教学过程中,学生的思想激烈奔放,智慧与错误并存在,此时,老师的引导作用也要及时体现出来,要认识到学生的错误也是一种教学资源,在与学生的错误辨析中实现教学的生成。对学生的错误的认识,教师要正确面对,教师应该理解学生的错误,正因为出错,才会有点拨、引导,才会有课堂生成性教学,才会有激情与亮点,才会有教育的机智和智慧。
例如:在学习苏教版选修4电化学这一节有这样一个习题:在电解含有Cu2+、Fe3+两种离子溶液时,通过放电顺序比较金属的活泼性。现象是阴极没有得到红色的单质铜;学生总结:说明Fe3+比Cu2+更容易在阴极得到电子,所以铜的金属活泼性比铁强?让有的同学则反对:认为与金属性活动顺序表相矛盾。很显然前者是错误的,但是在这种情况下老师要做的,不只是指出错误就完事,最关键是要引导学生,抓住这个“错误”所生成的问题,激发学生的探究激情,逐步分析出错误原因所在及正确答案。比较铁和铜的活泼性,应该比较的是Cu2+、Fe2+得电子的能力大小,而不能用Fe3+;显然Cu2+比Fe2+更容易得电子,便可得出两者的金属性强弱,与活动顺序表一致。同时,笔者课堂上又补充了电镀锌“反常情况”:按照放电顺序,Zn2+的放电能力不如H+,但是在真正工业生产中,可以实现Zn2+得电子。原因是单个的Zn2+得电子能力是不如H+,但是可以提高Zn2+的浓度,提高Zn2+得电子的机率,从而实现镀锌。
从这个事例可以看出,课堂上的学生的“错误”往往是教学生成资源,所以老师要敢于放手,让问题在交流中生成,在讨论中解决,从而不仅能顺利完成教学任务,更能拓宽教学视野,提高课堂的效率,提升学生的能力。
三、注重探究,在实验意外中重视生成性教学
著名教育家布鲁姆说过,人们无法预料教学所产生的成果的全部范围。没有预料不到的成果,教学也就不成为一种艺术了。课堂中的许多突发事件,是课程的资源。尤其是在化学实验课上,影响化学“实验的因素是多元的,除了常有的“异常现象”、稍纵即逝的“短暂现象”等出现之外,失败的几率相对也比较高。有些演示实验,在课堂上意外地失败了。教师对情况的处理得当与否,很大程度反映了教师思想观念的新旧与应变能力的高下。如果极力掩饰,则可能误了学生;如果能因势利导,组织学生共同探究失败的原因,则能及时扭转被动局面,收到意外的效果。
例如:在演示“二氧化硫使品红褪色”实验时为了帮助学生理解浓H2SO4的强氧化性,把浓H2SO4与Cu片在加热条件下产生的SO2通入品红溶液,红色很快褪去;为了让学生多看一会,通SO2没有停止,结果“意外”发生了,红色又恢复了。学生一片惊呼!我也很诧异。本来可以简单说明,完成预定的教学目标,但是此时学生感兴趣是“颜色”又怎么恢复了?他们觉得现象出乎意料、不可思议。学生正处于期盼、渴知、欲罢不能的心理状态,这是保护学生好奇心、激发求知欲和训练思维方法的良好时机。于是我就改变了教学的预设,组织学生充分思考:“颜色”恢复的原因可能是什么?如何证实你的猜测?学生经过一番激烈讨论,最后形成一致结论:SO2与品红溶液生成的不稳定无色物质,在受热情况下,又会恢复原来的颜色。这个实验中浓H2SO4与Cu片在加热条件下产生的SO2气体温度较高,促使无色物质分解而恢复了原有的颜色。我觉得时机已成熟,进一步引导学生思考与探究:如何设计实验证明是热的SO2使褪色的品红又恢复的呢?学生分组讨论,设计两种方案:一是直接在原有的装置加上一个冷凝管;二是改用Na2SO3与稀H2SO4,这样产生的SO2温度就不高了。按照学生的方案所言,上述的结论是正确的。
应该说“意外”的偶然性背后必有其必然性。通过上述教学生成可以说明,学生不仅深化巩固了已有的相关知识,同时也学会了怎样面对出其不意的新问题,切身体验到科学探究最基本的思想和方法。 虽没有完成预设的教学内容,但整个过程学生都很投入,处于一种积极的思维状态中,“浪费”一些时间应该还是值得的。
教学的生成性要求教师充分发挥主观能动性,不断提高自身业务素质,提高课堂教学的开放程度,有意识地对自己的课堂教学行为进行审视和反思,及时修订、更改、充实、完善自己的教学设计和方案,做到“腹中有案,行中无案”,寓有形的预设于无形的、动态的教学中,随时把握促使课堂教学动态生成的切人点,并有效地加以利用,使教学活动成为生成教学智慧和增强实践能力的过程并重视加以利用,从而真实地提高课堂教学的实效性。
但强调教学的生成并不否定教学的预设,充分的预设是课堂教学动态生成的保证。因为教学首先是一个有目标、有计划的活动,教师必须在课前对自己的教学任务有一个清晰、理性的思考与安排。生成与预设是教学中的一对矛盾统一体,忽视了教学的预设,就失去了教学的方向,忽视了教学的生成,就忽视了学生的差异,忽视了学生的发展。教师在教学中要重视教学的生成,但对价值不大的生成性问题,要及时地排除和处理,使课堂教学回到预设和有效的轨道上来,以保证教学的正确方向。
[1] 吴益平.浅谈化学教学中生成性教育资源的开发[J].化学教学,2004 ,(1-2)
[2] 郭强.一个“意外”引发的“多米诺”效应[J].中学化学教学参考,2010,(5):48-49
