双波长RP-HPLC法测定清开灵胶囊中栀子苷和黄芩苷的含量
2011-05-07师永花
师永花
清开灵组方源于中医治疗急性热病传统处方“温病三宝”中的安宫牛黄丸,由胆酸、猪去氧胆酸、黄芩苷、珍珠母、栀子、水牛角、板蓝根、金银花组成,迄今为止已形成系列产品[1]。中药制剂分析中,多使用反相高效液相色谱法(RP-HPLC)。清开灵胶囊中君药黄芩的黄酮类有效成分为黄芩苷,臣药栀子的环烯醚萜苷类的有效成分为栀子苷。为了更好地控制药品质量,本文采用双波长RP-HPLC法,同时测定该制剂中的栀子苷和黄芩苷含量。
1 仪器与试剂
1.1 实验仪器 Agilent 1200高效液相色谱仪(真空脱气机,四元泵,自动进样器,二级管阵列检测器),色谱柱:Hibor C18键合硅胶柱(4.6 mm×150 mm,5 μm);AS3120型超声波清洗器;Mettler Toledo AB204-S电子分析天平。
1.2 实验试剂 无水甲醇:分析纯、色谱纯,乙腈:色谱纯,水为重蒸馏水;栀子苷对照品:中国药品生物制品检定所,批号:0749-9401供含量测定用;黄芩苷对照品:中国药品生物制品检定所,批号:715-8501,供含量测定用;清开灵胶囊:广州白云山明兴制药有限公司,批号:MM3112、MM3111、MM3113,规格:0.25 g×12粒。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液的制备 精密称取减压干燥至恒重的黄芩苷对照品1.8 mg、栀子苷对照品1.6 mg,分别置于10 mL容量瓶中,加甲醇溶解后,定容至刻度,即得含黄芩苷、栀子苷分别为0.18 mg/mL、0.16 mg/mL的对照品储备溶液。分别精确量取上述标准品溶液,按体积1∶1混合,即得标准品混合溶液,其中栀子苷:0.08 mg/mL;黄芩苷:0.09 mg/mL。
2.1.2 样品溶液的制备 取样品适量,置研钵中研细,取粉末约0.25 g,精密称定,置25 mL容量瓶中,精确加入无水甲醇定容,超声提取30 min,放冷,擦净容量瓶外表水分,补足减失甲醇重量,摇匀,静置。用被甲醇润洗的注射器吸取适量上清液,再用0.45 μm的微孔滤膜滤过,取续滤液,即得。
2.1.3 阴性样品溶液的制备 分别制备不含黄芩、栀子阴性对照样品,并按供试品溶液的制备方法制备阴性对照溶液。
2.2 色谱条件 色谱柱:Hibor C18键合硅胶柱(4.6 mm ×160 mm,5 μm)。流动相:A 相为0.2%磷酸水溶液,B相为乙腈。梯度洗脱程序:0~10 min时,流动相为B相-A相(12∶88),流速:0.8 mL/min;10 min之后,流动相为B相-A相(25∶75),流速:1.0 mL/min。检测波长分别为240 nm(栀子苷)、278 nm(黄芩苷)。柱温:30℃。流动相梯度洗脱配比和流速数据见表1。
2.3 专属性试验 取对照品混合溶液、各阴性样品溶液、样品溶液,在上述色谱条件下分别进样分析。结果表明,在样品溶液色谱图中,有与对照品混合溶液栀子苷、黄芩苷保留时间一致的特征峰,保留时间分别为7.50 min、16.00 min,阴性样品无此特征峰,表明阴性样品对所测组分无干扰。色谱图见图1、图2。

表1 流动相梯度洗脱配比和流速数据(%)

图1 240 nm处色谱图注:A对照品,B样品,C缺桅子阴性样品;1桅子苷,2黄芩苷

图2 278 nm处色谱图注:A对照品,B样品,C缺黄芩阴性样品;1桅子苷,2黄芩苷
2.4 线性关系考察 分别精密吸取标准品混合溶液 2.0、4.0、6.0、8.0、10.0、12.0、30.0 μL,按“2.3”所述色谱条件分别进样分析,记录峰面积,以峰面积积分值Y为纵坐标、进样量X(μg)为横坐标,绘制标准曲线并进行线性回归,栀子苷回归方程:Y=1 417.7X+81.31,相关系数r=0.999 7(n=7);黄芩苷回归方程:Y=2 580.2X+40.314,相关系数r=0.999 9。结果表明,栀子苷在0.16~2.4 μg范围内线性关系良好,黄芩苷在0.18~2.7 μg范围内线性关系良好。
2.5 精密度试验 分别取同一浓度对照品溶液,按“2.3”所述色谱条件,自动重复进样6次,进样量6 μL,记录色谱图,结果如表3。栀子苷峰面积RSD为0.31%,黄芩苷峰面积RSD为0.19%。表明仪器和方法精密度良好。
2.6 重现性试验 分别精密称取同一批号(MM3112)样品6份,按“2.1.2”样品溶液的制备方法制备溶液。精密吸取制备好的样品溶液6 μL,在“2.3”所述色谱条件下分别进样,记录栀子苷和黄芩苷的峰面积,计算样品含量。结果,栀子苷的 RSD值为0.78%,黄芩苷的 RSD值为0.04%,表明样品和实验方法重复性好。
2.7 稳定性试验 取配置好的同一批号(MM3112)清开灵胶囊样品溶液,室温下放置,分别于制备后 0、2、4、6、8h各进一次样,进样量为6 μL。记录栀子苷和黄芩苷的峰面积,计算栀子苷的RSD值为0.79%,黄芩苷的RSD值为0.04%。结果表明,样品溶液在8h内稳定性良好。
2.8 含量测定 分别取3批不同批号(MM3112、MM3111、MM3113)的清开灵胶囊,样品量分别为0.250 5 g、0.250 9 g、0.250 1 g,去壳研细,按“2.1.2”样品溶液的制备方法制备。样品溶液进样量为6 μL,在“2.3”所述色谱条件下分别进样2次,记录栀子苷和黄芩苷的峰面积,计算每1 g样品中所含栀子苷和黄芩苷的量(mg/g),结果如表 2所示。
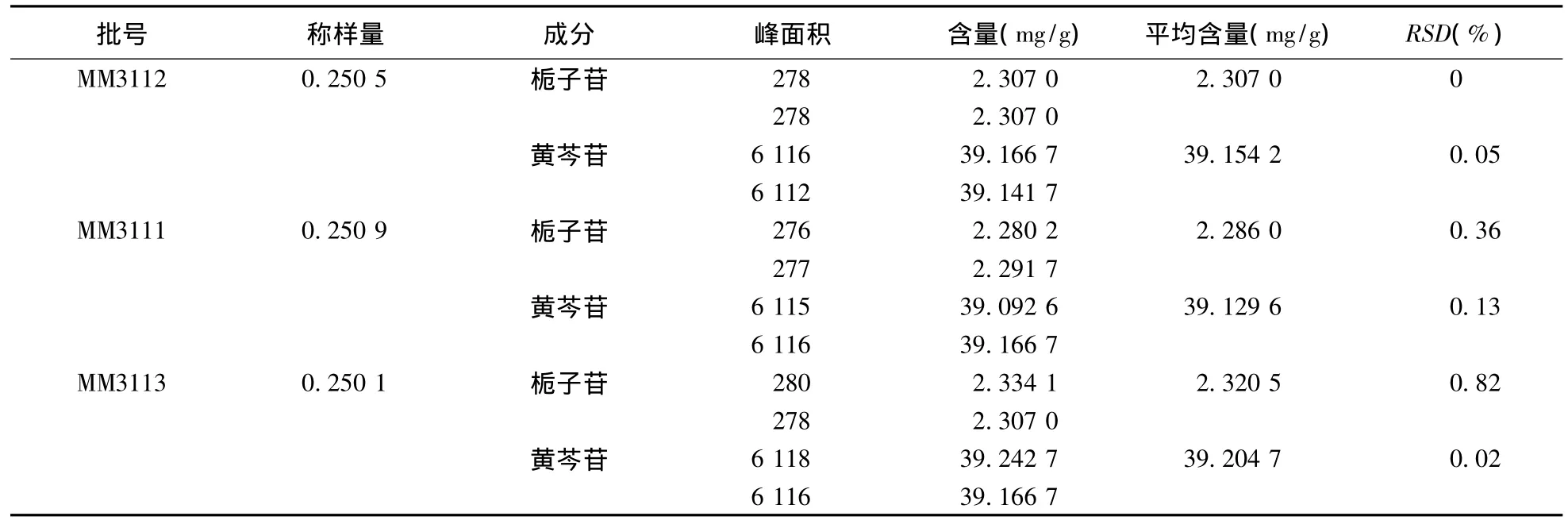
表2 样品含量测定结果
若将含量单位换算为mg/mL,则含栀子苷2.307 0mg/g的样品,含栀子苷的量为0.023 12 mg/mL;含黄芩苷39.154 2 mg/g的样品,含黄芩苷的量为0.392 5 mg/mL。
2.9 加样回收率实验 取已知含量同一批号(MM3112)的样品约0.12 g,精密称定,置25mL量瓶中,按“2.1.2”样品溶液制备方法制备样品溶液,取上述溶液2 mL(含栀子苷0.023 08 mg、黄芩苷约0.391 8 mg),置10 mL量瓶中,加栀子苷对照品储备液0.2 mL、黄芩苷对照品储备液2.0 mL,加无水甲醇定容。用0.45 μm的微孔滤膜滤过,取续滤液,按“2.3”所述色谱条件测定,进样分析,进样量20 μL,记录峰面积,计算回收率。栀子苷的平均加样回收率为96.94%,RSD为2.08%;黄芩苷的平均加样回收率为100.18%,RSD为2.01%,证明上述方法可靠。
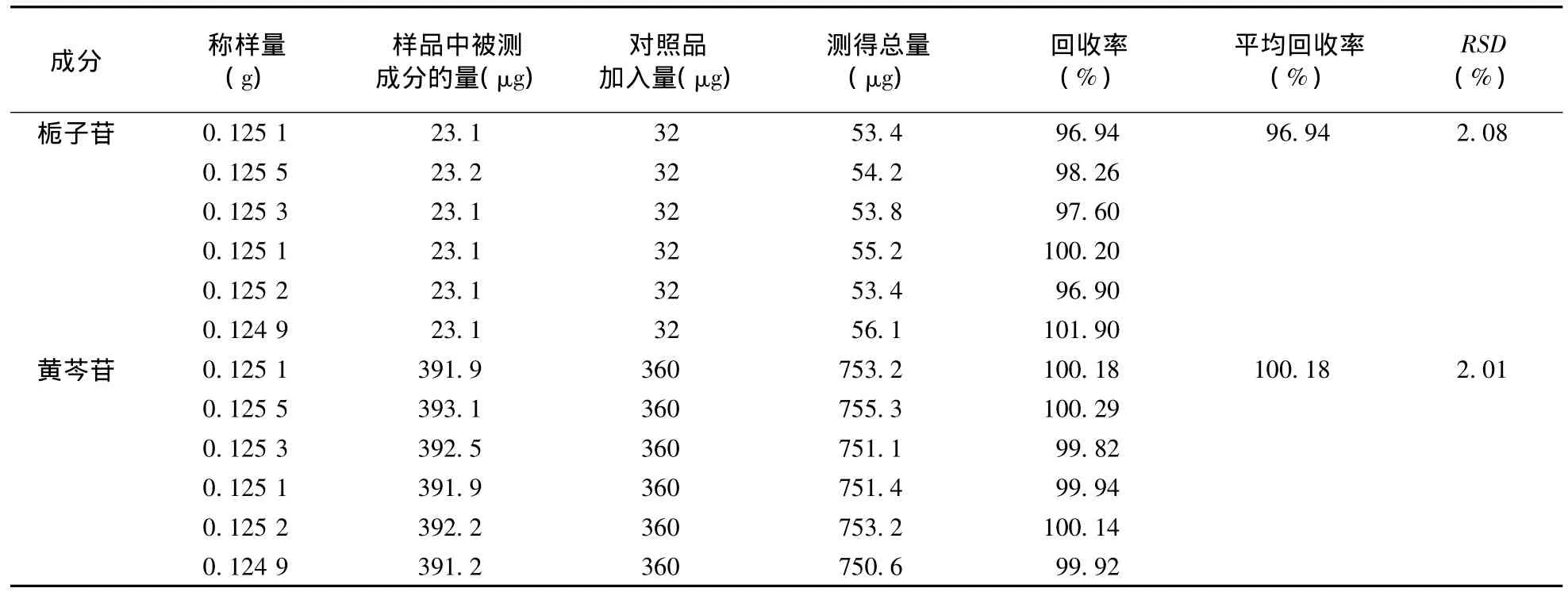
表3 加样回收率实验(n=6)
3 讨论
3.1 流动相的选择 实验过程中选用过很多色谱条件进行预实验,包括乙腈-水、甲醇-水、甲醇-0.2%磷酸水溶液等,但是分离效果都不好,目标成分和其他杂质成分分不开。实验过程中发现,流动相中乙腈的比例越高,洗脱能力越强,对化合物的选择性越高,分离出化合物越精细。但流动相中乙腈的比例过高,会导致样品液中各化合物过早出峰,不能完全分开,因此,只能运用梯度洗脱,通过预实验提高流动相中乙腈的比例,增大流动相流速,使各化合物先后出峰,找到最佳的有效成分分离条件。实验中选择乙腈-0.2%磷酸为流动相,栀子苷保留时间在7.5 min,黄芩苷保留时间在16.0 min。

图3 栀子苷色谱图
3.2 检测波长的选择 检测波长的选择会影响到色谱分析的结果,本实验采用二极管阵列检测器。据二极管阵列检测器吸收光谱图可以看出,栀子苷在240 nm处有最大吸收(见图3),黄芩苷在275 nm处有最大吸收(见图4)[2],所以实验中采用240 nm、278 nm为检测波长。
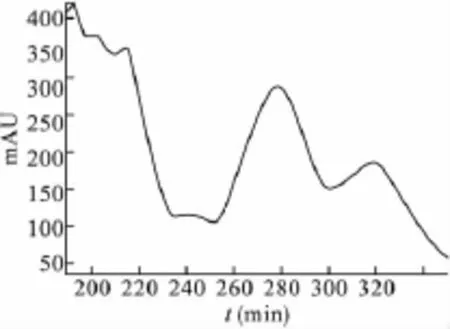
图4 黄芩苷色谱图
3.3 溶剂的选择 栀子苷易溶于水,溶于甲醇;黄芩苷微溶于水,溶于甲醇。实验中分别用30%、50%、70%和100%的甲醇溶液作为溶剂,进行超声提取,分别进样并记录色谱图,发现用70%的甲醇水溶液作为溶剂提取效果较好;黄芩苷在甲醇、水中的溶解度较小[2],所以在配制黄芩苷标样时浓度不宜太大。
3.4 提取时间的选择 实验时将研细后的药品用70%的甲醇(分析纯)转移,置于25 mL的容量瓶中,分别用超声仪提取20 min、30 min、40 min、60 min。通过比较发现,提取30 min的效果比提取20 min的效果好,和提取40 min效果一样。而提取60 min的样品分离出了太多杂质,影响样品的测定,所以,所有样品均超声提取30 min。
[1] 张妙媛,姚金成,赵绪元,等.清开灵不同制剂的高效液相指纹特征比较[J].时珍国医国药,2007,18(2):442-443.
[2] 国家药典委员会,中华人民共和国药典,2005年版(一部)[S].北京:化学工业出版社,2000:586,248.
