配位对二氢杨梅素晶体结构与抗氧化活性的影响
2011-04-01俞思明朱思明于淑娟林景聪
俞思明,朱思明*,于淑娟,林景聪,许 敏
(华南理工大学轻工与食品学院,广东 广州 510640)
配位对二氢杨梅素晶体结构与抗氧化活性的影响
俞思明,朱思明*,于淑娟,林景聪,许 敏
(华南理工大学轻工与食品学院,广东 广州 510640)
食用植物有效成分的非晶化配位可能会产生新的或更好的药物活性。本实验研究二氢杨梅素(DMY)与Cu配位的优化工艺条件、配位前后DMY的晶体结构和抗氧化活性的变化。结果表明:DMY与Cu配合的最佳工艺条件为40℃、反应时间60min、pH 9.5;配位后DMY的UV-Vis光谱最大吸收峰由292nm红移至332nm;经理论化学计算和FT-IR光谱证实,DMY的4位羰基和5位羟基O原子参与配位;配合物对羟自由基(·OH)的清除能力提高,这可能和配位后DMY出现的非晶化现象有关。
二氢杨梅素(DMY);Cu;配合物;抗氧化
食用植物有效成分配位后可能产生新的或更好的药物活性,中药配合物新药是中药新药研制的新方向[1]。据文献报道,某些食用植物有效成分的非晶化往往会提高其生物活性[2]。二氢杨梅素(3,5,7,3',4',5'-六羟基2,3-双氢黄酮醇,dihydromyricetin,DMY),又称蛇葡萄素,双氢杨梅素,是一类双氢黄酮醇类化合物[3]。其结构式见图l。在显齿蛇葡萄属植物中(如藤茶,主要分布于长江流域以南的广东、广西等地)其含量高达20%[4]。有关研究表明DMY具有清除氧自由基,防止油脂食品氧化变质及消炎、抑菌、降脂、抗肿瘤等生理活性[5-6]。有学者认为二氢杨梅素可以螯合金属离子并且螯合作用发生在3-羟基-4-羰基上或3',4'酚羟基上,从而消除金属离子对自由基氧化的催化作用[7-8]。国内外对DMY与铁、锌离子的螯合产物的研究已经很多。但是,有关DMY与Cu螯合产物的晶体结构、抗氧化性变化及两者之间关系的研究报道还较少,缺乏系统性的研究。
本实验探讨人体必需微量元素Cu与DMY的配合的最佳工艺条件,以及配位前后DMY抗氧化活性的变化和晶体结构变化,以期改善配体DMY的生物活性或发现新的生物活性,寻找DMY配位后反应活性变化的非晶化根据。
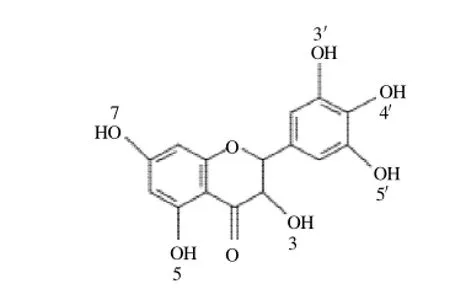
图1 二氢杨梅素的化学结构Fig.1 Chemical structure of dihydromyricetin (DMY)
1 材料与方法
1.1 材料、试剂与仪器
二氢杨梅素 参考文献[9]自制;无水乙醇 天津市凯通化学试剂有限公司;碳酸钠、氯化铜 天津市科茂化学试剂有限公司。
S11-2恒温水浴锅 上海跃进医疗器械厂;LDA-2A真空干燥箱 上海一恒科技有限公司;TU-1810 型紫外-可见分光光度计 北京普析通用仪器有限公司;FT-IR-650傅里叶红外光谱仪 天津港东科技发展股份有限公司;D8 ADVANCE XRD仪 德国Bruker公司。
1.2 方法
1.2.1 DMY-Cu配合物合成的单因素试验
1.2.1.1 反应pH值的确定
DMY在碱性条件下易与金属离子发生配合反应产生沉淀,但其在强碱作用下会发生彻底的不可逆解环[10],因此仅考察pH值范围8.0~10.0。将1.0×10-3mol/L的DMY乙醇溶液与等物质的量浓度等体积的CuCl2-乙醇溶液在带三口烧瓶(带搅拌和冷凝)中,在反应温度40℃和反应时间60min条件下进行试验,探讨pH值对配合反应的影响。反应液中会产生配合物的沉淀,根据离心分离后上清液的OD332nm(332nm是DMY-Cu配合物的特征吸收波长)大小确定最佳反应pH值。上清液于紫外-可见分光光度计中测定其OD332nm值,以其OD332nm值间接反映产率的大小(上清液的OD332nm反应结晶母液中残留配合物浓度,由于DMY和Cu的配比完全一致,则OD332nm越大,反应溶液中残留配合物越多,产率越低,下同)。
1.2.1.2 反应时间的确定
试验方法同上。选取反应时间15、30、45、60min和75min,反应pH 9.5,反应温度40℃的条件下进行试验,根据离心分离后上清液的OD332nm大小确定最佳反应时间。
1.2.1.3 反应温度的确定
试验方法同上。选取反应温度40、50、60℃和70℃,在pH9.5,反应时间60min的条件下进行试验,根据离心分离后上清液的OD332nm大小确定最佳反应温度。
1.2.2 二氢杨梅素Cu配合物的制备
在带有搅拌器、干燥管、冷凝管的三口烧瓶中加入0.02mol/L 的DMY的无水乙醇溶液,加入等物质的量的CuCl2的无水乙醇溶液,用5g/100mL的NaOH-乙醇溶液调节pH9.5,于40℃下反应回流lh,产生浅褐色沉淀。反应液冷却至室温后在4000r/min离心10min,分离上清液。沉淀先用乙醇洗涤,再用水洗数次,固体产物在40℃真空干燥箱中干燥即可。
1.2.3 量子化学计算[11]
运用Hyperchem 软件对DMY分子进行结构优化,并进行半经验的全略微分重叠(CNDO/2)计算,根据分子中各O原子所带电荷对DMY分子可能配位位点进行预测。
1.2.4 DMY及DMY-Cu对羟自由基的清除作用测定
在25mL比色管中依次加入3mL 2mmol/L Fe3O4、3mL 1mmol/L H2O2溶液,摇匀,再加入3mL 6mmol/L 水杨酸,摇匀,于37℃水浴加热15min后取出,测其吸光度A0。另取25mL 比色管依次加入3mL 2mmol/L FeSO4、3mL 1mmol/L H2O2溶液,摇匀,分别加入1.5×10-2mol/L待测液0.0、1.0、2.0、3.0mL,于37℃水浴中加热15min后取出,然后再加入6mmol/L 水杨酸溶液3mL,继续水浴加热15min,取出用蒸馏水补充至25mL,摇匀,测其吸光度Ai[12]。
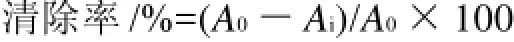
1.2.5 DMY及其Cu配合物的光谱分析和XRD分析
配制DMY及DMY-Cu的乙醇溶液并在200~600nm波长处测定其紫外吸收光谱。取约1mgDMY及其Cu配合物分别与约100mg的KBr在玛瑙研钵中研磨混合均匀,分别取少许上述混合物倒入压片模中,用压片器压制成透明薄片,进行红外光谱分析。在相同条件下使用X 射线衍射仪对DMY及其Cu配合物进行分析。实验条件:Cu靶,40kV,40mA,步长0.02°,扫描速度17.7s/步。
2 结果与分析
2.1 不同工艺条件对配合反应的影响
2.1.1 pH值对配合反应的影响

图2 pH值对配合反应的影响Fig.2 Effect of pH on coordination reaction
由图2可知,pH值对配合反应的影响较大,pH值在8.0~9.0间变化,上清液的OD332nm值急剧下降,说明在碱性条件下有利于配合反应进行,DMY-Cu配合物产率升高;pH 9.5时OD332nm值达到最小,产率达到最大;但当pH值超过9.5时上清液的OD332nm值又开始上升,分析其原因可能是由于pH值过高,DMY的分子结构遭到破坏,配合反应不能顺利进行导致产率下降。
2.1.2 温度对配合反应的影响

图3 温度对配合反应的影响Fig.3 Effect of temperature on coordination reaction
由图3可知,反应温度为40℃,温度升高配合反应正向进行,产率增加;反应温度在40~60℃范围内时,转化率虽增加,但配合物溶解度增加,沉淀量下降,产量下降,这可同任志秋等[13]的结果相验证;反应温度达到70℃后,高温下配合物可能不稳定,变成其他物质,产率下降。
2.1.3 时间对配合反应的影响

图4 时间对配合反应的影响Fig.4 Effect of time on coordination reaction
由图4可知,在15~60min的反应时间范围内,随着反应时间的增加,上清液的OD332nm值逐渐减小,在60min时达到最小值,此时产率达到最大;随着反应时间的进一步增加,上清液的OD332nm值略有增加,产率逐渐降低,分析其原因可能是随着反应时间的延长,出现一定程度的逆反应。
2.2 DMY及其Cu配合物的紫外-可见光谱分析

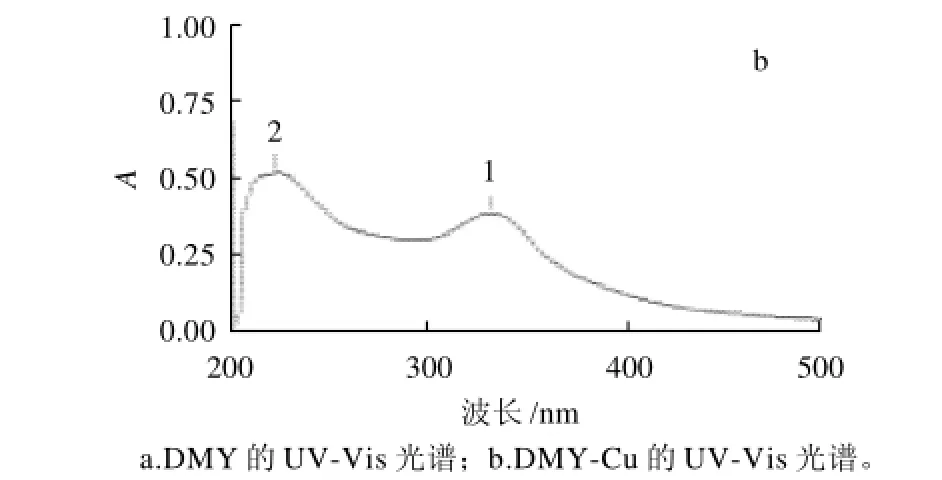
图5 DMY及DMY-Cu的紫外可见光谱图Fig.5 UV-visible spectra of DMY and DMY-Cu complex
由图5可知,DMY在292nm波长处有最大吸收,与Cu配位后,其在332nm波长处出现最大吸收,特征吸收峰发生40nm红移现象,说明有DMY-Cu配合产物的生成。
2.3 DMY及其Cu配合物的红外光谱分析
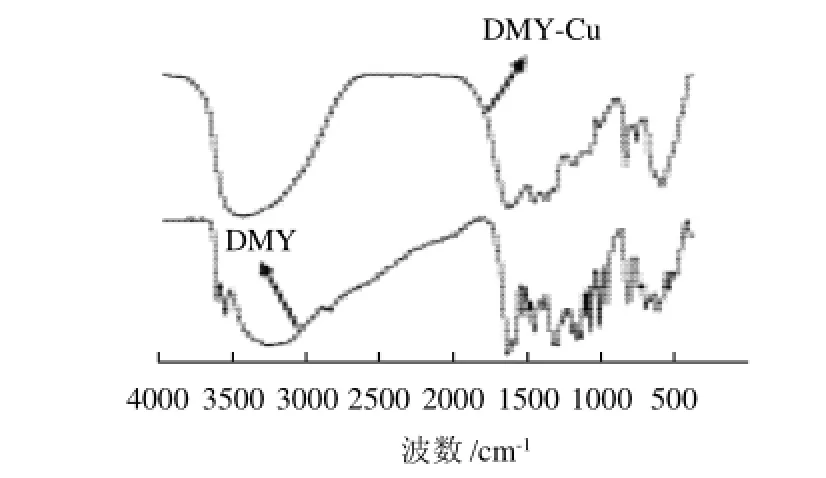
图6 DMY及DMY-Cu配合物的红外光谱Fig.6 FT infrared spectra of DMY and DMY-Cu complex
由图6可知,DMY-Cu配合物在3300~3500cm-1处有强吸收峰,这是O-H的特征峰,说明配合物中酚羟基的存在,但吸收峰的宽度没有DMY宽,说明DMY-Cu配合物中酚羟基数可能比DMY中少;DMY-Cu配合物在1467cm-1处仍存在强吸收峰,在芳环骨架振动C=C频率区1450~1600cm-1内,说明DMY-Cu苯环结构还存在;分子中C-O-C键的振动频率(1050~1250cm-1)基本未变,表明DMY的C环醚键在选用配位条件下未发生开环;DMY在1644cm-1处有强吸收峰,这是4位羰基产生的强吸收峰,DMY和Cu形成DMY-Cu后,由于金属的配合作用,降低了4位羰基上碳氧原子的电子云密度,使碳氧双键减弱,吸收峰的位置移至1626cm-1处。同时,在指纹区601cm-1处出现新的强吸收峰,这是M-O键的吸收峰,说明确实有DMY-Cu配合物的生成。
2.4 DMY配位位点的量子化学计算分析
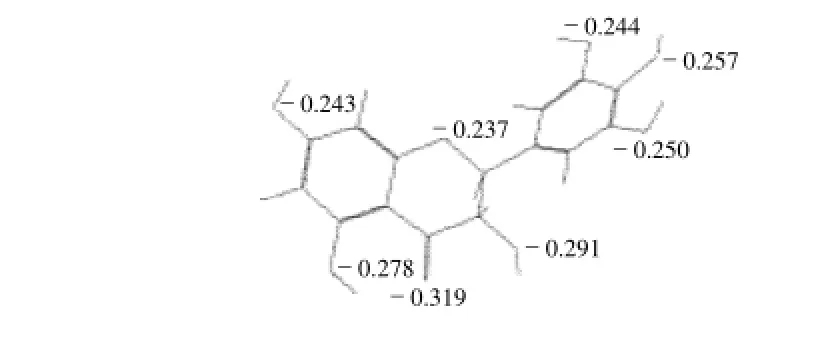
图7 计算后DMY分子的化学结构Fig.7 Chemical structure of DMY after theoretical quantum chemistry calculation
由图7可知,4位羰基O原子所带电荷为-0.319(相对电荷,相当于一个电子所带电荷的0.319倍,下同),在8个O原子的电荷值中最大,故预测DMY分子中4位羰基O原子肯定参与了配位,这可从2.3节的红外光谱分析中得到验证。另外,3位羟基和5位羟基O原子电荷值分别为-0.291和-0.278,明显大于其他O原子电荷值,故3位和5位羟基O原子是可能的配位位点。据文献[10]和[14]报道,DMY能以4位羰基和5位羟基与Zn和Cu配位,DMY与Cu配位的物质的量比为1:1,以4位羰基和5位羟基与Cu配位, 这与A环和4位羰基的π-π共轭有关。
2.5 DMY及DMY-Cu的XRD分析
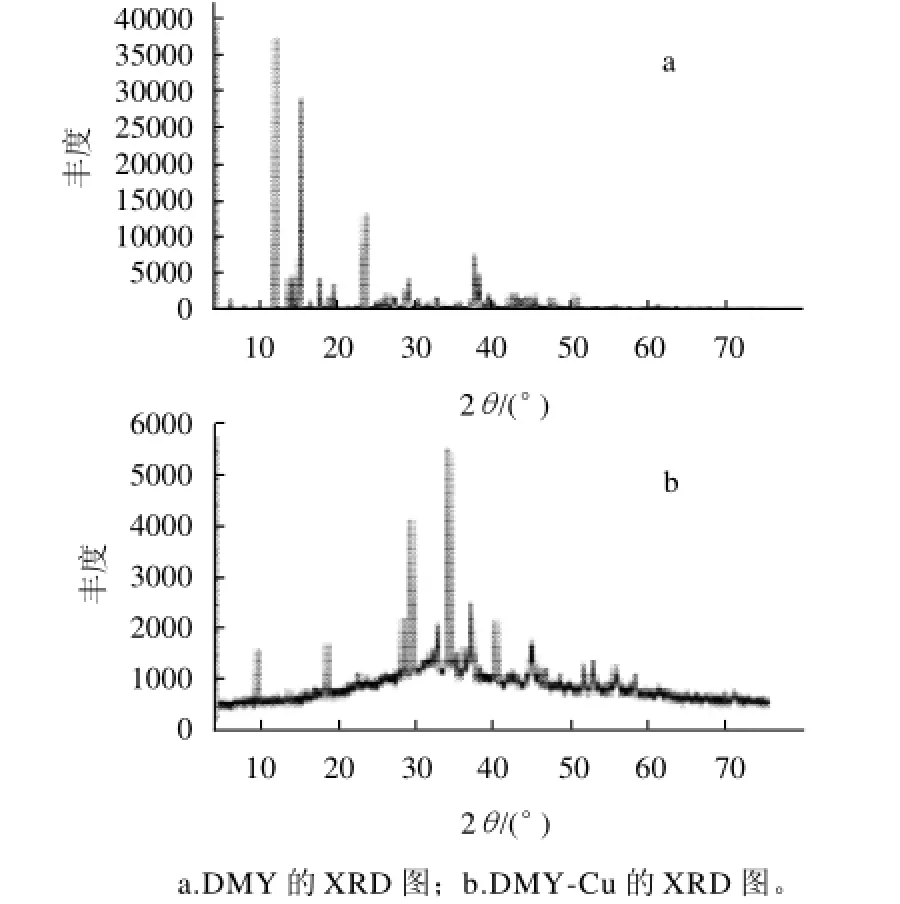
图8 DMY及其Cu配合物的衍射图谱Fig.8 XRD spectra of DMY and DMY-Cu complex
由图8可知,DMY在2θ为11.376°、14.589°和22.948°处有强衍射峰,而DMY-Cu的特征衍射峰出现在2θ为28.982°、33.787°处,而DMY在此处却无衍射峰,说明DMY与Cu发生了配位反应。而且,DMY和Cu配位后,出现弥散衍射特征,而DMY的XRD图中仅有尖峰衍射特征,说明DMY与Cu配位后出现非晶化现象[15]。
2.6 DMY及DMY-Cu对羟自由基的清除作用测定
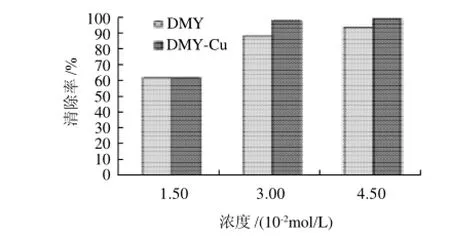
图9 DMY及DMY-Cu配合物对·OH的清除率Fig.9 Scavenging rates of DMY and DMY-Cu against hydroxyl free radicals
由图9可知,DMY及DMY-Cu对·OH有很好的清除效果,且清除效果随浓度的增大而增大。当浓度在1.5×10-2mol/L时,两者的清除率是一样的,但当浓度大于1.5×10-2mol/L时,DMY-Cu的清除效果优于DMY。分析其原因可能是DMY-Cu配合物有类似超氧化物歧化酶(SOD)的活性,并消除了金属离子对自由基氧化的催化作用;另外,DMY与Cu配位后的非晶化现象也是可能的原因。
3 结 论
3.1 通过单因素试验确定DMY-Cu配合反应的最佳工艺条件是温度40℃、pH9.5、反应时间为60min。
3.2 UV-Vis、XRD、FT-IR和理论量子化学计算分析结果表明,DMY的5位羟基和4位羰基与Cu发生非晶化配位。在实验条件下,DMY的C环没有开环,还有部分羟基未参与配位。
3.3 实验证明DMY-Cu配合物对·OH具有很好的清除能力,且清除效果明显优于DMY,即与DMY-Cu配合物的抗氧化能力优于DMY。这可能DMY配位后的非晶化以及DMY-Cu有类似超氧化物歧化酶活性有关。
[1] 周小华. 从柑橘加工废水中吸附回收橙皮苷[J]. 离子交换与吸附, 1994(5): 434-437.
[2] 秦慧明, 朱思明, 于淑娟. 橙皮苷及Cu配合物的抑菌抗氧化性研究[J]. 食品科技, 2006(6): 80-83.
[3] 林淑英, 高建华, 郭清泉, 等. 二氢杨梅素的稳定性及其影响因素[J].无锡轻工大学学报, 2004, 23(2): 17-21.
[4] 张友胜, 杨伟丽, 熊皓平. 显齿蛇葡萄基本成分研究[J]. 天然产物研究与开发, 2001, 13(5): 46-49.
[5] 李卫, 宁正祥. 逆流法提取二氢杨梅素研究[J]. 食品科学, 2004, 25 (11): 192-194.
[6] 李卫, 郑成, 宁正祥. 二氢杨梅素月桂酸酯在猪油中的抗氧化性研究[J]. 食品科学, 2005, 26 (9): 73-76.
[7] 林淑英. 显齿蛇葡萄中二氢杨梅素的提取纯化急抗氧化活性研究[D].华南理工大学, 2004.
[8] 李卫, 宁正祥. 黄酮类化合物的分子修饰[J]. 食品科学, 2005, 26(8): 505-507.
[9] ZIBELL S E. Chewing gum containing zein coated high-protency sweetener and method: US, 4863745[P]. 1989-06-29.
[10] 吴春, 郑新平, 车春波. 二氢杨梅素与锌配合反应的研究[J]. 化学与粘合, 2009, 31(4): 31-33.
[11] 刘本国, 杨继国, 郭烨, 等. 基于量子化学分析的类黄酮抗氧化功能区划分[J]. 食品科学, 2010, 31(15): 167-170.
[12] 张燕平, 戴志远. 紫苏提取物体外清除自由基能力的研究[J]. 食品工业科技, 2003, 24(10): 67-70.
[13] 任志秋, 陈平. 橙皮苷锌配合物合成及清除自由基能力的研究[J]. 哈尔滨商业大学学学报: 自然科学版, 2009, 25(6): 688-693.
[14] 严赞开, 陈冬丹. 二氢杨梅素Cu配合物的合成及其与牛血清白蛋白的相互作用[J]. 江西师范大学学报:自然科学版, 2009, 33(2): 175-179.
[15] 梁勇. 非晶颗粒态淀粉及其生物与化学反应活性研究[D]. 广州: 华南理工大学.
Effect of Coordination on Crystal Structure and Antioxidant Activity of Dihydromyricetin
YU Si-ming,ZHU Si-ming*,YU Shu-juan,LIN Jing-cong,XU Min
(College of Light Industry and Food Sciences, South China University of Technology, Guangzhou 510640, China)
Non-crystallization coordination of bioactive ingredients in edible plants can generate new or better pharmacological activity. In this paper, the optimal reaction conditions between dihydromyricetin (DMY) and Cu2+, the effect of coordination on the crystal structure and antioxidant activity of DMY were investigated. Results indicated that the optimal reaction conditions were reaction temperature of 40 ℃, reaction time of 60 min and reaction pH of 9.5. The characteristic absorption peaks were 332 nm for DMY-Cu complex and 292 nm for DMY, which may be ascribed to the oxygen from 4 carbonyl and 5 hydroxyl groups participated in coordination according to FT-IR analysis and theoretical chemical calculation of DMY or its complex. In addition, the scavenging capability of DMY against hydroxyl free radicals (·OH) was increased due to the non-crystallization coordination according to XRD analysis of DMY and its complex.
DMY;Cu;complex;antioxidation
O623.54
A
1002-6630(2011)07-0034-04
2010-05-26
广东省科技计划项目 (2008A080403009);2008—2009年度学生研究计划(SRP)项目(Y1090070)
俞思明(1985—),男,硕士研究生,主要从事制糖工程研究。E-mail:tayiya@126.com
*通信作者:朱思明(1976—),男,讲师,博士,主要从事植物有效成分的资源利用和化学改性研究。
E-mail:lfsmzhu@scut.edu.cn
