近三年理综化学高考试题解读
2011-03-24段昌平
■段昌平
近三年理综化学高考试题解读
■段昌平
2012年是湖北省进入新课程的第一年高考,根据此前进入新课程省、市、区理科综合考试情况,我省将加入由教育部考试中心命题考试的行列。为了加强理综化学复习备考的针对性,本人对教育部考试中心近三年为新课程(2009年的宁夏、海南卷,2010、2011年的海南及全国新课程卷)]命制的理综化学考题进行了分析,以供广大教师参考。
一、试卷结构与分值
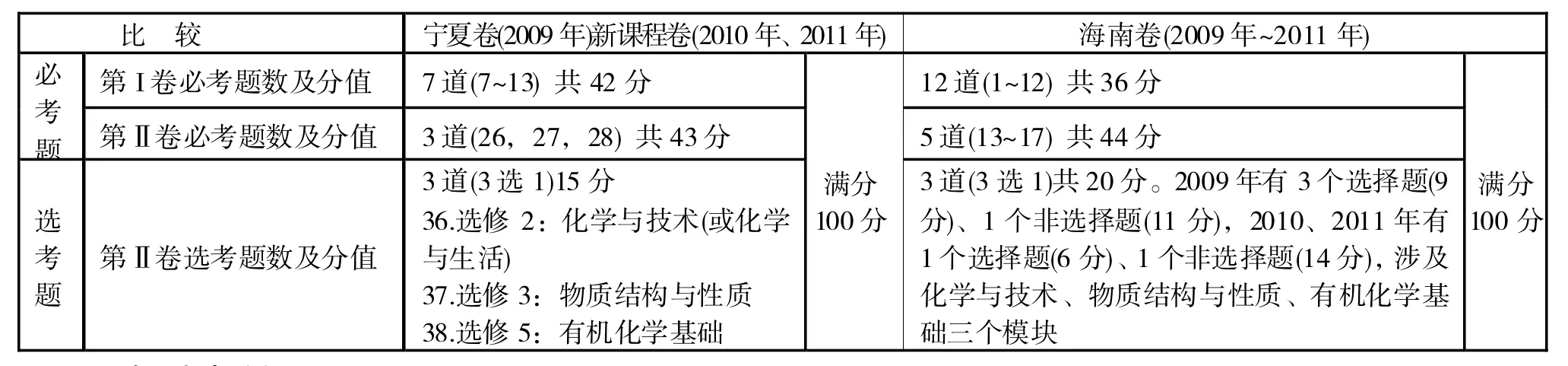
比 较 宁夏卷(2009年)新课程卷(2010年、2011年) 海南卷(2009年~2011年)必考第I卷必考题数及分值 7道(7~13) 共42分 12道(1~12) 共36分题 第Ⅱ卷必考题数及分值 3道(26,27,28) 共43分 5道(13~17) 共44分选考题满分100分满分100分第Ⅱ卷选考题数及分值3道(3选1)15分36.选修2:化学与技术(或化学与生活) 37.选修3:物质结构与性质38.选修5:有机化学基础3道(3选1)共20分。2009年有3个选择题(9分)、1个非选择题(11分),2010、2011年有1个选择题(6分)、1个非选择题(14分),涉及化学与技术、物质结构与性质、有机化学基础三个模块
二、试题考点分析
我省在教育部必考模块(化学1,化学2,化学反应原理)基础上,选修“物质结构与性质”、“有机化学基础”2个模块,下面对“化学课程标准”中增加知识点及近三年新课程卷涉考情况比较如下(括号里数字为年度):
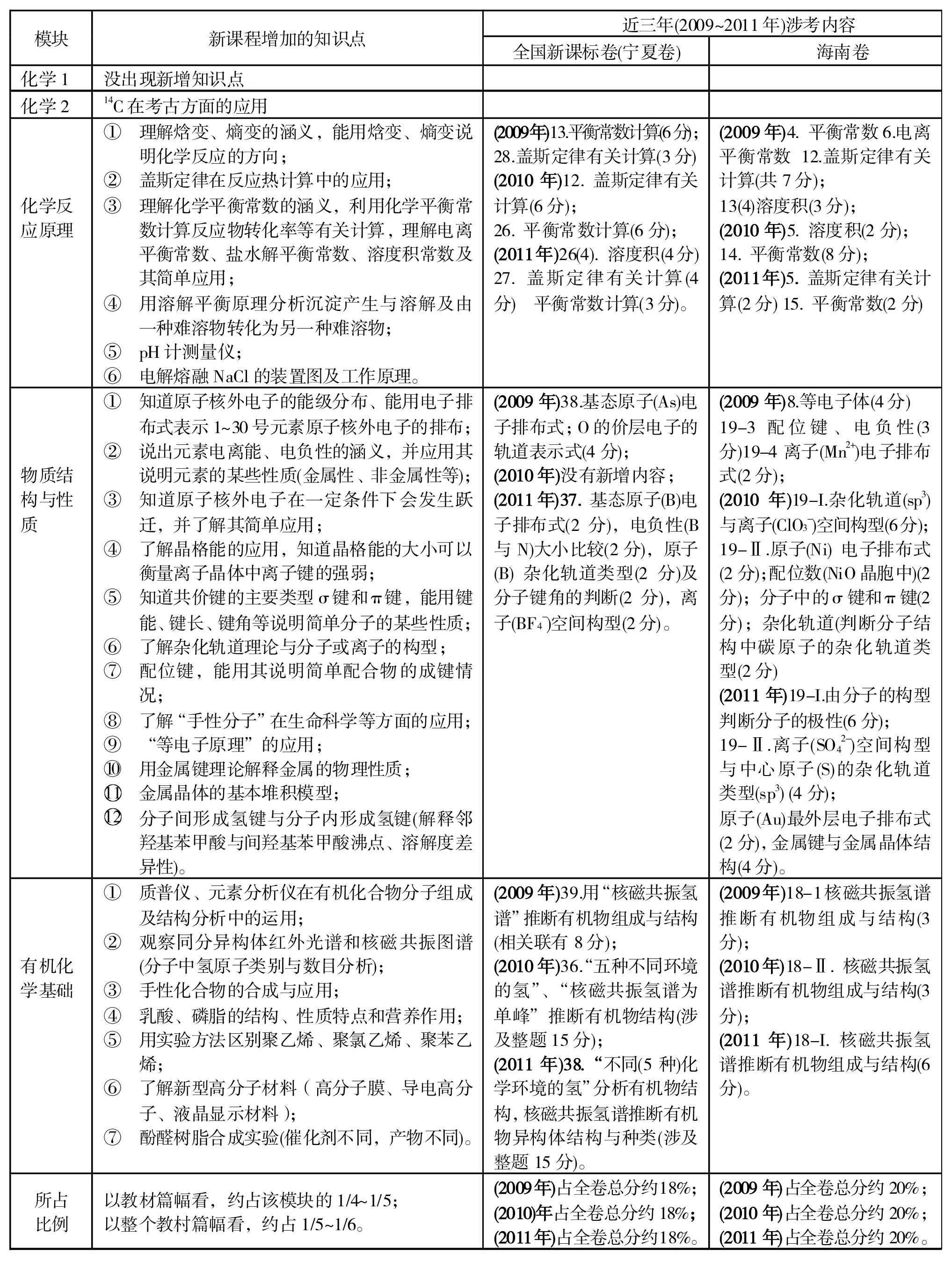
模块 新课程增加的知识点 全国新课标卷(宁夏卷) 海南卷近三年(2009~2011年)涉考内容化学1 没出现新增知识点化学2 14C在考古方面的应用化学反应原理① 理解焓变、熵变的涵义,能用焓变、熵变说明化学反应的方向;② 盖斯定律在反应热计算中的应用;③ 理解化学平衡常数的涵义,利用化学平衡常数计算反应物转化率等有关计算,理解电离平衡常数、盐水解平衡常数、溶度积常数及其简单应用;④ 用溶解平衡原理分析沉淀产生与溶解及由一种难溶物转化为另一种难溶物;⑤ pH计测量仪;⑥ 电解熔融NaCl的装置图及工作原理。(2009年)13.平衡常数计算(6分);28.盖斯定律有关计算(3分) (2010年)12. 盖斯定律有关计算(6分);26. 平衡常数计算(6分);(2011年)26(4). 溶度积(4分) 27. 盖斯定律有关计算(4分) 平衡常数计算(3分)。(2009年)4. 平衡常数6.电离平衡常数12.盖斯定律有关计算(共7分);13(4)溶度积(3分);(2010年)5. 溶度积(2分);14. 平衡常数(8分);(2011年)5. 盖斯定律有关计算(2分) 15. 平衡常数(2分)物质结构与性质① 知道原子核外电子的能级分布、能用电子排布式表示1~30号元素原子核外电子的排布;② 说出元素电离能、电负性的涵义,并应用其说明元素的某些性质(金属性、非金属性等);③ 知道原子核外电子在一定条件下会发生跃迁,并了解其简单应用;④ 了解晶格能的应用,知道晶格能的大小可以衡量离子晶体中离子键的强弱;⑤ 知道共价键的主要类型σ键和π键,能用键能、键长、键角等说明简单分子的某些性质;⑥ 了解杂化轨道理论与分子或离子的构型;⑦ 配位键,能用其说明简单配合物的成键情况;⑧ 了解“手性分子”在生命科学等方面的应用;⑨ “等电子原理”的应用;⑩ 用金属键理论解释金属的物理性质;金属晶体的基本堆积模型;分子间形成氢键与分子内形成氢键(解释邻羟基苯甲酸与间羟基苯甲酸沸点、溶解度差异性)。(2009年)38.基态原子(As)电子排布式;O的价层电子的轨道表示式(4分);(2010年)没有新增内容;(2011年)37. 基态原子(B)电子排布式(2分),电负性(B与N)大小比较(2分),原子(B) 杂化轨道类型(2分)及分子键角的判断(2分),离子(BF4-)空间构型(2分)。12 11 (2009年)8.等电子体(4分) 19-3配位键、电负性(3分)19-4离子(Mn2+)电子排布式(2分);(2010年)19-I.杂化轨道(sp3)与离子(ClO3-)空间构型(6分);19-Ⅱ.原子(Ni) 电子排布式(2分);配位数(NiO晶胞中)(2分);分子中的σ键和π键(2分);杂化轨道(判断分子结构中碳原子的杂化轨道类型(2分) (2011年)19-I.由分子的构型判断分子的极性(6分);19-Ⅱ.离子(SO42-)空间构型与中心原子(S)的杂化轨道类型(sp3) (4分);原子(Au)最外层电子排布式(2分),金属键与金属晶体结构(4分)。① 质普仪、元素分析仪在有机化合物分子组成及结构分析中的运用;② 观察同分异构体红外光谱和核磁共振图谱(分子中氢原子类别与数目分析);③ 手性化合物的合成与应用;④ 乳酸、磷脂的结构、性质特点和营养作用;⑤ 用实验方法区别聚乙烯、聚氯乙烯、聚苯乙烯;⑥ 了解新型高分子材料(高分子膜、导电高分子、液晶显示材料);⑦ 酚醛树脂合成实验(催化剂不同,产物不同)。有机化学基础(2009年)39.用“核磁共振氢谱”推断有机物组成与结构(相关联有8分);(2010年)36.“五种不同环境的氢”、“核磁共振氢谱为单峰”推断有机物结构(涉及整题15分);(2011年)38.“不同(5种)化学环境的氢”分析有机物结构,核磁共振氢谱推断有机物异构体结构与种类(涉及整题15分)。(2009年)18-1核磁共振氢谱推断有机物组成与结构(3分);(2010年)18-Ⅱ. 核磁共振氢谱推断有机物组成与结构(3分);(2011年)18-I. 核磁共振氢谱推断有机物组成与结构(6分)。以教材篇幅看,约占该模块的1/4~1/5;以整个教村篇幅看,约占1/5~1/6。所占比例(2009年)占全卷总分约18%;(2010)年占全卷总分约18%;(2011年)占全卷总分约18%。(2009年)占全卷总分约20%;(2010年)占全卷总分约20%;(2011年)占全卷总分约20%。
三、试题呈现形式创新
分析近三年新课程的六套高考试卷,总体感觉是在旧课程理科综合卷基础上呈现出不断创新的趋势(海南为单科卷),这是新课程改革成果的体现。新课程试卷新在以下五个方面:
1.元素及其化合物考题注重以新材料、新技术为依托的新型工业生产,引导学生关注社会热点问题,结合实际用所学知识分折和解决问题。2009年新课程宁夏卷37题,以“氯碱工业为高耗能产业以及新材料(离子交换膜)、新技术(燃料电池)”为背景,设计生产装置示意图(图1),要求学生阅读示意图回答问题。
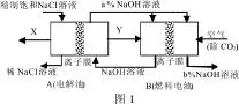
学生通过图中所提供的新科技信息,结合所学化学反应原理,理清脉络,形成工业化生产的整体认识,该题从多角度考查了学生掌握元素及化合物的知识和结合实际解决问题的能力。2011年新课程全国卷27题,以“科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池”为背景,考查了热化学方程式的书写、计算;通过观察反应变化曲线考查了化学反应速率、平衡移动原理应用于工业生产,同时结合当今能源的热点问题,考查了由化学能转变为电能的甲醇燃料电池的工作原理。
2.实验考题注重学生的参与性和答案的开放性。2011年新课程全国卷28题,关于CaH2的实验室制取及性质检验的实验。前一部分由命题者设问学生回答,后一部分则由学生自己设计实验方案:“用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象”。命题者对该实验设计没有定框框,完全由学生自主设计。该实验设计具有多样性。命题者提供的答案为:“取适量CaH2在加热条件下与干燥氧气反应,将反应的气相产物通过装有无水硫酸铜的干燥管,观察到白色变为蓝色;取钙做类似实验,观察不到白色变为蓝色。”我认为,只要所设计实验能反映出Ca与CaH2具有明显不同实验现象均可。例如用下列图2、图3装置来区分,并作适当说明亦可。
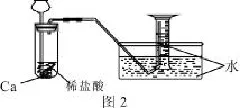
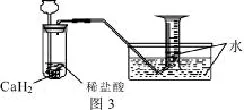
操作:①按图连接好装置并检查气密性,使量筒内充满水。②取等质量(或等物质的量)的钙、氢化钙于试管中,向长颈漏中注入等体积且足量的稀盐酸。
现象:①氢化钙产生气泡速率比钙更快(固体很快消失);②量筒中收集气体体积氢化钙约为钙的2倍。其它合理答案也可以。
2010年28题(4)的实验设计内容是:锌与稀硫酸反应制H2,在已加入少量CuSO4溶液的情况下,若要再加快产生气体速率,还可采取的措施有_____(答两种)。答案:①加热,②提高稀硫酸的浓度,③用锌片(或锌粉)代替相同质量的锌粒等。
3.有机化学考题注重将新的检测技术(质普仪、元素分析仪)和新的物质结构理论(杂化轨道理论)应用于有机物分子组成与结构分析。2010年新课程全国卷36题,物质推断第一步是丙烯与苯的加成反应产物(B)的结构判断,题给信息为“B中有五种不同化学环境的氢”。由此说明加成产物(B)只能为异丙苯,不是丙苯。如果这步推错,全题皆错。2011年新课程全国卷38题,物质推断第一步反应产物A(甲苯与Cl2在FeCl3催化时发生取代反应)中氯原子的位置,题给信息为“A中有五种不同化学环境的氢”。说明氯原子的位置只能是苯环上甲基的邻位或间位,不能在对位上,更不可能在甲基上。如果这步出错,全题也皆错。2009年新课程宁夏卷39题,框图中告知了F(C4H6O2)是E(C4H8O3)与浓硫酸共热反应的产物,F分子中氢原子结构特征为“核磁共振氢谱表明F分子中有三种氢,且峰面积之比为1︰1︰1”。这种转化(脱去一个水分子)有两种可能,一是消去反应产生碳碳双键,二是分子内脱水形成环酯,由质谱仪检测分析知,所发生的反应是酯化反应而不是消去反应。
4.考题体现了新课程理念,注重考查学生科学探究能力。探究学习是新课程提出的新学习方式,意在改变学生的学习方式,培养学生的探究意识和提高学生的探究能力。2011年新课程全国卷26题,命题者给考生创造的问题情景是:0.8gCuSO4·5H2O受热过程中的热重曲线(样品质量随温度变化的曲线,见图4)。要求学生依据题给情景,自主进行探究学习。该题将定性、定量分析解决问题融为一体,首先读懂图中温度变化体现出反应的阶段性,固体质量变化体现出反应产物及其化学计量数的变化,即反应过程可分为两类:一类是CuSO4·5H2O受热时失水反应,另一类是CuSO4在更高温度下的分解反应。这种认识过程就是一种探究学习。有了这些认识,后面的问题就不难回答了。
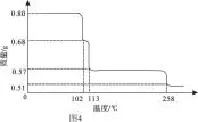
将CuSO4·5H2O受热时的脱水反应写成下式,再由曲线上的热重变化可得出如下关系:

由w的数值看n有三个值:2、4、5。当温度高于258℃时CuSO4才会分解,分解产物可能为CuO、SO3;也可能为CuO、SO2、O2;或Cu2O、SO2、O2。若图中258℃之后给出相应热重变化,各时段的分解产物也能确定。
5.新增知识点考的概率较大,但难度不大。据上述统计,新增知识点所占总分比值在18%~20%,考得最多的是:①平衡常数,②盖斯定律,③原子或离子的电子排布式、轨道表示式,④分子、离子的空间构型及轨道杂化,⑤质普仪、元素分析仪在有机化合物分子组成及结构分析中的应用。⑥溶度积常数、电离平衡常数应用。没有考或考得少的新增知识点有:①用焓变、熵变说明化学反应的方向,②电离能、电负性、晶格能的应用,③“手性分子”、“等电子原理”的应用,④分子内形成氢键,⑤共价键的主要类型σ键和π键,⑥金属晶体的堆积模型,⑦酚醛树脂合成实验中用酸或碱作催化剂时产物不同,⑧pH计测量仪的使用等。但这些内容在自主命题的省、市(如江苏、山东、浙江、上海等)考题中出现过。目前未考原因有三个:一是这些内容理论性较强,拔高需要一个过程;二是考卷容量较少,考虑到知识点的合理分布,新增知识点在整个教材中的份额限制(18%~20%左右);三是有些精密分析实验仪器在中学实际应用有限。
(作者单位:武汉市黄陂一中)
责任编辑 王爱民
