泥炭生物反应墙构建及修复地下水中石油烃
2011-03-06马会强张兰英张洪林
马会强,张兰英,张洪林,李 爽
(1.辽宁石油化工大学环境与生物工程学院,辽宁抚顺 113001;2.吉林大学环境与资源学院,长春 130026)
泥炭生物反应墙构建及修复地下水中石油烃
马会强1,张兰英2,张洪林1,李 爽1
(1.辽宁石油化工大学环境与生物工程学院,辽宁抚顺 113001;2.吉林大学环境与资源学院,长春 130026)
为有效修复地下水中溶解态石油烃污染物,在研究填充介质配比基础上,分别利用低温石油烃降解菌-泥炭-粗砂和泥炭-粗砂构建了泥炭生物反应墙和泥炭反应墙,考察了反应墙对地下水中BTEX、PAH s的修复效果。结果表明,泥炭与粗砂最适体积比为20:80,此时墙体渗透系数为1.17×10-4m/s,有效空隙率为7.5%;泥炭反应墙对BTEX去除率为32.63%~79.15%,吸附寿命为50~55 d,吸附能力大小为二甲苯>乙苯≈甲苯>苯,出水萘、α-甲基萘、β-甲基萘和菲浓度均低于2.85μg/L;泥炭生物反应墙对BTEX、PAH s修复效果良好,去除率分别为83.6%~97.83%、97.48%~99.85%,微生物降解作用明显,BTEX降解率为75.66%~90.16%。研究表明,泥炭生物反应墙内污染物去除过程为泥炭吸附和微生物降解,泥炭对石油烃特别是多环芳烃具有很强的吸附能力,生物降解能有效延长泥炭对污染物的吸附寿命。
泥炭;微生物;反应墙;地下水;石油烃
随着国民经济对石油工业依赖程度的日趋增加,在石油开采、储存、运输、加工及制品使用等过程中,频繁出现石油烃污染地下水事件,部分地下水源亦受到影响[1-2]。因溶解能力不同,芳香烃往往是石油烃在地下水中的主要存在形式,而此类物质又具有或可疑“致癌、致畸、致突变”效应[3],因此有必要对其进行有效的控制与治理。在众多USEPA推荐的石油烃污染地下水修复方法中,渗透反应墙(PRB)技术因修复费用相对节省、对周围环境扰动少等优点,被广泛应用于污染场地[4-6];因反应介质不同,PRB已发展成不同的吸附和生物式反应墙。沸石、活性炭、共代谢物质、释氧化物常用作PRB反应介质[7-8];但近年来,价格相对低廉的土壤有机材料和有机覆盖物常用于生物滞留系统中,来提高反应屏障的修复效率[9-11]。泥炭就是其中的代表,它是一种含有不同分解度有机物的复杂土壤材料,主要含有木质素、纤维素、半-纤维素、腐植酸、溶解性醚醇、丙酸盐和含氮化合物等,因廉价、容易获得、生态安全被认为是一种处理污染水的有效材料[12-14]。前期测试表明泥炭可有效吸附苯、甲苯、乙苯、五氯酚等疏水性污染物,其含有的丰富碳、氮源可为微生物代谢生长供给营养[15]。此外,许多芳香烃(BTEX、PAHs)可以在地下环境中被降解成二氧化碳和水等无害物质[16],以上为泥炭联合低温石油烃降解微生物进行原位生物强化修复地下水中石油烃污染物提供了新思路。
为此,设计了好氧生物渗透模拟系统,并在研究填充介质配比基础上,分别利用低温石油烃降解菌-泥炭-粗砂和泥炭-粗砂构建泥炭生物反应墙和泥炭反应墙,考察反应墙对地下水中溶解态石油烃:BTEX、PAHs的修复效果,并探讨泥炭和微生物的修复作用,力求建立一种行之有效的石油烃污染地下水修复方法,旨为项目后期工程化提供技术支持。
1 材料与方法
1.1 实验材料
0#柴油购于中国石油天然气公司。苯系物(苯,甲苯,乙苯,o、m、p-二甲苯)、萘系物(萘,α、β-甲基萘)和菲标准样品贮备液购于中国国家标准物质研究中心。
低温石油烃降解菌群源自吉林油田某长期受石油烃污染场地,经长期低温自然强化富集构建而成,具有低温(10℃)石油烃降解能力。
草本泥炭购于吉林省泥炭土基地,经低温阴干后,140℃热处理3 h;取粒径0.25~5 mm,超纯水浸泡24 h后制备成浆体。粗砂取自场地含水层,清洗后阴干;取粒径0.5~2mm,超纯水冲洗、浸泡24 h,阴干备用。介质相关特性见表1。
供试地下水采自东北某地下含水层,pH为7.53,电导率为390μs/cm。地下水中金属元素含量见表2。
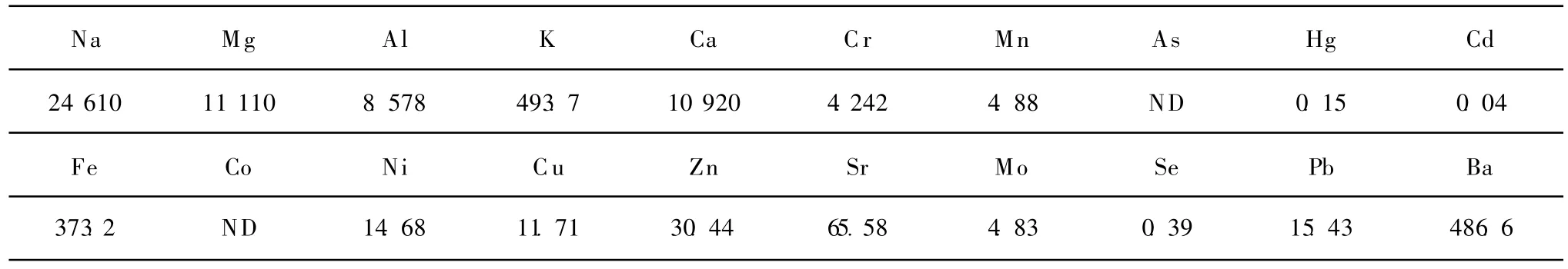
表2 地下水中金属元素含量 /(μg◦L-1)
1.2 实验装置
设计了如图1所示的生物渗透模拟系统,包括:供氧系统,供水系统及“L”型渗流柱,供氧系统采用电磁式空压机对地下水进行曝气充氧;供水系统采用蠕动式计量泵供水。“L”型渗流柱为树脂玻璃材料,长50 cm,高20 cm,内径10 cm,橡胶垫法兰密封;分为3区:Ⅰ区模拟污染源,10 cm厚,右侧为多孔布水板,区内投加轻非水相液体(LNAPL);Ⅱ区模拟反应墙,34 cm厚,装填泥炭、微生物及粗砂介质;Ⅲ区为承托层,6 cm厚,装填石英砂;末端为高度可调式出水口,调节反应墙水力坡度。P.1、P.2、P.3为取样口,分别代表反应墙进水、中间和末端出水。
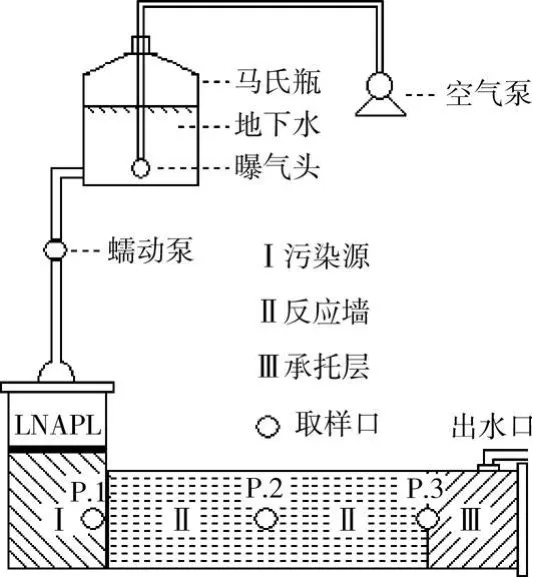
图1 实验装置示意图
1.3 实验方法
1.3.1 反应墙介质配比 泥炭浆与粗砂的体积比分别设定为0:100、10:90、20:80、30:70、40:60、50:50,在渗流柱内装填上述配比介质,分层装填,保持相同压实度;测定配比介质的渗透系数、有效孔隙率及容积密度。
1.3.2 反应墙构建 采用分层装填方法,每次称取240 g,铺平,均匀夯实,高度保持2 cm左右,取样管顶端置于柱中心位置,以防边际流效应;Ⅱ区装填介质3 600 g(干重),容积密度1.36×103kg/m3,有效孔隙率7.5%,总孔隙率37.1%;Ⅲ区装填粗砂3 164 g(干重),容积密度1.55×103kg/m3,有效孔隙率14.8%,总孔隙率40.2%。
实验装填2套模拟系统,标记为A、B。A代表泥炭生物反应墙,Ⅱ区装填一定比例粗砂、泥炭及功能微生物(已固定化于泥炭上);B代表泥炭反应墙,Ⅱ区装填一定比例已灭菌的粗砂和泥炭。
1.3.3 反应墙调试与运行 向马氏瓶中加入超纯水,开启蠕动泵,控制流量200 m L/h,升流式对反应墙饱水,每升高4 cm,停止供水,稳定30 min,重复以上过程直至饱水完全,稳定24 h后泄水,调整水位。然后向马氏瓶中加入地下水,此时B系统马氏瓶中加入叠氮化钠(1 g/L)作为抑菌剂。向Ⅰ区注入30m L 0#柴油模拟污染源,调节地下水流量380m L/d,反应墙开始运行,墙体水力坡度5‰~6‰(接近场地情况),水力停留时间约2 d,运行温度9~12℃,共运行80 d。定期取样测定污染物浓度,并补充地下水及叠氮化钠。
1.3.4 反应墙示踪 反应墙开始运行起,每隔一定时间从B系统的P.2、P.3点采集地下水样品,测定电导率。
1.3.5 污染物浓度测定 地下水中苯、甲苯、乙苯、二甲苯、萘、α-甲基萘、β-甲基萘测试参照EPA 5035、8260B方法,采用吹扫捕集浓缩仪-气相色谱质谱分析;菲测试参照EPA 8270C方法,采用液-液萃取-气相色谱质谱分析。
1.3.6 其它参数测定 渗透系数采用常水头试验确定;介质总孔隙率、有效孔隙率采用树脂玻璃渗流柱试验确定;电导率采用带温度校正的便携式电导率仪测定。
2 结果与讨论
2.1 反应墙介质配比
泥炭在一定压实密度下,渗透性很差,不利于实际工程应用。为使反应墙获得较高的水力传导能力,以及减少微生物生长时所造成的缺氧区域,实验采用渗透性相对较高且易获得的含水层介质——粗砂和泥炭进行配比,测试结果见图2、图3。
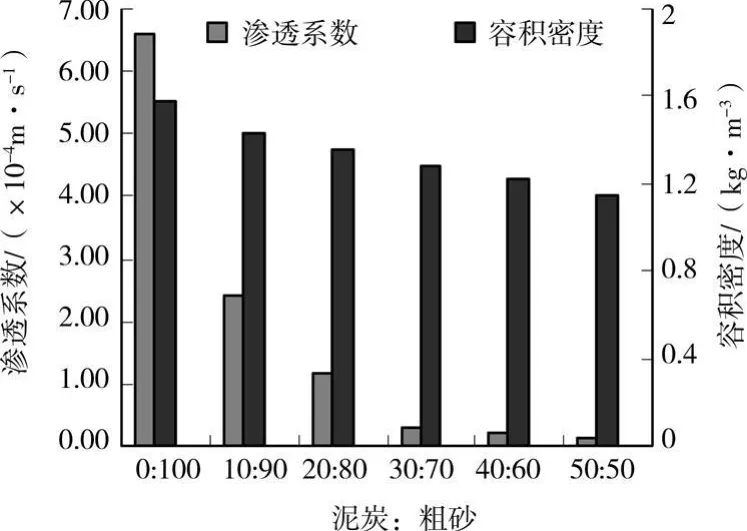
图2 介质配比对渗透系数、容积密度的影响
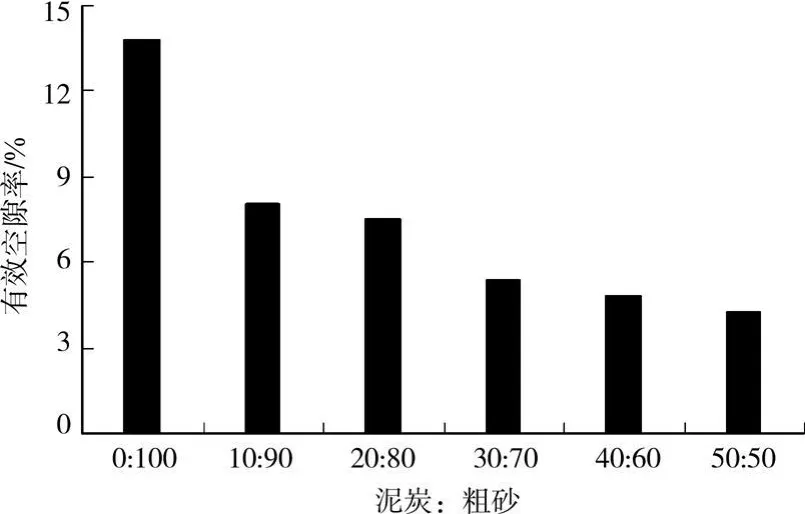
图3 介质配比对有效空隙率的影响
由图2可知,泥炭与粗砂的配比比例对混合介质渗透系数k影响很大,随着泥炭比例的增加,渗透系数逐渐降低,泥炭比例≤20:80时,k值大于10-4m/s,当比例≥30:70,k值小于10-5m/s。在相同压实条件下,随着泥炭比例增加,容积密度也呈现递减的趋势。
由图3可知,随着泥炭比例增加,介质有效空隙率逐渐降低。泥炭比例≥30:70时,有效空隙率降低迅速,均小于5.5%,当比例为10:90,20:80时,变化不大且均大于7%。
实际污染场地的上更新统孔隙潜水含水层结构为:上部黄土状亚砂土,夹粉细砂透镜体,下部砂层为浅黄色,以细砂为主,局部为粉细砂或中细砂,含水层颗粒细,透水性差,渗透系数在10-6~10-5m/s之间;因此在衡量场地含水层的渗透性和泥炭的吸附性能后,确定反应墙介质为:泥炭:粗砂体积配比为20:80,此时墙体渗透系数1.17×10-4m/s,容积密度1.36×103kg/m3,有效空隙率7.5%,总孔隙率37.1%。
2.2 反应墙示踪
图4为反应墙P.2、P.3点地下水的电导率穿透曲线。调试阶段反应墙使用超纯水饱水,出水电导率相对较低;而运行时使用地下水,其电导率相对较高,因此可通过地下水样品的电导率穿透曲线推算墙体水力停留时间。
由图4可知,P.2、P.3点地下水电导率完全穿透时间分别为37 h和60 h,间隔23 h,根据两点距离,推算反应墙水力停留时间为46 h。根据反应墙长度,渗透量及达西定律,求得地下水实际流速17.74 cm/d,渗流速度 4.84 cm/d,介质渗透系数9.68 m/d,有效渗透体积比为27.3%。
2.3 反应墙修复BTEX效果
因泥炭反应墙所用填充介质在墙体构建前均已灭菌,且运行时地下水中加入抑菌剂,因此,运行期该反应墙为无菌状态,其运行结果反映泥炭对污染物的吸附去除效果。泥炭生物反应墙中已固定化具有10℃低温降解石油烃功能的微生物(由耶氏酵母菌属、红球菌属、不动杆菌属、假单胞菌属、新鞘氨醇杆菌属等组成),则运行结果反映泥炭和功能微生物对污染物的吸附-生物降解效果;2个反应墙运行效果差异代表功能微生物的降解效果。图5为运行期泥炭及泥炭生物反应墙对地下水中苯系物:苯、甲苯、乙苯和二甲苯(间、对、邻)的修复效果。

图4 P.2、P.3点地下水电导率穿透曲线
由图5可知,污染源中BTEX以甲苯、二甲苯为主,运行期地下水的稀释、冲淡作用使得污染物进水浓度发生衰减,其中苯最为明显。
泥炭反应墙对苯的去除效果较差,泥炭吸附去除率约为32.63%,且出水在第12 d达到峰值22.12μg/ L,随后完全穿透并解吸。这说明泥炭对苯的吸附容量较小或苯浓度过低不能达到泥炭吸附阈值或稳定吸附;可判定墙体对苯的吸附寿命约为15 d。
泥炭生物反应墙出水苯浓度稳定于0.3~1.2μg/L,低于进水和泥炭反应墙出水,苯去除率约为83.6%;表明墙体已吸附苯的生物降解效果明显,降解率约为75.66%。
泥炭反应墙对甲苯、乙苯和二甲苯具有一定去除效果,去除率分别约为69.14%、79.15%、77.85%;且出水浓度变化相似,在第35、45和55 d达到峰值163.24、45.65和334.20μg/L,接近进水污染物浓度;其中甲苯、二甲苯浓度分别从55 d和60 d开始明显高于进水,发生解吸。以上表明泥炭墙体对甲苯、乙苯和二甲苯具有一定的吸附能力,判定其墙体吸附寿命分别约为35、45和55 d。
泥炭生物反应墙对地下水中甲苯、乙苯和二甲苯的处理效果良好,去除率约为93.90%、97.83%、96.81%,出水浓度均远低于进水和泥炭反应墙出水, 80 d内未发生穿透现象。以上表明功能微生物降解作用明显,墙体已吸附3种污染物的生物降解率分别约为81.27%、90.16%和85.63%。
图6为运行期泥炭/泥炭生物反应墙对地下水中苯系物的分段修复效果,BTEX为苯、甲苯、乙苯和二甲苯浓度之和。

图6 泥炭/泥炭生物反应墙对苯系物的分段修复效果
由图6可知,泥炭反应墙P.2第6 d检出BTEX,35 d达到最高值714.19μg/L;P.3第18 d检出BTEX,55 d达到最高值507.67μg/L;2点出水污染物浓度均在峰值后与进水相近,并在60 d时大于进水。以上表明泥炭介质对BTEX具有一定吸附性能,吸附能力大小为二甲苯>乙苯≈甲苯>苯(图5);污染物达到饱和吸附容量后出现解吸,判定泥炭墙对BTEX的吸附寿命约为50~55 d。泥炭中含有较多甲氧基、羧基、醇、酚、酮及醌型羟基官能团及一定量芳香碳基结构的木质素、单糖,这样的分子结构利于外部和内部的表面吸附及固定有机化合物;此外泥炭中含有邻甲氧苯基木质素和呋喃官能团,其芳香特性结构与该研究 BTEX化合物相似,所以BTEX的吸附情况主要决定于BTEX在水和泥炭有机质之间的分配比例。前期测试表明[15]:一定浓度下,BTEX的泥炭-水标化分配系数K oc分别为83.18~165.96 L/kg、100.00~213.80 L/kg、117.49~239.88 L/kg、213.80~354.81 L/kg,说明BTEX在泥炭上的分配能力大小为二甲苯>乙苯>甲苯>苯,因此泥炭反应墙运行期表现出对BTEX吸附去除效果的差异。
泥炭生物反应墙P.2第9 d检出BTEX,30 d达到最高值241.56μg/L,但浓度远低于进水;P.3运行期内BTEX浓度一直较低;2点出水浓度均从55 d起稳定于50~60μg/L。以上表明泥炭生物反应墙对苯系物修复效果较好,生物降解作用明显,且功能微生物的使用可有效延长泥炭介质墙体对苯系物的吸附寿命。泥炭生物反应墙中已固定化具有降解石油烃功能的微生物,当地下水中污染物吸附于泥炭介质后,部分BTEX会被微生物降解,但由于BTEX在泥炭介质上吸附能力、吸附浓度的差异以及微生物代谢活性的不同,导致BTEX在泥炭生物反应墙中的降解效率有所不同。
泥炭/泥炭生物反应墙出水中BTEX浓度具有相似的变化趋势;以P.2点为例:泥炭反应墙第9 d检出污染物,随后浓度逐渐升高,35 d完全穿透;泥炭生物反应墙出水也具有开始检出、峰值趋势,但出水浓度较低。这表明泥炭生物反应墙在不同运行期污染物的修复机理可能不同,运行初期(0~20 d)以泥炭吸附为主,中期(20~50 d)为泥炭吸附和生物降解共同作用,后期(50~80 d)以生物降解作用为主;此外,地下水中污染物浓度的急剧降低可能影响生物降解稳定性,导致出现一段适应过渡期。
2.4 反应墙修复PAHs效果
图7为运行期泥炭/泥炭生物反应墙对地下水中多环芳烃:萘、α-甲基萘、β-甲基萘及菲的修复效果。
由图7可知,污染源中多环芳烃以萘、α、β-甲基萘为主;运行期存在相似的衰减现象。泥炭/泥炭生物反应墙对多环芳烃的修复效果良好,萘、α、β-甲基萘及菲的去除率分别约为99.85%、99.59%、99.18%、97.48%,出水中污染物浓度变化一致且均较低,萘、α、β-甲基萘低于2.85μg/L,菲低于0.46μg/L;此外反应墙P.2出水未检出大量污染物;以上表明,泥炭介质对多环芳烃具有很强的吸附能力,这与前期试验结果一致[15];运行期未发现污染物穿透和解吸现象,表明80 d未达到泥炭介质对多环芳烃的吸附寿命,但从上图中未显示出功能微生物的降解效果。
3 结 论
1)泥炭与粗砂的比例对混合介质的渗透能力、有效空隙率影响较大;结合场地潜水含水层结构,确定反应墙中泥炭与粗砂体积比为20:80,此时墙体渗透系数1.17×10-4m/s,容积密度1.36×103kg/m3,有效空隙率7.5%,总孔隙率37.1%。
2)泥炭反应墙对地下水中的BTEX具有一定修复效果,泥炭吸附去除率约为 32.63%~79.15%,吸附寿命约为50~55 d,吸附能力大小为二甲苯>乙苯≈甲苯>苯;泥炭对多环芳烃具有很强的吸附去除能力,反应墙出水中萘、α-甲基萘、β-甲基萘和菲浓度均低于2.85μg/L。
3)泥炭生物反应墙对地下水中的BTEX、PAH s修复效果良好,去除率分别为83.6%~97.83%、97.48%~99.85%,去除机理主要为泥炭吸附和微生物降解;墙体内微生物降解作用明显,BTEX降解率约为75.66%~90.16%,生物降解作用能有效延长泥炭对污染物的吸附寿命。
[1]HE L,HUANG G H,ZENG G M,et al.An integrated simulation, inference, and optimization method for identifying groundwater remediation strategies atpetroleum contaminated aquifers in western Canada[J].Water Research,2008,42(10/11):2629-2639.
[2]罗兰.我国地下水污染现状与防治对策研究[J].中国地质大学学报:社会科学版,2008,8(2):72-75.
LUO LAN.Research on groundw ater pollution and its p revention contro l po licy in china[J].Journal of China University of Geosciences:Social Sciences Edition, 2008,8(2):72-75.
[3]王学彤,贾英,孙阳昭,等.典型污染区农业土壤中PAH s的分布、来源及生态风险[J].环境科学学报, 2009,29(11):2433-2439.
WANG XUE-TONG,JIA YING,SUN YANG-ZHAO,et al.Distribution,sources and ecological risk assessment of polycyclic aromatic hydrocarbonsin agricu ltural soils from a typical contaminated area[J]. A cta Scientiae Circumstantiae,2009,29(11):2433-2439.
[4]YEH C H,LIN CW,WU C H.A permeable reactive barrier for the bioremediation of BTEX-contam inated groundw ater:m icrobial community distribution and removal efficiencies[J].Journal of Hazardous Materials,2010,178(1/2/3):74-80.
[5]NOOTEN T V,DIELS L,BASTIAENS L.Design of a multifunctional permeable reac tive barrier for the treatment of landfill leachate contamination:laboratory column evaluation[J].Environmental Science & Techno logy,2008,42(23):8890-8895.
[6]GIBERT O,FERGUSON A S,KALIN R M,et a l. Performance of a sequential reac tive barrier for bioremediation of coal tar contam inated groundw ater [J].Environmental Science&Technology,2007,41 (19):6795-6801.
[7]HE Y T,W ILSON J T,W ILKIN R T.Transformation of reactive iron minerals in a permeable reactive barrier (Biowall)used to treat TCE in groundwater[J]. Environmental Science&Technology,2008,42(17):6690-6696.
[8]WO INARSK IA Z,SNAPE I,STEVENSG W,eta l. The effects of co ld tem perature on copper ion exchange by natural zeolite for use in a permeable reactive barrier in Antarctica[J].Co ld Regions Science and Technology,2003,37(2):159-168.
[9]SEO Y,LEEW H,SORIAL G,et al.The application of a mulch biofilm barrier for surfactant enhanced polycyclic aromatic hydrocarbon bioremediation[J]. Environmental Pollution,2009,157(1):95-101.
[10]SEO Y,BISHOP P L.The monitoring of biofilm formation in a mu lch biowall barrier and its effect on performance[J].Chemosphere,2008,70(3):480-488.
[11]TIEHMA,MULLER A,ALT S,et al.Development of a groundwater biobarrier for the removal of po lycyclic aromatic hydrocarbons, BTEX, and heterocyclic hydrocarbons[J].W ater Science and Technology,2008,58(7):1349-1355.
[12]YRJ゜AL゜A K,KESK INEN A K,゜AKERMAN ML. The rhizosphere and PAH amendmentmediate impacts on functional and structural bacterial diversity in sandy peat soil[J].Environmental Pollution,2010,158(5):1680-1688.
[13]GUPTA B S,CURRAN M,HASAN S,et al. Adsorption characteristics of Cu and Ni on Irish peat moss[J].Journal of Environmental Management, 2009,90(2):954-960.
[14]CALDERÓN M,MORAGA C,LEAL J,et al.The use of Magallanic peat as non-conventional sorbent for EDTA removal from wastew ater[J].Bioresource Technology,2008,99(17):8130-8136.
[15]马会强.石油烃污染地下水的原位生物修复研究[D].长春:吉林大学,2009.
[16]AZH ARIN E,LAMRANIMD,CHATAGN IER G, et al.Molecular analysis of the catechol-degrading bacterial community in a coal w asteland heavily contam inated w ith PAH s[J].Journal of H azardous Materials,2010,177(1/2/3):593-601.
(编辑 胡英奎)
Construction of Peat Biobarrier to Remediate Petroleum Hydrocarbon Contam inated Groundwater
MAHui-qiang1,ZHANGLan-ying2,ZHANGHong-lin1,LIShuang1
(1.School of Environmental and Biological Engineering,Liaoning Shihua University,Fushun 113001,Liaoning,P.R.China; 2.Co llege of Environment and Resources,Jilin University,Changchun 130026,P.R.China)
In order to effectively remediate the dissolved petroleum hyd rocarbon contam inants in aquifer, low temperature hydrocarbon degrading bacteria-peat-coarse sand and peat-coarse sand were adopted respectively to construct peat biobarrier and peat barrier.And the ratio of packing media,the removal efficiency of BTEX and PAH s were investigated through barriers in remediation of petroleum hydrocarbon contaminated groundw ater.It is found that the hydraulic conductivity and availableporosity ofmixedmedia were 1.17×10-4m/s,7.5%respectively when peat and coarse sand at the op timum volume ratio of 20:80. For peat barrier,the removal rates of BTEX were 32.63%-79.15%,sorption life was 50-55d,sorption capacity of peat barrier to BTEX was xy lene>ethy lbenzene≈toluene>benzene,effluent concentration of naphthalene,α-methy lnaphthalene,β-methy lnaphthalene and phenanthrenewere all below 2.85μg/L.The removal efficiency for BTEX,PAHswere83.6%-97.83%,97.48%-99.85%through rem ediation by peat biobarrier,and have an obviously effect on contaminants biodegradation,the degrading rates of BTEX were 75.66%-90.16%.The study indicated that removalmechanism s of hydrocarbon contam inants were peat sorption and biodegradation for peat biobarrier,peat had strong sorption capacity to petroleum hydrocarbon contaminants,especially for PAHs,contam inants biodegradation could efficiently prolong the sorption life of peat barrier.
peat;m icroorganism s;permeab le reactive barrier;groundwater;petro leum hyd rocarbon
X 523
A
1674-4764(2011)03-0129-07
2010-11-11
国家“863”计划项目(2007AA06Z343);国家自然科学基金资助项目(50879029)
马会强(1982-),男,博士,主要从事环境生物技术及地下水污染控制与修复研究,(E-mail)mahuiqiang0921 @126.com。
张兰英(通讯作者),女,教授,博士生导师,(E-mail)zhangly@jlu.edu.cn。
