医疗器械警戒快讯
2011-02-06
FDA发布关于Global Focus Marketing & Distribution公司离心机的召回通告
产品:Silencer S2200离心机。
范围:序列号为0493128至0798286、98267203至06067205,及04084R01至09274R01的产品。
FDA发布关于波科(Boston Scientific)公司Resolution II带有推送器的一次性使用止血夹的召回通告
产品:Resolution II带有推送器的一次性使用止血夹。
范围:具体产品如下。
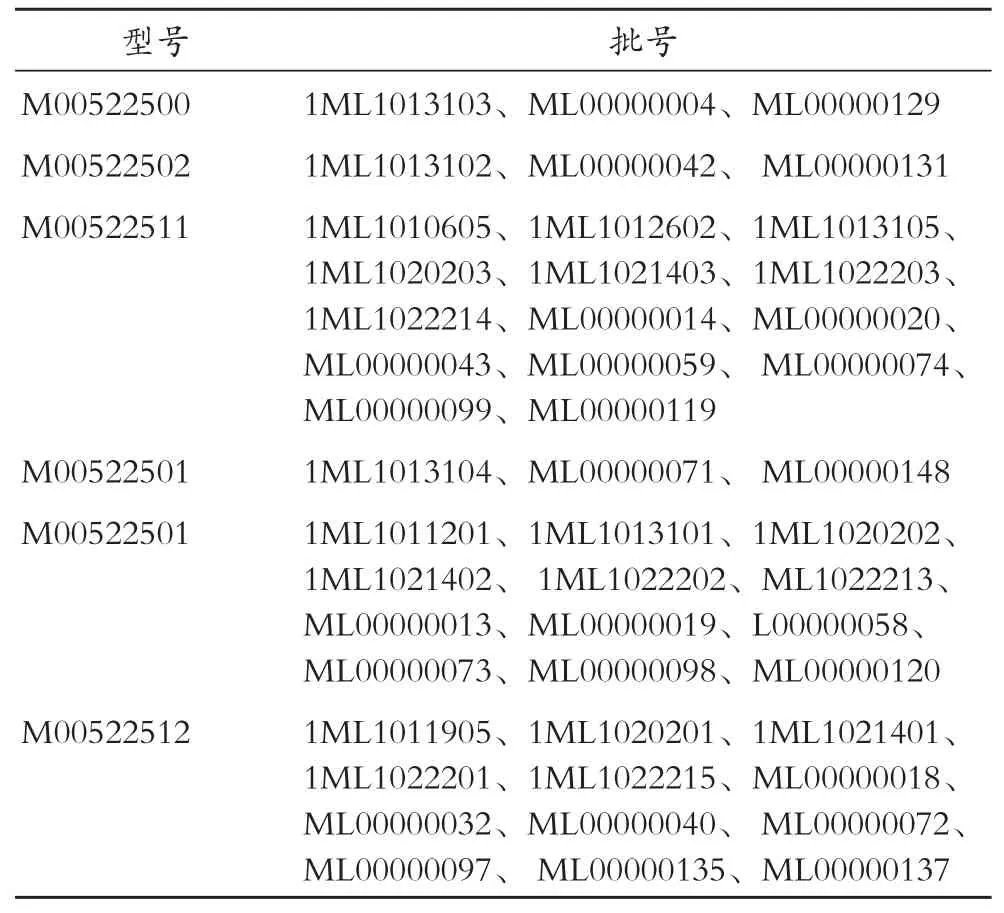
型号 批号M00522500 1ML1013103、ML00000004、ML00000129 M00522502 1ML1013102、ML00000042、 ML00000131 M00522511 1ML1010605、1ML1012602、1ML1013105、1ML1020203、1ML1021403、1ML1022203、1ML1022214、ML00000014、ML00000020、ML00000043、ML00000059、 ML00000074、ML00000099、ML00000119 M00522501 1ML1013104、ML00000071、 ML00000148 M00522501 1ML1011201、1ML1013101、1ML1020202、1ML1021402、 1ML1022202、ML1022213、ML00000013、ML00000019、L00000058、ML00000073、ML00000098、ML00000120 M00522512 1ML1011905、1ML1020201、1ML1021401、1ML1022201、1ML1022215、ML00000018、ML00000032、ML00000040、 ML00000072、ML00000097、 ML00000135、ML00000137
英国MHRA发布关于日机装(NIKKISO)公司Aquarius血液滤过设备的警戒通告
产品:Aquarius血液滤过设备。
范围:所有产品。
美国FDA发布关于酷柏(CooperVision)公司AVAIRA Toric软性接触镜的召回通告
产品:AVAIRA Toric(enfilcon A)软性亲水性接触镜。
范围:生产日期为2010年11月1日至2011年8月3日的产品。
英国MHRA发布关于康乐保(Coloplast)公司Assura和Sensura术后造口袋的警戒通告
产品:Assura和Sensura无菌术后造口袋。
范围:多个产品编号和批号的产品。
FDA发布关于贝克曼库尔特(Beckman Coulter)公司DEHA放射免疫检测试剂的召回通告
产品:DEHA放射免疫检测试剂。
范围:参考号DSL-8900,批号为991112,991346,991584,991857,992115,992359,992458,992854,100115A,100205A,100205RA,100226A,100226RA,100319A,100319RA,100409A,100409RA,100430A,100430RA,100521A,100611A,100611RA,100702A,100723A,100723B,100723RA,100813A,100813RB及100813C的产品。
FDA发布关于美敦力(Medtronic)公司SynchroMed II植入式输液泵的召回通告
产品:SynchroMed II植入式输液泵。
范围:型号为8637-20和8637-40,销售日期为2004年3月至2011年7月8日的产品。
美国FDA发布关于李医疗(Lee Medical)公司用户透析盘/套装的召回通告
产品:用户透析盘/套装。
范围:生产日期为2010年11月17日至2011年1月11日,且销售日期为2010年11月23日至2011年1月12日的产品。具体如下。

产品名称 包装 批号 失效期 BIN号ADV-CARE-ISL44 100/CS#K1018EXP 5-12 34B COMMUNITYCATH 150/CS#K1052 EXP 5-12 36B COLUMBUS-CATH 50/CS #1080 EXP 5-12 39B RENALSG-CATH 75/CS #L1046 EXP 6-12 40B SUNYDOWNHEMO 100/CS #l1015 EXP 6-12 28A KIDNEYCARE 125/CS #l1070 EXP 6-12 -METHODIST-CATH 75/CS #L1072 EXP 6-12 -METHODIST-HEMO 150/CS#L1073 EXP 6-12 -MERCYMED-CATH 75/CS #L1077EXP 6-12 39A SANTACLA-CATH 75/CS #A1118EXP 7-12 44A
FDA发布关于IL公司GEM Premier 4000 PAK 测试卡片的召回通告
产品:GEM Premier 4000全自动分析仪使用的 PAK 测试卡片。
范围:生产日期为2006年5月至2011年7月的下列产品。

产品描述 型号GEM 4000 BG/Hct/Lytes/CO-Ox-iQM 00027407508,00027415008,00027430008,00027445008,00027360008 GEM 4000 BG/Hct/Lytes/G/L/CO-Ox-iQM 00027407510,00027415010,00027430010,00027445010,00027360010 GEM 4000 BG/Hct/Lytes/CO-Ox/tBili-iQM 00027407509,00027415009,00027430009,00027445009,00027360009 GEM 4000 BG/Hct/Lytes/G/L/CO-Ox/tBili-iQM 00027407511,00027415011,00027430011,00027445011,00027360011
FDA发布关于Vital Signs公司人工鼻的召回通告
产品:人工鼻。
范围:具体产品如下。
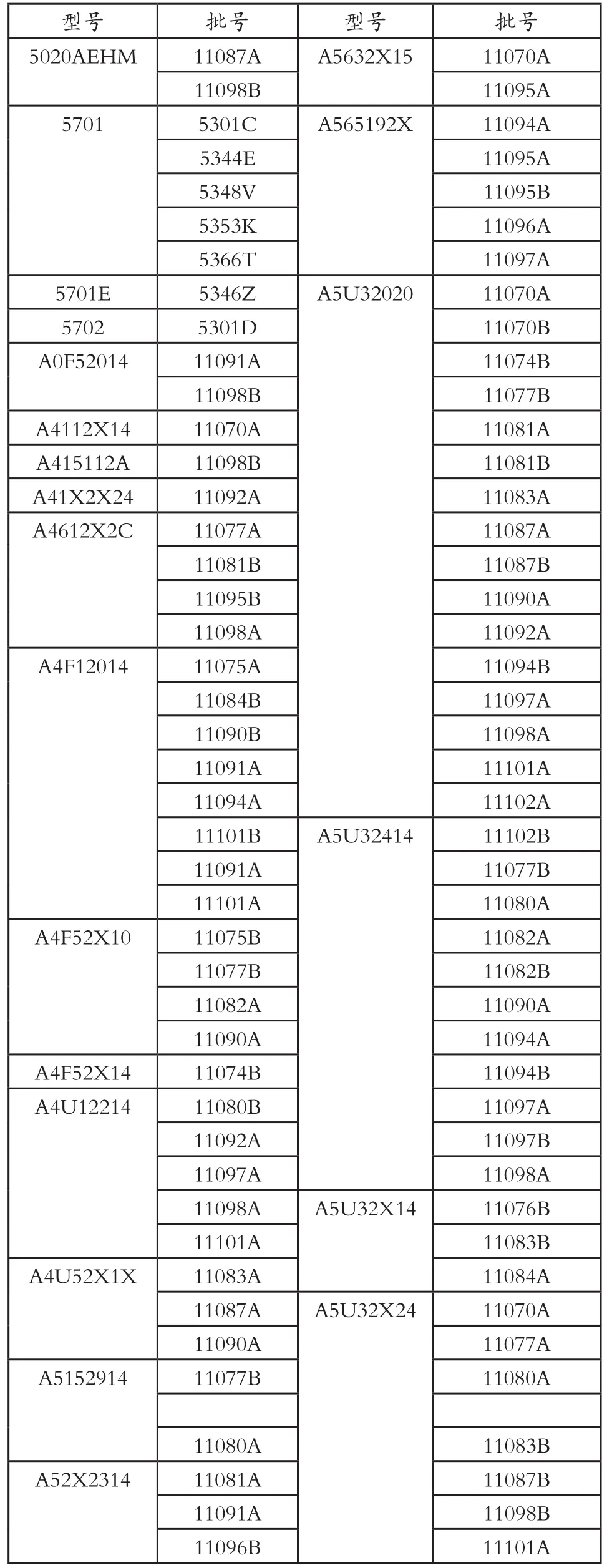
型号 批号 型号 批号5020AEHM 11087A A5632X15 11070A 11098B 11095A 5701 5301C A565192X 11094A 5344E 11095A 5348V 11095B 5353K 11096A 5366T 11097A 5701E 5346Z A5U32020 11070A 5702 5301D 11070B A0F52014 11091A 11074B 11098B 11077B A4112X14 11070A 11081A A415112A 11098B 11081B A41X2X24 11092A 11083A A4612X2C 11077A 11087A 11081B 11087B 11095B 11090A 11098A 11092A A4F12014 11075A 11094B 11084B 11097A 11090B 11098A 11091A 11101A 11094A 11102A 11101B A5U32414 11102B 11091A 11077B 11101A 11080A A4F52X10 11075B 11082A 11077B 11082B 11082A 11090A 11090A 11094A A4F52X14 11074B 11094B A4U12214 11080B 11097A 11092A 11097B 11097A 11098A 11098A A5U32X14 11076B 11101A 11083B A4U52X1X 11083A 11084A 11087A A5U32X24 11070A 11090A 11077A A5152914 11077B 11080A 11080A 11083B A52X2314 11081A 11087B 11091A 11098B 11096B 11101A
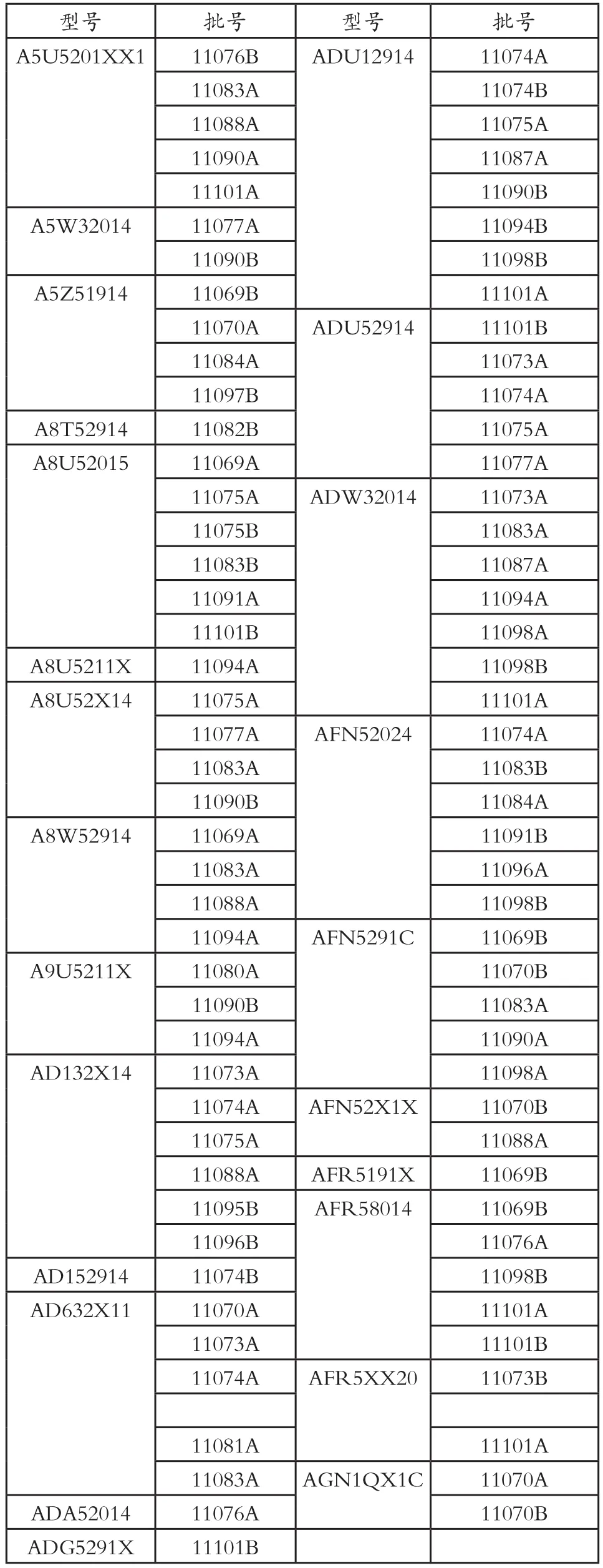
型号 批号 型号 批号A5U5201XX1 11076B ADU12914 11074A 11083A 11074B 11088A 11075A 11090A 11087A 11101A 11090B A5W32014 11077A 11094B 11090B 11098B A5Z51914 11069B 11101A 11070A ADU52914 11101B 11084A 11073A 11097B 11074A A8T52914 11082B 11075A A8U52015 11069A 11077A 11075A ADW32014 11073A 11075B 11083A 11083B 11087A 11091A 11094A 11101B 11098A A8U5211X 11094A 11098B A8U52X14 11075A 11101A 11077A AFN52024 11074A 11083A 11083B 11090B 11084A A8W52914 11069A 11091B 11083A 11096A 11088A 11098B 11094A AFN5291C 11069B A9U5211X 11080A 11070B 11090B 11083A 11094A 11090A AD132X14 11073A 11098A 11074A AFN52X1X 11070B 11075A 11088A 11088A AFR5191X 11069B 11095B AFR58014 11069B 11096B 11076A AD152914 11074B 11098B AD632X11 11070A 11101A 11073A 11101B 11074A AFR5XX20 11073B 11081A 11101A 11083A AGN1QX1C 11070A ADA52014 11076A 11070B ADG5291X 11101B
信息来源:国家药品不良检中心/国家食品药品监督管理局药品评价中心网站
http://www.cdr.gov.cn/gxzy/_ywjjkx_/_ylqxjjkx_/index.shtml
