应用组织多普勒研究厄贝沙坦对房内传导的影响*
2011-01-23焦玉燕
刘 锦 杜 波 焦玉燕
(1.青岛大学医学院,山东 青岛 266021;2. 山东省泰山医院,山东 泰安 271000;3. 泰山医学院附属泰山医院,山东 泰安 271000)
高血压病并发症中房性心律失常较常见,有创性电生理检查结果提示,心房内传导延迟是心房纤颤(AF)的重要特征[1]。AF的发病机制尚未十分明确,近年来的研究表明肾素-血管紧张素系(rennin-angiotensinsystemRAS)的激活在心房重构中发挥重要作用。阻断RAS系统可以抑制心房重构,从而有利于AF的转复和窦性心律的维持,该观点为血管紧张素Ⅱ(AngⅡ)受体阻滞剂(ARB)防治心房纤颤提供了理论依据[2]。组织多普勒成像(tissue Doppler imaging, TDI)是一种显示心肌组织运动时序的技术,已有应用这一技术测定正常人心房收缩和电-机械时间的报道[3]。本研究应用TDI技术,探讨血管紧张素Ⅱ受体阻滞剂对心房内传导时间的影响,以研究该类药物减少心房颤动的可能机制。
1 资料与方法
1.1研究对象 2009年1月至2009年12月于山东省泰山医院住院或门诊就诊的高血压病患者60例,入选标准为①符合WHO与国际高血压学会的高血压诊断标准:在未使用抗高血压药物的情况下,收缩压≥140mmHg和(或)舒张压≥90mmHg,②既往未使用过ACEI和ARB类药物或停用上述药物5个半衰期以上,且无ARB类药物用药禁忌症,③心功能(NYHA分级) ≤Ⅲ级。④除外房室传导阻滞,病态窦房结综合征,先天性或获得性长Q-T间期综合症。将符合标准的60例患者随机分为对照组30例和试验组30例。
1.2研究方法 仪器采用Vivid7型彩色多普勒,探头频率2-4 MHz,取组织多普勒的速度模式,取心尖四腔切面,取样容积分别放置在三尖瓣、室间隔与房间隔交界处、二尖瓣环处, 获得满意图像,扫描速度为100 m/s,探及心房收缩波A波最为清晰为止,同步记录心电图, 测量心电图P波起始点到多普勒组织显像A波起始点的时间,分别用P-AR、P-AS及P-AL表示。试验组口服厄贝沙坦,起始剂量150 mg,每日一次,必要时加大药量。对照组患者给予钙通道阻滞剂或与利尿剂联合控制血压。两组降压的目标血压均为收缩压<140 mmHg,舒张压<90 mmHg,两组患者在治疗前及治疗后6个月时分别行组织多普勒测量房内传导间期。
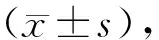
2 结 果
试验组服药前后心房内传导间期变化有显著统计学差异,见表1,图1,2。对照组服药前后心房内传导间期变化无统计学差异,见表2,图3,4。

表1 厄贝沙坦组服药前后心房内传导间期比较
治疗前后比较P值均<0.01

图1 患者服药前P-AL间期测量值

图2 为同一患者服药6月后P-AL间期测量值

房内传导间期 P-AR P-AS P-AL治疗前54.37±16.9164.67±19.9388.77±16.78治疗后53.93±17.0665.37±19.8189.07±16.69
治疗前后比较P值均>0.05

图3 患者服药前 P-AL 测量值

图4 为同一患者服药6月后P-AL 测量值
3 讨 论
高血压病常见的并发症之一为房性心律失常[4],近年来的研究表明心房结构重构(atrial structuralremodeling ASR)和心房电生理重构(atrial electrial remodeling AER)与心房纤颤的发生、发展关系密切。AF的发生和维持与肾素-血管紧张素系统(RAS)激活有关。病理学研究发现,心房间质纤维化是AF患者ASR最突出的表现[5],AngⅡ可加重心房间质纤维化。Nakashima等[6]发现,坎地沙坦醋(ARB)和卡托普利(ACEI)能有效抑制AER,证实血管紧张素参与AER。低剂量胺碘酮联合ARB或ACEI可提高心功能正常的阵发性AF患者窦性心律的维持率,减少复发。Wachtell等[7]对氯沙坦干预降低高血压患者终点事件研究(LIFE)的资料进行分析时发现,在相同血压水平下,ARB可明显减少高血压患者新发AF,其作用优于β受体阻断剂。ARB不仅可以减少高血压、心室肥厚或心功能不全患者的AF的发生率,而且与抗心律失常药联用可提高对于AF复律患者AF的转复率和减少AF的复发。
判断左右心房电机械时间及收缩活动对了解心房的生理及病理现象以及药物的作用机制极有帮助,但以往均通过有创性检查来实现。自从组织多普勒技术出现后,TDI技术在心脏电生理学领域中的应用受到关注[8]。本研究应用TDI技术,测量了实验组和对照组服药前后左、右心房和左、右心房交界处的电-机械收缩时间, 实际包括传导时间及兴奋-收缩偶联时间[9],该法简便易行,重复性好。
心脏电生理研究证实,房颤患者有房内或心房间的传导延迟[10],本研究结果显示, 试验组左、右心房和左、右心房交界处的P-A值均较对照组显著缩短,说明ARB药物能缩短高血压患者房内传导间期,此可能为其能预防及治疗AF的原因之一,分析其缩短房内传导间期的机理,可能为ARB通过抑制AngⅡ,从而抑制或减轻由AngⅡ介导的ASR或AER。
综上所述, TDI技术为研究ARB药物对患者的心电生理影响提供了一种无创性的新方法,但本文仅作了初步探讨,有关P-A的正常值及P-A对AF的预防以及治疗价值等尚需大样本的深入研究。ARB除了具有降压、改善心功能、减少尿蛋白等临床作用外,又增加了防治AF发生的额外效应,给ARB的临床应用无疑增添了新的亮点,但要确定其在AF防治中的意义仍需进一步的研究。而应用组织多普勒研究ARB药物对房内传导的影响,是一个新颖的研究方法,有着较为广阔的前景,能直观的展现药物对房内传导的影响,更好的评价药物的作用。
[1] Shimizu A,Fukatani M,Tanigawa M,et al.Intra-atrial conduction delay and fragmented atrial activity in patients with paroxysmal atrial fibrillation[J].Jpn Circ J,1989, 53:1023-1030.
[2] 罗骏.肾素-血管紧张素系统与心房颤动[J].国际心血管病杂志,2007,34(4):261-264.
[3] Rein AJ, o Donnell CP, Colan SD, et al.Right and left atrialcontraction time and electromechanical coupling using tissuevelocity imaging[J]. Circulation, 2000,102(18):383.
[4] Martinez Lopez JI. Pauses and causes[J]. J La State Med Soc,1996 Apr,148(4):139-141·
[5] Corradi D,Callegari S,Benussi S,et al. Regional left atrial interstitial remodeling in Patients with chroic atrial fibrillation undergoing mitral一valve surgery. VirehowsAreh,2004,445(5):498-505.
[6] Nakashima H,Kumagai K,Urata H,et al. AngiotensinⅡantagonist prevents electrical remodeling in atrial fibrillation.Circulation,2000,101(22):2612-2617.
[7] Wachtell K,Lehto M,Gerdts E,et al. AngiotensinⅡreceptor blockade reduces newonset artria fibrillation and subsequent stroke compared to atenolol ;The losartan intervention for end point reduction in hypertension (LIFE)study. J Am Coll Cardiol,2005,45(5):712-715.
[8] Sutherland S,Bartel T, Schurger D ,et al .Doppler myocardial imaging in the evaluation of normal and abnormal ventricular depolarization (Abstract). Br Heart J, 1995, 73 (suppl 3) :85.
[9] R Mizuno, S Fujumoto , H Nakano. Atrial conduction abnormality in patients with systemic progressive sclerosis[J]. Eur Heart J, 1997, 18:1995-2001.
[10] Spodick DH,Olds PA,Saad KM. Electromechanical disease of the left atrium -interatrial block. Eur Heart J,2000,2(suppl K):K76-K77.
