丁二酸酐修饰啤酒废酵母菌去除Cu2+、Cd2+的性能研究
2011-01-23李步海郭海霞孙小梅中南民族大学化学与材料科学学院分析化学国家民委重点实验室武汉430074
李步海,郭海霞,孙小梅(中南民族大学 化学与材料科学学院,分析化学国家民委重点实验室,武汉 430074)
含重金属离子的废水直排到水中,影响生态环境和人体健康,造成资源浪费.镉、铜超量排放,引起了社会的广泛关注.被污染的水用传统的处理方法费用很高.用微生物吸附能力又有限,如通常对微生物进行酸处理[1]、碱处理[2]、丙酮处理[3]、热处理[4]、乙醇处理[5]、饱和碳酸氢钠处理[6-8]等,方法简单, 但菌体表面并未增加新的活性功能团,因此吸附能力提高不明显.
啤酒酵母是重要的微生物之一,广泛用于食品和饮料工业.废弃的啤酒酵母菌仍然与活体菌一样,表面含有羟基、氨基等官能团,是良好的低成本废水处理材料,不过有表面结构疏散,粒径较小,不利于相分离,吸附容量低等缺点.直接用于处理废水吸附容量低.一般通过交联改善机械强度[9,10],但是交联反应会占据部分活性基团,降低吸附效果,因而在菌体表面接枝活性基团,增加活性位点数是提高吸附量的有效方法.本法采用丁二酸酐作修饰剂,增加吸附剂表面的羧基.通过菌体表面的氨基和修饰的羧基对重金属离子的协同作用提高吸附容量.
1 实验
1.1 仪器与试剂
AA-6300型原子吸收光谱仪(日本岛津公司);JJ-1000W 精密增力电动搅拌器(金坛市科兴仪器厂;DF-101S集热式恒温加热磁力搅拌器(上海羌强仪器设备有限公司);SHZ-03恒温水浴摇床(上海堪鑫仪器设备有限公司);Multilab 2000型电子能谱仪(XPS)(英国 VG公司);NEXUS 470 智能型傅立叶红外光谱仪(美国珀金-埃尔默公司).
啤酒废酵母菌(武汉某啤酒厂);50%戊二醛(天津市科密欧化学试剂有限公司);丁二酸酐(国药集团化学试剂有限公司);氯化铜、氯化镉(北京化工厂);N,N二甲基甲酰胺(DMF,国药集团化学试剂有限公司);无水乙醇(国药集团化学试剂有限公司);蒸馏水.
1.2 吸附剂的制备
称取1.0 g经水洗干燥的啤酒废酵母菌于250 mL的锥形瓶中,加入2 mL戊二醛,50 mL蒸馏水,25 ℃水浴摇床振荡14 h,过滤,水洗,醇洗,40℃真空烘干,得交联啤酒废酵母菌.
称取1.0 g交联的啤酒废酵母菌于100 mL的圆底烧瓶中,将0.5 g丁二酸酐溶入50 mL的DMF中,加入烧瓶中,65 ℃搅拌反应12 h,过滤,水洗,醇洗,40 ℃真空烘干,得丁二酸酐修饰啤酒废酵母菌(修饰菌1);常温下,将修饰菌1用饱和碳酸氢钠于摇床中振荡反应2 h,过滤,水洗,醇洗,40℃的真空烘干,得碱处理的丁二酸酐修饰啤酒废酵母菌(修饰菌2).
1.3 静态吸附实验
将1.2节制备的0.05 g吸附剂分别与25.00 mL不同浓度的Cu2+和Cd2+溶液移入锥形瓶中,用NaOH或HCl稀溶液调节溶液pH值,25℃于摇床(130 r/min)中吸附1 h,离心,取上清,用原子吸收法测定剩余金属离子浓度,计算吸附量Q(mg/g).
1.4 分析与表征
用红外光谱、光电子能谱仪分析表征产物.
2 结果与讨论
2.1 红外光谱分析
图1为未修饰和不同温度下制备的修饰菌1的红外光谱图,未修饰菌在1740 cm-1无峰,说明菌表面无羧基,随制备温度的递增,修饰菌1在1740 cm-1处羧基峰形不断增大,表明菌体表面的羧基增多,说明温度升高有利于修饰反应的进行. 80℃时,部分菌体溶解,因而制备的温度确定为65℃.

λ/cm-11) 未修饰菌; 2 ~ 4) 依次为50, 65, 80 ℃时的修饰菌图1 未修饰菌和不同温度下修饰菌的红外光谱 Fig.1 FTIR spectra of unmodified and modified biomass at different temperature
图2为修饰菌1和修饰菌2的红外光谱,修饰菌1在1740 cm-1处明显有峰,修饰菌2在1740 cm-1处无明显峰形,即菌体表面的羧基减小,其原因为经饱和碳酸氢钠处理后转化为—COONa形态.
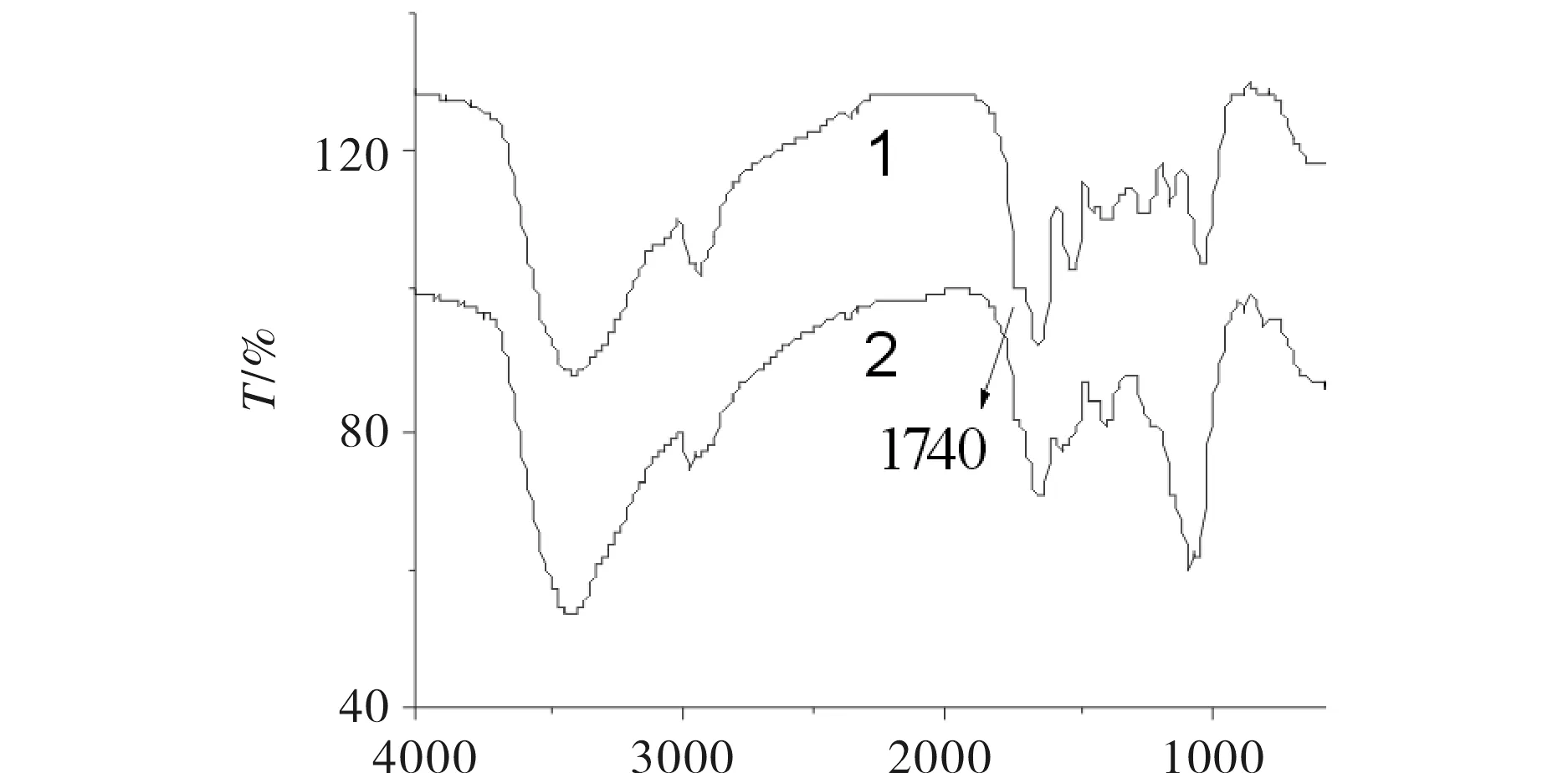
λ/cm-1图2 修饰菌1和修饰菌2的红外图谱Fig.2 FTIR spectra of the modified biomass 1 and modified biomass 2
2.2 光电子能谱解析
表1为修饰前后菌体表面元素的比较. 由表1可知,菌体修饰前后表面的O原子增加了2.68 %. 表 2为修饰菌2及未修饰菌表面各氧原子峰的峰面积之比. 由表2可知,O1s羧基氧增加了20.3 %,而未修饰菌表面无羧基氧,与红外结果一致,证明O原子的增加来自丁二酸酐,说明丁二酸酐已修饰到菌体表面.

表1 修饰前后菌体表面元素比较Tab.1 Comparison of elements of the biomass before and after modified
图3为修饰菌2和未修饰菌的O1s能谱图,未修饰菌(见图3a)中仅有531.5和528.6 eV,无530.0 eV峰,表明未修饰菌表面不存在羧基氧;修饰菌2(见图3b)中呈现3个峰: 531.5, 530.0和528.6 eV, 分别对应于O―C、O=C―O 和O=C―NH2中的氧原子结合能峰.
She was busily searching through the neighbourhood for a proper situation for her daughter...[3]
3个峰的峰面积之比见表2,修饰后O1s峰的峰面积比明显改变,羧基氧的氧含量由0 %提高至20.3 %,双键氧含量明显增加,印证丁二酸酐已修饰到菌体表面.而羟基氧含量由87.0 %降至69.9 %,羟基氧的减少可能是羟基与羧基发生了部分酯化反应.

表2 修饰菌2及未修饰菌表面各氧原子峰的峰面积之比Tab.2 Peak area ratios of the oxygen of the unmodified biomass and the modified biomass 2

图3 未修饰菌(a) 及修饰菌2 (b)的O1s的XPS谱图.Fig.3 O 1s XPS spectra of before (a) and after (b) modified biomass 2
2.3 Cu2+和Cd2+的吸附性能
2.3.1 动力学曲线
图4为Cu2+和Cd2+的吸附动力学曲线.由图4可见,修饰菌2对Cu2+和Cd2+的吸附在前20 min吸附速度较快,并迅速达到平衡; 20 min后,菌体表面的活性吸附位点(—COO-)逐渐被Cu2+、Cd2+离子取代,吸附速度降低.

1) 未修饰菌; 2) 修饰菌2吸附条件:CCu2+=130.0 mg/ L, CCd2+=161.0 mg/ L, pH=5.0, T=298 K图4 菌体对Cu2+和Cd2+的吸附动力学曲线Fig.4 Adsorption kinetic curve of the biomass for Cu2+ and Cd2+
实验所得的数据用准二级方程拟合,动力学参数见表3,修饰菌2的所有判定系数R2>0.999说明对Cu2+和Cd2+的吸附符合准二级动力学方程.

表3 菌体吸附Cu2+和Cd2+的准二级动力学曲线模拟方程参数Tab.3 Kinetic parameters of the pseudo-second-order equation for Cu2+ and Cd2+ adsorption
注:V0为反应速率;qe为平衡吸附容量;k为速率常数
2.3.2 p H值的影响
pH对Cu2+和Cd2+的吸附性能的影响见图5. 当pH>3.0,修饰菌2对Cu2+的吸附率达98 %,其原因为经饱和碳酸氢钠处理后,菌表面的—COOH转变为—COONa,Na+比H+更容易完成离子交换,有利于金属离子的吸附.同样对Cd2+的吸附率也达98 %,证实此吸附剂表面的活性官能团为—COONa,起离子交换作用的为该官能团中的Na+.

1) 未修饰菌;2) 修饰菌2吸附条件:CCu2+=25.0 mg/L, CCd2+=25.0 mg/L, T=298 K, t=30 min图5 pH对Cu2+和Cd2+吸附率的影响Fig.5 Effect of pH on adsorption rates of Cu2+ and Cd2+
2.3.3 吸附等温线

1) 未修饰菌;2) 修饰菌2吸附条件: T=298 K, t=30 min, pH=5.0图6 Cu2+和Cd2+的吸附等温线Fig.6 Adsorption isotherms of Cu2+ and Cd2+
分别用Langmuir[11]和Freundlich[12]模型对图6数据进行拟合.模拟参数见表4,所得判定系数R2>0.99,说明修饰菌2对Cu2+和Cd2+的吸附过程更符合Langmuir等温模式.

表4 菌体对Cu2+和Cd2+吸附的Langmuir和Freundlich吸附等温线模拟参数Tab.4 Langmuir and Freundlich parameters for the absorption of Cu2+ and Cd2+ on the biomass
注:b、KF为吸附常数;qm为吸附容量
同样,根据公式ΔGθ= -RTlnKc和Kc=qe/Ce可计算出吸附反应的ΔGθ(见表5),其中,R为常数(8.314J/(mol· K)),T(K)为吸附反应时的绝对温度,Kc为平衡常数,通过ln(qe/Ce)对qe作图,当qe=0时,Y轴上的截距即为lnKc.
表5为吸附剂对Cu2+和Cd2+的热力学参数. 由表5可见,各ΔGθ<0,表明修饰菌2和未修饰菌对Cu2+和Cd2+的吸附反应均为自发反应,且ΔGθ值还表明修饰菌2对Cu2+、Cd2+的吸附较未修饰菌更容易.

表5 吸附剂对Cu2+和Cd2+的热力学参数Tab.5 Hermodynamic constants of Cu2+ and Cd2+
2.4 吸附机理探讨
图7为修饰菌2吸附Cu2+和Cd2+前后的红外图谱. 由图7可见,修饰菌2在1570 、1400 cm-1呈现2个峰,分别对应于羧酸中C=O的对称和不对称伸缩振动峰. 吸附Cu2+和Cd2+后, 2峰的强度均发生改变,并产生位移:吸附Cu2+后,2峰分别位移至1530 cm-1和1410 cm-1;吸附Cd2+后,分别位移至1550cm-1和1410 cm-1,可表明羧基参与了吸附.在吸附Cu2+和Cd2+后,位于1090 cm-1的氨基、羟基峰位移至1060 cm-1, 表明氨基、羟基也参与了吸附. 因此修饰菌2的吸附主要源于其表面的羧基, 氨基, 羟基官能团的作用, 还可能通过离子交换、范德华力、配位作用与Cu2+、Cd2+结合.

λ/cm-11) 修饰菌2 ; 2) 吸附Cd2+后; 3) 吸附Cu2+后 图7 修饰菌2吸附Cd2+和Cu2+前后的红外图谱Fig.7 FTIR spectra of modified biomass 2, modified biomass 2 with Cd2+ adsorption, modified biomass 2 with Cu2+ adsorption
2.5 模拟水样处理
取南湖水,过滤,得废水样底液,加入一定量的氯化铜和氯化镉溶液,并调节溶液的pH为5.0,得模拟废水样液.从中取25.00 mL.按1.3节操作,所得结果见表6.

表6 修饰菌对废水处理结果Tab.6 Results of the modified biomass in treating simulated wastewater
注:C0为初始溶液中金属离子的浓度,Ce为吸附后溶液中金属离子的浓度
3 结语
丁二酸酐修饰的啤酒废酵母,合成方法简单,原料易得、吸附条件温和,能快速有效地从废水样中吸附重金属离子Cu2+和Cd2+,修饰后的吸附能力分别为未修饰的3.3和11.5倍,去除率高.说明修饰啤酒废酵母明显提高了对重金属离子Cu2+和Cd2+的吸附能力.吸附过程符合准二级动力学方程,吸附模式为Langmuir单分子层吸附.
[1] Arica M Y, Tuzun I, Emine Y, et al. Utilisation of native, heat and acid-treated microalgae chlamydomonas reinhardtii preparations for biosorption of Cr(VI) ions[J]. Process Biochem, 2005, 40: 2351-2358.
[2] Tan T W,Cheng P. Biosorption of metal ions with penicillium chrysogenum[J]. Appl Biochem Biotechnol,2003,104(2):119-128.
[3] Ashkenazy R, Gottlieb L, Yannai S. Characterization of acetone-washed yeast biomass functional groups involved in lead biosorption[J]. Biotechnol Bioeng, 1997, 55 (1) : 1-10.
[4] Guvenc U,Goksungur Y,Uren S.Biosorption of cadmium and lead ions by ethanol treated waste baker′s yeast biomass[J]. Bioresour Technol, 2005, 96: 103-109.
[5] Rinco′n J, Gonza′lez F, Ballester A, et al. Biosorption of heavy metals by chemically activated alga Fucus vesiculosus[J]. J Chem Technol Biotechnol, 2005, 25: 2568-2575.
[6] Lodeiro P, Cordero B, Grille Z, et al. Physicochemical studies of cadmium (II) biosorption by the invasive alga in Europe, sargassum muticum[J]. Biotechnol Bioeng, 2004, 88: 237-247.
[7] Loukidou M X, Matis K A, et al. Removal of As (V) from wastewaters by chemically modified fungal biomass[J]. Water Res, 2003, 37: 4544-4552.
[8] Leandro V A G., Osvaldo K J, Ros P G, et al. Adsorption of Cu(II), Cd(II), and Pb(II) from aqueous single metal solutions by cellulose and mercerized cellulose chemically modified with succinic anhydride[J]. Biores Technol, 2008, 99: 3077-3093.
[9] Chen J P, Yang L. Chemical modification of Sargassum sp. for prevention of organic leaching and enhancement of uptake during metal biosorption [ J ] . Ind Eng Chem Res,2005,44(26):9 931-9942.
[10] Jalali -Rad R, Ghafourian H, Asef Y, et a1. Biosorp-tion of cesium by native and chemically modified biomass of marine algae:introduce the new biosorbents for biotechnology applications [ J ]. Hazard Mater,2004,116(1/2 ):125 -134.
[11] Wang R, Liao X P, Shi B. Adsorption behaviors of Pt(II) and Pd(II) on collagen fiber immobilized bayberry tannin[J]. Ind Eng Chem Res, 2005,44 : 4221-4226.
[12] Crini G. Non-conventional low-cost adsorbents for dye removal: a review[J]. Bioresour Technol,2006, 97:1061-1085.
