RP-HPLC法同时测定不同产地红参中 6种人参皂苷的含量
2011-01-12濮社班朱玲英钱士辉
刘 丹 , 濮社班 , 朱玲英 , 钱士辉*
(1.江苏省中医药研究院中药化学研究室,江苏南京 210028;2.中国药科大学生药学研究室,江苏南京 211198)
红参是由五加科植物人参 (Panax ginseng C.A.M eyer)的栽培品经蒸制后所得的干燥根和根茎[1]。人参皂苷是其最主要的有效成分之一[2],也是判断其质量优劣的重要指标之一。目前国内外采用高效液相色谱法测定红参中人参皂苷的研究报道较多[3-7]。2010年版《中国药典》(一部)红参项下要求对其主要成分 Rg1、Re和 Rb1的含量进行测定[1]。此外,Ro也是红参中人参皂苷的主要成分之一,其含量对红参药材质量的评价有重要意义[4]。本课题组从红参中分离得到了人参皂苷Rg1、Re、R f、Rb1、Rc和 Ro。本文采用反相高效液相色谱法同时测定不同产地红参中上述各皂苷成分的含量,旨在为红参药材质量标准的提高提供依据。
仪器与试药
1.1 仪器
W aters2695高效液相色谱仪(四元泵自动进样系统);W aters 2996二极管阵列紫外检测器; Empower化学工作站(美国沃特世公司);M ETTLER TOLEDO AT-201十万分之一电子天平 (梅特勒-托利多仪器上海有限公司);BUCH IR-200旋转蒸发仪(瑞士步琪公司);KQ-500B型超声波清洗器 (功率: 250W,频率:50 kHz,昆山市超声仪器有限公司)。
1.2 试药
人参皂苷 Rg1、Re、R f、Rb1、Rc和 Ro对照品均为自制,归一化法测得其纯度均大于 98%。不同产地药材共 10批,购于吉林 (集安、抚松、通化北、长白山、汪清县、安图、靖宇)和辽宁 (抚顺、本溪、新宾),经江苏省中医药研究院钱士辉研究员鉴定为红参。乙腈(美国 TED IA公司)、甲醇 (江苏汉邦科技有限公司)均为色谱纯;磷酸为分析纯;水为重蒸馏水(M illi-Q纯水器制得)。
方法与结果
2.1 色谱条件
色谱柱为 A lltim aTM-C18(250 mm×4.6 mm, 5μm),流动相为乙腈-0.1%磷酸水溶液,梯度洗脱(0~35 m in,19%乙腈;35~55 m in,19%乙腈→29%乙腈;55~60 m in,29%乙腈;60~85 m in, 29%乙腈→40%乙腈);流速:1.0 m L·m in-1;检测波长:203 nm;柱温:30℃,进样量:10μL。
2.2 溶液的制备
2.2.1 对照品溶液的制备 取已干燥至恒重的人参皂苷 Rg1、Re、R f、Rb1、Rc和Ro对照品各约5m g,精密称定,分别置 5mL容量瓶中,以甲醇溶解稀释并定容至刻度,摇匀,即分别得人参皂苷 Rg1、Re、R f、Rb1、Rc和 Ro对照品储备液。取 10m L量瓶一只,分别精密加入上述对照品储备液 2.0、0.5、0.5、2.5、1.0和 2.5mL,加甲醇稀释至刻度,摇匀,得混合对照品溶液,上述各成分质量浓度分别为 0.201、0.051、0.052、0.253、0.102和 0.256 g·L-1。
2.2.2 供试品溶液的制备 取红参粉末 (过 4号筛,孔径 4.75mm)约 1 g,精密称定,置索氏提取器中,加三氯甲烷适量,加热回流 3 h,弃去三氯甲烷液,药渣挥干溶剂,连同滤纸筒移入具塞锥形瓶中,精密加入水饱和的正丁醇 50mL,密塞,放置过夜,超声处理 30m in,滤过,精密吸取续滤液 25 m L,置蒸发皿中蒸干,残渣加甲醇溶解并转移至5mL量瓶中,加甲醇至刻度,摇匀,即得。
2.3 系统适用性试验
按“2.2”项下方法制得混合对照品和供试品溶液,并按“2.1”项下条件进样测定,结果显示,混合对照品中各人参皂苷的保留时间与供试品中的一致,供试品中各人参皂苷成分达到有效分离。结果见图1。
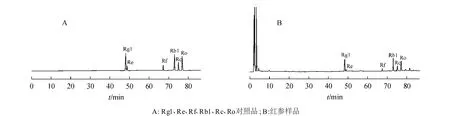
图1 Rg1、Re、R f、Rb1、Rc和 Ro对照品及红参样品色谱图Figure 1 HPLC chrom atogram sof reference substancesof Rg1,Re,R f,Rb1,Rc,Ro and samp le of red ginseng
2.4 线性关系的考察
分别精密吸取“2.2.1”项中制备的混合对照品溶液 3、10、15、20、25和 30μL,进样测定,记录色谱图。以峰面积为纵坐标 (Y),待测组分的质量 (μg)为横坐标(X),绘制标准曲线并进行线性回归。结果显示,Rg1、Re、R f、Rb1、Rc和 Ro的质量分别在0.603~6.03μg、0.153~1.53μg、0.157~1.57μg、0.758~7.58μg、0.306~3.06μg和 0.768~7.68μg范围内时,质量与峰面积均呈良好的线性关系,线性方程分别为:

2.5 精密度试验
精密吸取“2.2.1”项中制备的混合对照品溶液10μL,连续进样 6次,测定峰面积,结果得 Rg1、Re、R f、Rb1、Rc和 Ro峰面积的 RSD(n=6)分别为1.0%、1.3%、1.8%、1.2%、1.4%和 1.2%。表明本方法精密度良好。
2.6 重复性试验
取同一产地(吉林靖宇)药材 1.0 g,精密称定,平行 6份,按“2.2.2”项下方法制得供试品溶液,进样测定,结果得Rg1、Re、R f、Rb1、Rc和 Ro含量的平均值(n=6)分别为 0.230%、0.044%、0.064%、 0.344%、0.130%和 0.364%,RSD分别为 1.3%、1.5%、1.7%、0.8%、1.7%和 1.0%。表明本方法重复性良好。
2.7 稳定性试验
取同一产地 (吉林靖宇)药材,按“2.2.2”项下方法制得供试品溶液,分别于 0、2、4、8、12 h进样,测定峰面积,结果得 Rg1、Re、Rf、Rb1、Rc和Ro峰面积的 RSD(n=5)分别为 1.4%、1.3%、1.9%、0.90%、1.8%和 1.1%。表明供试品溶液在 12 h内基本稳定,本方法有良好的稳定性。
2.8 加样回收率试验
取已知含量的红参粉末 (吉林靖宇),过 4号筛,取约 0.5 g,精密称定,人参皂苷 Rg1、Re、Rf、Rb1、Rc和 Ro的含量分别为 0.228%、0.044%、0.063%、0.339%、0.130%和 0.302%,分别加入Rg1、Re、R f、Rb1、Rc和 Ro对照品 1.140、0.219、0.316、1.705、0.650和 1.510 m g,平行 6份,按“2.2.2”项下方法制备回收率测试溶液,进样测定,结果得人参皂苷 Rg1、Re、Rf、Rb1、Rc和 Ro平均回收率 (n=6)分别为 101.3%、99.2%、98.1%、97.6%、100.7%和 99.0%,RSD分别为 0.41%、2.03%、1.03%、0.33%、2.31%和 1.87%。
2.9 样品含量测定
取不同产地的样品各 3份,精密吸取按“2.2.2”项下方法制备的供试品溶液,进样测定,按外标法计算样品中 Rg1、Re、R f、Rb1、Rc和 Ro的平均含量,结果见表1。

表1 不同产地红参中人参皂苷 Rg1、Re、Rf、Rb1、Rc和 Ro的平均含量(n=3)Tab le 1 Determ ination resultsof ginsenosidesRg1,Re,R f,Rb1,Rc,Ro in red ginseng of differentorigins
讨论
本试验分别比较了索氏脱脂后超声提取、加热回流提取、超声提取 3种不同方法的提取效果,结果发现按药典方法进行脱脂后超声提取效果较好。
对乙腈-水、乙腈-0.1%磷酸水溶液 2种不同流动相的考察结果表明,以乙腈-0.1%磷酸水溶液为流动相时可获得较好的分离效果,原因可能是人参皂苷Ro为齐敦果烷型酸性皂苷,加入0.1%磷酸可改善峰形。人参皂苷 Rg1、Re的结构相似,保留时间非常相近,故较难分离,经反复摸索,发现在50m in左右才能完全达到基线分离;比较不同梯度下的色谱图,仅在“2.1”项中所用梯度下各成分均能达到基线分离,其他梯度条件虽能缩短分析时间,但各成分不能达到基线分离,故此梯度为最佳条件。
本实验对10批药材中的人参皂苷 Rg1、Re、Rf、Rb1、Rc、Ro的含量测定结果显示,Rg1、Re和 Rb1的含量分别介于 0.189%~0.236%、0.045%~0.137%和 0.215%~0.654%,表明不同产地的红参药材中人参皂苷 Rg1、Re、Rb1的含量均能达到2010年版《中国药典》红参项下的要求[1]。另 3种人参皂苷 Rf、Rc和 Ro的含量分别介于 0.030%~0.089%、0.106%~0.275%和 0.139%~0.576%。表2结果显示,吉林长白山所产红参中 6种皂苷的总量较高,辽宁新宾所产红参中 6种皂苷的总量偏低;此外,不同产地人参皂苷Rb1、Ro的含量差异也较大。
荆淑芹等[6]测定了红参中 Rb2、Rd等 7种人参皂苷的含量,未报道人参皂苷 Ro的含量。本实验未从红参样品中检出人参皂苷 Rb2、Rd,也未分离纯化到 Rb2、Rd的对照品;而从样品中某一成分与标准品中 Ro的保留时间和吸收光谱值相同,且在样品中加入标准品 Ro后样品中该成分色谱峰的峰面积增大等现象可确定样品中该成分为 Ro。以上结果的差异可能与红参产地的生态环境及红参的种植、采收、加工炮制有关,应重视人参的种植、采收、加工炮制等的进一步规范化研究。
[1] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2010:143.
[2] 杨秀伟.红参的化学、药理和临床研究进展[J].中成药研究,1984,28(5):30-33.
[3] Sam ukawa Keiichi,Yamashita H ideyuki,M atsuda H ideaki,et a l.Sim ultaneous analysis of saponins in Ginseng Rad ix by high perform ance liquid chrom atography[J].Chem Pharm Bu ll,1995,43(1):137-141.
[4] Sam ukawa Keiichi,H ideyuki Yam ashita,M atsuda H ideaki,et a l.Sim u ltaneous analysis of ginsenosides of various ginseng radix by HPLC[J].Yakugaku Zasshi,1995,115 (3):241-249.
[5] W ashida Daisuke,Kitanaka Susum u.Determ ination of polyacetylenes and ginsenosides in Panax species using high perform ance liquid chrom atography[J].Chem Pharm Bu ll,2003,51(11):1314-1317.
[6] 荆淑芹,姜海平,刘凤云,等.生晒参红参林下参中 7种人参皂苷含量的比较 [J].中华中医药学刊,2009, 27(1):207-209.
