克氏螯虾壳聚糖抗疲劳作用研究
2011-01-09徐刚马正荣王亚娜郑铁生
徐刚, 马正荣, 王亚娜, 郑铁生
(1.江苏省扬中市人民医院,江苏扬中 212200;2.镇江科力生物技术有限公司,江苏镇江 212001;3.江苏大学医学技术学院,江苏镇江 212013)
克氏螯虾壳聚糖抗疲劳作用研究
徐刚1, 马正荣1, 王亚娜2, 郑铁生*3
(1.江苏省扬中市人民医院,江苏扬中 212200;2.镇江科力生物技术有限公司,江苏镇江 212001;3.江苏大学医学技术学院,江苏镇江 212013)
将小鼠分为壳聚糖高、中、低3个剂量组和正常对照组,分别每天灌胃200、400、600 mg/kg壳聚糖和0.9 g/dL生理盐水,10 d后记录小白鼠负重游泳时间,比较实验前后各组小鼠的体重,采血分离血清及取组织样,测定血清尿素、肝糖元、肌糖元含量,以及乳酸脱氢酶活力等生化指标,研究克氏螯虾壳聚糖的抗疲劳作用。结果表明,克氏螯虾壳聚糖能延长小白鼠的游泳时间,抑制小鼠体重的增长,降低运动后血清尿素的增量,提高血清乳酸脱氢酶活力,显著增加肌糖元和肝糖元的储备量具有良好的抗疲劳生理活性。
克氏螯虾壳聚糖;小鼠;抗疲劳
克氏螯虾壳聚糖作为一种天然功能因子,在降 血糖[1]、降血脂[2]、抗菌[3-4]、提高免疫力等方面发挥着重要作用,但在提高机体耐力和抗疲劳方面尚未见报道。本实验选用运动耐力实验和肝糖元及肌糖原储备量、血尿素(urea nitrogen,BU)含量、血清乳酸脱氢酶(lactate dehydrogenase,LDH)活力为生化测定指标,研究克氏螯虾壳聚糖的抗疲劳作用,为壳聚糖抗疲劳活性应用提供理论基础。
1 材料与方法
1.1 材料与试剂
克氏螯虾壳聚糖由镇江科力生物技术有限公司制备。肌糖元、肝糖元、乳酸脱氢酶和血尿素测定试剂盒均购自南京建成生物工程研究所。昆明种小白鼠(动物合格证号:SCXK2003-0002),均为雄性,体质量(22±2)g,由江苏大学实验动物中心提供。
1.2 仪器
6010紫外可见分光光度计:安捷伦中国上海分公司生产;A 1604电子天平:上海天平仪器厂生产;101-2型恒温干燥箱:上海市实验仪器厂生产;RE52-4旋转蒸发仪:上海亚荣生产;HH-SH-4型电热恒温水浴锅:北京长安科学仪器厂生产;LXJ-ⅡB型离心机:上海安亭科学仪器厂生产;DNP-9052电热恒温培养箱:上海精宏实验设备有限公司生产;3K15型台式高速冰冻离心机:Sigma公司生产。
1.3 方法
1.3.1 动物分组与给药剂量及方式 小鼠于实验环境下适应3 d后随机分成4组,每组30只。正常对照组每天 0.9 g/dL生理盐水灌胃;壳聚糖低剂量组每天200 m g/kg、中剂量组400 m g/kg、高剂量组600 mg/kg,每天上午9:00灌胃给药,给药剂量为每10 g体质量0.1 mL;连续10 d,灌胃期间自由取食和饮水[5]。
1.3.2 负重游泳实验 每组随机选取10只小鼠,末次灌胃30 min后(灌胃之前不空腹),置小鼠在游泳箱中游泳。水深60 cm,水温(25 ±0.5)℃,距尾尖1 cm处,用细棉绳系体质量分数5%的铅皮。棉绳的长度要求相等,系绳时力度适中,既不可使铅皮在游泳时脱落,又不能对小鼠尾部造成痛伤。记录小鼠自游泳开始至沉至水底的时间,作为小鼠游泳时间。
1.3.3 肌糖元及肝糖元测定 每组随机选取10只小鼠,末次灌胃前空腹12 h,灌胃30 min后颈椎脱臼处死,解剖取肝脏和小鼠后腿肌肉,生理盐水漂洗,滤纸吸干,称体质量,然后进行肌糖元及肝糖元测定。具体操作按肌糖元及肝糖元测定试剂盒说明书进行。
1.3.4 乳酸脱氢酶和尿素测定 LDH测定理论表明,只有短时剧烈运动,乳酸产生量才增加[6]。运动时产生的肌乳酸可以很快进入血液,如果游泳时间过长,小鼠还可能喝了较多的水使血液稀释而降低了游泳后的血乳酸浓度,因此试验应选择短时间(8 min)剧烈运动。末次灌胃前空腹12 h,灌胃30 m in后,置小鼠在游泳箱中游泳(方法同1.3.2,不负重游泳)8 min,眼眶采血,于4℃,6 000 r/min离心10 min分离出血清,冰箱保存备用。血清乳酸脱氢酶活性和尿素含量测定,按乳酸脱氢酶和尿素测定试剂盒说明书方法进行。
1.3.5 数据处理 所有数据经统计学处理后用X±SD表示,采用SPSS13.0统计软件进行统计比较[7]。
2 结果与讨论
2.1 壳聚糖对小鼠血清生化指标的影响
通过不同的灌胃处理后,各组小鼠游泳时间和肝糖元、肌糖原、血尿素、LDH等生化指标测定结果见表1。
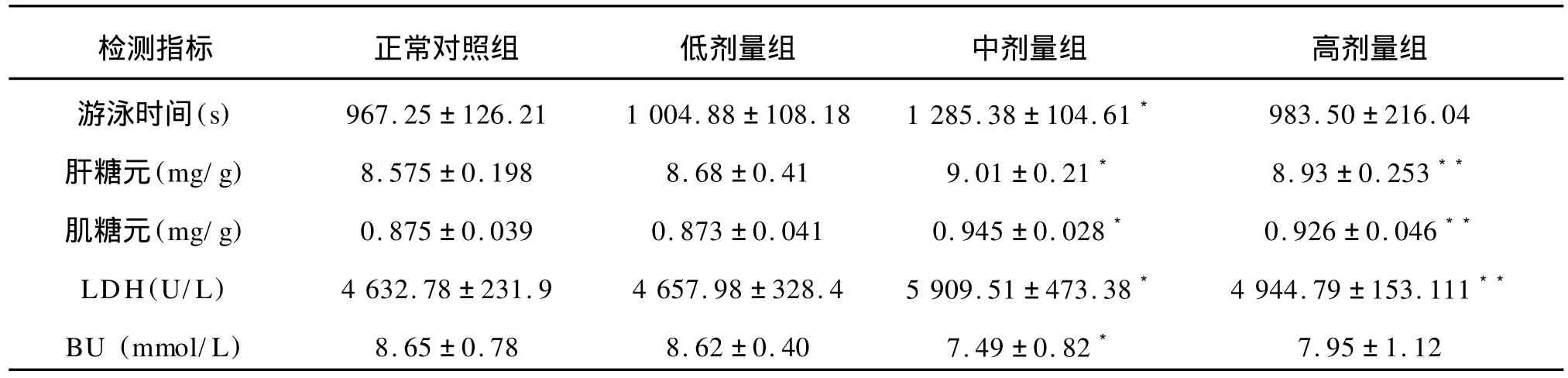
表1 抗疲劳实验结果(n=10,X±SD)Tab.1 Result of anti-fatigue experiment(n=10,X±SD)
从表1数据得知,各壳聚糖组小鼠负重游泳时间、糖元储备量、血清LDH活力均高于正常对照组,血尿素含量则低于正常对照组。其中低剂量组、中剂量组、高剂量组的负重游泳时间分别比正常对照组增加了 34.63、318.13、16.25 s;中剂量组、高剂量组肝糖元分别比正常对照组增加了5.13%和4.2%,肌糖元的质量分数分别增加了8%和5.8%,呈显著或极显著差异。
机体疲劳时,会发生相应的生化改变,包括糖元储备量降低、LDH活力下降、血清尿素水平升高等。体内的糖元是运动时能量的来源,糖元储备充足,供应的能量就多,抗疲劳能力就强[9]。紧张运动中体力的衰竭总是和肌糖元的耗竭同时发生,肌糖元消耗的同时,为维持血糖水平,肝糖元储备量减少,因此糖元的含量能说明疲劳发生的快慢或程度;机体剧烈运动时细胞相对缺氧,糖酵解加快,产生大量乳酸,使肌肉中 H+浓度上升,p H值下降,从而引起疲劳。LDH能催化乳酸生成丙酮酸进行进一步的代谢转变,清除肌肉中过多的乳酸,可延缓和消除疲劳。动物体内LDH活力越高,则抗疲劳能力越强;此外机体剧烈运动时,蛋白质及氨基酸的分解代谢增强,氨基酸会代谢转化生成尿素进入血液,使血尿素含量增加,与血乳酸一样,血尿素也是疲劳时肌肉酸痛的主要原因,因此血尿素水平的高低是判断机体疲劳程度的重要指标,运动后血尿素清除越快,则疲劳消除得越快,抗疲劳的效果亦越明显。
本实验结果显示,壳聚糖各剂量均能延长小鼠游泳时间,作用效果以中剂量组为佳,高剂量组和低剂量组作用相对较弱。中剂量组LDH活力高于正常对照组27.57%,呈极显著差异(P<0.01),高剂量组的LDH活力比正常对照组高6.73%,呈显著性差异(P<0.05)。壳聚糖各剂量组小鼠的BU水平均低于正常对照组,中剂量组、高剂量组小鼠运动后血尿素氮含量分别比正常对照组低13.4%、8.09%。呈显著或极显著差异。
有文献报道,用壳聚糖涂膜处理油豆角,能降低油豆角多酚氧化酶和过氧化物酶的活性,抑制膜质过氧化作用[10]。因此,克氏螯虾壳聚糖抗疲劳作用的机制可能与抑制氧自由基-脂质过氧化作用有关。
2.2 壳聚糖对小鼠体重增长的影响
通过对实验前后小鼠体质量进行称量和比较发现,在饲料量不加控制而自由摄食的情况下,各剂量壳聚糖对小鼠体质量增长均有不同程度影响具体数据见表2。

表2 壳聚糖对小鼠体重增长的影响(X±SD)Tab.2 Effect of chitosan on the weight of m ice(X±SD)
从表2可知,低剂量组、中剂量组和高剂量组小鼠实验末均质量与初始均质量相比较分别增加了55.1% 、53.2%和47.5%,正常对照组则增加72.5%,高剂量组小鼠从外观上看明显较瘦长,而正常对照组小鼠与中、低剂量组小鼠体型相对丰满,表明壳聚糖对小鼠体质量的增长具有显著的抑制作用,比照昆明种小鼠体质量增长的情况,中剂量组小鼠体质量增长最接近体重正常增长幅度[8],正常对照组小鼠由于没有控制饲料量反而出现体质量超重的现象。
从表2可以看出,克氏螯虾壳聚糖对小鼠体重的增长具有显著的抑制作用,作用效果依次为高剂量组>中剂量组>低剂量组。但是,克氏螯虾壳聚糖对小鼠抗疲劳作用的影响没有显现出明显剂量效应关系,分析其原因,一方面可能与克氏螯虾壳聚糖对小鼠体质量增长抑制效应有关;另一方面,也可能与高剂量组克氏螯虾壳聚糖应用剂量偏高有关,有研究表明壳聚糖的抗疲劳作用在超过一定剂量后就会表现出“超量抑制效应”[11]。
3 结 语
1)克氏螯虾壳聚糖能延长小鼠负重游泳时间,增加小鼠肝糖元及肌糖元储备量,提高血清乳酸脱氢酶活力,显著降低小鼠剧烈运动后血尿素含量,具有较强的增强动物运动耐力、缓解动物体力疲劳的作用。对于其抗疲劳作用的机制尚有待于一步研究。
2)克氏螯虾壳聚糖具有显著抑制小鼠体质量增长的作用,作用效果随壳聚糖剂量增加其抑制作用增强。
(References):
[1]郑铁生,王亚娜,宗爱萍.龙虾壳聚糖干预后糖尿病小鼠血糖和糖耐量的变化[J].中国临床康复,2006,10(31):67-69.
ZHENG Tie-sheng,WANG Ya-na,ZONG Ai-ping.Influence of lobster chitosan on blood sugar and glucose tolerance in diabetic mice[J].Chinese Journal of Clinical Rehabilitation,2006,10(31):67-69.(in Chinese)
[2]郑铁生,王亚娜,宗爱萍.壳聚糖对实验大鼠降血脂作用的初步研究[J].现代检验医学杂志,2005,20(6):26-27.
ZHENG Tie-sheng,WANG Ya-na,ZONG Ai-ping.Primary research on chitosan to the experiment big rat of cholesterollowering action[J].Journal of Modern Laboratory Medicine,2005,20(6):26-27.(in Chinese)
[3]郑铁生,王亚娜,宗爱萍.壳聚糖体外抗幽门螺杆菌的作用及其影响因素[J].世界华人消化杂志,2006,14(10):993-996.
ZHENG Tie-sheng,WANG Ya-na,ZONG Ai-ping.In vitro action of chitosan against helicobacter pylori and its influential facto rs[J].World Chinese Journal of Digestology,2006,14(10):993-996.(in Chinese)
[4]朱旭明,郑铁生.克氏螯虾壳聚糖对细菌表面作用机理研究[J].食品科学,2009,3(09):155-157.
ZHU Xu-ming,ZHENG Tie-sheng.Mechanism analysis of effect of chitosan from redswamp crayfish on bacterial cell surface[J].Food Scionce,2009,3(09):155-157.(in Chinese)
[5]徐淑云.药理实验方法学[M].北京:人民卫生出版社,1991,1269-1274.
[6]郑铁生,樊绮诗,姜旭淦主编.临床生物化学实验诊断与病例解析[M].北京:中国医药科技出版社,2010:75.
[7]盖钧镒.试验统计方法[M].北京:中国农业出版社,2000,74-96.
[8]苗明三.实验动物和动物实验技术[M].北京:中国中医药出版社,1997:91.
[9]IV YJL.Musel glycogen synthesis before and after exercise[J].Sports Med,1991,11(1):6-19.
[10]连玉晶,赵海田,姚磊,等.壳聚糖可食用膜对油豆角贮藏生理的影响[J].食品与生物技术学报,2006,25(3):72-74.
L IAN Yu-jing,ZHAO Hai-tian,YAO Lei,et al.Effect of chitosan edible coating on physiology of snap beans during storage[J].Journal of Food Science and Biotechnology,2006,25(3):72-74.(in Chinese)
[11]张民,王建华,甘璐,等.枸杞多糖-4组成分析及其生理活性研究[J].食品与发酵工业,2003,29(2):22-25.
ZHANG Min,WANG Jan-hua,Gan Lu,et al.Study only ciumbarbarum polysaccharide-4[J].Food and Fermentation Industries,2003,29(2):22-25.(in Chinese)
Study on Anti-fatigue Effect of Chitosan from Red Swamp Crayfish
XU Gang1, MA Zheng-rong1, WANG Ya-na2, ZHENG Tie-sheng*3
(1.People’s Hospital of Jiangsu Yang Zhong,Yang Zhong 212200,China;2.Zhenjiang Koly Bioligy-technology Co.,L TD,Zhenjiang 212001,China;3.College of Medical Science Technology,Jiangsu University,Zhenjiang 212013,China)
Them ice were divided into high(600 m g/kg),medium(400 mg/kg)and low(200 mg/kg)group and the normal control group according to the dose of chitosan and then record the mice burden swimming time after 10 days.ecord The anti-fatigue effect of Crayfish chitosan was evaluated by comparing the biochemical index such as the weight of mice,the content of serum urea,liver glycogen,muscle glycogen and lactate dehydrogenase activity.The results show ed that the Crayfish chitosan could extend the swimming time of mice,inhibit the grow th of mouse body weight,reduce the increment of serum urea after exercise,increase of serum lactate dehydrogenase activity,a significant increase in the reserve of muscle glycogen and glycogen element,has a good anti-fatigue physiological activity.
Crayfish chitosan,mice,anti-fatigue
TS 201.12
A
1673-1689(2011)03-0363-04
2010-05-06
徐刚(1976-),男,江苏杨中人,药剂师,主要从事中西药结合的药用机制研究。
*通信作者:郑铁生(1948-),男,江苏省镇江人,教授,主要从事临床疾病生化机制及生化检验技术方面的教学和研究工作。Email:jsdxzts@163.com
book=366,ebook=529
