单质碘、碘酸根和碘离子的吸附研究进展
2011-01-09张慧芳高晓雷刘海宁叶秀深吴志坚
张慧芳,高晓雷,郭 探,李 权,刘海宁,叶秀深,郭 敏,吴志坚,*
1.中国科学院青海盐湖研究所,青海西宁 810008;2.中国科学院研究生院,北京 100049
单质碘、碘酸根和碘离子的吸附研究进展
张慧芳1,2,高晓雷1,2,郭 探1,2,李 权1,刘海宁1,叶秀深1,郭 敏1,2,吴志坚1,*
1.中国科学院青海盐湖研究所,青海西宁 810008;2.中国科学院研究生院,北京 100049
本文综述了单质碘、碘酸根和碘离子吸附的最新研究进展,对吸附机理进行了详细讨论。活性炭和有机聚合物是单质碘比较有效的吸附剂,吸附主要靠疏水作用和络合作用来实现。碘酸根的吸附主要靠酸碱作用来实现,由于碘酸根不易与吸附剂产生特异的强相互作用,因而缺乏选择性好的碘酸根特效吸附剂。碘离子被吸附时主要靠化学反应和静电作用,将单质银、氯化银、氧化亚铜等负载到沸石、氧化铝、活性炭、聚合物等基质上可制备出对碘离子产生特效化学吸附的吸附剂,这样的吸附剂虽然吸附容量高,选择性好,但化学稳定性较差,脱附也比较困难。因而制备化学稳定性好、易脱附再生、可循环使用的碘离子特效吸附剂是需要关注的重要问题。
单质碘;碘酸根;碘离子;吸附
对碘的关注主要基于三方面的考虑。(1)碘是动物必需的一种微量元素,动物体内的碘有三分之一以上以甲状腺素的形式存在,甲状腺素的所有生理功能均与碘直接相关。碘对动物机体的作用是双重的,碘缺乏与碘过多都会对动物的健康造成危害[1-2]。所以,环境和食物中碘含量的监控尤为重要。采用吸附法[3-4]不仅可将环境和食物中不同化学形态的碘分离后测定,以准确评价其对人体的有益性和毒理性,也可去除水中的碘离子,这对预防高碘疾病有着重要意义。(2)129I是核污染地下水的主要放射性核素之一,由于129I具有较长的半衰期(1.57×107a)、在地质层中的活动性强且能在动物及人体重要器官富集,因而其放射性危害得到了广泛的关注[5-6]。放射化学家们研究了人工和天然的屏障材料(如膨润土、花岗岩、页岩、凝灰岩、混凝土、大理石、天然岩盐、灰硒汞矿等)对放射性碘的吸附规律[7],以期找到较好的阻滞材料,减弱放射性碘在地质层中的活动性,尽量降低其毒性。(3)碘素及其化合物是药物、染料、农药、食品添加剂及其它化学品制备合成的重要反应原料或催化剂,已经用于甲状腺肿防治、肿瘤放射治疗、化学激光器和太阳能电池制备、人工降雨成核、金属或非金属的提炼及铜、银、铅、锡、锌、汞、镉、铋、砷、锑等离子的测定等[8-15]。随着科技的不断进步,碘系化学品的应用领域在不断扩展,市场需求量也随之增大,原料供应日趋紧张,碘及其化合物的分离提取与制备越来越受到重视。目前,碘的分离提取方法主要有空气吹出法[16]、溶剂萃取法[17]、液膜萃取法[18]、吸附法[19]等,其中吸附法因具有试剂用量少、工艺简单、低污染、低能耗等优点,而受到了普遍重视。
碘可以以无机碘和有机碘的形式存在,无机碘包括单质碘、碘酸根和碘离子。碘存在的化学形态因体系的氧化还原性质不同而不同,采用吸附法进行分析或分离时,所用的吸附剂及相应的吸附机理也不尽相同。在海水中,碘以碘酸根、碘离子和有机碘的形式存在,海水中的I-是由于对IO-3的生物还原而产生的。在具有氧化环境的水体中,I-是热力学不稳定的物质形态,其含量比IO-3含量低。
本文拟综述单质碘、碘酸根和碘离子的吸附研究进展,并对吸附机理进行分析。
1 单质碘的吸附
自然界中不存在单质碘,所以,在吸附单质碘之前,一般是首先将碘转入液相,即制得含碘的原料液,然后通过氧化或还原的方法,将原料液中的碘变成单质碘[19]。目前将碘离子氧化成单质碘最常用的氧化剂是氯气,其次是亚硝酸盐。氯气价廉易得,但由于稍过量的氯气就能使碘进一步氧化成碘酸根,因而必须严格控制操作条件。亚硝酸盐价格较高,且仅在p H<2.0的酸性介质中方能有较好的氧化效果,但因其过量时无过氧化现象,因而在工业上也常用。在p H=4.0~4.5的条件下,加入极少量的亚硝酸钠并鼓入空气氧化,能促进 I-转变为 I2,可大大降低氧化剂亚硝酸钠的用量[19]。
利用活性炭吸附法可以从油田水中回收碘,河南中原油田莘县采油区水处理厂的油田水中含碘21.2 mg/L,在p H=4.0~4.5的条件下,用亚硝酸钠氧化,煤质焦炭型活性炭吸附,350~420℃升华精制,可以得到国家规定的二级或三级碘产品[22-23]。用聚亚胺酯(PU)、三聚氰胺-甲醛(MF)泡沫吸附升华碘、正己烷和甲苯溶液中碘的研究结果表明,从溶液中吸附碘时,平衡吸附符合分配定律,分配系数与溶剂有关。MF泡沫不吸附升华碘,也不吸附溶液中碘,这可能和缺乏电荷转移作用有关[24]。
在核电站,235U、239Pu裂变以及乏燃料元件处理过程都会产生放射性气态单质碘[25],因此,气态单质碘的吸附或吸收是控制放射性污染的主要手段。由于环糊精能够与单质碘或 I-3形成络合物,所以利用环糊精的聚合物可以有效吸附气态单质碘。吸附前将环糊精聚合物用 KI溶液处理后,吸附效果更好。在60℃下用环糊精聚合物吸附时,碘的挥发损失明显低于活性炭[25]。以微孔 SiO2和Al2O3等为载体,在AgNO3溶液中反复浸泡,之后干燥,就得到了负载银盐的吸附剂,将该吸附剂在250℃下进行热处理使负载的银盐转化成Ag2O,再在氢气流中还原,就可得到负载单质银的吸附剂,利用该吸附剂也可以吸附气态单质碘[26]。
2 碘酸根的吸附
水滑石(Hydrotalcite,HT)曾被用于从溶液中吸附碘酸根。水滑石的化学式一般可表示为Mg6Al2(OH)16CO3·4H2O,其结构类似于水镁石Mg(OH)2,由MgO6八面体共棱形成层,Mg2+可在一定范围内被Al3+同晶取代,层间有可交换的阴离子与正电荷平衡,此外,层间也存在一些水分子[27-28]。型和 NO-
3型水滑石(HTCO3和 HTNO3)对碘酸根吸附的研究结果表明,HTCO3的吸附速率比 HTNO3的吸附速率快。碘酸根被 HTCO3吸附时,碘酸根吸附在HTCO3的外表面;碘酸根被 HTNO3吸附时,与HTNO3层间的硝酸根发生离子交换反应,随交换量的增大,吸附剂的结晶度降低[29]。
氧化铝、离子交换树脂以及某些天然矿物对碘酸根和碘离子都能吸附,但吸附存在差别。以氧化铝作为色谱柱填料进行碘物种分离时,发现碘质量浓度为0.000 1~0.1 mol/L,硝酸钠溶液中碘酸根的吸附分配系数为266~760 mL/g,而碘离子的吸附分配系数为1~4 mL/g[30]。而在离子交换树脂上,碘离子的吸附分配系数是碘酸根的30~60倍[31]。在p H=7的体系中,赤铁矿对碘酸根的吸附量比对碘离子的吸附量高;在p H=5的体系中,高岭石对碘酸根有一定的吸附,对碘离子则不吸附[32-33]。
另外,碘酸根和碘离子均可被单质银或者载银盐吸附剂吸附,但吸附机制不同。碘离子吸附在单质银表面会导致银易被氧化最终生成碘化银,而碘酸根的吸附只改变单质银胶体颗粒的形貌。二者均可与载银盐吸附剂生成相应的难溶银盐(ksp(AgI)=8.3×10-17,ksp(AgIO3)=3.0×10-8)而被吸附[34-35]。
3 碘离子的吸附
对碘离子吸附的研究报道比较多,所用的吸附剂主要分三类:(1)离子交换树脂[20];(2)能对碘离子进行化学吸附的复合吸附剂[36],这类吸附剂中能与碘离子发生化学反应的活性成分包括单质银、氯化银、氧化亚铜、二价汞离子[37]等,所用吸附剂的基质材料包括沸石、氧化铝、活性炭、聚丙烯腈纤维等;(3)天然矿物、土壤等。
用第(1)类吸附剂,即离子交换树脂吸附分离碘离子时,虽然吸附容量较大,但选择性差,不过可以靠控制洗脱条件实现碘离子与其它阴离子的分离。强碱性阴离子交换树脂如 Dowex-1、Dowex-2和AG-1等都可用于分离 Cl-、Br-、I-等阴离子,AG-1对各种阴离子的亲和力由大到小的顺序为I->HSO-4>ClO-3>NO-3>Br->CN->HSO-3>NO-2>Cl->HCO-3>IO-3>HCOO->Ac->OH->F-,I-和IO-3的亲和力存在明显差异。有机碘(例如甲状腺素和蛋白质中的碘)不被离子交换树脂吸附,或者可以很容易用去离子水洗脱。靠控制吸附和洗脱条件,用离子交换吸附法可以将不同化学形态的碘相互区分[20]。用离子交换树脂吸附后,采用 0~0.5 mol/L的 KNO3溶液可以将Cl-和Br-洗脱,而要洗脱I-,需要采用2.0 mol/L的 KNO3溶液。在Cl-浓度较高的情况下,IO-3吸附很少[20]。
第(2)类吸附剂虽然选择性好,但存在成本高、在酸性条件下化学稳定性差[36]、不易脱附等问题。另外,当吸附的活性成分为贵金属时,其表面吸附碘离子等亲核试剂后,容易被氧化[34]。将活性炭用银和氯化物处理后,对碘离子的吸附量明显增大。用含有痕量碘离子的溶液进行柱吸附实验的研究结果表明,处理碘离子浓度为10-7mol/L的数千倍床层体积的溶液后,98%的碘离子被去除[36]。
Cu比Ag廉价,毒性比 Pb和 Hg小,Cu+和I-之间能产生较强的相互作用,一价是铜唯一能与I-产生有效相互作用的铜的价态。p H值较高时,Cu2O被氧化成 Cu(OH)2或 CuO,这两种二价的化合物对 I-皆不吸附。低p H值时,Cu2O部分溶解,Cu+进入溶液中。在 I-存在下,热力学计算表明可以形成CuI沉淀[38]:
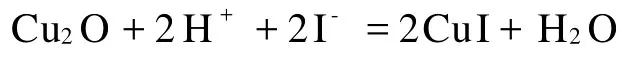
如果没有沉淀剂或络合剂,Cu+会发生歧化反应生成Cu和Cu2+:
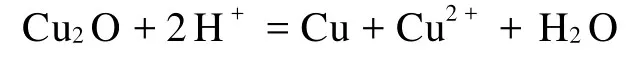
在近中性溶液中,Cu2O稳定,且表面有羟基,能够对碘离子产生有效的吸附[38]。
在氯离子的存在下,单质铜/蓝铜矿[Cu3(OH)2(CO3)2]的混合物能选择性地吸附碘离子,整个过程分两步:(1)蓝铜矿释放出可溶性二价铜离子;(2)可溶性二价铜离子在金属铜的表面被还原后生成CuI,沉淀的形成促进了Cu2+的还原[39]:
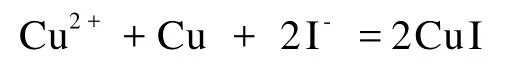
第二步是控制步骤,吸附动力学与铜比表面积有直接关系[39]。
铂炭(Pt-C)吸附剂是由活性炭和金属铂复合而成的吸附剂,对硝酸溶液中的I-和都能够吸附,并且有比较高的交换容量。采用NaOH为解吸液,碘的解吸率可以达到90%以上[40]。
对聚丙烯腈纤维进行N H2OH化学改性,以制得的含有偕胺肟基的螯合纤维为原料,经Hg(NO3)2化学处理,制得的阴离子交换纤维可以吸附碘离子,该离子交换纤维对碘离子的吸附具有交换速度快、交换量大、再生处理便利和重现性好等优点[37]。化学处理用的 Hg(NO3)2的浓度为0.1 mol/L时,所制得的交换纤维对碘离子的交换能力最大;当 Hg(NO3)2的浓度在0.1 mol/L以下时,随 Hg2+浓度的增加,纤维中的偕胺肟基与 Hg2+络合的数目也增大,使交换I-的中心增多,交换率增大;当 Hg(NO3)2的浓度在0.1 mol/L以上时,随 Hg2+浓度的增加,络合数目也增加,但溶液中NO3-的浓度也增大,NO3-与I-产生交换竞争,使得 I-的交换率下降[37]。在p H=6~10的溶液中,离子交换纤维对碘离子的交换能力最佳。离子交换纤维为弱有机碱,当p H值较低时,由于酸效应的影响,离子交换纤维的稳定性下降,从而导致交换率的下降;当p H>10时,由于 OH-浓度的增加,与 I-形成竞争吸附,交换率下降。碘离子为大阴离子,空间位阻较大,吸附速率较慢,吸附达到平衡的时间较长[37]。利用该吸附剂吸附碘离子时,虽然形式上是离子交换,但 Hg2+与碘离子的化学作用可能对吸附有重要影响。
对第(3)类吸附剂吸附碘离子的研究工作,主要是出于对碘离子生态和环境效应的考虑。碘离子在天然沉积物上的吸附,与沉积物中有机物和氧化铁的含量及沉积物的p H有关,碘离子被天然沉积物的吸附,有时是被沉积物中的有机物和氧化铁吸附。碘离子在有机物和氧化铁上的吸附与这些p H依赖的带电物质表面的正电荷点位有关,随着p H的减小,能够用于吸附碘离子的正电荷点位增加[32]。在天然水体中,金属氧化物和金属氢氧化物对阴离子的吸附起着重要作用。I-被石英砂、Al2O3和 Fe2O3吸附的实验结果表明,石英砂和Al2O3的吸附量较小,而 Fe2O3的吸附量则较大[5]。水合γ-Al2O3吸附 F-、Cl-、Br-、I-、ClO3-、BrO3-、IO3-和IO4-的研究结果表明 γ,-Al2O3对各种阴离子的亲和次序为I- 碘在土壤中的吸附受土壤类型、p H、Eh、温度、铁铝氧化物、有机质等的影响。另外,土壤微生物在土壤对碘的吸附过程中也起重要作用[2]。微生物、葡萄糖氧化酶、脲酶、纤维素酶及其催化底物葡萄糖、尿素和纤维素影响土壤吸附I-的研究结果表明,微生物能显著提高 I-的吸附量,而葡萄糖氧化酶、脲酶、纤维素酶及葡萄糖、尿素和纤维素对I-的吸附并无促进作用。向土壤中添加微生物后,土壤吸附 I-量增加。在吸附的前3天,I-吸附量增加缓慢,3天后则出现较大增幅,这与微生物的生长曲线相符合。微生物分泌的胞外酶可促进土壤中腐殖质的碘化作用,从而提高了土壤对I-的吸附能力。另外,微生物在生长过程中也可将碘作为营养物质吸收,使其成为微生物有机体的组成部分[2]。 有学者[42]将卤化银作为添加剂,研究了加入添加剂之后的矿物对放射性碘的吸附性能。实验发现 AgCl、AgBr吸附效果较好,尤其是 AgBr对125I(用125I代替129I)的吸附能力比杏壳活性炭更强,远大于粘土矿、水滑石等材料。认为如果在高放废物处置库的缓冲回填材料中加入少量AgBr,可抑制129I-的迁移扩散。 此外,由于有机离子交换剂交换容量较低、在放射性环境中稳定性较差,也有人[43]合成出了无机阴离子交换剂(如BiPbO2(NO3)),并研究了所得交换剂的交换容量、抗酸碱性及热稳定性等性质,认为可用于固定地下水中的放射性碘。 除了对上述三类吸附剂吸附碘离子的研究报道外,对细菌吸附碘离子也开展了相关工作。天然水体中的细菌能通过其细胞壁上的有机官能团与阳离子、阴离子和矿物表面等产生作用[44],革兰氏阳性细菌Bacillus subtilis对碘离子吸附的研究结果表明,p H=2.5~6.5时,吸附量随p H值的增大而减小,随离子强度的增强也减小。吸附具有可逆性,静电作用是吸附的主要机制,吸附时发生的主要反应为[44]: 单质碘的吸附机理主要是疏水作用和络合作用。用活性碳对含有I-、I2和I-3的溶液进行吸附的研究结果表明,活性碳只吸附 I2[45],说明了疏水作用对单质碘吸附的重要性。将活性碳用盐酸处理后,对单质碘的吸附量增大,这是由于活性碳表面与羧基结合的金属离子被氢离子置换后,活性碳的疏水性增强的缘故[46],这进一步证明了疏水作用对单质碘吸附的重要性。 单质碘具有与某些化合物、尤其是π电子给予体(如富电子的芳香化合物)形成电荷转移(CT)络合物的能力。单质碘被聚亚胺酯(PU)吸附后,与PU中的苯环形成CT络合物,促进了碘的吸附[24]。PU和三聚氰胺-甲醛(MF)虽然都是π电子给予体,但PU对单质碘的吸附能力更强。PU的主要电子受体是苯环,MF的主要电子受体是三氮苯和三胺。苯环中的碳原子被氮原子取代后,芳香稳定性减弱,π供电子能力减弱,供电子能力按照苯>嘧啶>二氮苯>三氮苯的顺序递减。MF对单质碘的吸附能力差是由于其供电子能力差造成的[24]。 碘酸根的吸附机理主要是“硬-硬”酸碱作用。根据软硬酸碱理论,体积小、正电荷数高、可极化性低的阳离子(或离子团)为硬酸;而电负性高、极化性低且难被氧化的阴离子(或离子团)为硬碱,反之则为软酸软碱,并且有“硬亲硬、软亲软、软硬一起不稳定”的反应经验规则。其中的“硬-硬”酸碱作用实质上是电子云较难极化的阴阳离子(或离子团)之间的以离子键为主的化学作用。碘酸根可以靠“硬-硬”酸碱作用被吸附,并因酸碱软硬程度的不同而被选择性吸附。IO-3和 I-吸附行为的差异就可能是由于这两种碱软硬程度的不同而造成的,一般认为 IO-3是比 I-更硬的碱,与矿物表面的硬酸点更易形成“硬-硬”作用[32-33]。在被氧化铝吸附的研究中[30],碘酸根的分配系数远大于碘离子的,就可能是由于碘酸根可与Al3+形成“硬-硬”酸碱作用,促使其更易与氧化铝表面羟基发生交换被吸附。 有时碘酸根也可靠络合作用被吸附,IO-3被赤铁矿吸附可能是由于形成了 Fe-OIO2键,该机理和亚硒酸盐被针铁矿吸附、磷酸根被赤铁矿吸附的机理类似[32],即靠矿物表面的过渡金属离子与酸根阴离子的络合作用使酸根阴离子被吸附。 碘离子基本不显示疏水性,被吸附时主要靠化学反应或静电作用[38,44,47-49]。 用负载了氯化银的活性炭吸附碘离子时,碘离子去除的原理可能是基于AgCl和AgI溶度积的差异(分别为10-10和10-17),发生了如下反应: 碘离子被Cu2O吸附的研究结果表明,有两种依赖于p H的吸附机制,p H低于6.5时,在Cu2O表面产生CuI沉淀[38]: 在碱性更强的介质中,碘离子的吸附是由于与Cu2O的表面羟基发生了交换反应: 碘离子被化学吸附时,碘离子与吸附剂之间作用力的强弱与软硬酸碱作用有关。例如,Cu+和I-之间能产生较强的相互作用,而Cu2+和 I-之间的作用则较弱。根据软硬酸碱理论,I-是软碱,Cu+是软酸,能产生较强的亲和力;而Cu2+是边界酸,因而与I-之间的作用较弱[38]。 对碘的关注主要基于其生理功能、放射性核素的环境效应及资源的提取利用。在空气吹出法、溶剂萃取法、液膜萃取法、吸附法等碘的分离提取方法中,吸附法引起了普遍的重视。 吸附单质碘时,活性炭和有机聚合物是比较有效的吸附剂,吸附主要靠疏水作用和络合作用来实现。对于碘酸根的吸附,主要靠酸碱作用来实现,也可以靠络合作用来实现吸附。由于碘酸根不易与吸附剂产生特异的强相互作用,因而缺乏选择性好的碘酸根特效吸附剂。碘离子基本不显示疏水性,被吸附时主要靠化学反应和静电作用。将单质银、氯化银、氧化亚铜等负载到沸石、氧化铝、活性炭、聚合物等基质上可制备出对碘离子产生特效化学吸附的吸附剂,这样的吸附剂吸附容量高,选择性好,但吸附剂的化学稳定性较差,脱附也比较困难。 在自然界中不存在单质碘,碘以单质形式被吸附之前,要将其它化学形态的碘(一般为碘离子)转化成单质碘,因而整个过程比较长。使碘以碘离子的形式被吸附,再以碘离子的形式被洗脱,是最直接的方式。目前存在的比较大的问题是碘离子被碘特效吸附剂吸附后,脱附困难,或者脱附后,吸附剂受到了破坏,而不是再生,不能再对碘离子产生特效吸附。因而,制备化学稳定性好、易脱附再生、可循环使用的碘离子特效吸附剂是需要关注的重要问题。 [1]张根红,李素梅.水源性高碘研究进展[J].河南预防医学杂志,2006,17(1):48-50. [2]吴世军,陈繁荣,程 俊,等.土壤酶对碘离子在土壤中吸附行为的影响[J].地球化学,2008,37(1):37-44. [3]李洪伟,刘晓瑞,李保山.地下水和土壤中不同形态碘的分离测定[J].岩矿测试,2009,28(4):337-341. [4]张 伟,于祚斌,龚泰石,等.Dx树脂对试验水中高碘离子去除效果的观察[J].中国公共卫生,2000,16(12):1 105-1 106. [5]Nagata T,Fukushi K,Takahashi Y.Prediction of Iodide Adsorption on Oxides by Surface Complexation Modeling With SpectroscopicConfirmation[J].J Colloid Interface Science,2009,332(2):309-316. [6]叶玉星,Marx G.碘(I-)在水泥、氢氧化铁和岩盐中吸附行为的研究[J].核化学与放射化学,1995,17(1):7-12. [7]谢武成.碘在矿物上的吸附与扩散行为研究[D].北京:中国原子能科学研究院,2001. [8]沈舒苏,徐小平,纪顺俊.分子碘催化有机反应研究进展[J].有机化学,2009,29(5):806-811. [9]Chen D B,Shen G D,Bao W L.An Efficient Cascade Synthesis of Various 2H-1,4-Benzoxazin-3-(4H)-Ones From o-Halophenols and 2-Halo-Amides Catalyzed by CuI[J].Org Biomol Chem,2009,7(9):4 067-4 073. [10]郭汝海.化学氧碘激光器(COIL)的研究进展[J].光机电信息,2010,27(5):22-28. [11]Wang M K,Nathalie C,Livain B.An Organic Redox Electrolyte to Rival Triiodide/Iodide in Dye-Sensitized Solar Cells[J].Nature Chemistry,2010,2(5):385-389. [12]徐 华,陈 佳,肖建英.NIS研究进展及其在肿瘤治疗中的应用[J].辽宁医学院学报,2008,29(6):557-559. [13]黄学楼,李爱民.碘及碘化物临床新用途[J].成空药学,1992,6(1):31-32. [14]于 洋,陈 涛,卢婷利.碘造影剂脂质体的研究进展[J].中国医学影像技术,2008,24(6):968-971. [15]杨 华.碘——多方面的社会应用[J].化学教育,1996(6):12-13. [16]罗 静,钟 辉,徐粉燕.从卤水中提取碘的研究进展[J].内蒙古石油化工,2007(11):3-5. [17]Brown C F,Geiszler K N,Vickerman T S.Extraction and Quantitative Analysis of Iodine in Solid and Solution Matrixes[J].Anal Chem,2005,77(21):7 062-7 066. [18]Ensafi A A,Eskandari H.Efficient and Selective Extraction of Iodide Through a Liquid Membrane[J].Microchem J,2001,69(1):45-50. [19]王景刚,冯丽娟,相湛昌,等.碘提取方法的研究进展[J].无机盐工业,2008,40(11):11-14. [20]Hou X L,Dahlgaard H,Rietz B,et al.Determination of Chemical Species of Iodine in Seawater by Radiochemical Neutron Activation Analysis Combined With Ion-Exchange Preseparation[J].Anal Chem,1999,71(14):2 745-2 750. [21]Ito K.Determination of Iodide in Seawater by Ion Chromatography[J].Anal Chem,1997,69(17):3 628-3 632. [22]王 淼.新活性炭法从低含碘油田水中回收碘[J].精细石油化工,2003(5):30-31. [23]王 淼,刘茜毓,范金石,等.油气田水提碘的研究[J].山东轻工业学院学报,2003,17(1):1-4. [24]Wang Y B,Sotzing G A,Weiss R A.Sorption of Iodine by Polyurethane and Melamine-Formaldehyde Foams Using Iodine Sublimation and Iodine Solutions[J].Polymer,2006,47(8):2 728-2 740. [25]Szente L,Fenyvesi,Sefszejtli J.Entrapment of Iodine With Cyclodextrins:Potential Application of Cyclodextrins in Nuclear Waste Management[J].Environ Sci Technol,1999,33(24):4 495-4 498. [26]Engelhardt T,H hn R.Iodine Adsorption Agent:US,5750461[P].1998-5-12. [27]淳 宏,谢文磊,杨劲峰,等.水滑石类化合物结构和性能影响因素的研究进展[J].精细石油化工进展,2008,9(10):32-37. [28]Paredes S P,Fetter G,Bosch P,et al.Iodine Sorption by Microwave Irradiated Hydrotalcites[J].J Nucl Mater,2006,359(3):155-161. [29]Toraishi T,Nagasaki S,Tanaka S.Adsorption Behavior ofHydrotalcite[J].Appl Clay Sci,2002,22(1-2):17-23. [30]Machado E C,Bellido L F,Bellido Jr A V.Separation of Iodine Species by Adsorption Chromatography[J].J Radioanal Nucl Chem,2001,249(3):653-656. [31]Dybczyński R,Kulisa K.Observations onthe Effect of Temperature on Performance and Stability of Anion Exchange Columns in Ion Chromatography[J].Chromatographia,2003,57(7-8):475-484. [32]Kaplan D I,Serne R J,Parker K E,et al.Iodide Sorption to Subsurface Sediments and Illitic Minerals[J].Environ Sci Technol,2000,34(3):399-405. [33]Hu Q H,Zhao P H,Moran J E,et al.Sorption and Transport of Iodine Species in Sediments From the Savannah River and Hanford Sites[J].J Contam Hydrol,2005,78(3):185-205. [34]Zhang A P,Tie X Y,Zhang J Z,et al.Adsorption of Iodide and Iodate on Colloidal Silver Surface[J].Appl Surf Sci,2008,255(5):3 184-3 187. [35]康静娟,叶明吕,饶友平,等.附银硅胶除碘的机理研究[J].核科学与工程,1991,11(1):67-72. [36]Hoskins J S,Karanfil T.Removal and Sequestration of Iodide Using Silver-Impregnated Activated Carbon[J].Environ Sci Technol,2002,36(4):784-789. [37]吴友吉,金 盈,吴之传,等.阴离子交换纤维的制备及其对碘离子交换性能的影响[J].安徽化工,2005(4):18-20. [38]Lefèvre G,Walcarius A,Ehrhardt J J,et al.Sorption of Iodide on Cuprite(Cu2O)[J].Langmuir,2000,16(10):4 519-4 527. [39]Lefèvre G,Alnot M,Ehrhardt J J,et al.Uptake of Iodide by a Mixture of Metallic Copper and Cupric Compounds[J].Environ Sci Technol,1999,33(10):1 732-1 737. [40]邓启民,李茂良,程作用.铂炭交换剂用于硝酸溶液中碘的提取[J].核动力工程,2008,29(1):70-72. [41]Szczepaniak W,Kos’cielna H.Specific Adsorption of Halogen Anions on Hydrousγ-Al2O3[J].Anal Chim Acta,2002,470(2):263-276. [42]陈 涛,田文宇,孙 茂,等.卤化银添加剂对125I在北山花岗岩岩粉中的吸附作用研究[J].无机化学学报,2009,25(5):761-766. [43]Kodama H,Ysuchiura.Bismuth Lead Compound:US,5720883[P].1998-2-24. [44]MacLean L C W,Martinezc R E,Fowle D A.Experimental Studies of Bacteria-Iodide Adsorption Interactions[J].Chem Geol,2004,212(3-4):229-238. [45]王留成,刘大壮,杨碧光.碘化钾水溶液中碘在活性炭上的吸附等温线[J].化学工程,1994,22(6):28-30. [46]Guo Y P,Zhang H,Tao N N,et al.Adsorption of Malachite Green and Iodine on Rice Husk-Based Porous Carbon[J].Mater Chem Phys,2003,82(1):107-115. [47]Devivier K,Devol-Brown I,Savoye S.Study of Iodide Sorption to the Argillite of Tournemire in Alkaline Media[J].Appl Clay Sci,2004,26(1-4):171-179. [48]Riebe B,Dultz S,Bunnenberg C.Temperature Effects on Iodine Adsorption on Organo-Clay Minerals.I.Influence of Pretreatment and Adsorption Temperature[J].Appl Clay Sci,2005,28(1-4):9-16. [49]Dultz S,Riebe B,Bunnenberg C.Temperature Effects on Iodine Adsorption on Organo-Clay Minerals.II.Structural Effects[J].Appl Clay Sci,2005,28(1-4):17-30. Research Progress on Adsorption of Iodine,Iodate,and Iodide ZHAN G Hui-fang1,2,GAO Xiao-lei1,2,GUO Tan1,2,LI Quan1,LIU Hai-ning1,YE Xiu-shen1,GUO Min1,2,WU Zhi-jian1,* 1.Qinghai Institute of Salt Lakes,Chinese Academy of Sciences,Xining 810008,China;2.The Graduate University of Chinese Academy of Sciences,Beijing 100049,China The research progress in the adsorption of iodine,iodate,and iodide was reviewed and the related adsorption mechanisms were discussed.Activated carbons and organic polymers are effective adsorbents for iodine with hydrophobic attraction and complexation as the main adsorption mechanisms.Iodate is mainly adsorbed through the acid-base interaction.In general,there are no effective adsorbents for iodate because of the lack of specific interactions between iodate and the adsorbents.Iodide is adsorbed mainly through chemical reaction and electrostatic attraction.Iodide specific adsorbents can be prepared by loading Ag,AgCl,Cu2O,etc.on zeolite,alumina,activated carbons,polymers,etc..Such adsorbents have a high adsorption capacity and a good selectivity,but a poor chemical stability.Usually they are not easy to regenerate.Therefore,to prepare iodide specific adsorbents with a good chemical stability and reusability is attractive. iodine;iodate;iodide;adsorption O647.3 A 0253-9950(2011)03-0129-07 2010-09-02; 2010-12-27 国家自然科学基金资助项目(50972151,51002164);2009年度"西部之光"人才培养计划资助项目(科发人教字[2009]236号);中国科学院"百人计划"资助项目(0660011106) 张慧芳(1985—),女,内蒙古呼和浩特人,硕士研究生,无机化学专业 *通信联系人:吴志坚,男,博士,研究员,博士生导师,主要从事无机分离和无机材料研究,E-mail:zjw6512@hotmail.com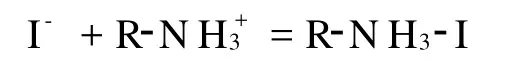
4 吸附机理
4.1 单质碘的吸附机理
4.2 碘酸根的吸附机理
4.3 碘离子的吸附机理
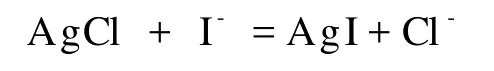
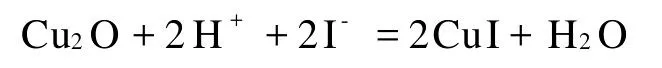

5 结 论
