炭载体改性对炭载Pd催化剂电催化性能的影响
2010-12-05丁良鑫王士瑞郑小龙陆天虹曹殿学唐亚文
丁良鑫 王士瑞 郑小龙 陈 煜,*陆天虹 曹殿学 唐亚文,*
(1南京师范大学化学与环境科学学院,南京 210097;2哈尔滨工程大学材料科学与化学工程学院,哈尔滨 150001)
炭载体改性对炭载Pd催化剂电催化性能的影响
丁良鑫1王士瑞2郑小龙1陈 煜1,*陆天虹1曹殿学2唐亚文1,*
(1南京师范大学化学与环境科学学院,南京 210097;2哈尔滨工程大学材料科学与化学工程学院,哈尔滨 150001)
研究了硝酸和氨水改性处理对活性炭表面基团、炭载Pd纳米粒子的形态及其对甲酸氧化电催化性能的影响.傅里叶变换红外(FT-IR)光谱、X射线光电子能谱(XPS)及Boehm滴定结果表明,硝酸和氨水处理分别增加了活性炭表面含氧基团和含氮基团的含量.透射电镜(TEM)及电化学测试显示,活性炭经硝酸处理后,表面负载的Pd粒子粒径降低,催化剂对甲酸氧化活性和稳定性提高.进一步用氨水处理后,Pd粒子的粒径没有明显变化,但催化剂中Pd0的含量增加,催化剂性能进一步提高.
活性炭;炭载Pd催化剂;硝酸处理;氨水处理;甲酸氧化
活性炭具有较高的比表面积和丰富的孔结构,是一类重要的催化剂载体.许多研究表明[1-4],活性炭表面含氧基团能够有效减弱其表面疏水性并作为活性沉积中心,使金属前驱体溶液更易接近其表面,从而有效提高金属纳米粒子的分散度.另外,活性炭表面基团与负载金属之间存在着明显的相互作用,这种作用能够改变金属纳米粒子的表面电子状态,直接影响着催化剂的活性及稳定性[5].所以,对活性炭表面进行改性处理非常有意义.
目前对活性炭的表面修饰分为化学法和物理法[6-11].通常是将炭材料在强氧化剂,如 H2SO4、HNO3、H2O2等液体介质中进行表面氧化处理或者表面修饰,在其表面形成许多含氧官能团.然而,含氧基团的引入也有一定问题,如含氧基团的增加也容易造成活性炭电导率的降低[12-13].因此,研究对含氧基团的优化及其对炭载贵金属催化剂催化性能的影响非常重要.本文通过对活性炭进行硝酸氧化处理后,进一步采用氨水处理以引进含氮基团,并将含有不同表面官能团的活性炭作为载体,制得炭载Pd金属催化剂.并通过电化学方法研究了活性炭表面基团对催化剂电催化性能的影响.
1 实验部分
1.1 试剂和仪器
Vulcan XC-72活性炭为美国Cabot公司产品, 5%(w)的Nafion溶液为美国Aldrich化学公司产品,其余试剂均为分析纯.所有溶液均用三次蒸馏水配制.FT-IR测量用Tensor 27(德国布鲁克公司)红外光谱仪;元素分析及Pd金属价态分析采用Thermo ESCALAB 250(美国)XPS光谱仪,X射线激发源为单色Al Kα(hν=1486.6 eV),功率150 W,X射线束斑500 μm,能量分析器固定透过能为20 eV,以C 1s结合能284.6 eV作为内标;TEM测量用Tecnai G2205-TWTN(美国FET公司);X射线能量色散谱(EDS)测量用Vantage IV型X射线能谱仪(美国热电公司);电化学测试采用CHI600电化学分析仪(美国CHI仪器公司)和常规三电极体系的电化学池进行.
1.2 活性炭处理
Vulcan XC-72活性炭的预处理:(a)将Vulcan XC-72活性炭在含30%(w)HNO3中,在80℃下处理2 h,HNO3处理的活性炭标记为C-H;(b)将C-H在含25%(w)氨水中,在60℃下处理4 h,所得的活性炭标记为C-HN.2种处理的炭在处理后都用去离子水充分洗涤至中性,然后在真空干燥箱中恒温80℃干燥12 h;(c)作为对比,未经处理的Vulcan XC-72活性炭标记为C-U.
1.3 催化剂的制备
分别取上述活性炭60 mg,加6.0 mL 0.0471 mol·L-1Pd(NO3)2溶液和10 mL H2O,超声30 min后,再继续搅拌4 h后,用Na2CO3调节悬浮液的pH值到8-9,滴加10 mL 2.0 mg·mL-1NaBH4溶液,超声20 min,搅拌1 h后,过滤、洗涤,60℃真空干燥12 h.即制得含Pd 20%(w)的炭载钯催化剂,并分别标记为Pd/C-H、Pd/C-HN和Pd/C-U.EDS分析表明各催化剂样品中Pd载量均为19.2%左右,此值与理论计算值基本相同.
1.4 工作电极制备和性能测试
工作电极的制备采用文献报道的方法进行[14].工作电极基体为直径4 mm的玻碳电极,每次实验前,将玻碳电极依次用5#金相砂纸、0.3和0.05 μm的Al2O3粉磨至镜面,超声波洗涤.将8 mg催化剂与4 mL无水乙醇配制成2 mg·mL-1的悬浮液,超声分散30 min,移取8.9 μL悬浮液至电极表面,50℃干燥后,移取4.5 μL Nafion溶液于催化剂表面,电极表面的Pd载量为28 μg·cm-2.对电极为Pt片,参比电极为Ag/AgCl电极,本文所述电位均相对于Ag/AgCl电极.在电化学测试前,溶液通高纯N210 min以除去溶解的氧,测量时溶液上方通N2保护.循环伏安法测量时,电位扫描速率为50 mV·s-1.实验在(30±1)℃下进行.
2 结果与讨论
2.1 改性对活性炭表面基团的影响
图1为不同活性炭样品的FT-IR谱图.与未改性的活性炭相比,经HNO3处理后的样品在1750-1680 cm-1之间及3600-3300 cm-1之间的含氧基团的吸收峰[9]均明显增强,表明经过浓HNO3处理后,活性炭表面确实引进了含氧基团,这些含氧基团主要以酸性基团的形式存在.再经氨水处理后(曲线c),在3600-3300 cm-1和1750-1680 cm-1之间的吸收峰发生了分裂,这主要是由于活性炭表面含氧酸性基团与氨水作用,产生了N—H的伸缩振动[15].这证实了在活性炭表面的确引入了含氮基团.
不同活性炭样品的C、N、O元素分析结果列于表1.与未改性的活性炭相比,经硝酸处理后的活性炭表面氧、氮两种元素含量均显著增加,表明硝酸氧化确实能在活性炭表面引进含氧基团,而氮元素的增加可能是由于硝酸根离子的吸附所致.再经氨水处理后,活性炭表面N元素含量增加,O元素含量则相对减少,这说明活性炭经氨水改性后其表面含氮基团含量增加,而含氧基团含量减少,这与潘红艳等人[16]的研究结论一致.
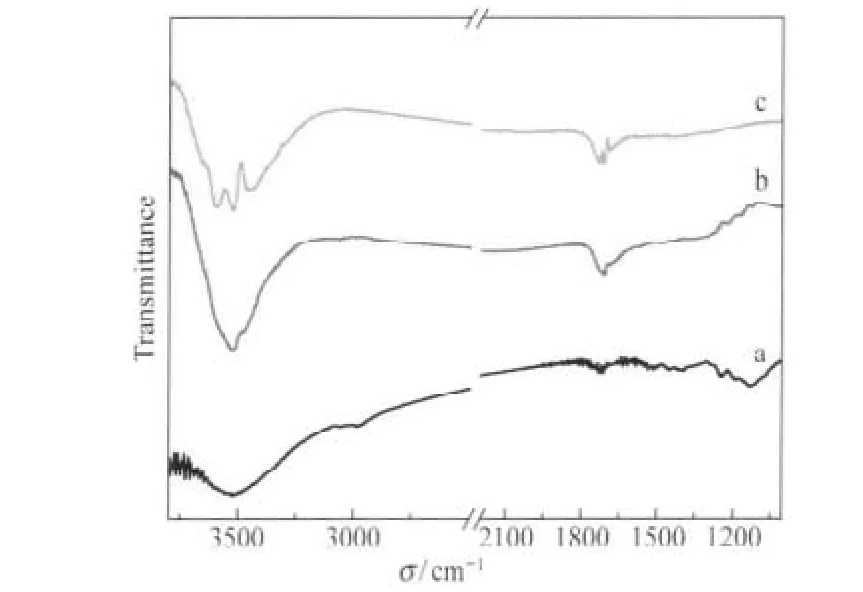
图1 不同活性炭的FT-IR光谱Fig.1 FT-IR spectra of different activated carbons(a)sample C-U(untreated);(b)sample C-H(HNO3treated); (c)sample C-HN(HNO3and NH·3H2O treated)

表1 不同活性炭的元素含量Table 1 Elements contents of different activated carbons
表2为不同活性炭的Boehm滴定结果[17].由表2可见,活性炭经硝酸处理后,酸性基团含量增加,碱性基团则明显减少.Figueiredo等[9]研究表明,硝酸处理引进的主要是羧基等酸性含氧基团,这与本实验的结果一致.经氨水进一步处理后,酸性基团含量减少,碱性基团含量增加.这证明氨水处理在活性炭表面引进了碱性含氮基团.
2.2 改性对Pd/C催化剂组成和形态的影响
图2为Pd/C-U、Pd/C-H和Pd/C-HN催化剂的TEM照片及对应的Pd粒子粒径分布图.由图可见, Pd/C-U、Pd/C-H和Pd/C-HN催化剂中Pd粒子的平均粒径分别为4.62、2.35和2.70 nm.同时,从TEM照片可发现,经过表面改性处理后获得的催化剂中的Pd金属粒子粒径大小更为均一.不同催化剂中Pd粒子的表面平均分散度(D)能通过Borodzinski和Bonarowska模型[18]计算获得:

表2 不同活性炭的Boehm滴定结果[17]Table 2 Boehm titration result of different activated carbons[17]
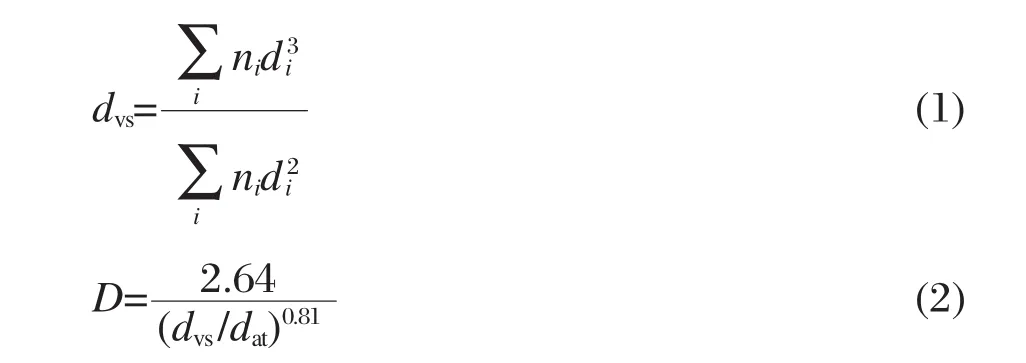
式中,dvs为Pd粒子的体表面平均粒径;di为TEM粒子分布图中统计得到的Pd粒子粒径;ni为对应的Pd粒子数目;dat为原子直径.由于Borodzinski和Bonarowska模型考虑到了粒子大小分布的影响,因此比其它通常使用的模型更加准确.通过使用该模型计算获得的不同粒径Pd粒子的D值分别为26.3%、41.2%和39.0%,说明对活性炭载体进行表面处理,能够有效提高Pd金属纳米粒子的分散度.
图3为不同催化剂样品中Pd 3d的XPS谱,键合能位于336.5和341.3 eV左右处的峰分别属于Pd 3d5/2和Pd 3d3/2特征峰.Pd 3d5/2峰能够被拆分成两个峰,键合能位于336.0和337.5 eV左右处的峰分别属于Pd0和氧化态的Pd.Pd/C-U、Pd/C-H和Pd/ C-HN催化剂中Pd0与氧化态Pd的原子比依次为1.9、1.8和3.1,说明在Pd/C-H催化剂中,Pd0含量最少,这可能是活性炭表面含氧基团的增加导致的.而在Pd/C-HN催化剂中,Pd0的含量最多,说明含氮基团的引入有助于增加Pd0的含量.这进一步说明活性炭的表面基团与负载的金属之间存在着明显的相互作用[5].
2.3 不同催化剂对甲酸氧化的电催化活性
图4为不同催化剂电极在0.5 mol·L-1H2SO4溶液中的循环伏安曲线.由低电势区部分(-0.2-0.1 V)氢的脱附峰面积可以计算得吸附氢所需的电量(Qd)和相对电化学活性面积(Aec),所得结果列于表3中.很明显,Pd/C-HN催化剂具有最大的电化学活性面积.
图5为不同催化剂电极在0.5 mol·L-1H2SO4+ 0.5 mol·L-1HCOOH溶液中的线性扫描伏安曲线.在每条曲线中,都可观察到位于0.23和0.60 V的两个氧化峰.前者表示甲酸是通过直接途径氧化,而后者是通过CO途径氧化[19].在0.23 V处的峰电流密度远大于在0.60 V处的峰电流密度,表明甲酸在Pd催化剂上的氧化主要是通过直接路径氧化.三个催化剂的氧化峰峰电位都基本相同,但峰电流密度却有明显区别.在Pd/C-HN催化剂电极上的峰电流密度为15.70 mA·cm-2,而在Pd/C-H、Pd/C-U催化剂电极上峰电流密度分别为13.44和7.60 mA·cm-2. Pd/C-H催化剂电催化活性的增加可能是由于Pd粒子的粒径较小,比表面积较大所致.而Pd/C-HN催化剂活性的增加可能是由于含氮基团通过静电效应或配位作用改变了Pd的表面电子状态,从而导致催化剂中Pd0含量较高.Roy[20]和Schukla[21]等在研究活性炭表面基团对Pt粒子对甲醇氧化电催化活性影响时,也有类似发现.
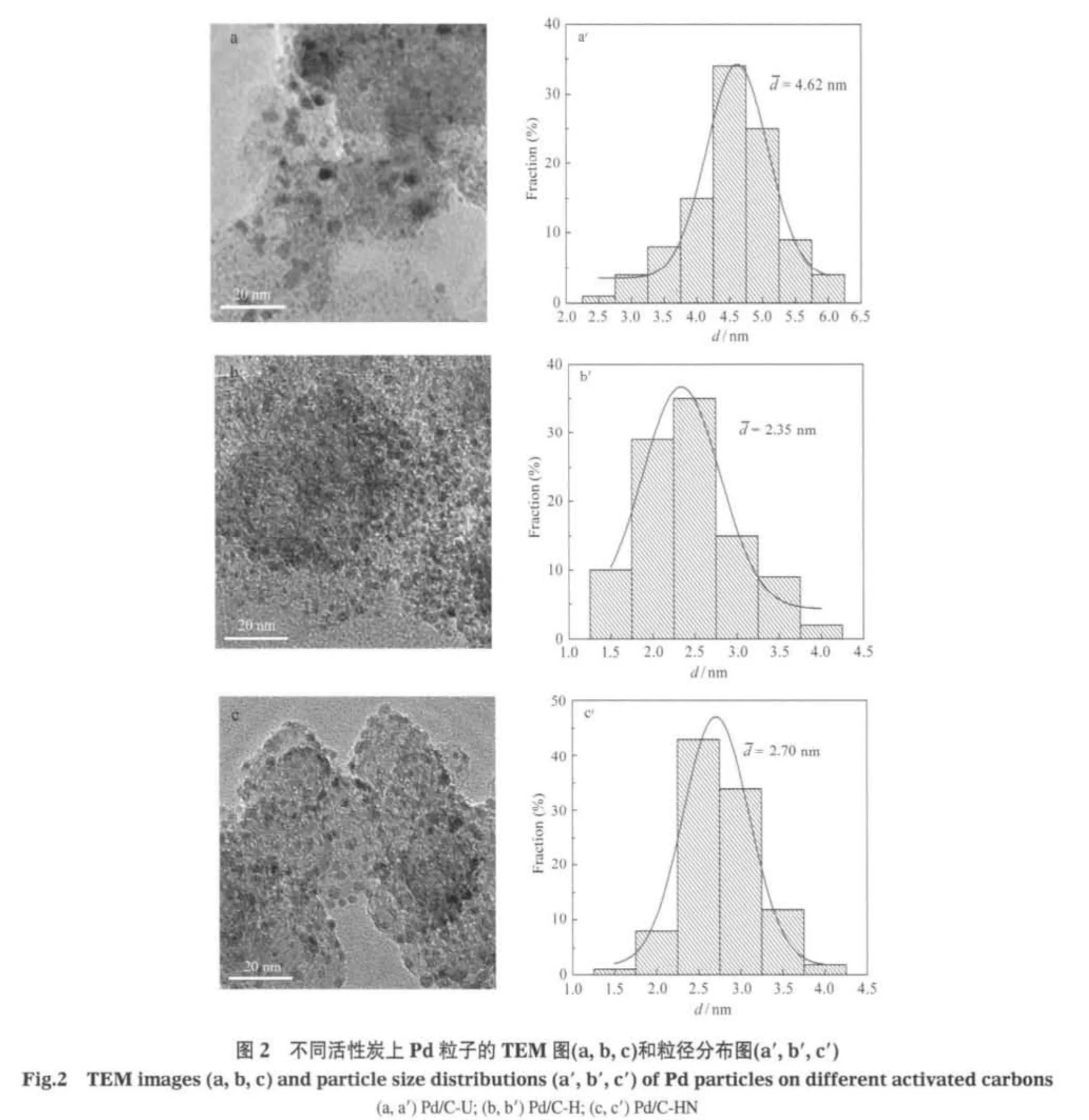


图4 不同炭载钯催化剂在0.5 mol·L-1H2SO4溶液中的循环伏安曲线Fig.4 Cyclic voltammograms of different carbon supported Pd catalysts in 0.5 mol·L-1H2SO4solution(a)Pd/C-U,(b)Pd/C-H,(c)Pd/C-HN; scan rate:50 mV·s-1,T=30℃

表3 不同炭载钯催化剂中活性Pd含量的分析Table 3 Content analysis of active Pd in different carbon supported Pd catalysts
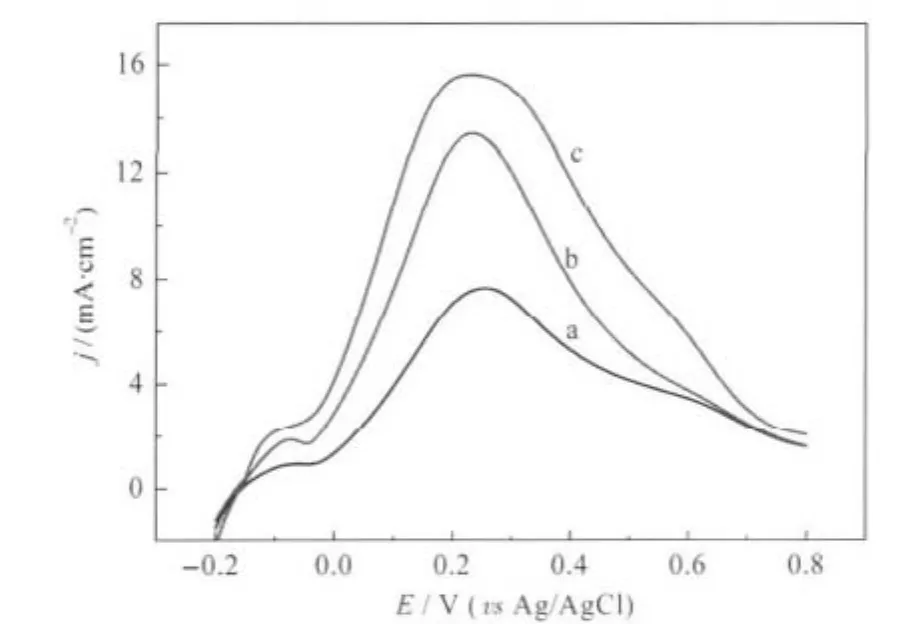
图5 不同炭载钯催化剂在0.5 mol·L-1H2SO4+ 0.5 mol·L-1HCOOH溶液中的线性扫描曲线Fig.5 Linear sweep voltammograms of differentcatalysts in 0.5 mol·L-1HCOOH+0.5 mol·L-1 H2SO4solution(a)Pd/C-U,(b)Pd/C-H,(c)Pd/C-HN;scan rate:50 mV·s-1,T=30℃
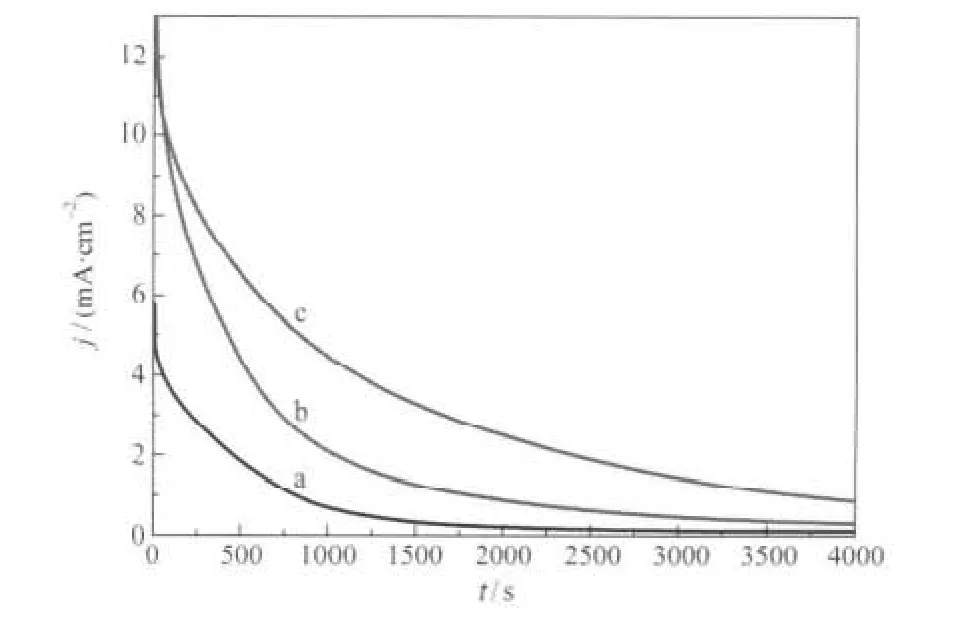
图6 不同炭载钯催化剂在0.5 mol·L-1H2SO4+0.5 mol·L-1 HCOOH溶液中,在30℃和0.2 V下的计时电流曲线Fig.6 Chronoamperometric curves of different carbon supported Pd catalysts in 0.5 mol·L-1HCOOH+ 0.5 mol·L-1H2SO4solution at 0.2 V and 30℃(a)Pd/C-U,(b)Pd/C-H,(c)Pd/C-HN
图6为三种催化剂电极在0.5 mol·L-1H2SO4+ 0.5 mol·L-1HCOOH溶液中,电位恒定在0.2 V时的计时电流曲线.由图可见,在达到相对稳定状态时(4000 s),甲酸在Pd/C-U、Pd/C-H和Pd/C-HN催化剂电极上氧化电流密度分别为 0.11、0.43和1.0 mA·cm-2,这证明不同催化剂对甲酸氧化的电催化稳定性依次为Pd/C-HN>Pd/C-H>Pd/C-U催化剂,表明在活性炭中引入含氧和含氮官能团能提高Pd催化剂对甲酸氧化的电催化稳定性.
3 结论
活性炭经硝酸处理后,表面含氧官能团数量显著增加,制得的Pd/C-H催化剂中的Pd粒子粒径减小,电化学活性比表面积增加,催化剂对甲酸氧化的电催化活性和稳定性提高.将获得的活性炭进一步用氨水处理,活性炭表面的含氮基团增加,同时,催化剂中Pd0的含量增大,催化剂性能进一步提高.因此,载体改性对于炭载贵金属催化剂的电催化性能影响较大.
1 Aksoylu,A.E.;Madalena,M.;Freitas,A.;Fernando,M.;Pereira, R.;Figueiredo,J.L.Carbon,2001,39:175
2 Han,W.F.;Huo,C.;Liu,H.Z.J.Chem.Eng.Chin.Univ.,2002, 16:565 [韩文锋,霍 超,刘化章.高校化学工程学报,2002, 16:565]
3 Rodriguez-Reinoso,F.Carbon,1998,36:159
4 Cabiac,A.;Delahay,G.;Durand,R.;Trens,P.;Coq,B.;Plée,D. Carbon,2007,45:3
5 Antonucci,P.L.;Alderucci,V.;Giordano,N.;Cocke,D.L.;Kim, H.J.Appl.Electrochem.,1994,24:58
6 Zeng,Y.K.;Yang,Q.S.;Sun,J.;Zhu,B.Y.;Pan,L.J.;Wen,Y. Z.;Zhang,Z.X.Tanium Industry Progress,2007,24:42 [曾永康,杨乔森,孙 洁,朱柏烨,潘丽娟,文永忠,张之翔.钛工业进展,2007,24:42]
7 Vinke,P.;van der Eijk,M.;Verbree,M.;Voskamp,A.F.;van Bekkum,H.Carbon,1994,32:675
8 Pradhan,B.K.;Sandle,N.K.Carbon,1999,37:1323
9 Figueiredo,J.L.;Pereira,M.F.R.;Freitas,M.M.A.;Órfão,J.J. M.Carbon,1999,37:1379
10 Biniak,S.;Szymański,G.;Siedlewski,J.;Wiatkowski,A.S'. Carbon,1997,35:1799
11 S'wiątkowski,A.;Grajek,H.;Pakuła,M.;Biniak,S.;Witkiewicz, Z.Colloid.Surf.A-Physicochem.Eng.Aspects,2002,208:313
12 Román-Martínez,M.C.;Cazorla-Amorós,D.;Linares-Solano,A.; Salinas-Martínez de Lecea,C.;Yamashita,H.;Anpo,M.Carbon, 1995,33:3
13 Li,X.G.;Xing,W.;Yang,H.;Lu,T.H.Chin.J.Anal.Chem., 2002,30:788 [李旭光,邢 巍,杨 辉,陆天虹.分析化学, 2002,30:788]
14 Tang,Y.W.;Ma,G.X.;Zhou,Y.M.;Bao,J.C.;Lu,L.D.;Lu,T. H.Acta Phys.-Chim.Sin.,2008,24:1615 [唐亚文,马国仙,周益明,包建春,陆路德,陆天虹.物理化学学报,2008,24:1615]
15 Leuch,L.M.L.;Bandosz,T.J.Carbon,2007,45:568
16 Pan,H.Y.;Li,Z.;Xia,Q.B.;Xi,H.X.;Li,J.J.Funct.Mater., 2008,39:324 [潘红艳,李 忠,夏启斌,奚红霞,李 晶.功能材料,2008,39:324]
17 Boehm,H.P.Adv.Catal.,1966,16:179
18 Borodzinski,A.;Bonarowska,M.Langmuir,1997,13:5613
19 Wang,X.;Tang,Y.W.;Gao,Y.;Lu,T.H.J.Power Sources, 2008,175:784
20 Roy,S.C.;Harding,A.W.;Russell,A.E.;Thomas,K.M. J.Electrochem.Soc.,1997,144:2323
21 Schukla,A.K.;Ravikumar,M.K.;Roy,A.;Barman,S.R.;Sarma, D.D.;Aricò,A.S.;Antonucci,V.;Pino,L.;Giordano,N. J.Electrochem.Soc.,1994,141:1517
October 9,2009;Revised:January 4,2010;Published on Web:April 1,2010.
Effect of Carbon Modification on Electrocatalytic Performance of Carbon Supported Pd Catalysts
DING Liang-Xin1WANG Shi-Rui2ZHENG Xiao-Long1CHEN Yu1,*
LU Tian-Hong1CAO Dian-Xue2TANG Ya-Wen1,*
(1School of Chemistry and Environmental Science,Nanjing Normal University,Nanjing 210097,P.R.China;2College of Material Science and Chemical Engineering,Harbin Engineering University,Harbin 150001,P.R.China)
The effect of carbon modification on electrocatalytic performance of carbon supported Pd catalysts was investigated.Fourier transform infrared(FT-IR)spectrometer,X-ray photoelectron spectroscopy(XPS)and Boehm titration measurements demonstrate that the contents of O-containing groups and N-containing groups on the activated carbon surface increase via HNO3and NH4OH treatment.Transmission electron microscope(TEM)and electrochemical measurements indicate that the treatment of activated carbon with HNO3can decrease the size of the Pd particles.Thus, the electrocatalytic activity and stability of the carbon supported Pd catalyst for the oxidation of formic acid are enhanced.The treatment of activated carbon with NH4OH has almost no effect on the Pd particles size,however,the content of Pd0in the Pd/C catalyst enhances,which leads to the further increase in the electrocatalytic performance the Pd/C catalyst.
Activated carbon;Carbon supported Pd catalyst;Nitric acid treatment;Ammonia treatment; Formic acid oxidation
[Article] www.whxb.pku.edu.cn
*Corresponding authors.Email:tangyawen@njnu.edu.cn,nsdchenyu@126.com;Tel:+86-25-85891651.
The project was supported by the National High Technology Research and Development Program of China(863)(2006AA05Z137,2007AA05Z143, 2007AA05Z159)and National Natural Science Foundation of China(20873065).
国家高技术研究发展计划(863)(2006AA05Z137,2007AA05Z143,2007AA05Z159)和国家自然科学基金(20873065)资助项目
O643;O613.71
