SnO2/中空洋葱状碳纳米复合材料的制备及电化学性能
2010-12-05张慧娟宋怀河周继升张洪坤陈晓红
张慧娟 宋怀河 周继升 张洪坤 陈晓红
(北京化工大学,化工资源有效利用国家重点实验室,北京 100029)
SnO2/中空洋葱状碳纳米复合材料的制备及电化学性能
张慧娟 宋怀河*周继升 张洪坤 陈晓红
(北京化工大学,化工资源有效利用国家重点实验室,北京 100029)
以炭黑为原料,硝酸铁为催化剂前驱体,氮气气氛下1000℃高温炭化制备了直径为40 nm的中空洋葱状碳纳米颗粒(OC).用SnCl2/乙醇溶液浸渍,空气中350℃氧化得到SnO2/OC复合材料.进一步对该复合材料进行酸处理制备OC包覆的SnO2电极材料.采用X射线衍射(XRD)、扫描电镜(SEM)、透射电镜(TEM)和热失重分析(TGA)对OC和SnO2/OC复合材料进行表征;利用恒电流充放电和循环伏安(CV)方法对复合材料作为锂离子电池负极材料的电化学性能进行表征.结果表明:酸处理后的复合材料的循环性能得到明显改善,50次循环后可逆容量保持为446 mAh·g-1,OC起到了缓冲SnO2膨胀和阻止团聚的作用.
洋葱状碳纳米颗粒;二氧化锡;复合;负极材料;锂离子电池
作为锂离子二次电池负极材料,锡及其氧化物具有比容量高(Sn:991 mAh·g-1,SnO2:781 mAh·g-1),安全性好的优点.但是限制其实际应用的最大问题在于,电池充放电过程中形成锡锂合金时会产生巨大的体积膨胀,造成电极粉化甚至脱落,使电接触变差,导致循环性能恶化[1-8].改善锡及其氧化物负极材料的循环稳定性成为当前研究的热点之一.众所周知,碳材料在充放电过程中体积变化小,具有良好的循环稳定性和高的电导率.制备锡/碳复合材料成为解决这一问题的有效办法之一.一些研究表明,不同结构的碳材料(如石墨[2]、碳纳米管[3]、膨胀碳微球[4]、石墨烯[5]等)与锡或其氧化物复合后都能起到良好的缓冲作用,提高锡电极材料的循环稳定性.在这些结构中,具有中空结构的球形碳材料被认为是最理想的缓冲材料.因为锡与碳可以形成核壳型碳包覆结构,具有良好弹性和电导性的空心碳壳,既能缓冲合金形成时产生的体积膨胀又可作为合金与集流体间的导电通道,同时球形碳有较大的堆积密度,体积比能量大[1,6].Zhang等[7]利用SiO2为模板, Na2SnO3为锡源,加热分解得到SnO2空心球壳,再以葡萄糖为碳源,制备了碳包覆SnO2的空心核壳结构复合材料,经高温处理,SnO2被还原为Sn,最终得到碳包覆锡复合材料,其中Sn颗粒粒径约为100 nm.电化学研究表明,75%(w)锡含量的该材料100次循环后容量保持在550 mAh·g-1.Wang等[8]利用硅球做模板,苯蒸汽为碳源,制备了粒径约为750 nm的中空碳球.再与SnO2颗粒复合得到C/SnO2复合材料,当SnO2含量为25.6%(w)时,这种复合材料在60个循环内的可逆比容量保持在450 mAh·g-1.模板法制备的锡/碳复合材料,虽然有效地改善了锡电极的循环性能,但是工艺过于复杂,不适用大量的制备.并且碳球受到模板颗粒大小的影响,粒径一般大于500 nm[7-9].
本工作的思路是先采用本实验室发明的催化热解法制备洋葱状中空纳米碳颗粒(OC)[10],继而通过溶液浸渍和氧化手段制备中空碳壳包覆纳米氧化锡复合材料,研究其作为锂电池电极材料使用时的电化学性能,以期揭示炭壳层对SnO2材料的阻隔和缓冲作用,利于开发具有优越综合性能的电极材料.
1 实验
1.1 材料的制备
1.1.1 中空洋葱状碳颗粒的制备[10]
按碳与铁原子比为1∶0.24的比例称取一定量的炭黑(惰性气体保护下,激光灼烧乙炔气体获得)和硝酸铁(Fe(NO3)3·6H2O,分析纯,广东西陇化工厂).将二者放入烧杯中,倒入定量乙醇(分析纯,北京世纪红星化工有限责任公司),搅拌72 h后,80℃水浴蒸发乙醇至样品呈膏状,干燥.将干燥后的混合物放入炭化炉内,氮气气氛下,2℃·min-1速率升温到1000℃,保温10 h.
将上述制得的样品加入到4 mol·L-1的盐酸溶液中,搅拌三天后用去离子水抽滤洗涤直至滤液呈中性,然后干燥得到OC.所用盐酸溶液由浓盐酸(分析纯,北京化学试剂厂)和去离子水配制得到.
1.1.2 SnO2/OC复合材料的制备
将0.1 g OC加入到25 mL、2 mol·L-1的SnCl2/乙醇溶液中,40℃恒温搅拌三天,经离心分离,3次乙醇洗涤后,干燥得到OC/SnCl2复合物,所用氯化亚锡(SnCl2·2H2O)为分析纯,北京化学试剂公司生产.称取一定量的复合物放入马弗炉中于350℃焙烧氧化1 h,使其发生反应:2SnCl2·H2O+O2→2SnO2+ 4HCl[3],锡盐氧化为二氧化锡,得到SnO2/OC复合材料(记为SnO2/OC-1),TG分析确认其中SnO2含量为70.9%(w).为了除净OC表面的SnO2,获得纯净的OC包覆的SnO2电极材料,将0.2 g的SnO2/OC-1粉末加入到4 mL,2 mol·L-1的HCl溶液中浸泡2 h,离心清洗至中性,真空干燥得到纯净样品(记为SnO2/ OC-2),其SnO2含量为63.0%(w).将SnO2/OC-1复合材料在马弗炉中800℃灼烧20 min以完全除去炭,得到白色粉末,即为纯SnO2.
1.2 材料的表征
采用透射电子显微镜(日本日立H-800型)和扫描电镜(日本日立S-4700)研究样品的形貌和结构.借助X射线衍射仪分析样品晶体结构(日本理学RICOND/MAX2400X,操作条件:铜靶辐射CuKα,λ= 0.154 nm,管压40 kV,管流140 mA,扫描范围5°到90°,步进宽度0.02°,步进速率10(°)·min-1).使用德国NETZSCH STA449C综合热分析仪测定复合材料中的SnO2含量,测试条件:高纯氧气气氛,流量25 mL·min-1,升温速率10℃·min-1,终温1000℃.
1.3 电化学性能测试
电化学性能测试采用扣式模拟电池方法.锂片作对电极和辅助电极,电解质为1 mol·L-1六氟磷酸锂(LiPF6)的乙烯碳酸酯(EC)/和二甲基碳酸酯(DMC) (1∶1体积比)溶液(德国Merck公司).工作电极的制备:将活性物质、粘结剂聚偏氟乙烯和导电剂乙炔黑以质量比80∶10∶10的比例均匀混合.用N-2-甲基-吡咯烷酮调制成膏状物后均匀地涂抹在集流体泡沫镍上,放入真空烘箱中80℃干燥4 h,而后在10 MPa压力下压片,真空烘箱中120℃干燥12 h得到工作电极炭膜.以该炭膜作为工作电极,金属锂作为对电极组装成CR2032型钮扣电池,模拟电池的组装在充满氩气的德国M.BRAUN公司UNILAB型手套箱内完成,水、氧指标均低于1×10-6MPa.在电池程控测试仪(CT2001A型,武汉兰电测试设备有限公司)上进行充放电性能测试(充放电电流密度0.2 mA· cm-2,电压测量范围为0.01-2.5 V).循环伏安测试采用CHI 660B电化学工作站(上海辰华仪器公司),电压扫描范围为2.5-0.01V,扫描速率为0.1mV·s-1.
2 结果与讨论
图1给出了OC和SnO2/OC-1样品的XRD谱图.从图中可以看出,OC在26.3°出现明显的碳(002)峰,较窄的峰型说明制备的OC属于半结晶碳.少量的杂质可能为未除尽的催化剂Fe、Fe3C[11]和酸处理过程中氧化生成的Fe3O4,TGA分析其残留质量为3.59%(w).SnO2/OC-1在26.4°、33.6°、51.2°和64.2°出现的特征峰分别对应于SnO2的(110)、(101)、(211)和(301)晶面(JCPDS卡号72-1147),峰型宽而弥散,说明掺杂的SnO2颗粒小且为无定型相.谢乐公式计算表明SnO2平均粒径为12 nm.谱图中未出现前驱物的峰,说明SnCl2完全分解生成SnO2.
图2为样品OC、SnO2/OC-1和SnO2/OC-2的SEM和TEM照片.由图2(a,b)可见,OC为粒径40 nm左右、分布均匀的纳米中空球.比较酸处理前后的SEM图(图2(c,e))可以看出,处理前由于OC的表面被粒径细小的非晶SnO2颗粒包裹,OC的形貌不明显,SnO2颗粒的形貌也较模糊;处理后复合材料中的SnO2的含量降低了8%(w),OC颗粒的形貌显现出来,说明酸处理有效地减少了包覆在OC表面的SnO2的量,更多的SnO2处于OC的内部,这将会更有利于SnO2电化学性能的提高.由图2(d,f)的TEM还可以看出,SnO2为OC中空碳球的复合结构.

图2 样品的SEM(a,c,e)和TEM(b,d,f)图Fig.2 SEM(a,c,e)and TEM(b,d,f)images of samples(a,b)OC;(c,d)SnO2/OC-1;(e,f)SnO2/OC-2
图3为四种样品组成电极的循环性能曲线.可以看出,OC电极的充放电容量基本稳定在140 mAh·g-1,显示出很高的循环稳定性,50次循环后的容量保持率D50/D1=100%(Dn表示第n次循环的放电容量),这与炭材料的结构本质有关.纯SnO2电极首次放电容量为849 mAh·g-1,50次循环后,容量迅速衰减至123 mAh·g-1,D50/D1=14.5%,显示很差的循环性能.与OC复合后,SnO2/OC-1电极的可逆容量达到728 mAh·g-1,经50次循环下降至293 mAh· g-1,D50/D1=40.2%.与纯SnO2电极相比,循环性能有大幅改善.对于SnO2/OC-2负极材料,尽管其SnO2含量有所下降,但容量衰减却显著减缓,首次放电容量为755 mAh·g-1,50次循环稳定后仍然保持有446 mAh·g-1,D50/D1=59.1%,显示较好的应用前景.需要指出的是,OC、SnO2、SnO2/OC-1和SnO2/OC-2的首次循环效率分别为33.7%、58.7%、48.9%和54.6%.首次不可逆容量损失可能主要来源于SnO2不可逆还原为Sn和电极表面生成SEI膜的过程.OC具有最小首次效率的原因在于它的多孔性[10,12].众所周知,纯SnO2和石墨的理论容量分别为781和372 mAh· g-1,依此计算可以得到SnO2/OC-1和SnO2/OC-2的理论容量分别为662和630 mAh·g-1,实际循环容量(728和755 mAh·g-1)要高于此理论值,许多研究也发现过该现象[13-16],其原因可以归结于在空心纳米颗粒表面形成了溶胶状的有机层,以及纳米复合材料的表面和中空内壁具有更多的储锂位.
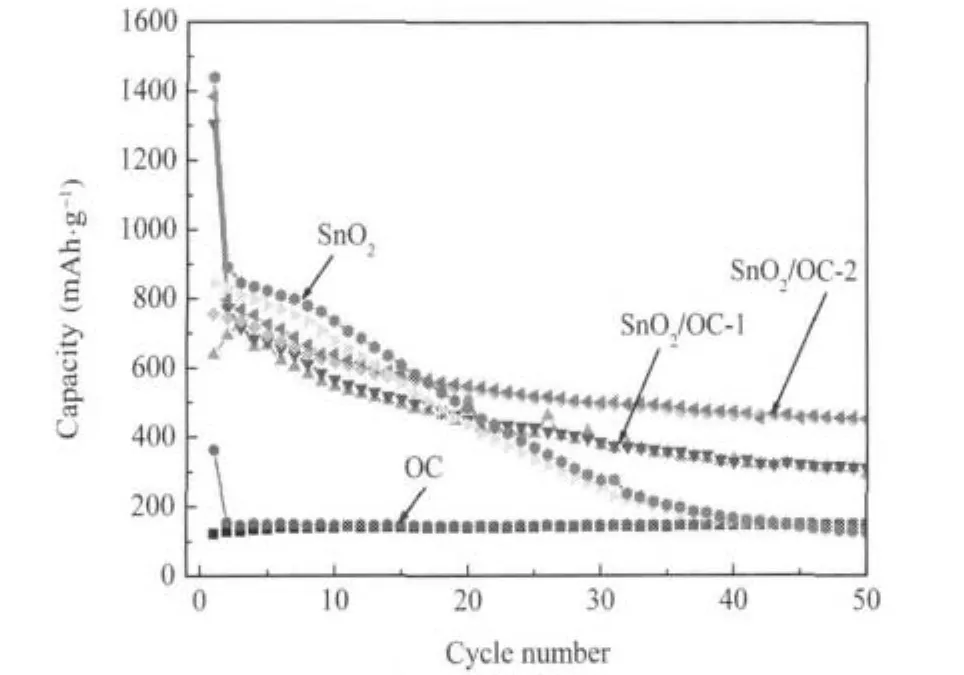
图3 样品的循环性能Fig.3 Cycling performance of samples
尽管SnO2/OC-1中SnO2的含量高于SnO2/OC-2,50次循环后SnO2/OC-2的容量明显高于SnO2/ OC-1,这是因为在SnO2/OC-1样品中,OC的表面存在一定量的SnO2颗粒.在循环过程中,这些存在于碳壳表面的纳米SnO2颗粒由于“粉化”和“团聚”,使容量迅速下降,同时还会阻塞Li+嵌入/脱出OC的通道,导致Li+不能有效的嵌入到OC壳层内的SnO2中,OC没有起到明显的缓冲作用,导致SnO2/ OC-1负极的容量衰减仍然较大,50次循环后的容量保持率仅为理论容量的44.3%.而酸处理后的样品循环性能明显改善,50次循环后的容量保持率达到70.8%.这说明表面的SnO2被大量去除后,在Li+插入/脱出的过程中,OC壳层起到了缓冲样品膨胀和阻止团聚的作用.
图4为OC和SnO2/OC-2复合材料的前三次循环伏安曲线.对纯OC电极,从图4(a)中可以看出,首次循环曲线分别在0.56和0.02 V出现两个还原峰,在0.26 V出现一个氧化峰.0.56 V出现的还原峰对应于电解质在OC电极表面分解形成固体表面电解质膜(SEI膜)的过程.这个峰在第二和第三次循环曲线中消失,说明SEI膜主要在第一次的充电过程中形成.0.02和0.26 V出现的还原氧化峰为锂离子嵌入OC碳壳形成锂碳化合物和从中脱出的过程[4],这个过程在图4(b)中0.01-0.2 V区间同样出现,在图5的充电曲线中表现为0.25 V左右形成的平台.图4(b)中SnO2/OC-2复合材料的首次扫描曲线在0.9 V左右处出现的还原峰,对应于复合材料电极表面SEI膜的形成过程和SnO2和Li+之间发生不可逆的置换反应生成金属Sn和非晶态Li2O的过程[3,17],即,SnO2+4Li+4e→Sn+2Li2O.在第二和第三次循环的1.1和0.6 V左右处出现的还原/氧化峰,应为复合材料中锡与锂形成合金/去合金化的过程,即:Sn+ xLi++xe→LixSn.分别对应于图5中放电曲线在1.4 V左右和充电曲线在0.75 V左右形成的平台[18].然而随着充放电次数的增加,图5中放电曲线在1.4 V处的平台最后变得不明显,成为可逆容量损失的原因之一,这可能与部分SnO2与锂离子反应过程中的“粉化”失活有关[5].
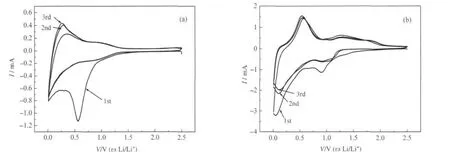
图4 OC(a)和SnO2/OC-2(b)的循环伏安曲线Fig.4 Cyclic voltammetry curves of OC(a)and SnO2/OC-2(b)composite materials
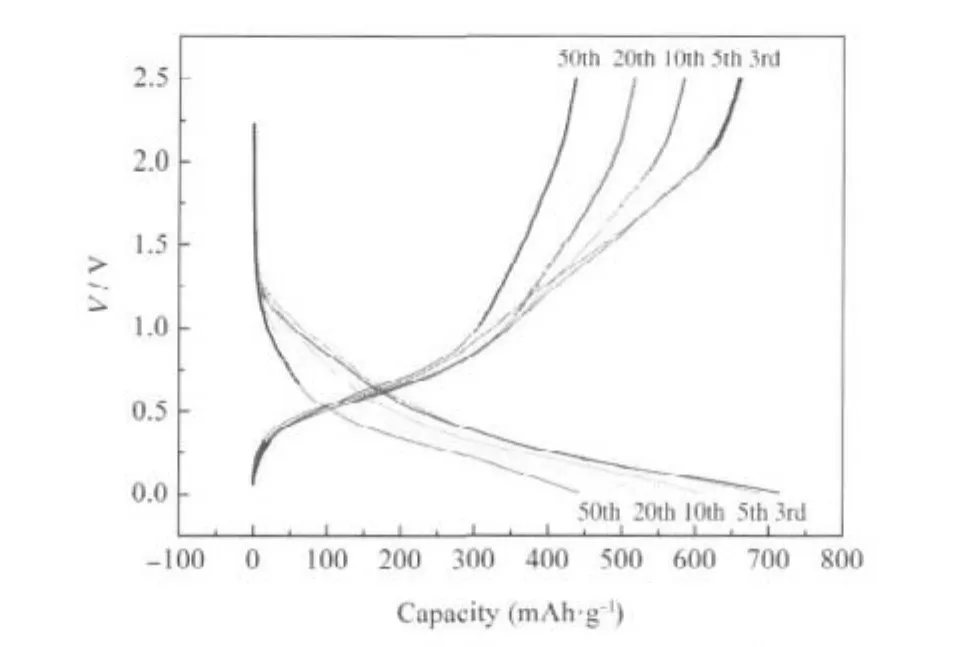
图5 不同循环次数时SnO2/OC-2的充放电曲线Fig.5 Charge/discharge curves of SnO2/OC-2 composite materials at different cycles
3 结 论
以炭黑为原料,硝酸铁为催化剂前驱体制备得到粒径在40 nm左右的纳米中空洋葱状碳颗粒(OC),将其作为缓冲材料与SnO2复合,得到SnO2和OC的复合材料.利用稀盐酸溶液浸泡清洗,以除去OC表面的SnO2颗粒.电化学性能测试表明:酸处理后,复合材料的循环性能得到明显的改善,50次循环后可逆容量达到446 mAh·g-1,OC起到了缓冲样品膨胀和阻止团聚的作用.
1 Wang,Z.;Tian,W.H.;Li,X.G.Chinese Journal of Power Sources,2007,31(11):926 [王 忠,田文怀,李星国.电源技术,2007,31(11):926]
2 Chang,C.C.;Liu,S.J.;Wu,J.J.;Yang,C.H.J.Phys.Chem.C, 2007,111:16423
3 Wang,Z.Y.;Chen,G.;Xia,D.G.J.Power Sources,2008,184: 432
4 Yang,S.B.;Song,H.H.;Chen,X.H.J.Power Sources,2007, 173:487
5 Paek,S.M.;Yoo,E.J.;Honma,I.Nano Lett.,2009,9(1):72
6 Ren,M.M.;Zhou,Z.;Gao,X.P.;Yan,J.Progress in Chemistry, 2008,20(5):771 [任慢慢,周 震,高学平,阎 杰.化学进展, 2008,20(5):771]
7 Zhang,W.M.;Hu,J.S.;Guo,Y.G.;Zheng,S.F.;Zhong,L.S.; Song,W.G.;Wan,L.J.Adv.Mater.,2008,20:1160
8 Wang,Y.;Su,F.B.;Lee,J.Y.Chem.Mater.,2006,18:1347
9 Lee,K.T.;Jung,Y.S.;Oh,S.M.J.Am.Chem.Soc.,2003,125: 5652
10 Lian,W.T.;Song,H.H.;Chen,X.H.;Li,L.X.;Huo,J.P.;Zhao, M.;Wang,G.Q.Carbon,2008,46(3):525
11 Huo,J.P.;Song,H.H.;Chen,X.H.;Zhao,S.Q.;Xu,C.M. Materials Chemistry and Physics,2007,101:221
12 Zhao,M.;Song,H.H.;Chen,X.H.;Lian,W.T.Acta Materialia, 2007,55:6144
13 Zhou,J.S.;Song,H.H.;Chen,X.H.;Zhi,L.J.;Yang,S.B.;Huo, J.P.;Yang,W.T.Chem.Mater.,2009,21:2935
14 Wang,P.C.;Ding,H.P.;Bark,T.;Chen,C.H.Electrochim.Acta, 2007,52:6650
15 Rosso,M.;Brissot,C.;Teyssot,A.;Dolle,M.;Sannier,L.; Tarascon,J.M.;Bouchetc,R.;Lascaud,S.Electrochim.Acta, 2006,51:5334
16 Laruelle,S.;Grugeon,S.;Poizot,P.;Dolle,M.;Dupont,L.; Tarascon,J.M.J.Electrochem.Soc.,2002,149:A627
17 Lou,X.W.;Deng,D.;Lee,J.Y.;Archer,L.A.Chem.Mater., 2008,20:6562
18 Yang,T.H.;Guo,Y.L.;Zhou,X.C.;Liu,Y.M.Journal of Inorganic Materials,2009,24(1):147 [杨同欢,郭永榔,周学酬,刘永梅.无机材料学报,2009,24(1):147]
September 17,2009;Revised:November 27,2009;Published on Web:February 3,2010.
Preparation and Electrochemical Properties of SnO2/Onion-Like Hollow Carbon Nanoparticle Composites as Anode Materials for Lithium-Ion Batteries
ZHANG Hui-Juan SONG Huai-He*ZHOU Ji-Sheng ZHANG Hong-Kun CHEN Xiao-Hong
(State Key Laboratory of Chemical Resource Engineering,Beijing University of Chemical Technology,Beijing 100029)
Newkindsofonion-likehollowcarbonnanoparticles(OC)withameandiameterof40nmweresynthesized by the pyrolysis of carbon black at 1000℃in a nitrogen atmosphere using ferric nitrate as the catalyst precursor.By impregnating with a SnCl2/ethanol solution and oxidation in air at 350℃,OC doped SnO2nanoparticle composites were obtained.Then,by rinsing with hydrochloric acid to remove the coated SnO2nanoparticles,OC-encapsulated SnO2nanoparticle composites were prepared.The morphologies and structures of OC and the composites were characterized by X-ray diffraction(XRD),scanning electron microscopy(SEM),and transmission electron microscopy (TEM).The content of SnO2in the composite was measured by thermogravimetric analysis(TGA).The electrochemical properties of the composites as anode materials for lithium-ion batteries were evaluated by galvanostatical method and cyclic voltammetry(CV).We found that after acid treatment the sample possessed a reversible capacity of 446 mAh·g-1after 50 cycles and excellent cycle stability.This indicates that OC is a suitable matrix to buffer against volume expansion and to prevent the agglomeration of SnO2nanoparticles.
Nano onion-like carbon;Tin dioxide; Composite;Anode materials;Lithium-ion battery
[Article] www.whxb.pku.edu.cn
*Corresponding author.Email:songhh@mail.buct.edu.cn;Tel:+86-10-64434916.
The project was supported by the National Natural Science Foundation of China(50572003,50972004)and Excellent PhD Thesis Foundation of Beijing,China(YB20081001001).
国家自然科学基金(50572003,50972004)和北京市优秀博士学位论文基金(YB20081001001)资助项目
O646
