甾体激素引入6α氟原子的各种方法
2010-11-07郭罕奇
郭罕奇 裴 文
(浙江工业大学化学工程与材料学院,杭州310014)
甾体激素引入6α氟原子的各种方法
郭罕奇 裴 文*
(浙江工业大学化学工程与材料学院,杭州310014)
叙述了利用氟化氢、三氟化硼、过氯酰氟、2-氯-1,1,2-三氟三乙胺氟化溴、亲电试剂NFPy和N-氟代磺酰亚胺氟化剂向甾体激素引入6α氟原子的方法,比较了各种方法的优缺点,认为N-氟代磺酰亚胺为氟化试剂引入6α氟原子的方法N-氟代磺酰亚胺氟化试剂,具有高立体选择性,毒性小,反应相对温和、安全。
甾体激素;氟化;N-氟代磺酰亚胺合成
甾体激素分子中引入6α氟原子后,常能使其母体的生理作用大为加强,或者出现新的生理作用,其原因可能是引入6α氟原子后,可阻止其氧化代谢失活[1]。因此含6α氟甾体激素的研究对甾体药物的发展占有十分重要的地位。目前临床上应用的特别有效的许多甾体激素药物,其分子中经常含有6α氟原子。
随着含氟甾体药物工业生产上改进的要求、新的含氟甾体激素的研究和合成,以及新的氟化试剂的发现,对于在甾体环核中引入6α位氟原子的方法有了很大的发展。
欲在甾体环核的6α位引入1个氟原子,通常利用甾体分子中在该位置上的某一官能团与适当的氟化试剂作用而得,文献上所报道的用于引入6α氟原子的氟化试剂有氟化氢、三氟化硼、过氯酰氟、氟化溴、2-氯-1,1,2-三氟三乙胺、NFPy、N-氟代磺酰亚胺等[2-10]。本文按各种氟化试剂介绍引入6α氟原子的方法。
1 氟化氢为氟化剂
氟化氢的化学性质和一般卤化氢相似,可以使氧环断裂、在烯键上加成反应、与羟基置换等。如果在反应介质中加入有机碱,氟氢酸的离解会增加,因而有利于反应的进行,使产物的产量增加。通常应用四氢吠喃作为有机碱。
用氟化氢处理5α,6α-环氧甾体1时可在C6位置引入1个氟原子后生成2[2-4],再将它的C3取代基改变成C3-酮基化合物3后用酸消除5α-羟基并使6β-氟原子转位,则可生成 6α-氟-4-烯-3-酮甾体4[11-12]。 反应式为:

2 三氟化硼为氟化剂
5α,6α-环氧甾体5用三氟化硼的乙醚溶液处理后,所得的产物和用无水氟化氢处理的结果相同,生成5α-羟基-6β-氟甾体6,再将6化合中的3-羟基或3-乙二醇缩酮基变为3-羰基化合物7,消除其5α-羟基并使6β-氟原子转位,最后生成6α-氟-4-烯-3-酮甾体8[5,11-12]。反应式为:

3 过氯酰氟为氟化剂
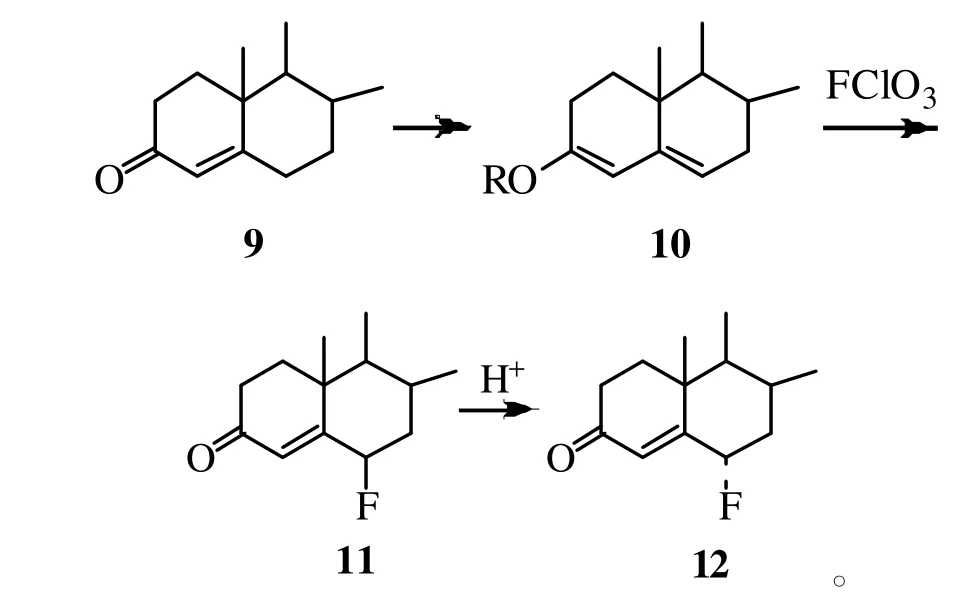
将4-烯-3-酮甾体9所形成的烯醇醚或酯10与过氯酰氟反应,引入一个 6β-氟原子而得 11[6,13-15];再用盐酸-氯仿溶液处理,则6β-氟原子转位,生成稳定的6α-氟甾体12[11-12]。反应式为:
4 氟化溴为氟化剂
△5-3β-羟基甾体13非常容易与氟化溴反应生成相应的5α-溴-6β-氟的衍生物14。此反应在低温下进行,通常将△5-甾烯13溶于二氯甲烷-四氢呋喃中,在-80℃下加入大量的无水氟化氢(约25~100 mol),然后再加1 mol的N-溴代乙酞胺,保持一定时间后即得化合物14。如再将所得产物14的3-羟基氧化成酮15,用甲醇-醋酸钠消除5α-溴原子后,可得 6β-氟-4-烯-3-酮甾体 16,再用氯化氢-氯仿溶液处理,使6β-氟原子转位,生成6α-氟-4-烯-3-酮甾体17[7,11-12]。反应式为:

5 2-氯-1,1,2-三氟三乙胺为氟化剂
当2-氯-1,1,2-三氟三乙胺为氟化试剂时,甾体激素引入6α氟原子的效果不是很理想,6β-羟基甾体18与2-氯-1,1,2-三氟三乙胺作用时,只生成少量的6α-氟甾体19,而甾体Ⅲ主要生成消除产物Ⅳ[8,16]。 反应式为:

6 NFPy为氟化剂
应用亲电氟化试剂NFPy引入1个C-6位氟原子,6β甾体的异构化速度较快,从4-烯-3-酮甾体22所形成的烯醇酯23与NFPy氟化试剂反应,引入1个氟原子而得6α、6β的混合物24,再通过异构化处理,生成稳定的6α-氟甾体25[9]。其反应式为:
7 N-氟代磺酰亚胺为氟化剂
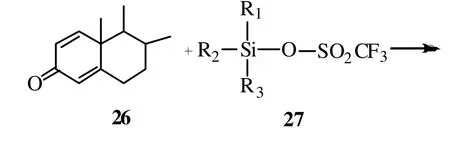
Umemoto等人应用N-氟代吡啶盐作为氟化试剂,但6β异构体总是主要产物[17-18]。Taylor等人报道了N-氟代苯磺酰亚胺作为氟化试剂的应用,但是对于高立体选择性在6α位引入氟原子没有得到满意的结果[19]。Jose等人在此基础上采用N-氟代磺酰亚胺为氟化试剂,一步反应得到相应的反应产物6α-氟代甾体,不需要经过6β-氟代甾体的异构化过程,具有较高的立体选择性,从起始物26到产物29,产率超过75%[10]。反应式为:

8 总结与展望
对于传统的氟化试剂氟化氢、三氟化硼、过氯酰氟、氟化溴,立体选择性较差,首先生成6α、6β混合物,其中6β异构体的含量较高,需要通过对6β异构体的异构化过程才能得到具有生理活性的6α异构体,并且氟代反应较为剧烈危险,氟化试剂毒性较大。而对于N-氟代磺酰亚胺氟化试剂,具有高立体选择性可以直接向甾体6α位引入氟原子,并且毒性比传统氟化试剂要小,反应相对温和、安全。
甾体激素正在向多方面用途发展,希望在抗肿瘤药物、心血管药物、计划生育及老年骨质疏松治疗药方面能寻找出新药。通过引入6α-氟原子将在寻找新药过程中发挥巨大的作用。
[1]祝翠红.地塞米松合成新工艺的研究[D].天津:天津大学,2005:7-8.
[2]Hogg J A,Spero G B,Thompson J L,et al.6-Fluoro analogues of Steroid Hormones[J].Chem And Ind,1958:1002-1003.
[3]Schneider W P,Lincoln F H,Spero G B,et al.6α-Fluoro-16α-Methyl Analogs of cortical Hormones[J].J Am Chem Soc,1959,81:3167-3168.
[4]Enger C R,Reghenghi R.Steroids and Related Products.VIII.The Synthesis of 6α-Fluoro-17α-bromoprogesterone[J].Can J Chem,1960,38:452-456.
[5]Mills J S,Bowors A,Dierassi C,et al.Steroids CXXXVII.Synthesis of a New Class of Potent Cortical Hormones.6α,9α-Difluoro-16α-hydroxyprednisolone and its Acetonide[J].J Am Chem Soc,1960,82:3399-3404.
[6]Timko J M.Introduction of a fluoring atom:US,4383947[P].1983-05-17.
[7]Grabbé P,Ringold H J,Zdoric J A.Steroids CLXVIII.Une Nouvelle Voie D'acces a la Acetonide de la 6α,9α-Difluoro-16α-hydroxyprednisolone[J].Bull Soc Chem Belges,1961,70:271-284.
[8]Ayer D E.New Method for the Preparation of Fluoro Steroids[J].Tetrahedron letters,1962:1065-1069.
[9]Yearn S C,John A K.Synthesis of C-6 fluoroandrogens:E-valuation of ligands for tumor receptor imaging[J].Steroid-s,1995,60(5):414-422.
[10]Carrido J V M,Guisasola L O S,Juarez J M.Stereoselect-ive process for the production of 6 al pha-fluorpregnanesand intermediates:US,20040181055[P].2004-09-16.
[11]Shephard K P.Process for producing 6α-fluoro-△1,4-3-keto steroids:US,4340538[P].1982-07-20.
[12]Cainelli G,Umani-Ronchi A,Sandri S,et al.Process for the prepapation of 6alpha-fluoro steroids by isomerisationof 6beta-fluoro-steroids:US,20050192437[P].2005-09-01.
[13]Nakanishi S,Morita K,Jensen E W.The Reaction of Perchloryl Fluoride with Enol Ethers[J].J Am Chem Soc,1959,81:5259-5260.
[14]Magerlein B J,Lincoln F H,Birkinmeyer R D,et al.6α-Fluoro-and 6α-Methyl-16α-fluoro-prednisolones[J].Chem And Ind,1961:2050-2051.
[15]Bloom A M,Bogert V V,Pinson R A.New Synthesis of 6-Fluoro Steroids[J].Chem and Ind,1959:1317-1317.
[16]Knox L H,Velarde E,Berger S,et al.The Reactions of Steroidal Alcohols with 2-chloro-1,1,2-trifluorotriethylamine[J].Tetrahedron letters,1962:1249-1255.
[17]Umemoto T,Fukami S,Tomizawa G,et al.power-and structure-variable fluorinating agents.The N-fluoropyridinium salt system[J].J Am Chem Soc,1990,112(23):8563-8575.
[18]Umemoto T,Tomizawa G.Highly selective fluorinating agents:acounteranion-boundN-Fluoropyridiniumsaltsystem[J].J Org Chem,1995,60(20):6563-6570.
[19]Taylor S D,Kotoris C C,Hum G.Recent advances in electrophilic fluorination[J].Tetrahedron,1999,55(43):12431-12477.
TQ467.8
A DOI10.3969/j.issn.1006-6829.2010.03.0001
。E-mail:pei_wen58@hotmail.com
2010-03-09
