碳羟基磷灰石对废水中Ni2+的吸附性能研究
2010-11-07董春华张永霞邯郸学院化学系056005
董春华 张永霞 邯郸学院化学系 056005
碳羟基磷灰石对废水中Ni2+的吸附性能研究
董春华 张永霞 邯郸学院化学系 056005
1 引言
目前,人们越来越关注环境的可持续发展,对重金属造成的污染治理日益重视。随着低碳经济的提出,人们也在积极寻求节能环保的治污材料。利用废弃蛋壳为主要钙原合成的碳羟基磷灰石(CHAP),由于其特殊的晶体化学特征,具有良好的离子交换性能,可用于吸附并回收利用废水中大多数的重金属离子[1,2]。本研究将其用于对含镍废水的处理,以期达到以废制废,变废为宝的目的。
2 实验部分
2.1 试剂和仪器
碳羟基磷灰石,自制。硫酸镍,高纯,天津市光复化工研究所;硝酸,优级纯,天津市化学试剂三厂;无水乙醇,分析纯,天津市红岩化学试剂厂;溴化钾,光谱纯,天津市化学试剂三厂。傅立叶变换红外光谱仪,美国尼高力仪器公司,MAGNA-IR550Ⅱ;原子吸收分光光度计,北京普析通用仪器公司,TAS-986F。
2.2 CHAP的合成
以蛋壳粉和CaHPO4·2H2O为反应物,按钙磷物质的量比为1.67进行反应。将蛋壳粉和CaHPO4·2H2O在研钵中研细混匀,于90℃水浴,恒温加热磁力搅拌6 h,抽滤,烘干,转移至坩埚,放入箱式电阻炉中,900℃煅烧6h。产物经抽滤并用蒸馏水及无水乙醇洗涤至pH值约为7[3]。所得产物在远红外干燥箱中烘干。
2.3 实验方法
先配制Ni2+的标准溶液, 绘制Ni2+的标准曲线,再稀释标准溶液得到所需浓度的Ni2+溶液,然后配制含Ni2+的废水溶液100mL进行吸附实验。用原子吸收分光光度计分析残留液中Ni2+的含量,并计算其吸附容量和去除率,从而得出羟基磷灰石吸附Ni2+的最佳吸附条件[4]。
3 结果与讨论
3.1 CHAP的表征
IR分析结果见图1。图1中549.3cm-1,574.2cm-1处是磷酸根的弯曲振动吸收峰;607.4cm-1是结构羟基的弯曲振动吸收峰;972.4cm-1,1042.9cm-1,1092.6cm-1处是磷酸根的伸缩振动吸收峰;碳酸根在1457.6cm-1,1470.0cm-1处出现分裂,呈现两个吸收峰,说明碳酸根进入了羟基磷灰石结构中;3568.7cm-1是结构羟基的伸缩振动吸收峰[5]。

图1 碳羟基磷灰石红外谱图
3.2 碳羟基磷灰石对Ni2+的最佳吸附条件的确定
3.2.1 Ni2+的初始浓度对吸附效果的影响。常温常压下,分别配制体积为100 mL,浓度为10 mg/L~100 mg/L的含Ni2+溶液,放入锥形瓶中。测得其pH值均为6~7;再分别投入0.1 g的CHAP吸附剂,用磁力搅拌器搅拌1h,使吸附反应充分进行。最后再测定残留液中Ni2+的浓度。从表1和图2中可以看出,在吸附剂投入量不变的情况下,Ni2+初始浓度从10 mg/L至30mg/L, 去除率均能保持在98 %以上,当浓度超过30mg/ L, 去除率呈明显下降趋势,浓度增加到50mg/L时,去除率则仅为93.12%,去除效果较差。
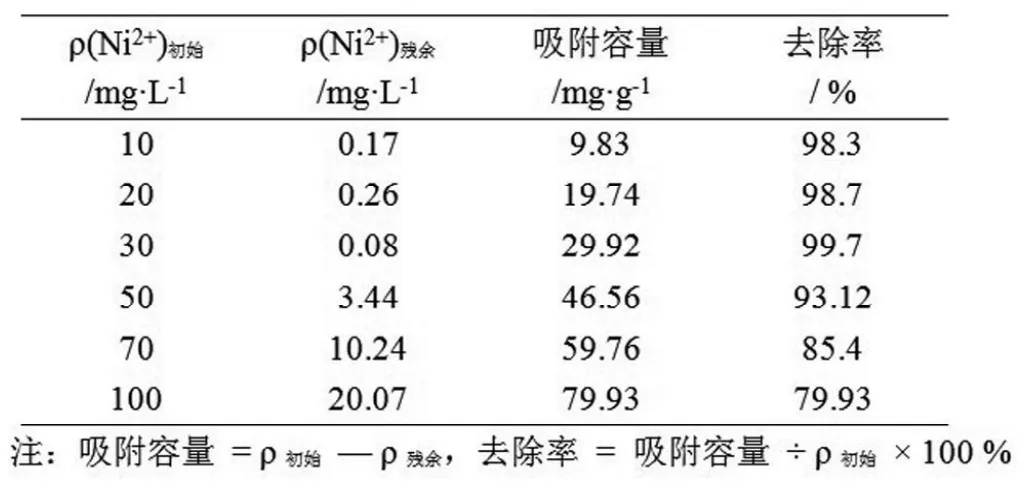
表1 Ni2+初始浓度对吸附效果的影响
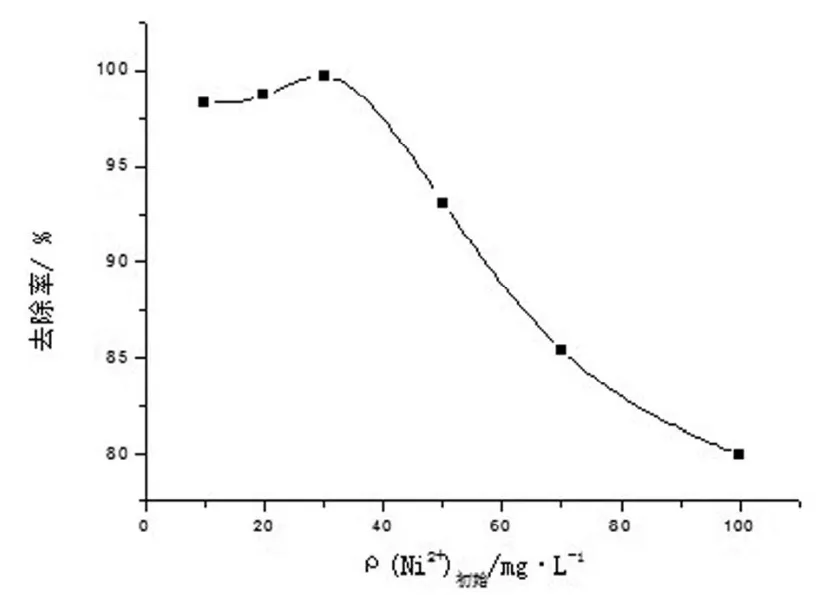
图2 Ni2+初始浓度与去除率的关系
3.2.2 吸附时间对吸附效果的影响。常温常压下,分别取10组100mL浓度为30mg/L的Ni2+溶液作为待吸附液,均调节pH值为6~7,再分别加入0.1gCHAP作为吸附剂,用磁力搅拌器分别搅拌2 min~60min后, 测定残留液中Ni2+的浓度。从表2和图3中可以看出,CHAP吸附Ni2+时间为10min时, 其吸附基本上达到平衡,对30mg/L的含Ni2+溶液去除率接近100%。
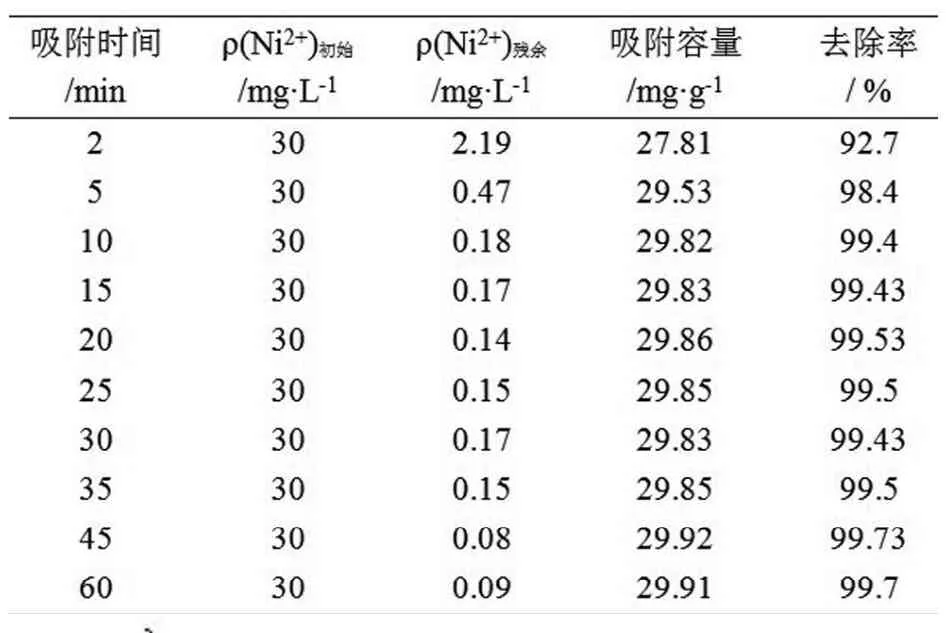
表2 吸附时间对吸附效果的影响
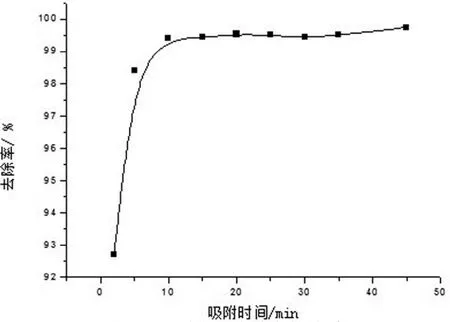
图3 吸附时间与去除率的关系
3.2.3 吸附剂用量对吸附效果的影响。常温常压下,分别配制100mL浓度为30mg/L的Ni2+溶液作为待吸附液,均调节pH值为6~7,再分别加入0.05g~0.11g的CHAP作吸附剂,用磁力搅拌器搅拌10min后, 测定残留液中Ni2+的浓度。从表3和图4可以看出, 随着CHAP的增加, 吸附容量和去除率都跟着上升,当用量达到0.08g时,Ni2+的去除率已达99.5%。
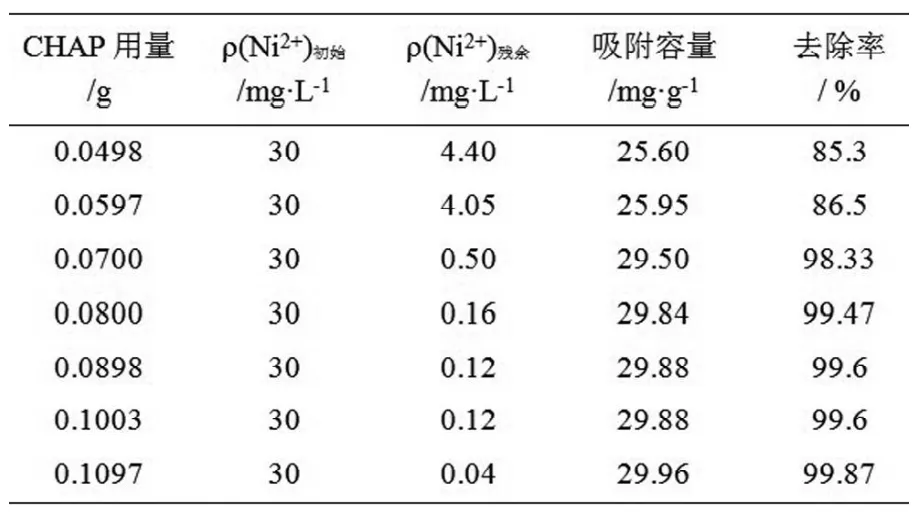
表3 吸附剂用量对吸附效果的影响
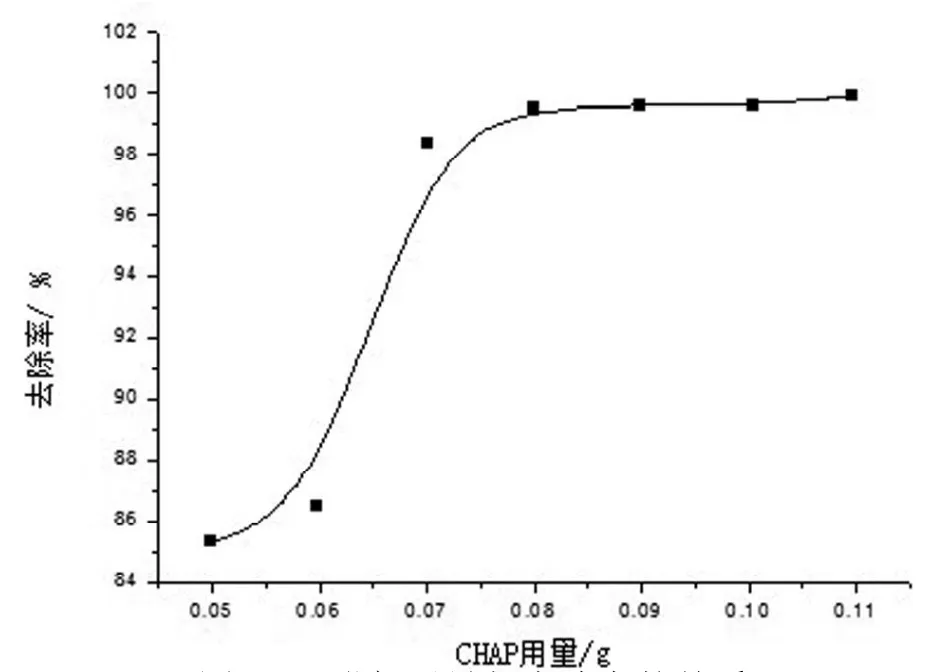
图4 吸附剂用量与去除率的关系
3.2.4 pH值对吸附效果的影响。常温常压下,分别配制100mL浓度为30mg /L的Ni2+溶液作为待吸附液,再分别加入0.08g HAP作吸附剂,依次调节pH值为2.0~7.0。用磁力搅拌器搅拌10min,测定残留液中Ni2+的浓度。从表4和图5可知,随着pH值的增加,吸附容量和去除率都呈上升的趋势。在pH=2时,HAP对Ni2+的去除率很低, 只有16.1%。说明在强酸性条件下对Ni2+的吸附不利。这是因为在强酸性条件下HAP的溶解度增大。随着pH值的增加,去除率也增加。这是由于随着pH值的增加,HAP的表面负电荷也增加,更有利于对阳离子的吸附。当pH值为7左右时去除率已经接近100%,这说明最适合Ni2+去除的pH值为中性条件。
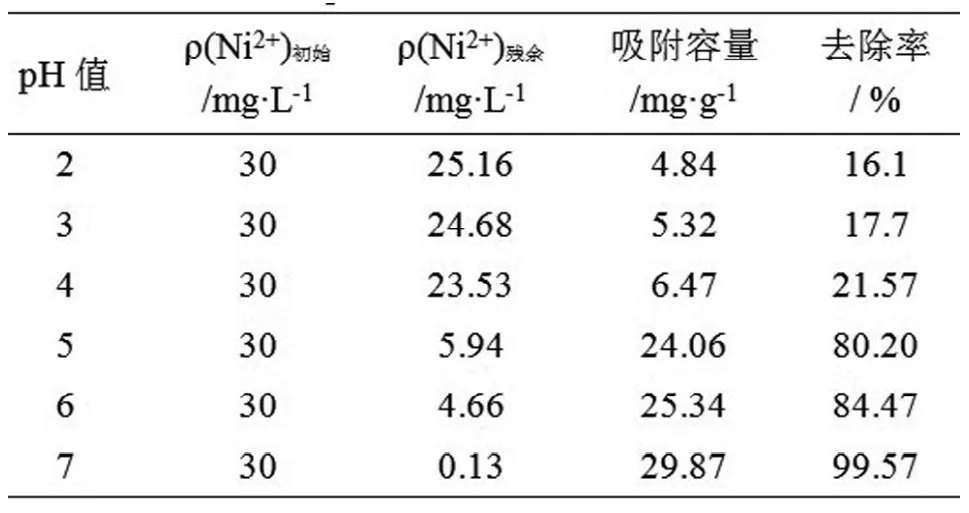
表4 pH值对吸附效果的影响

图5 pH值与去除率的关系
3.2.5 温度对吸附效果的影响。分别配制100mL浓度为30mg/L的Ni2+溶液作为待吸附液,均调节pH值为6~7,再分别加入0.08g HAP作吸附剂,分别在25℃~75℃水浴中,恒温磁力搅拌10min后, 测定残留液中Ni2+的浓度。从表5和图6可以看出,一开始随着温度升高,去除率呈上升趋势,35℃时达到99.6%,高于35 ℃时, 去除率呈下降趋势, 然后趋于平衡。
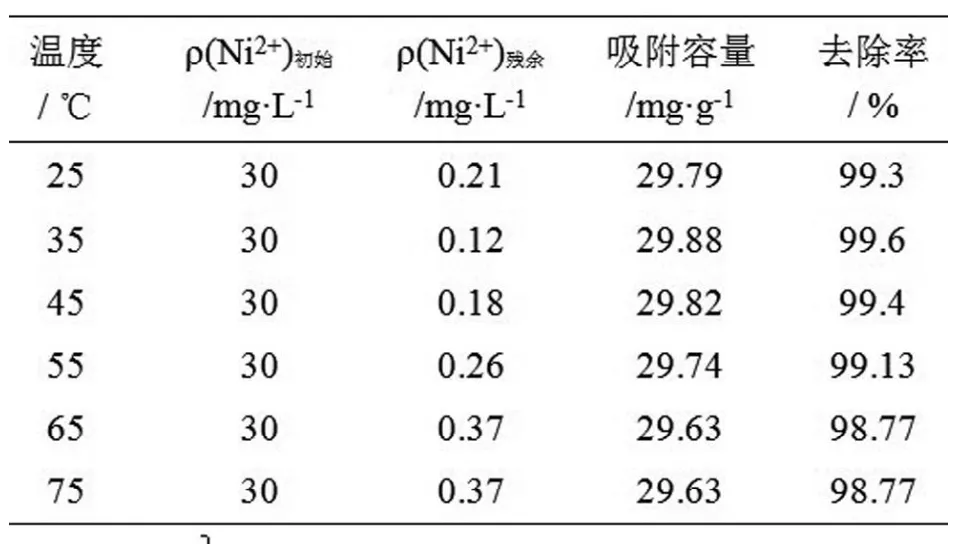
表5 温度对吸附效果的影响
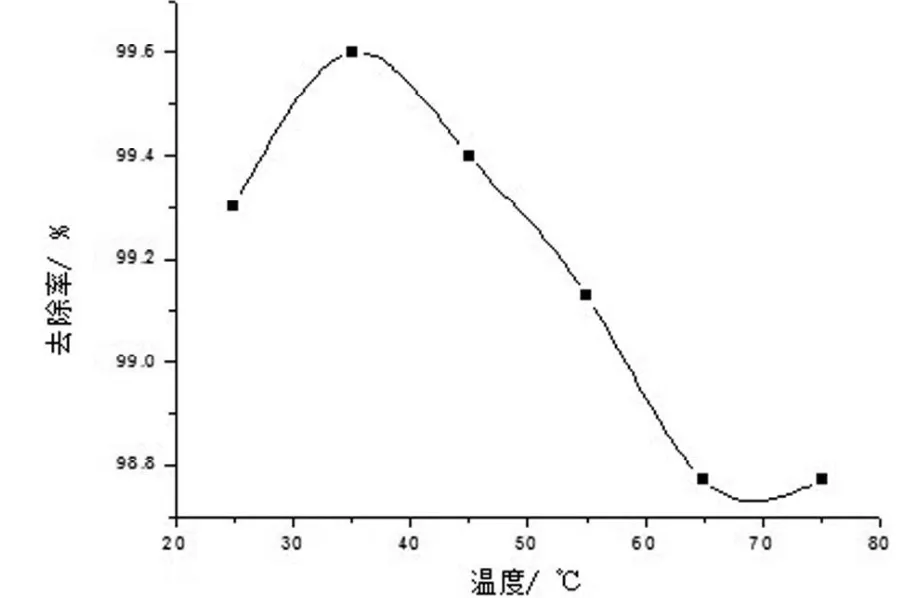
图6 温度与去除率的关系
4 结论
4.1 由废弃蛋壳制备的碳羟基磷灰石可作为环境功能材料吸附废水中的Ni2+,达到废物利用的目的。
4.2 CHAP对Ni2+离子有较好的吸附效果,吸附速度比较快,在10 min左右基本达到吸附平衡。
4.3 CHAP对30 mg/LNi2+溶液的最佳吸附条件为:pH值为7,吸附时间为10min,吸附剂用量为0.08g,温度为35℃。
[1] 韩松, 冯如彬, 张杰.羟基磷灰石对水溶液中Cu2+的吸附动力学研究[J].河北工程大学学报.2007,1: 78-80.
[2] 唐文清, 曾光明, 蓝俊康, 等.碳羟基磷灰石对废水中Cd2+的吸附[J].桂林工学院学报.2006, 3: 388-391.
[3] 张力, 王辉, 汪超, 等.载银羟基磷灰石的合成及其抗菌测试[J].研究论著.2004,7: 22-23.
[4] 张洪利, 贾兰珍, 邢光印.火焰原子吸收法测水中钴[J].仪器仪表与分析监测.2006,1: 31- 32.
[5] 唐文清, 曾光明, 曾荣英, 等.碳羟基磷灰石对废水中Zn2+的吸附性能及机理研究[J].金属矿山.2007,3: 73-77.
Study on Carbonate Hydroxyapatite’s Adsorption Capacity for Nickel(Ⅱ)from Waste water
Dong Chunhua Zhang Yongxia
(Department of Chemistry, Handan College, Handan, 056005, P.R.China.)
以废弃蛋壳为原料,通过煅烧法合成了碳羟基磷灰石。采用红外光谱法对其结构进行了表征。利用碳羟基磷灰石吸附模拟废水中的Ni2+,考察Ni2+初始浓度、pH值、吸附时间、吸附剂用量以及温度等因素对吸附效果的影响。结果表明:当废水中Ni2+初始浓度为30mg/L、pH=7、吸附时间为10min、吸附剂用量为0.08g、温度为35℃时,羟基磷灰石对Ni2+去除率接近100%。
碳羟基磷灰石;镍(Ⅱ);吸附
Carbonate hydroxyapatite was prepared from abandoned eggshell by calcined synthesis.The propertie of hydroxyapatite was characterized by IR spectroscopy.Hydroxyapatite was used to remove Ni2+ from simulated wastewater.The results showed that the adsorption effect was controlled by the initial concentration of Ni2+, pH value in wastewater, adsorption period, the consumption of hydroxyapatite and the reaction temperature.The results showed that the rate of the removal of Ni2+by hydroxyapatite was about 100 %, when the initial concentration of Ni2+in wastewater was 30 mg/L, pH value was 7, adsorption period was 10 min, the consumption of hydroxyapatite was 0.08 g, and the reaction temperature was 35 ℃.
Carbonate hydroxyapatite; Nickel(Ⅱ); Adsorption
10.3969/j.issn.1001-8972.2010.09.002
董春华,硕士,讲师,研究方向:无机化学。