毛细管整体柱在线二维分离系统应用于人体软骨的蛋白质组分析
2010-10-21谢沙洁王方军周广东叶明亮邹汉法
谢沙洁, 王方军, 晏 丹, 周广东, 叶明亮, 邹汉法*
(1.中国科学院大连化学物理研究所,中国科学院分离分析化学重点实验室,国家色谱研究分析中心,辽宁大连116023;2.组织工程国家工程研究中心,上海交通大学医学院附属第九人民医院整形外科,上海200011)
毛细管整体柱在线二维分离系统应用于人体软骨的蛋白质组分析
谢沙洁1, 王方军1, 晏 丹2, 周广东2, 叶明亮1, 邹汉法1*
(1.中国科学院大连化学物理研究所,中国科学院分离分析化学重点实验室,国家色谱研究分析中心,辽宁大连116023;2.组织工程国家工程研究中心,上海交通大学医学院附属第九人民医院整形外科,上海200011)
将已建立的7cm柱长的磷酸基团强阳离子交换富集整体柱与85cm柱长的C12烷基反相整体柱结合的在线二维分离平台应用于软骨提取蛋白的蛋白质组分析。对20μg软骨提取蛋白的酶解产物进行14个盐梯度的分级,然后对14个馏分进行反相色谱梯度分离及串联质谱鉴定,成功地鉴定得到了7 434个独立肽段对应的1 901个非冗余蛋白质。对所鉴定到的蛋白质进行定位分类,结果表明鉴定到的大部分蛋白质是来自于软骨细胞内部的低丰度蛋白质,这对于许多关节类疾病的研究有重要意义。
整体柱;在线二维分离;蛋白质组学;软骨组织
Abstract:In Shotgun proteome analysis,where nano-flow is adopted to increase the sensitivity as w ell as extrem ely com p licated samples such as proteolytic digest are inevitably confronted,monolithic capillary columns are widely used to improve the liquid Chromatography separation performance.It is known that cartilage contains extensive amounts of extracellular matrix(ECM),in which collagens and aggrecans being the most abundant macromolecules.It is obvious that the high content of ECM components causes a challenge in the comprehensive proteome analysis of cartilage.In this study,a7cm×150μmi.d.phosphate strong cation exchange(SCX)monolithic capillary column was coup led with an85cm×75μmi.d.C12reversed-phase monolithic capillary column for online two-dim ensional separation of20μg tryp tic digest of proteins extracted from hum an cartilage.After14salt steps fractionation and following gradient separation coup led with tandem mass spectrometry detection,finally7 434unique pep tides,corresponding to1 901distinct proteins were positively identified.Then,the identified proteins were analyzed by Gene Ontology(GO),and it was found that most of the identified proteins were com e from articular chondrocytes with low abundance,which is important for the researches of articular diseases.
Key words:monolithic column;online two-dimensional separation;proteomics;cartilage tissue
“鸟枪法”(Shotgun)蛋白质组学是将蛋白质混合物先进行酶解,然后通过鉴定酶解后的肽段来鉴定蛋白质的一种“从下至上”(bottom up)的蛋白质组学研究策略[1-3]。毛细管纳升液相色谱与串联质谱联用(μHPLC-MS/MS)是“鸟枪法”蛋白质组学的技术核心,通过毛细管液相色谱对微量蛋白质酶解样品的高效分离,极大地提高了质谱对复杂样品进行蛋白质鉴定分析的能力[4]。在蛋白质组学样品中具有重要生物学意义的蛋白质往往是低丰度蛋白质,进一步提高毛细管液相色谱的分离能力对低丰度蛋白质的质谱鉴定具有重要意义。多维液相色谱分离是最强大的液相色谱分离模式[5-7],而在线多维液相色谱分离又具有高效快速、样品用量小、样品损失少、无样品污染等诸多优点。在蛋白质组学研究中,对于微量的蛋白质样品,在线多维分离具有更大的优势[8-10]。
Yates等[11-13]在同一根100μm的毛细管中以先后顺序分别填充了反相(RP)分离填料和强阳离子交换(SCX)填料,将蛋白质的酶解物先上样到SCX部分,然后通过不同的盐梯度将富集在SCX部分的肽段分级冲洗到RP部分,再分别进行反相梯度分离和串联质谱的检测,从而实现了在线二维分离和串联质谱检测联用,对蛋白质样品具有强大的分离鉴定能力。这种方法也被称为“多维蛋白质鉴定技术(M uD PIT)”的方法,在蛋白质组学研究中得到了广泛的应用。但是由于Yates等人应用的是毛细管填充柱,分离柱的反压大,上样速度慢;而且为了保证反相部分的分离能力,强阳离子交换填料填充部分不能太长,上样能力受到限制的同时也降低了第一维的分级分辨率[14]。相对于填充柱而言,整体柱具有的多孔结构使其具有很高的渗透性和传质速率,从而实现高效快速分离。近年来,毛细管整体柱已经被广泛地应用到纳升毛细管液相色谱中,极大地推动了蛋白质组学的发展[15-21]。
关节软骨包括软骨细胞(~1%,体积分数)和细胞外基质(ECM),其中ECM的主要组成部分包括胶原蛋白和蛋白聚糖。由于大量细胞外基质的存在,要对软骨细胞中的蛋白质进行充分的提取就必须对软骨组织进行充分的切片或研磨。但软骨组织被充分破坏后将导致大量的胶原和蛋白聚糖进入提取液,由于其丰度非常高,将极大地影响液相色谱-质谱联用对蛋白质样品中低丰度蛋白质的分析鉴定[22]。现阶段人们对软骨组织蛋白质的组成了解不多,对软骨蛋白的大规模鉴定到现在为止还是一个难题。在已有的文献报道中,采用双向电泳方法的软骨蛋白质组分析只鉴定了不到200个蛋白质[23,24]。
我们以带有磷酸基团的SCX整体柱为富集柱,以带有C12基团的整体柱为反相分离柱组成二维分离系统,以串联质谱作为检测手段构建了一套自动在线多维分离-串联质谱联用系统[14,25,26]。本文将该系统应用于软骨蛋白质组分分析,通过对20 μg软骨提取蛋白质的胰蛋白酶酶解物进行分析,在假阳性率(FPR)小于1%的情况下共鉴定得到了7 434个独立肽段(unique pep tide),对应于1 901个非冗余蛋白质。
1 实验部分
1.1 仪器与试剂
2-(甲基丙烯酰氧)乙基磷酸酯(EGM P)、亚甲基双丙烯酰胺(bis-acrylam ide)、二甲基亚砜(DMSO)、十二醇、二甲基甲酰胺(DM F)、十二烷基甲基丙烯酸酯(LMA)、二甲基丙烯酸乙二酯(EDMA)和γ-甲基丙烯酰氧基丙基三甲氧基硅烷(γ-MAPS)均购于美国Sigm a公司;偶氮二异丁腈(A IBN)购于上海第四试剂厂;胰蛋白酶购于美国Prom ega公司;二硫苏糖醇(D TT)、碘代乙酰胺(IAA)和蛋白酶抑制剂购于北京Sino-Am erican生物技术公司;75 μm和150μm内径毛细管购于美国Polym icro公司;乙腈为色谱纯,购于美国M erck公司;实验用水为M illi-Q超纯水。
Surveyor HPLC液相色谱系统(美国热电公司),配有脱气机和四元液相泵。3种分离流动相为:流动相A,0.1%甲酸水溶液;流动相B,0.1%甲酸乙腈溶液;流动相C,1mol/L醋酸铵溶液(pH 3)。流动相从液相色谱流出后通过一个三通阀分流,使其达到分离所需的200nL/m in的流速。LTQ线性离子阱质谱(美国热电公司),配有纳升电喷雾离子源和一个六通阀。
1.2 软骨蛋白的提取和酶解
100m g人体软骨(上海第九人民医院提供)放置于研钵中,加入液氮,充分多次研磨。然后将研磨后的软骨粉末转移到1.5mL的离心管中,加入1mL含有6mol/L盐酸胍、0.1mol/L Tris和蛋白酶抑制剂的蛋白质提取液(pH7.4),在室温下充分振荡2h。将离心管在9 100r/m in(6 000g)离心5m in,上清液转移到10mL离心管中并用氯仿/甲醇沉淀法将上清液中的蛋白质沉淀出来。离心出来的沉淀物在用甲醇清洗后复溶于1mL含8mol/L尿素和0.05mol/L Tris(pH8.1)的变性试剂中,蛋白质浓度通过B radford方法进行测定。然后该蛋白质样品在37℃用D TT还原2h,并在避光的环境下用IAA对打开的二硫键进行封端40m in。随后用0.05mol/L的Tris溶液(pH8.1)将溶液的尿素浓度稀释到1mol/L。最后加入胰蛋白酶(其质量为蛋白质总量的1/25),并在37℃下保持24h。所得到的胰蛋白酶酶解物用实验室自制的C18固相萃取柱进行除盐纯化并复溶于0.1%的甲酸水溶液中。该样品储存于-20℃冰箱中待用。
1.3 整体柱的制备
两种整体柱的制作与以前报道的方法一致[14,16,25]。制作强阳离子交换毛细管整体柱时,将80μL EGM P、60m g亚甲基双丙烯酰胺、270μL DMSO、200μL十二醇、50μL DM F和2m g A IBN混合并超声振荡15m in。配制的聚合溶液通过虹吸进入150μm内径毛细管,将毛细管两端用硅橡胶封口,然后放入60℃水浴反应12h;最后用甲醇冲洗出未反应的聚合单体及致孔剂即可。制作反相毛细管整体柱时,将100μL LMA、100μL EDMA、170μL正丙醇、130μL1,4-丁二醇、20μL水和2 m g A IBN混合,然后通过虹吸进入75μm内径毛细管,其余步骤与SCX整体柱制作步骤相同。对于反相毛细管整体柱,在制作完成后还要在冲水的情况下在柱子的出水端用丁烷焰拉制一个内径约为5 μm的电喷雾针头。
1.4 样品自动进样及液相色谱分离
样品自动进样及在线二维分离系统如图1所示。7cm长的150μm内径SCX整体柱通过四通阀和六通阀与85cm长的75μm内径RP柱相连,RP分离柱通过电喷雾针头直接与质谱偶联,电喷雾的电压通过铂丝加在四通阀的一个出口上。在上样时,六通阀处于实线位置,蛋白酶解样品以10 μL/m in的流速上样到SCX整体柱上,废液通过六通阀排出;分析时六通阀切换至虚线位置开启分流通路,流动相通过三通阀分流后以200nL/m in的流速通过两种整体柱进行分离。
在进行在线二维分离时,先将20μg软骨提取蛋白的胰蛋白酶酶解物自动上样到SCX整体柱上,然后将流动相A(0.1%甲酸水溶液)和流动相C(pH值为3的1mol/L醋酸铵水溶液)以不同的比例混合得到不同浓度的NH4Ac盐溶液流动相,14种不同浓度的盐溶液以200nL/m in的流速将SCX整体柱上富集的肽段分级洗脱到RP整体柱上。分离梯度设置:循环1由流动相A和流动相B组成的混合流动相以0%B到8%B洗脱2m in,从8%B到30%B洗脱90m in,从30%B到0%B洗脱2m in,然后整个系统用100%A平衡25m in。接下来的12个分离循环都为250m in,其设置如下:先用X%(以流动相C比例计)的混合流动相(由流动相A和C混合所得)冲洗5m in,100%A平衡10 m in,然后由流动相A和B组成的RP分离梯度进行分离,其梯度程序为:从0%B到8%B洗脱5m in,从8%B到30%B洗脱205m in,从30%B到0%B洗脱5m in,然后整个系统用100%A平衡20 m in;其中5分钟的X%设置为:循环2,5%;循环3,10%;循环4,15%;循环5,20%;循环6,25%;循环7,30%;循环8,35%;循环9,40%;循环10,45%;循环11,50%;循环12,60%;循环13,80%。最后一个分离循环设置为:100%C冲洗10m in,100%A平衡10m in,然后由流动相A和B组成的RP分离梯度进行分离,其梯度程序为:从0%B到8%B洗脱5m in,从8%B到30%B洗脱205m in,从30%B到80%B洗脱10m in,保持80%B冲洗10m in,然后整个系统用100%A平衡25m in[14,25]。
图2是20μg软骨提取蛋白的胰蛋白酶酶解物经14个盐梯度分级后反相色谱梯度分离的质谱检测基峰图。

图1 整体柱在线二维分离系统示意图Fig.1 Schematic diagram of the on line multidimensional separation system using monolithic capillary columns
1.5 质谱检测条件及数据库搜索
LTQ质谱在正离子模式下操作,离子传输毛细管的温度为200℃,喷雾电压为1.8kV,归一化碰撞能量为35%。所有一级谱(MS)和二级谱(MS/MS)在Data Dependent Analysis(DDA)模式下操作。一个一级谱扫描后对其中强度最高的6个峰进行二级质谱分析。系统的操作和数据的采集都使用Xcalibur软件(v1.4,热电公司)完成。
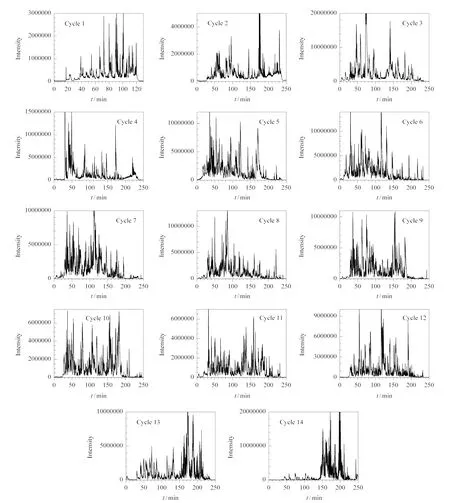
图2 20μg软骨提取蛋白质的胰蛋白酶酶解物14个循环在线二维色谱分离的纳升电喷雾质谱检测基峰图Fig.2 Base peak chromatograms of a14-cycle on line two-d imensional analysis of20μg cartilage proteins tryptic digest
所收集的MS/MS谱图通过SEQU EST程序(B ioW orks3.2,热电公司)进行数据库检索。为了评价检索结果的假阳性率,将人IPI(InternationalProtein Index)蛋白质数据库(v3.17)(包含60 236个蛋白质条目)的反库与正库合并。半胱氨酸残基在数据库搜索过程中带有57.021 5D a的固定修饰;甲硫氨酸残基在数据库搜索过程中带有15.994 9D a的可变修饰。肽段在数据库搜索中应用两端完全酶解限制,允许2个漏切位点。对母离子的质量偏差允许为2D a,对碎片离子的质量偏差允许为1D a。Xcorr函数值设定为对于单电荷肽段大于1.9,双电荷肽段大于2.2,三电荷肽段大于3.75。ΔCn值设置为0.3,保证鉴定的FPR小于1%。
2 结果与讨论
2.1 色谱分离与蛋白质鉴定效果
从图2中可以看出富集于SCX整体柱上的肽段被充分地分级为14个馏分,每个馏分肽段的基峰强度都是较为一致的,证明了在线二维色谱分离的有效性。另外也可以看到,当用1mol/L的醋酸铵冲洗时(图2循环14)所得到的峰的数目明显比其他组分少,说明富集到SCX整体柱上的肽段已经基本上被完全洗脱下来了。将所收集到的串联质谱数据用SEQU EST按照实验部分所述的方法进行数据库检索,最后鉴定得到了7 434个独立肽段和1 901个非冗余蛋白质(蛋白质簇,每一个蛋白质簇中包含的多个可能蛋白质只记为一个鉴定到的非冗余蛋白质)。其中,由两段或两段以上肽段所鉴定到的蛋白质有1 112个,占鉴定蛋白质总数的58.5%。该数目远远多于以往文献所报道的已鉴定得到的软骨蛋白质数目,充分证明了该在线二维分离系统在大规模蛋白质组学鉴定中的优势。为了证明该在线二维分离串联质谱检测系统的重现性,相同的实验又重复进行了一次。在相同的数据筛选条件下,成功鉴定到了7 487个独立肽段和2 014个非冗余蛋白质(蛋白质簇)。由两段或两段以上肽段所鉴定到的蛋白质有1 129个,占鉴定蛋白质总数的56.1%。在两次实验中都得到鉴定的独立肽段和非冗余蛋白质的数目分别为5 229和1 458个,占到了实验鉴定总数的70.3%和76.7%。
图3是14个盐梯度上新鉴定到的独立肽段和非冗余蛋白质数目的分布情况,从中可以看出实验中鉴定到的肽段和蛋白质充分对称地分布于14个盐梯度上。最后一个1mol/L的盐梯度上鉴定到的蛋白质和肽段数目都明显变少,再次证明了富集到的肽段已经基本上洗脱完全了。14个盐梯度上肽段和蛋白质的分布结果与图2中所得到的基峰图的分布结果是一致的,也说明了该在线二维分离的有效性,SCX整体柱与RP整体柱良好的正交性对肽段和蛋白质的鉴定有很大的帮助。

图3 经14个盐梯度在线二维分离新鉴定到的(a)肽段和(b)蛋白质的分布图Fig.3 Distribution of the newly identified(a)unique peptides and(b)distinct proteins by the14 salt steps in on line two-dimensional separation
第一维分离与第二维分离的正交性是决定二维分离能力的关键因素。在以往的研究中,SCX与RP的填充柱被广泛地应用于离线和在线多维分离中,取得了很好的结果[5-10]。在本工作中,我们应用了7cm长的SCX整体柱,提高了分级的分辨率[27]。基峰图和鉴定到的肽段和蛋白质在14个盐梯度上的对称分布都很好地说明了这一点。另外,由于整体柱良好的渗透性,在反相梯度分离中应用了85cm长的C12有机整体柱,保证了第二维的分离能力,这也是该系统能很好地分离肽段、鉴定得到1 901个软骨蛋白质的原因之一。
2.2 蛋白质分类分析
软骨组织中存在着大量的细胞外介质,其中主要是胶原蛋白和蛋白聚糖,它们是提取出来的蛋白质中的主要成分。大量的高丰度蛋白质极大地阻碍了广泛存在的低丰度蛋白质的鉴定,这也是软骨蛋白鉴定的难点所在。在本工作中,我们通过整体柱和在线二维分离的应用极大地提高了系统的分离能力,从而成功地鉴定到了1 901个软骨蛋白质。采用蛋白质分类软件Gene O ntology(GO)对所鉴定到的蛋白质按其来源进行分类,结果见表1。可以看出,丰度排名前30位的高丰度蛋白质来自于细胞外基质的有16种而只有9种来自软骨细胞内,说明细胞外基质中的高丰度蛋白质在样品中是大量存在的;但对所鉴定得到的所有软骨蛋白来说,有938种蛋白质来自于软骨细胞内部,只有68种来自于细胞外基质。该表充分说明了虽然高丰度的蛋白质大量存在,但是由于该二维系统的分离能力,软骨细胞内部的低丰度蛋白质也得到了充分的鉴定,这对于研究许多软骨疾病如关节炎等都是非常有帮助的[22-24]。

表1 蛋白质在软骨组织中的来源分类表Table1 Categorization of the identified cartilage proteins based on cellular component
3 结论
本文将7cm长的SCX整体柱和85cm长的RP整体柱所构建的在线自动二维分离平台应用于软骨蛋白质组分析。20μg软骨提取蛋白质的胰蛋白酶酶解产物经μLC-MS/MS分离鉴定分析,最后成功地鉴定得到了7 434个独立肽段和1 901个非冗余蛋白质。据我们的文献调研,这是迄今有关软骨蛋白质组学大规模鉴定的最好结果。根据生物信息学的分析,大部分鉴定到的蛋白质都是来自于软骨细胞内部的低丰度蛋白质,这对于许多关节类疾病的研究有重要意义。
[1] Aebersold R,Mann M.Nature,2003,422:198
[2] Peng J M,Schwartz D,Elias J E,et al.Nat Biotechnol,2003,21:921
[3] Beausoleil S A,Villén J,Gerber S A,et al.Nat Biotechnol,2006,24:1285
[4] Ye M L,J iang X G,Feng,S,et al.Trends Anal Chem,2007,26:80
[5] Link A J.Trends B iotechnol,2002,20(12,Supp l):S8
[6] Vollm erM,Hörth P,Nägele E.Anal Chem,2004,76:5180
[7] J in W H,Dai J,Li S J,et al.J Proteom e Res,2005,4:613
[8] Peng J,Elias J E,Thoreen C C,et al.J Proteom e Res,2003,2:43
[9] Jiang X G,Feng S,Tian R J,et al.Proteom ics,2007,7:528
[10] Wagner K,M iliotis T,Marko-Varga G,et al.Anal Chem,2002,74:809
[11] Link A J,Eng J,Schieltz D M,et al.Nat B iotechnol,1999,17:676
[12] Wolters D A,washburn M P,Yates J R III.Anal Chem,2001,73:5683
[13] washburn M P,Wolters D,Yates J R III.Nat B iotechnol,2001,19:242
[14] Wang F J,Dong J,Ye M L,et al.J Proteom e Res,2008,7:306
[15] Xie C H,Ye M L,J iang X G,et al.mol Cell Proteom ics,2006,5:454
[16] Wu R A,Hu L H,W ang F J,et al.J Chromatogr A,2008,1184:369
[17] Yue G H,Luo Q Z,Zhang J,et al.Anal Chem,2007,79:938
[18] Luo Q Z,Yue G H,Valaskovic G A,et al.Anal Chem,2007,79:6174
[19] W ei F,Lin B,Feng YQ.Chinese Journal of Chromatography(魏芳,林博,冯钰锜.色谱),2007,25(2):150
[20] Xie J X,B i K S,Q ian X H,et al.Chinese Journal of Chromatography(谢晶鑫,毕开顺,钱小红,等.色谱),2009,27(2):186
[21] Gu C Y,Lin L,Fang N H,et al.Chinese Journal of Chromatography(谷从影,蔺丽,方能虎,等.色谱),2007,25(2):174
[22] Lamm i M J,Häyrinen J,M ahonen A.Electrophoresis,2006,27:2687
[23] Vincourt J B,Lionneton F,Kratassiouk G,et al.Mol Cell Proteom ics,2006,5:1984
[24] Garcia B A,Platt M D,Born T L,et al.Rap id Comm un mass Spectrom,2006,20:2999
[25] W ang F J,Dong J,J iang X G,et al.Anal Chem,2007,79:6599
[26] W ang F J,Dong J,Ye M L,et al.J Chromatogr A,2009,1216:3887
[27] Gu B H,Chen Z Y,Thulin C D,et al.Anal Chem,2006,78:3509
Application of on line two-dimensional separation system using monolithic columns for proteome analysis of human cartilage
XIE Shajie1,WANG Fangjun1,YAN D an2,ZHOU Guangdong2,YE Mingliang1,ZOU Hanfa1*
(1.Key Laboratory of Separation Science for Analytical Chemistry,National Chromatographic R.& A.Center,Dalian Institute of Chemical Physics,Chinese Academy of Sciences,Dalian 116023,China;2.National Tissue Engineering Center of China,Department of Plastic and Reconstructive Surgery,Shangha i 9th People’s Hospital,Shanghai Jiao Tong University School of Medicine,Shanghai 200011,China)
O658
A
1000-8713(2010)02-0140-06
*通讯联系人:邹汉法,博士生导师,研究员.Tel:(0411)84379610,Fax:(0411)84379620,E-m ail:hanfazou@dicp.ac.cn.
国家自然科学基金项目(Nos.20675081,20735004).
2009-08-11
DO I:10.3724/SP.J.1123.2010.00140
