沸石的改性及除磷性能研究
2010-10-17孙兴滨韩金柱潘华崟
孙兴滨,韩金柱,潘华崟
(1.东北林业大学环境科学系,哈尔滨150040;2.哈尔滨工业大学市政与环境工程学院,哈尔滨150090)
磷是引起水体富营养化的主要元素之一,受磷污染的水体藻类和浮游生物急剧增殖,水体溶解氧下降,水质恶化,并引鱼类及其他水中生物大量死亡.目前国内外常用的除磷方法主要有沉淀法,结晶法,生物除磷,吸附与离子交换等[1].就运行情况来看,生物法的反应速度慢,对于高质量浓度含磷废水处理后难以使水质达到排放标准,而混凝沉淀法则存在运行成本高,后处理困难,水质难达标等缺点[2].其中吸附与离子交换法由于其占地面积小,工艺简单,脱磷效率高得到人们的关注,除磷材料成为研究热点.
改性沸石就是一种新型的除磷吸附材料.天然沸石是呈架状结构的多孔性含水铝硅酸盐晶体的总称,具有四面体骨架结构,其化学组成通式为:[M2(Ⅰ),M(Ⅱ)]O◦Al2O3◦nSiO2◦mH2O,式中,M(Ⅰ)和M(Ⅱ)分别为一价和二价金属离子,通常为钠、钾、钙、锶、钡等.沸石晶体内部有很多大小均一的空穴和通道,使沸石具有巨大的比表面积,达400~800m2/g[3-4],具有良好吸附性能.在沸石构架中,阴离子晶格上的负电与平衡阳离子的正电电荷中心在空间上是不重叠的,具有较大的静电吸引力.然而天然状态下,沸石的孔道常被沸石水及其它杂质堵塞,孔道间相互连通的程度较差,在很大程度上限制了天然沸石的吸附能力[5].目前国内一般对天然沸石进行热处理、酸处理、盐处理以及直接氧化改性等,以提高其吸附交换性能,而且多为处理金属阳离子,而有关沸石改性处理阴离子的信息较少.本文以天然沸石为原料,通过碱浸泡、盐浸渍与高温焙烧的综合处理,旨在研究一种经济有效、操作简单的改性沸石除磷材料,应用于含磷废水的处理.
1 实验材料与方法
1.1 试验仪器
分光光度计,马弗炉,干燥箱,电热鼓风干燥箱,空气浴振荡器,水浴振荡器,Quanta200扫描电子显微镜.
1.2 试验材料
20~40目锦州产天然沸石,实验所用化学试剂均为分析纯,试验用水为去离子水.
1.3 试验方法
采用静态试验法.在烧杯中加入模拟磷水样及改性沸石,在室温下置于空气震荡浴箱中,震荡速度为150 r/min,吸附完成后,静置,取上清液,用钼锑抗分光光度法测定滤液中磷质量浓度,计算磷的去除率和沸石吸附容量.
磷吸附量:q=V×(C0-Ce)/m,磷的吸附率=(C0-Ce)/C0×100%,,式中,m为吸附剂质量,C0和Ce分别为初始和吸附后磷质量浓度,V为磷溶液体积.
微观表征利用美国FEI公司的Quanta200扫描电子显微镜,放大倍数为5 000或10 000倍,显示反映样品表面各种特征.
2 试验结果与讨论
2.1 改性方法的确定
将20~40目的天然沸石洗净烘干,分别采用以下5种方式对其改性:①用20%MgCl2浸泡2 d后洗净烘干;②用1mol/L的氢氧化钠浸泡1 h洗净烘干;③用1 mol/L的氢氧化钠浸泡1 h,20%MgCl2浸泡2 d后洗净烘干;④用1mol/L的氢氧化钠浸泡1 h,20%MgCl2浸泡2 d后洗净烘干,在500℃下焙烧2 h.通过对几种改性的沸石的吸附容量进行分析,得出氯化镁溶液的浸泡可以提高沸石的除磷效果,其中碱的预处理可以进一步提高沸石的除磷容量,经1mol/L的氢氧化钠预处理效果理想,而经过高温焙烧使得效果更加增强.因此本试验选用1 mol/L的氢氧化钠浸泡1 h,20%MgCl2浸泡2 d后洗净烘干,在500℃下焙烧2h后所选的沸石.
2.2 时间对吸附的影响
室温(25℃)下,取2 g改性沸石投加到50mL质量浓度为5mg/L的含磷水样中.由图1可知,去除率与吸附容量在吸附一段时间内增加很快,随着时间的延长,180min后,吸附趋于平衡,吸附容量稳定在0.11 mg/g左右,对磷的去除率达到90%.这说明在吸附时应保证沸石与溶液有一定的接触时间,充分利用沸石的吸附能力.本次相关试验的接触时间选择为180min.
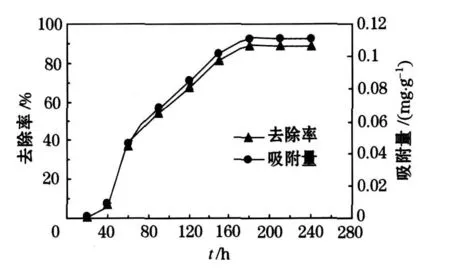
图1 时间对吸附的影响
2.3 投加量对吸附的影响
为了考察吸附剂用量对吸附效果的影响,取不同量的改性沸石材料1、2、3、4、5 g处理质量浓度为5mg/L的模拟磷水样50 m L,吸附3 h后测定.试验结果如图2所示.随着吸附剂用量的增加,沸石对磷的吸附容量逐渐减少而去除率逐渐增加,当沸石投加量在4 g时,去除率基本稳定,随后增加投加量去除率增加缓慢,吸附量降低,这是因为水样中所含有的磷是一定的,增加沸石量会导致个体间的竞争,所以总体看会出现吸附量下降的趋势,而从经济上讲过多的投加量不合理,所以本试验最佳固液比为4∶50.
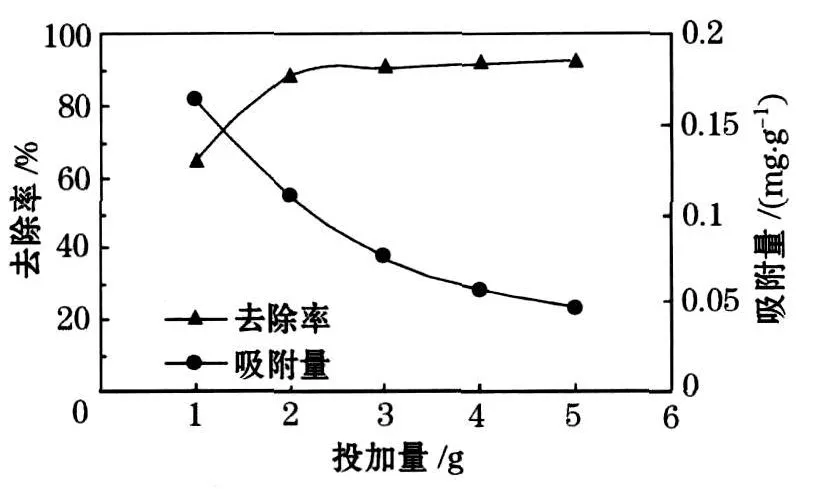
图2 投加量对吸附的影响
2.4 原水质量浓度对吸附速容量的影响
在室温25℃下,取4 g改性沸石投加到50m L质量浓度分别为10、30、50、80mg/L的含磷水样,控制不同的反应时间,吸附容量与反应时间的关系如图3.由图3可知,对于不同质量浓度的含磷水样,总体趋势是反应最初吸附容量增加稍快,随着时间的延长,吸附容量增加缓慢,最后趋于平衡,而且原溶液磷的质量浓度越大,达到平衡时的吸附容量越大.对80 mg/L的含磷水样,3 h后,吸附量可达0.76mg/g左右.
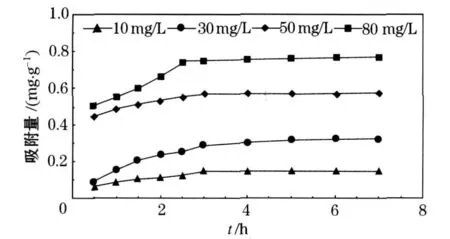
图3 原水质量浓度对吸附速容量的影响
2.5 吸附速率分析
如果在时间t内的吸附量以q来表示,则吸附速率可表示为

其中:q为t时刻的吸附量,m为常数.对此式进行积分,得到:

对于吸附平衡过程中的吸附速率,与吸附推动力和时间有关,斑厄姆提出了如下吸附速率公式:

其中:qe为平衡吸附量,k′和m为常数.积分式为:

根据式(4),用ln{ln[qe/(qe-q)]}和lnt作图,可以得到一条直线.将初始质量浓度为5mg/L的溶液中氟离子质量浓度随时间变化的数据,按斑厄姆公式整理如图4所示.
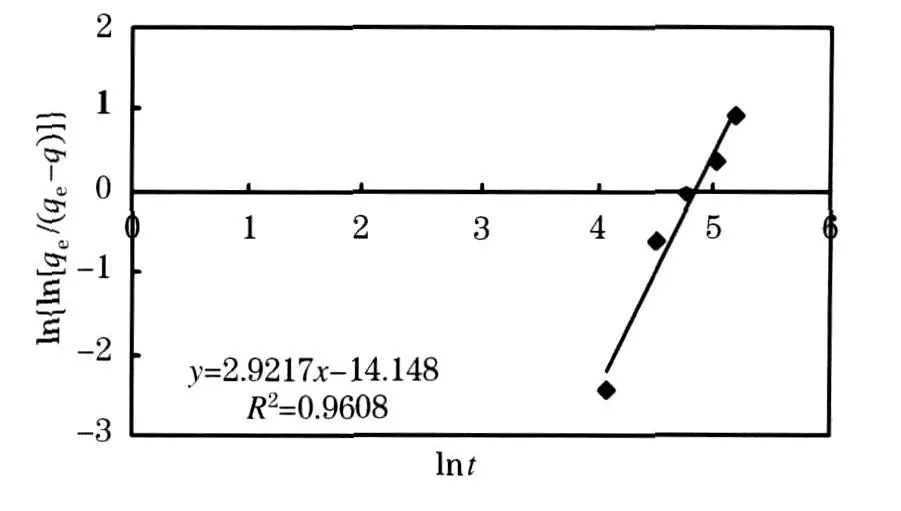
图4 改性沸石除磷线性化
从图4可以看出,沸石的吸附速度按斑厄姆公式整理得线性关系较好,拟合优度R2=0.960 8,说明符合斑厄姆吸附速度公式.其公式形式为:
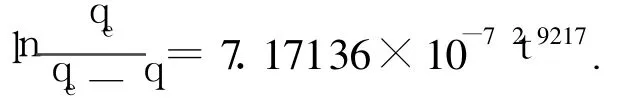
2.6 吸附等温线拟合
分别称取2、3、4、5 g样品,放入250 mL锥形瓶,加入50mL 5mg/L含磷水样,空气浴振荡器25℃振荡180 min.取样5 m L于比色管中,按实验方法操作,用平衡质量浓度和吸附量的对数值做Freundlich等温吸附图,见图5.经计算得n=-0.5363,k=0.1289.
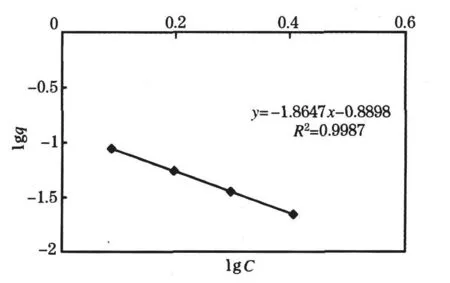
图5 Freund lich等温吸附
根据Freundlich等温吸附,其相关性R2=0.998 7,表明该吸附过程符合Freundlich等温吸附,但n=-0.536 3<1,表明该吸附过程以物理吸附为辅,化学吸附为主,所利用的是改性后沸石其表面和孔道内附着的水合镁对磷酸根的固定作用.其反应式如下:Z◦MgO◦式中Z表示沸石骨架[4].
2.7 改性沸石微观表征
见图6.

图6 不同阶段沸石表观
从图6(A)中可以明显看到,原沸石的表面形貌不太规则,粒度不够均一,晶形较模糊,且空隙较小,虽然分布较多孔道,但表面上黏附的杂质碎屑也比较多,占据了沸石的部分表面积.这说明天然沸石中有很多杂质阻塞了其孔道,不利于磷离子的吸附.图6(B)显示改性后的沸石表面层次更加鲜明,层状结构逐渐消失,并且沸石表面的孔隙大大增多,最终形成很多珊瑚状的表面结构,并伴有网格状的细小的微孔,这种结构变化增加了沸石表面的比表面积,从而提高了沸石的吸附性能.图6(C)表明吸附磷后,沸石表面以及大部分的孔道均被占据或阻塞,沸石的表面包含有吸附的磷、本身固有的结构、还有其他干扰吸附的杂质成分,并且部分水和氧化镁溶出.
3 结 语
天然沸石经1mol/L的氢氧化钠浸泡1 h,再用20%的氯化镁浸泡2 d,在500℃下焙烧2 h,在静态条件下吸附容量有较大提高,对于原水质量浓度80mg/L,吸附容量可达0.76 mg/g左右,改性
后的沸石以化学吸附为主,物理吸附为辅.吸附速度按斑厄姆公式整理得线性关系较好,静态饱和吸附容量可以用Freundlich吸附等温线描述.接触时间、投加量及原水质量浓度对改性沸石吸附效果的影响显著.本试验吸附平衡时间大约为180min,最佳固液比为4∶50.电镜扫描的结果从微观上进一步显示改性后沸石比表面积增加,沸石吸附性能增强.
[1]肖举强,李玉金,郑 辉.沸石除磷性能研究[J].甘肃环境研究与监测,2003,9(3):252-254.
[2]北京市环境保护科学研究所.水污染防治手册[M].上海:上海科学技术出版社,1989.
[3]周明达,张 晖,邵 凯,等.改性沸石处理含磷废水的实验研究[J].环境污染与与防治,2005,27(2):137-138.
[4]张兰泉,崔金贵,肖举强.沸石复合吸附剂除磷性能研究[J].兰州铁道学院学报,1999,18(2):116-120.
[5]孙兴滨,席承菊.改性沸石的除氟性能研究[J].哈尔滨商业大学学报:自然科学版,2008,24(5):539-542.
