消脂护肝片中总黄酮的含量测定
2010-10-16陈蕾姜林
陈蕾,姜林
(新疆维吾尔自治区区中医医院,新疆 乌鲁木齐 830000)
消脂护肝片中总黄酮的含量测定
陈蕾*,姜林
(新疆维吾尔自治区区中医医院,新疆 乌鲁木齐 830000)
目的:建立消脂护肝片中总黄酮的含量测定方法。方法:采用分光光度法,以芦丁为对照品,对其进行络合显色,在510 nm波长处测定吸光度,从而测定消脂护肝片中总黄酮的含量。结果:线性范围在0.008~0.08 mg·mL-1(r=0.999 7),平均回收率为97.0%,RSD=1.84%(n=6)。结论:该法简便易行、重现性好、结果可靠,可用于该制剂的质量控制。
消脂护肝片;总黄酮;分光光度法
消脂护肝片为新疆维吾尔自治区区中医医院院内制剂。由郁金、赤芍、白芍、丹参、山楂、决明子、瓜蒌、海藻、昆布、香附、鸡内金、党参、西红花13味中药组成,具有疏肝、行气、活血的功能,用于高血脂症、脂肪肝、早期肝纤维化。主要化学成分有黄酮类、苷类、有机酸、生物碱类、多糖等。该制剂原质量标准除片剂检查通项外,只有芍药苷的薄层色谱。本实验采用分光光度法对总黄酮进行含量测定,通过对消脂护肝片中总黄酮的含量测定,为该制剂的质量标准提供定量依据。现将结果报道如下。
1 仪器与试药
UV-cintra20紫外分光光度计(澳大利亚GBC scientific Equipment),芦丁对照品(中国药品生物制品检定所,批号100080-200707),消脂护肝片(批号080707,081223,、090511),水为本院实验中心超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 对照品溶液制备[1-2]
精密称取芦丁对照品40 mg,置100 mL容量瓶中,加入甲醇50 mL溶解,再加甲醇稀释至刻度,摇匀,即得0.4 mg·mL-1的对照品溶液。
2.2 供试品溶液制备[3-4]
精密称取样品1 g,加入70%乙醇50mL,超声提取30 min(功率250 W,频率59 KHz),放冷,过滤待用,作为供试品溶液。
2.3 波长的选择[5-6]
对芦丁对照品溶液和供试品溶液从400~800 nm进行扫描,得到紫外-可见吸光图谱,见图1。从图1可知510 nm为最大吸收波长。

图1 芦丁及供试品溶液的紫外-可见图谱
2.4 标准曲线的制备[7-8]
精密量取对照品溶液0.5,1.0,2.0,3.0,4.0,5.0 mL,分别置于25 mL容量瓶中,各加水至6 mL。加入5%亚硝酸钠溶液1 mL,使混匀,放置6 min;加入10%硝酸铝溶液1 mL,摇匀,放置6 min;加入氢氧化钠试液10 mL,再加入水至刻度,摇匀,放置15 min。在510 nm的波长处测定吸收度。以吸收度为横坐标,浓度为纵坐标,绘制标准曲线,并计算得回归方程Y=0.053 7X+0.001 0(r=0.999 7),表明芦丁对照品溶液在0.008~0.08 mg·mL-1呈良好的线性关系。
2.5 稳定性试验
取同一供试品溶液,分别于配制后0,10,20,30,40,50,60,90 min,依照“2.4”项方法测定吸光度,计算RSD=2.33%,结果表明溶液制备后90 min稳定。
2.6 精密度试验
取同一供试品溶液6份,依照“2.4”项方法测定吸光度,计算RSD=1.39%,结果表明仪器精密度良好。
2.7 重复性试验
取供试品溶液1份,依照“2.4”项方法重复测定吸光度值6次,计算RSD=0.40%,结果表明重复性良好。
2.8 重现性试验
制备同一浓度供试品溶液6份,依照“2.4”项方法测定吸光度,计算RSD=0.98%,结果表明重现性良好。
2.9 加样回收率试验
精密称取样品1.0 g,按2.2项下方法制备成供试品溶液,分别精密量取供试品溶液1mL,共6份,每份分别加入一定量芦丁对照品,按2.4项下方法测定吸光度,计算回收率,结果见表1。
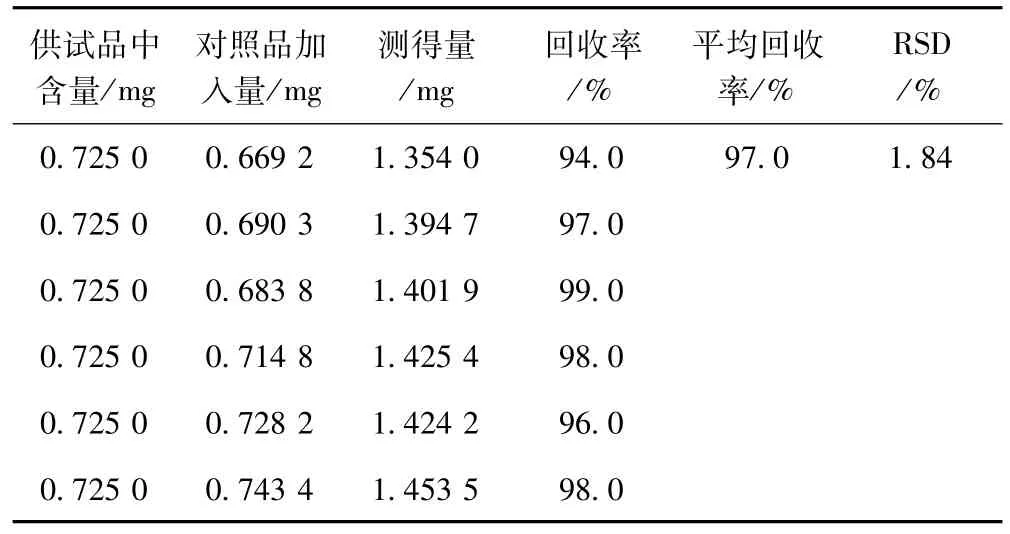
表1 芦丁对照品加样回收率
2.10 样品含量测定
取批号080707,081223,090511的消脂护肝片,分别按2.2项下方法制备成供试品溶液,各精密量取1 mL按2.4项下方法测定吸光度,代入回归方程计算消脂护肝片中总黄酮含量,结果见表2。

表2 样品中总黄酮含量测定
根据以上结果,确定该制剂中总黄酮含量应不低于35 mg·g-1。
3 讨论
目前,文献报道总黄酮的含量测定方法[1-9],主要有紫外分光光度法、HPLC、荧光光度法等。本试验采用分光光度法测定消脂护肝片中总黄酮的含量,简便易行、重现性好、结果可靠。本实验以芦丁为对照品,经波长扫描确定最大吸收波长510 nm为检测波长。
黄酮类化合物易溶于甲醇、乙醇等溶剂,甲醇毒性大,且浸透能力强,提取范围广,杂质较多,故采用乙醇做溶剂提取消脂护肝片中总黄酮。通过比较超声提取、回流提取,结果表明超声提取效率明显高于回流提取,且超声提取时间短,操作方便,而且不用加热,避免高温对黄酮结构的影响,故采用超声提取法。
在实验中,我们通过考察样品、芦丁对照品在400~800 nm波长范围的光谱图,结果样品与芦丁对照品的吸收光谱在510 nm为一平峰,故选择510 nm为测定波长。在实验中我们发现供试品溶液的显色受温度影响且随时间有变化,因此比色测定应平行操作,并按照规定时间进行。黄酮类化合物母核上多带有酚羟基,对光和空气中的氧很敏感,其溶液长时间久置后吸光度会下降,因此,待测液不宜久放,并避光低温保存。
[1]邵彩云.蒙药文冠木不同部位总黄酮的含量测定[J].中国民族医药杂志,2005,11(1):28-29.
[2]刘斌,石任兵,周素蓉.苦参汤有效部位总黄酮含量测定方法研究[J].中国实验方剂学杂志,2004,10(6):24-26.
[3]黄永林,赵志国,文永新.不同部位艾纳香中总黄酮的含量测定[J].广西植物,2006,26(4):453-455.
[4]黄永林,阮俊,文永新,等.不同部位紫玉盘总黄酮的含量测定[J].时珍国医国药,2006,17(10):1900-1901.
[5]宋永强,湛乐刚.分光光度法测定裸花紫珠片中总黄酮含量[J].海南医学,2005,16(6):152.
[6]谢鸣,彭镶心,刘超,等.紫外分光光度法侧定夏枯草微丸中总黄酮的含量[J].西南民族大学学报,2006,32(1):136.
[7]郭亚健,范丽,王晓强.关于NaNO2-Al(NO3)3-NaOH比色法测定总黄酮方法的探讨[J].药物分析杂志,2002,22(2):97-99.
[8]马陶陶,张群林,李俊,等.三氯化铝比色法测定中药总黄酮方法的探讨[J].时珍国医国药,2008,19(1):54-56.
[9]杨书良.HPLC测定双果胶囊中总黄酮的含量[J].中国中药杂志,2004,29(6):586.
Determination of Total Flavones in Xiaozhihugan Tablets
Chen Lei,Jiang Lin
(Traditional Chinese Medical Hospital of Xinjiang Uygur Autonomous Region,Urumqi Xinjiang830000,China)
Objective:To establish ultraviolet sepctrophotometry for the determination of total flavones in Xiaozhihugan tablets.Methods:Quercetin was selected as reference material,and the samples were determined at510 nm.Results:The linear range for quercetin was 0.008~0.08 mg·mL-1(r=0.999 7).The recovery rate was 97.0%,RSD=1.84%(n=6).Conclusion:This method is easy to handle with good accuracy and reproducibility,and is suitable for the quality control of Xiaozhihugan tablets.
Xiaozhihugan tablets;Total Flavones;Sepctrophotometry
*陈蕾,E-mail:leibaobao@sina.cn
2010-06-05)
