甲苯歧化与烷基转移催化剂的积碳行为
2010-10-14孔德金祁晓岚许中强
蒙 根 孔德金 祁晓岚 许中强
(中国石油化工股份有限公司上海石油化工研究院,上海 201208)
甲苯歧化与烷基转移催化剂的积碳行为
蒙 根 孔德金*祁晓岚 许中强
(中国石油化工股份有限公司上海石油化工研究院,上海 201208)
采用热重-差热分析(TG-DTA)、X射线光电子能谱(XPS)、傅里叶变换红外(FT-IR)光谱、低温氮吸附/脱附和氨程序升温脱附(NH3-TPD)等技术对甲苯歧化与烷基转移催化剂的积碳行为进行了研究.结果表明:硬积碳的烧碳动力学过程近似符合一级反应,表明它是以单层分散状态存在,其表观烧碳活化能为110 kJ·mol-1;反应1000 h后Cat-1000催化剂的近表面主要存在三种碳物种,其中以碳氧单键方式存在的C占C总量的22.7%,以碳氧双键方式存在的C占C总量的9.1%,以—C—C—方式存在的C占C总量的68.1%,表明形成的碳物种主要是石墨型碳;催化剂Cat-1000上的积碳主要是硬积碳,占总积碳量的3/4,其余为软积碳;尽管反应1000 h后催化剂的比表面积下降较多,但酸强度基本未改变,仍具有良好的反应活性和稳定性,表明覆盖在催化剂活性位上的积碳较少,积碳可能更易于沉积在载体的孔道中.
甲苯歧化; 烷基转移; 积碳; 催化剂; 热重-差热分析
Abstract:The nature of carbon deposition on a toluene disproportionation and transalkylation catalyst was characterized using thermogravimetry and differential thermal analysis(TG-DTA),X-ray photoelectron spectroscopy(XPS),Fourier transform infrared(FT-IR)spectroscopy,N2adsorption/desorption and NH3-temperature programmed desorption(NH3-TPD).Result showed that the kinetics of hard coke combustion approximately fitted a first order reaction with respect to the amount of coke and,therefore,most of the coke existed in a monolayer state and the corresponding apparent activation energy was about 110 kJ·mol-1.There were three kinds of carbon species on the surface of the Cat-1000 catalyst,which presented the catalyst after 1000 h reaction.The C atom fractions in the presence of C—O,C=O,and—C—C—were 22.7%,9.1%,68.1%,respectively.The formed carbon species on the Cat-1000 catalyst surface was mostly a graphite structure.The results showed that three quarters of the total carbon deposition on Cat-1000 was hard coke and the rest was soft coke.The specific surface area of the Cat-1000 catalyst decreased obviously compared with the catalyst without reaction(Cat-0).The Cat-1000 had almost unchanged acid intensity as well as high activity and stability.This shows that the cokes mainly deposit on the binder.
Key Words: Toluene disproportionation;Transalkylation;Carbon deposition;Catalyst;Thermogravimetry and differential thermal analysis
对二甲苯(PX)是重要的有机化工基础原料之一,其直接下游产品是对苯二甲酸(PTA)和对苯二甲酸二甲酯(DMT),PTA用来制造聚对苯二甲酸乙二醇酯(PET)和聚对苯二甲酸丁二醇酯(PBT)等聚酯产品.目前已工业化的PX生产技术主要有二甲苯吸附分离异构化工艺和甲苯选择性歧化结晶分离工艺[1].甲苯歧化和烷基转移单元是芳烃联合装置的重要组成部分,生产的混二甲苯经分离转化后获得的PX占芳烃联合装置PX总产量的一半以上.充分利用工业上廉价的甲苯(T)、碳九芳烃(C9A)和碳十芳烃(C10A),使其转化为混二甲苯(C8A)是提高芳烃联合装置经济效益的有效途径,其技术核心在于催化剂.目前,甲苯歧化和烷基转移催化剂都采用分子筛为活性组分,一般都采用丝光沸石[2-4].
分子筛催化剂以其高活性、高选择性和良好的热稳定性得到广泛应用[5],但在使用过程中活性总会下降.在工业催化反应中,尤其是涉及烃类的反应如催化裂化、加氢裂化、重整、异构化、烷基化等反应中,催化剂表面的积碳是一种不可避免的现象.随着积碳量的增加,催化剂的比表面积、孔容、表面酸度及活性中心数等皆会下降,积碳量达到一定程度必将导致催化剂的失活.沸石积碳失活机理通常有两种:堵孔机理和活性位覆盖机理[6].前者是积碳影响反应物分子的扩散,后者是减少了酸中心数量.失活机理一般受沸石结构、反应类型和反应条件的影响而不同[6-7].
目前,国内外对甲苯歧化与烷基转移催化剂的积碳行为研究甚少[8].Tsai等[9]通过动力学研究讨论了丝光沸石催化剂催化甲苯歧化反应时的失活机理,他们把结焦丝光沸石上的积碳按照TGA曲线不同温度区间分为“软积碳”(423-573 K)和“硬积碳”(573-1073 K),发现不同反应时间下的软积碳量基本保持不变,而硬积碳量随反应时间的延长而增加;积碳量为7.1%时,强Brönsted酸(B酸)中心减少,孔体积明显减少,当积碳量超过7.1%以后,孔体积不再减少,失活仅受外表面酸中心被覆盖影响.韩崇文等[10]采用积分反应器研究了甲苯非临氢歧化反应中ZSM-5沸石催化剂的积碳规律,发现提高反应温度及使用低硅铝比的沸石催化剂,均导致积碳及失活速率加快.
本文采用热重-差热分析(TG-DTA)、X射线光电子能谱(XPS)、傅里叶变换红外(FT-IR)光谱、低温氮吸附/脱附和氨程序升温脱附技术,考察了T-08甲苯歧化与烷基转移催化剂的积碳行为.
1 实验部分
1.1 反应性能测试
T-08催化剂由中石化催化剂上海分公司提供,原料T、C9A和C10A为上海石化股份有限公司的工业级产品,根据实验要求配制混合原料,原料组成(质量比)为 m(T)∶m(C9A)∶m(C10A)=50∶40∶10.催化剂的反应性能测试在等温固定床反应器中进行,催化剂装填量40 g,在温度653 K,空速2.5 h-1,氢烃摩尔比3.0,压力3.0 MPa条件下反应1000 h.原料和液相产物组成均使用Agilent 7890气相色谱仪分析,其色谱柱为PEG20M毛细管柱(50 m×0.32 mm),新鲜T-08催化剂和反应1000 h后的T-08催化剂分别记为Cat-0和Cat-1000.转化率(C)和选择性(S)计算如下:
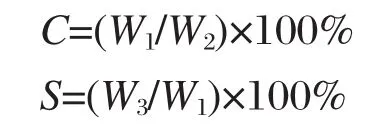
其中W1为已反应的T、C9A与C10A质量,W2为进反应器的T、C9A与C10A质量,W3为生成的苯与C8A的质量.
1.2 催化剂表征
催化剂的热重-差热分析在美国TA公司SDTQ600综合热分析仪上进行,在空气气氛下由室温升至1073 K,升温速率为10 K·min-1.
X射线光电子能谱数据是在英国生产的Kratos Axis Ultra DLD型多功能电子能谱仪上测定,其中X 射线源是 Al Kα(hν=1486.7 eV),功率 45 W,工作电压15 kV,发射电流3.0 mA.
傅里叶变换红外光谱测试采用美国DIGILAB公司FTS-25PC傅里叶红外光谱仪,扫描范围400-4000 cm-1,分辨率为4.0 cm-1,100次扫描累加,KBr压片制样.
NH3-TPD测定在天津市鹏翔科技有限公司的PX 200A型TPD/TPR装置上完成,样品首先在823 K活化1 h,然后在408 K下饱和吸附NH3,再在408 K恒温吹扫至基线走平后开始NH3脱附,以15 K·min-1的升温速率升到873 K,载气流量为30 mL·min-1,热导检测.
比表面、孔体积和孔分布采用低温氮吸附分析,在美国Micromeritics公司ASAP 2020型表面分析仪上测定,操作温度为77 K,测定前试样在573 K活化6 h.根据Brunauer-Emmett-Teller(BET)模型计算比表面积和孔体积.
2 结果与讨论
2.1 催化剂的反应性能
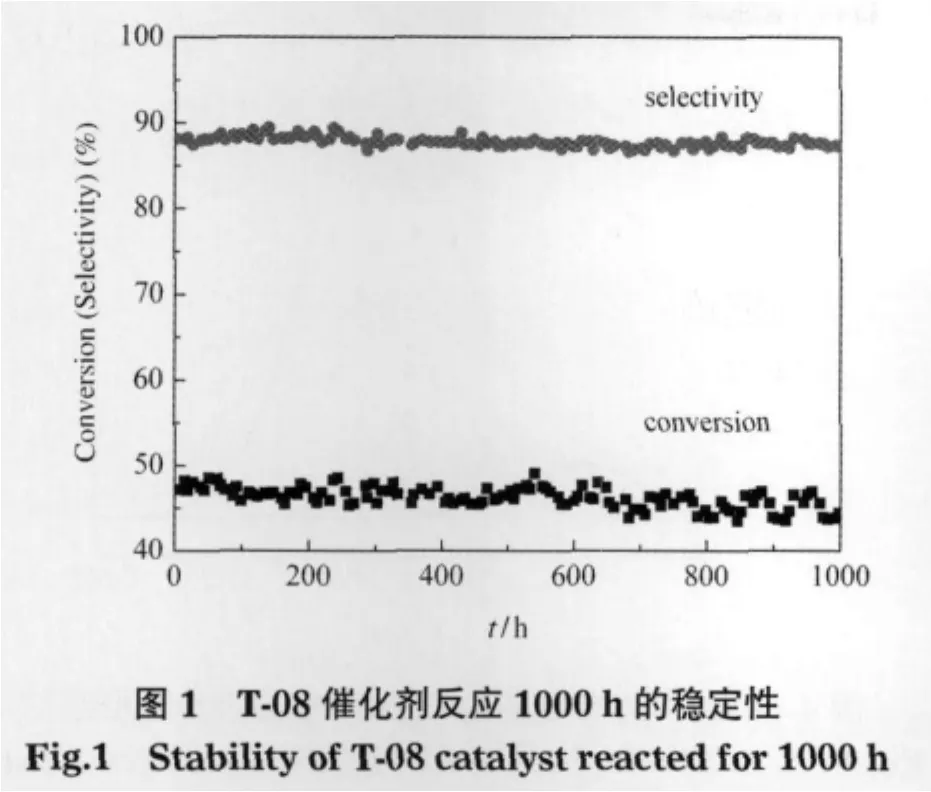
T-08催化剂1000 h稳定性实验结果见图1.由图1可见,T-08催化剂具有良好的稳定性,选择性基本保持不变.
反应初期(0-50 h),平均转化率为47.6%;反应后期(940-1000 h),平均转化率为45.5%.反应1000 h后,催化剂的反应活性(即转化率)仅下降约2%,表明催化剂具有良好的反应活性.
2.2 积碳物种的分析
Cat-0和Cat-1000催化剂的TG-DTG分析结果见图2.由图2(a)可见,Cat-0催化剂在473 K前有一段明显的失重,此阶段的失重率达12.19%,最大失重速率温度在349 K处,这部分失重应由分子筛催化剂脱吸附水所造成,573 K后曲线基本趋于水平.从图2(b)可看出,Cat-1000催化剂的TG曲线上有三个失重阶段:423 K前为第一失重阶段,失重率达8.38%,表明在催化剂表面有低沸点物质吸附,可能是水或其它杂质;423-573 K为第二失重阶段,失重率达2.75%,通常认为这部分失重是“软积碳”所致;573-973 K为第三失重阶段,失重率达8.06%,最大失重速率温度在780 K处,表明积碳主要集中在此范围内,此积碳属于“硬积碳”,占总积碳量的四分之三,主要为芳香族化合物.
Cat-0和Cat-1000催化剂的差热分析结果见图3.由图3(a)可见,Cat-0催化剂仅在约350 K处有一吸热峰,是催化剂表面的脱水峰.从图3(b)可看出,Cat-1000催化剂除了在约336 K有一吸热脱水峰外,在553和763 K左右还有两个放热峰,并对应于TG曲线中的失重部分,表明催化剂上有两种不同类型的积碳[11-12],其中,高温烧碳放热峰较宽且对称性较差,说明高温烧除的积碳中可能存在的物质种类较多[11].Rossetti等[13]也认为催化剂表面的积碳有两种类型:一种是轻质碳,在453-493 K可燃烧除掉;另一种是类石墨的碳,这类积碳在873-973 K的高温才能燃烧除掉.
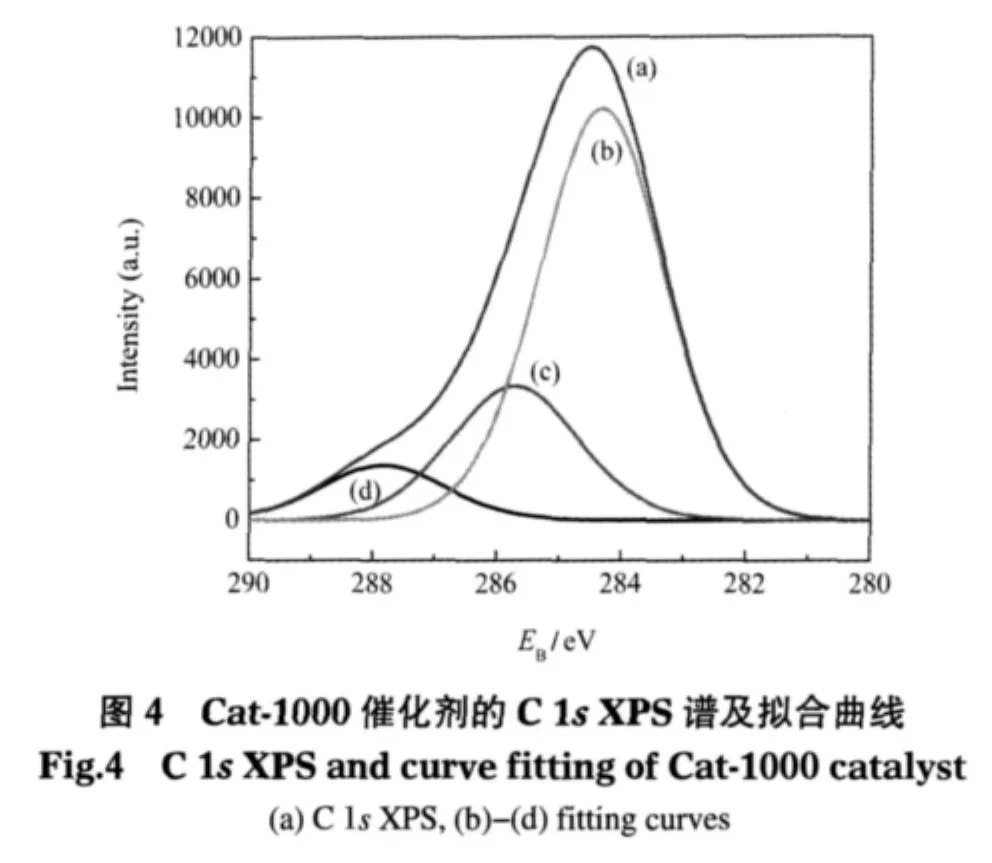
为了进一步了解催化剂表面的积碳状况,采用XPS对Cat-1000催化剂样品的表面积碳物种进行了研究.图4为Cat-1000催化剂的XPS谱,通过对谱图拟合,发现Cat-1000催化剂的近表面主要存在三种碳物种,其结合能分别为284.3、285.8和287.9 eV.根据文献报道[14],结合能为(284.6±0.3)eV的峰相应于趋于石墨化或已经石墨化的—C—C—键,在(286.2±0.3)eV的峰对应于碳氧单键,大于287 eV的峰对应的是卫星边峰和碳氧双键.各拟合峰面积和碳元素的相对质量分数列于表1.由表1可看出,Cat-1000催化剂表面以—C—C—方式存在的C占C总量的68.1%,以碳氧单键方式存在的C占C总量的22.7%,以碳氧双键方式存在的C占C总量的9.1%,表明形成的碳物种主要是石墨型碳,还有约三分之一是以碳氧化物形式存在[14-16].由文献[14-15,17]可知,积碳催化剂表面上的碳物种一般都含有石墨型积碳,石墨碳含量较高容易导致催化剂失活,减少表面非活性的石墨化碳的生成对于增加催化剂的稳定性有十分重要的意义.
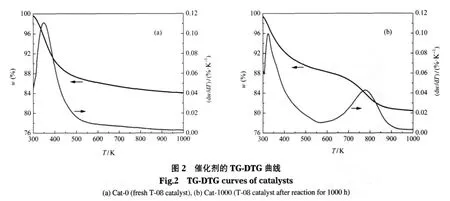
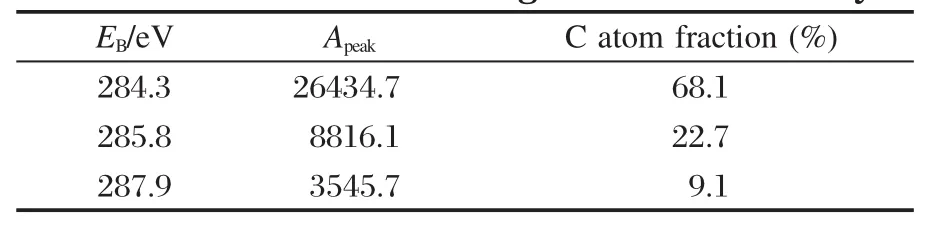
表1 Cat-1000催化剂的C 1s的拟合结果Table 1 Result of C 1s fitting for Cat-1000 catalyst
2.3 烧碳活化能的分析
Querini等[18]认为化学反应速率与载体的比表面积成正比,当积碳在载体上呈单层分散时,该过程是简单一级反应.卓润生等[19]认为,反应温度大于723 K时,HZSM-5分子筛上所形成积碳的烧碳过程为一级反应.研究表明乙苯歧化过程中不同分子筛的积碳模式相似[20],对于T-08积碳催化剂,如果烧碳过程是非扩散控制的简单级数的反应过程,则烧碳过程可看作[21]:

即催化剂表面的积碳在高温下同O2反应生成COx(x=1,2)的过程.其烧碳动力学方程为
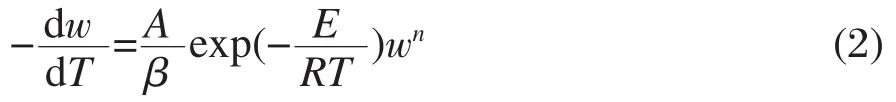

其中w为温度T时未烧掉积碳量的质量分数,β为升温速率(K·min-1),A为频率因子(min-1),n为反应级数,R为气体常数(J·mol-1·K-1),E为表观烧碳活化能(kJ·mol-1).
根据烧碳反应的动力学公式,当反应为一级反应时[21-22]:
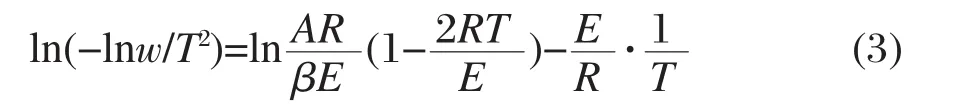
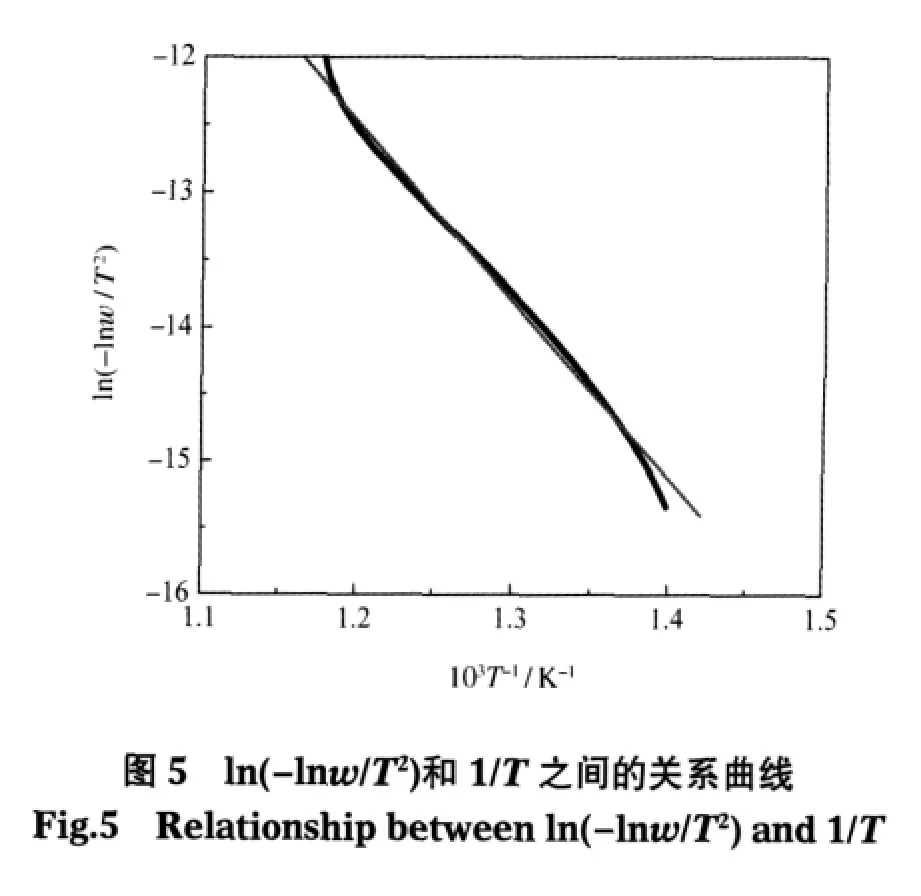
如果催化剂上的积碳呈单层分散,烧碳过程可按一级反应处理[21].通过对Cat-1000催化剂的烧碳曲线进行处理,发现在高温阶段(715-849 K)的烧碳曲线近似为直线,因而可认为该烧碳过程是一级反应.以ln(-lnw/T2)对1/T在715-849 K之间作图,得到如图5所示的直线.所得直线的斜率为-E/R,由直线的斜率计算出表观烧碳活化能E≈110.3 kJ·mol-1.这表明尽管硬积碳在Cat-1000催化剂中占约为8%,大多数硬积碳可能不会形成大的颗粒,而是以单层分散状态存在[22].
2.4 积碳对催化剂结构的影响
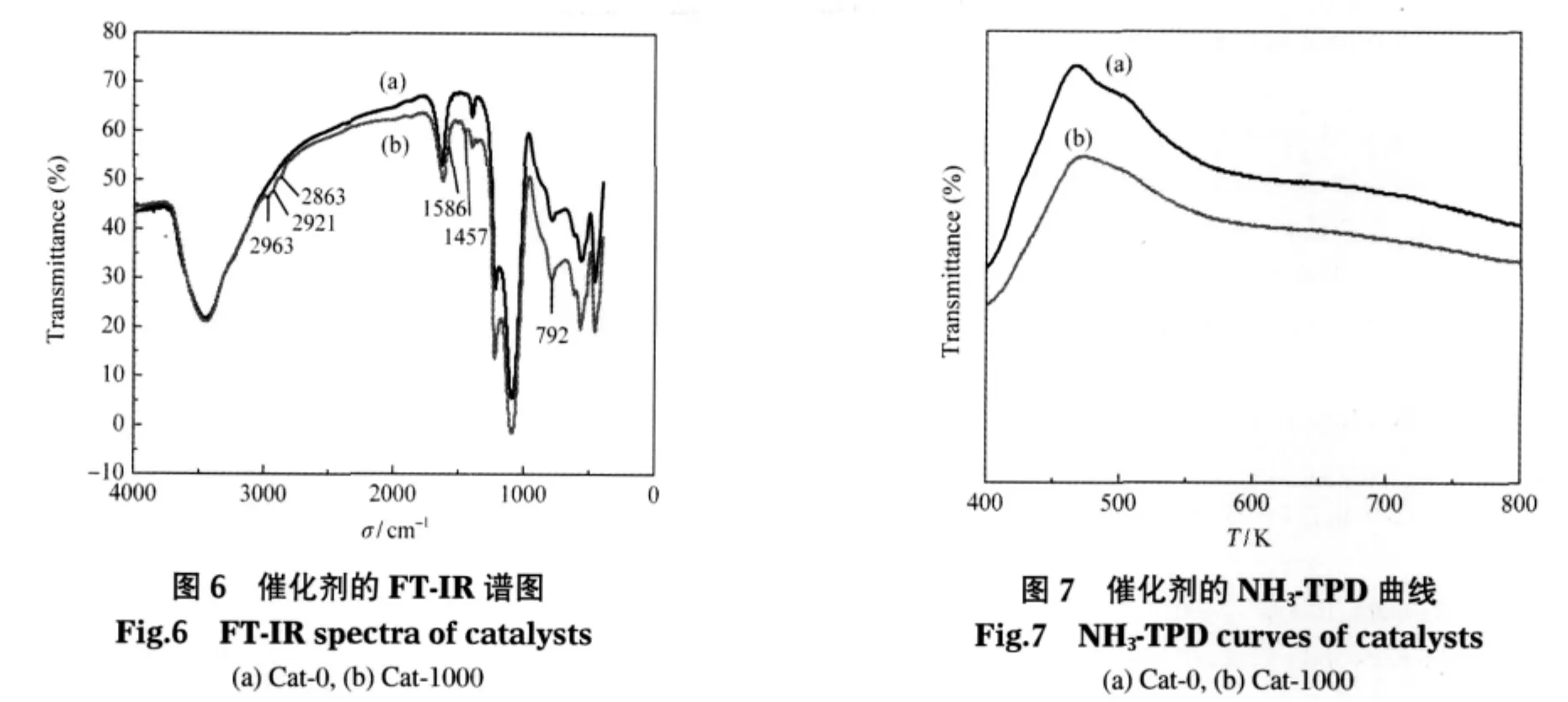
Cat-0和Cat-1000催化剂的FT-IR光谱如图6所示.与Cat-0相比,Cat-1000催化剂在792 cm-1处的吸收峰强度略有增强,该峰可归属于Si(Al)—O—Si(Al)面外对称伸缩振动,强度增加表明反应前后分子筛骨架硅铝摩尔比略有增大,反应过程中发生轻微骨架脱铝[23].
Cat-1000催化剂在2963,2921,2863,1586,1457 cm-1处均出现了新的吸收峰.在1457和1586 cm-1处出现的吸收峰为芳香族化合物的伸缩振动峰[24-26],在2963,2921,2863 cm-1处出现的吸收峰为甲基和亚甲基的伸缩振动峰[27-28],表明积碳物种主要是芳香族化合物,这与热重的表征结果一致.
Cat-0和Cat-1000催化剂的比表面积和孔体积的测定结果见表2.从表2可看出,反应1000 h后,催化剂的比表面积由 379 m2·g-1降到 275 m2·g-1,降幅为27.4%,其中,微孔比表面积由221 m2·g-1降到150 m2·g-1,降幅为 32.1%,介孔比表面积由 158 m2·g-1降到125 m2·g-1,降幅为20.9%,孔体积和微孔体积下降的幅度基本相同.而催化剂的活性仅下降约2%,这表明覆盖在催化剂活性位上的积碳不多,催化剂微孔的积碳程度大于介孔.尽管微孔体积和比表面积均下降,但催化剂活性未受太大影响,微孔中的积碳可能更易于沉积在载体的孔道中[29].
图7为Cat-0和Cat-1000催化剂的NH3-TPD谱图.由图7可见,与Cat-0相比,Cat-1000催化剂的酸量略有下降,但酸强度基本没有变化,表明反应过程中酸中心上的积碳不多.

表2 催化剂的比表面积和孔体积Table 2 Specific surface area and pore volume of catalysts
3 结 论
(1)Cat-1000催化剂的积碳主要是硬积碳,积碳物种主要为芳香族化合物,硬积碳的烧碳动力学过程近似符合一级反应,表明其是以单层分散状态存在,其表观烧碳活化能约为110 kJ·mol-1.
(2)XPS研究表明,Cat-1000催化剂的近表面主要存在三种碳物种,其中以碳氧单键方式存在的C占C总量的22.7%,以碳氧双键方式存在的C占C总量的9.1%,以—C—C—方式存在的C占C总量的68.1%,表明形成的碳物种主要是石墨型碳.
(3)尽管反应1000 h后催化剂的比表面积下降较多,但酸强度基本未改变,仍具有良好的反应活性和稳定性,表明覆盖在催化剂活性位上的积碳较少,积碳可能更易于沉积在载体的孔道中.
1 Chen,Q.L.;Kong,D.J.;Yang,W.S.Petrochemical Technology,2004,33(10):909 [陈庆龄,孔德金,杨卫胜.石油化工,2004,33(10):909]
2 Cheng,W.C.;Kong,D.J.;Yang,D.Q.;Fu,P.A.;Chen,F.C.;Wang,L.PetrochemicalTechnology,1999,28(2):107 [程文才,孔德金,杨德琴,符盼安,陈凤池,王 磊.石油化工,1999,28(2):107]
3 Bao,Y.Z.;Yang,D.Q.;Qi,X.L.;Kong,D.J.Chemical Reaction Engineering and Technology,2007,23(1):79 [鲍永忠,杨德琴,祁晓岚,孔德金.化学反应工程与工艺,2007,23(1):79]
4 Li,B.J.;Leng,J.C.;Wei,J.S.;Shi,B.Q.;Guo,H.L.;Kong,D.J.Chemical Reaction Engineering and Technology,2006,22(3):271[李保军,冷家厂,魏劲松,时宝崎,郭宏利,孔德金.化学反应工程与工艺,2006,22(3):271]
5 Stöcker,M.Microporous Mesoporous Mater.,2005,82(1-3):257
6 Bhatia,S.;Beltramini,J.;Do,D.D.Cat.Rev.-Sci.Eng.,1989,31(4):431
7 Niu,F.H.;Hofmann,H.Appl.Catal.A,1995,128:107
8 Xie,Z.K.Synthesis of β zeolite and toluene disproportionation and C9aromatics transalkylation reation[D].Shanghai:East China University of Science and Technology,2009 [谢在库.β 沸石合成和甲苯歧化与C9芳烃烷基转移反应过程研究[D].上海:华东理工大学,2009]
9 Tsai,T.C.;Chen,W.H.;Lai,C.S.;Liu,S.B.;Wang,I.;Ku,C.S.Catal.Today,2004,97:297
10 Han,C.W.;Han,S.H.;Wang,W.T.Petrochemical Technology,2004,33(1):9 [韩崇文,韩书红,王文婷.石油化工,2004,33(1):9]
11 Huang,X.H.;Zhang,G.L.;Shang,Y.C.;Yang,X.C.;Zhang,W.X.;Wu,T.H.Petrochemical Technology,2006,35(4):314 [黄小鸿,张光林,商永臣,杨笑春,张文祥,吴通好.石油化工,2006,35(4):314]
12 Li,X.M.;Zhang,W.X.;Zhu,X.M.;Shan,H.Y.;Zhou,X.Q.;Jiang,D.Z.;Wu,T.H.;Tang,A.Q.Chinese Journal of Catalysis,2003,24(5):364 [李雪梅,张文祥,朱小梅,善洪岩,周秀清,蒋大振,吴通好,唐敖庆.催化学报,2003,24(5):364]
13 Rossetti,I.;Bencini,E.;Trentini,L.;Forni,L.Appl.Catal.A,2005,292:118
14 Yao,S.L.;Yang,C.H.;Tan,Y.S.;Han,Y.Z.Journal of Fuel Chemistry and Technology,2006,34(6):706 [姚素玲,杨彩虹,谭猗生,韩怡卓.燃料化学学报,2006,34(6):706]
15 Wang,H.X.;Tan,D.L.;Xu,Y.D.;Bao,X.H.Chinese Journal of Catalysis,2004,25(6):445 [王红霞,谭大力,徐奕德,包信和.催化学报,2004,25(6):445]
16 Pinheiro,A.N.;Valentini,A.;Sasaki,J.M.;Oliveira,A.C.Appl.Catal.A,2009,355:156
17 Li,C.L.;Fu,Y.L.Acta Phys.-Chim.Sin.,2004,20(special issue):906 [李春林,伏义路.物理化学学报,2004,20(专刊):906]
18 Querini,C.A.;Fung,S.C.Catal.Today,1997,37:277
19 Zhuo,R.S.;Tan,C.Y.;Cheng,C.R.Petrochemical Technology,1992,21(12):815 [卓润生,谭长瑜,程昌瑞.石油化工,1992,21(12):815]
20 Zhu,Z.R.;Ruan,T.;Chen,Q.L.;Chen,W.C.;Kong,D.J.Zeolites and mesoporous materials at the dawn of the 21st century.Amsterdam:Elsevier,2001:271
21 Tian,B.L.;Shu,Y.Y.;Liu,H.M.;Wang,L.S.;Xu,Y.D.Chinese Journal of Catalysis,2000,21(3):255 [田丙伦,舒玉瑛,刘红梅,王林胜,徐奕德.催化学报,2000,21(3):255]
22 Liu,H.M.;Su,L.L.;Wang,H.X.;Shen,W.J.;Bao,X.H.;Xu,Y.D.Appl.Catal.A,2002,236:263
23 Qi,X.L.;Wang,Z.;Li,S.J.;Li,B.;Liu,X.Y.;Lin,B.X.Acta Phys.-Chim.Sin.2006,22(2):198 [祁晓岚,王 战,李士杰,李 斌,刘希尧,林炳雄.物理化学学报,2006,22(2):198]
24 Zhou,L.W.;Wang,F.;Luo,M.;Xiao,W.D.;Cheng,X.W.;Long,Y.C.Petrochemical Technology,2008,37(4):333 [周丽雯,王 飞,罗 漫,肖文德,程晓维,龙英才.石油化工,2008,37(4):333]
25 de Lucas,A.;Canizares,P.;Duran,A.;Carrero,A.Appl.Catal.A,1997,156:299
26 Ibarra,J.V.;Royo,C.;Monzon,A.;Santamaría,J.Vib.Spectrosc.,1995,9(2):191
27 Trombetta,M.;Busca,G.;Rossini,S.A.;Piccoli,V.;Cornaro,U.J.Catal.,1997,168(2):334
28 Bian,J.J.;Liu,J.;Liu,Y.H.;Wang,X.S.;Liu,X.M.;Bao,X.H.Chinese Journal of Catalysis,2001,22(5):415 [卞俊杰,刘 靖,刘毅慧,王祥生,刘秀梅,包信和.催化学报,2001,22(5):415]
29 Pradhan,A.R.;Wu,J.F.;Jong,S.J.;Chen,W.H.;Tsai,T.C.;Liu,S.B.Appl.Catal.A,1997,159:187
Carbon Deposition on a Toluene Disproportionation and Transalkylation Catalyst
MENG Gen KONG De-Jin*QI Xiao-Lan XU Zhong-Qiang
(Shanghai Research Institute of Petrochemical Technology,SINOPEC,Shanghai 201208,P.R.China)
O643.36
Received:April 22,2010;Revised:July 7,2010;Published on Web:September 24,2010.
*Corresponding author.Email:kongdj.sshy@sinopec.com;Tel:+86-21-68462542;Fax:+86-21-68462283.
The project was supported by the Scientific and Technological Project of Shanghai Science and Technology Commission,China(08521101900).
上海市科委科技攻关项目(08521101900)资助
