LiNi0.5Mn0.5O2制备及表征
2010-09-20郎丰饶赵立竹
郎丰饶,赵立竹
(1.吉林农业科技学院机械建筑学院,吉林吉林132011; 2.东北师范大学物理学院,吉林长春130024)
LiNi0.5Mn0.5O2制备及表征
郎丰饶1,赵立竹2
(1.吉林农业科技学院机械建筑学院,吉林吉林132011; 2.东北师范大学物理学院,吉林长春130024)
采用共沉淀法制备了LiNi0.5Mn0.5O2.XRD,Raman测试都表明材料是六方结构.XPS检测得出镍主要以正二价存在,锰元素主要以正四价存在.合成的LiNi0.5Mn0.5O2得到了50次的循环,但比容量较低.充放电循环性能比较研究表明,经过40次循环后,0.3,0.6,1.5 C的放电比容量分别是65.88,61.56,52.23 mA·h·g-1.
锂离子电池;正极;层状LiNi0.5Mn0.5O2;共沉淀法
1 引 言
金属锂的相对原子质量为6.94,在已知金属中是最小的,标准电极电压为-3.045 V[1].锂离子电池是一种新型能源,它以无污染、可以降低碳排放量等优势,开始作为一些传统能源的替代品,如汽车等行业已经使用锂离子电池取代传统的能源.但容量小,输出电压低,循环寿命短已经制约了锂离子电池的发展.LiCoO2作为正极材料使用有着成本高和污染大的缺点,LiNiO2合成困难,LiNi0.5Mn0.5O2兼具锰氧化物和镍氧化物的优点,成为锂离子电池发展的新方向.开发廉价、高性能、安全性锂离子电池成为锂离子电池工业发展的中心[2].层状锰系锂离子电池正极材料正符合此背景需要.
LiNi0.5Mn0.5O2的制备方法有许多种,其中比较普遍的是共沉淀法、sol-gel法等.Ohzuku等[3]在400℃下让Ni(OH)2和Mn(OH)2脱水形成镍锰氧化物混合物,然后加入锂盐高温下合成了LiNi0.5Mn0.5O2正极材料,在2.5~4.5 V进行充放电测试,可逆比容量为200 mA·h·g-1,循环性能良好,30次循环后没有衰减.S.Gopukumar等[4]用sol-gel法合成了LiNi0.5Mn0.5O2材料,2.5~4.5 V进行充放电测试,可逆比容量为125 mA·h·g-1.本文选取Ni(NO3)2· 6H2O和Mn(Ac)2·4H2O为原料,用共沉淀方法制备了LiNi0.5Mn0.5O2,并对其表征和测试.
2 实 验
2.1 共沉淀法制备LiNi0.5Mn0.5O2
Ni(NO3)2·6H2O与Mn(CH3COO)2· 4H2O按物质的量之比为1∶1配成溶液,将溶液缓慢滴入LiOH溶液中,并保持p H值为11.为了加速氧化,向溶液中滴入H2O2,要控制速度,然后进行超声,待溶液完全静止后,上下分离,反复多次清洗,除去剩余的LiOH,此时应保持p H值为7.进行离心分离后,100℃真空干燥10 h,加入LiOH固体并以n(Li)∶n(Ni)∶n(Mn)= 1.05∶0.5∶0.5混合,研磨2~3 h后.900℃煅烧12 h.
2.2 钮扣电池的组装
正极:将准备好的LiNi0.5Mn0.5O2、乙炔黑、聚偏氟乙烯三者按质量比为75∶15∶10混合,研磨4 h后,加入一定量的N-甲基吡咯烷酮(NMP),再研磨2 h.用酒精棉反复清洁表面,除去氧化物,再将其均匀涂在铝箔上,将其置于电烤灯下,烘干6 h,然后放入烘干箱中烘干8 h,取出后碾压成片,用手术刀片切成0.5 cm×0.5 cm的正方形片.
负极:在氩气手套箱内,用刮刀除去锂片表面的氧化物,用圆冲切成直径为15 mm的圆片作为负极材料.
隔膜:隔膜使用聚丙烯2400隔膜,厚度为0.02 mm.切成直径20 mm的圆片.
电解液:电解液为含1 mol/L LiPF6的EC (碳酸乙烯酯)和DMC(碳酸二甲酯)(体积比是1∶1)的混合液.
在氩气手套箱完成后,将电池放入LANDdt的测试柜,静置放电之后,再充电测量.
3 结果与讨论
3.1 样品的XRD分析
图1为900℃煅烧12 h的3个样品的XRD谱图.可以看出,合成的材料都生成了a-NaFeO2型结构,属于R-3m空间群.
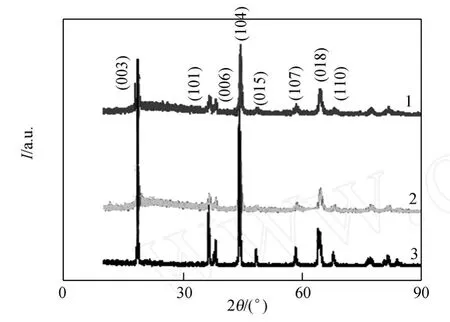
图1 LiNi0.5Mn0.5O2的XRD谱图
煅烧温度一定程度上决定着正极材料的晶型生成,煅烧温度较高时有利于晶体结构生成,结晶性好,有序化程度高,层状结构优良,致密性强.伴随温度升高,粉体结构发育趋于完善,有序化程度提高.但是温度太高,团聚现象严重,对材料的电化学性能影响比较大,影响电池的使用寿命.温度过高超900℃时,(003)峰会出现杂相,峰变得平缓,这主要是因为在合成过程中温度升高,锂盐挥发,改变了元素配比,晶体的结构就发生了变化,Ni2+很容易进入Li层,最终导致材料层状结构发生变化.
用最小二乘法计算晶格参量如表1所示.
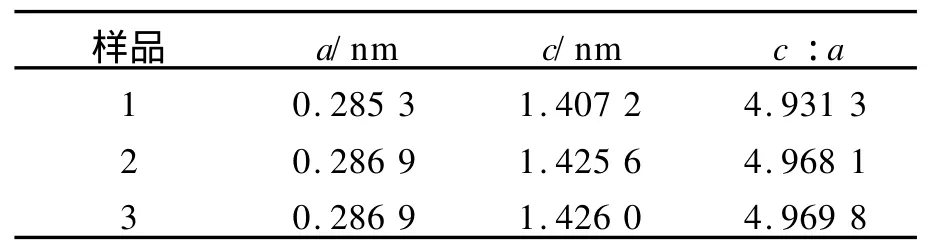
表1 LiNi0.5Mn0.5O2样品的晶格参量
晶格参量值与Ohzuku和Makimura[5]及Lu[6]等报道的很相近.c/a比值也是对晶格形成程度优良的一个很有用的描述,以4.93为标准,如果c/a的值高于4.93,则认为晶型结构优良,层状结构生成良好.
3.2 拉曼光谱研究
测试条件:采用J Y HR800微区拉曼测试仪,使用氩离子激光器,波长488 nm.
图2为LiNi0.5Mn0.5O2的拉曼光谱图.

图2 LiNi0.5Mn0.5O2的拉曼光谱图
图2中LiNi0.5Mn0.5O2样品有2个散射峰,它们分别来自A1g和Eg振动模式的贡献.A1g振动模式主要与锰氧键和镍氧键的伸缩振动有联系,Eg振动模式由O—Ni—O和O—Mn—O弯曲振动引起,A1g振动表现为比Eg振动更强.拉曼光谱证明了材料生成的是R-3m空间群.
3.3 扫描电子显微镜(SEM)形貌
样品的SEM图像如图3所示,颗粒大小相同,分布较为均匀;颗粒呈球型,应用Scherer公式计算得粒径尺寸为200 nm,表面光滑,部分粒子聚集紧密,大小适中.
Croguennec等[7]对o-LiMnO2研究后发现,当正交结构的LiMnO2作为正极材料使用时,晶粒尺寸与电化学性能是有密切关系的,只有当晶粒尺寸φ<1μm时,o-LiMnO2作为正极材料使用,才最有利于其电化学性能的发挥.例如, Wu[8]等使用水热法合成的材料,平均晶粒尺寸达到35 nm的o-LiMnO2,最高比容量达232 mA· h·g-1,并且循环性能也非常优良.以上研究都证明了合成纳米级的材料可能会提高材料的电化学性能.
图3 LiNi0.5Mn0.5O2的SEM图
3.4 X射线光电子能谱(XPS)分析
对LiNi0.5Mn0.5O2材料合成样品做XPS测试,如图4所示.XPS测得了各元素的结合能, Mn2p3/2的结合能为642.2 eV,表现为Mn4+,Mn3p的结合能为49.8 eV,这2个锰元素的结合能充分地证明在材料中以Mn4+存在.Ni2p3/2结合能为8 54.4eV,表现为Ni2+.O1s的结合能分别是529.7 eV和531.2 eV,其中O1s在529.7 eV对应的是Mn—O键能,O1s在531.2eV处对应的是Ni—O,Li—O键能,这样就可以肯定样品中的Ni,Mn元素主要以Ni2+和Mn4+存在.其中Li1s结合能为54.7 eV.从上述分析中可以看到,镍元素主要是以正二价形式存在,锰元素主要是以正四价存在,没有表现出正三价的锰,这是很理想的结果,因为三价锰有高自旋态,结构很不稳定,正四价的锰材料的结构更加稳定.
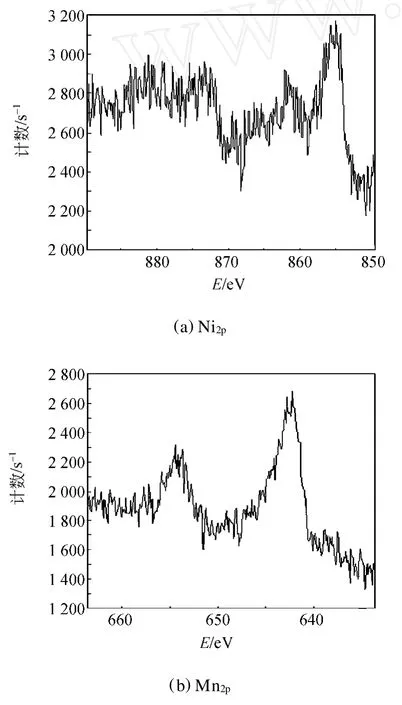
图4 LiNi0.5Mn0.5O2的XPS谱
3.5 电化学性能
图5为锂电池分别在在0.3,0.6,1.5 C放电倍率下的电压-比容量曲线图.图中显示,0.3 C放电倍率最小,可是具有最大的放电比容量,伴随着放电倍率的增大,放电比容量却在下降;1.5 C放电倍率最大,放电比容量锐减,放电电压也在下降,但程度不大,且也很缓慢.在40次循环时,放电比容量分别是65.88,61.56,52.23 mA·h· g-1,对比于首个循环0.3,0.6,1.5 C放电倍率下的放电比容量分别为90.38,88.23,82.46 mA· h·g-1,放电比容量下降,通过比较发现,0.3 C放电倍率下的放电比容量较0.6 C和1.5 C放电倍率下的比容量下降少,所以,材料更适合0.3 C放电倍率,也就是说,在0.3 C放电倍率下能将材料的特性发挥出来,大于0.3 C放电倍率不适合该材料,反而使特性材料的放电倍率特性变差.

图5 不同放电倍率第40个循环下放电压-比容量曲线图
高放电倍率下,放电倍率特性变弱,放电比容量锐减,放电电压略微下降,其原因应该符合A. K.Padhi[9]对LiFePO4容量损失研究得出的结果.LiNi0.5Mn0.5O2材料的电导率低,无法经受电流密度较大的冲放电偱环.一旦使用了高密度电流循环,会使其放电倍率特性出现衰减,对于LiNi0.5Mn0.5O2来说,假设材料正处于放电状态,那么在此过程中,锂离子在不断地嵌入正极材料过程中,材料也经历着由外向内发生的转变,由LiNi0.5Mn0.5O2——LixNi0.5Mn0.5O2/Li1-xNi0.5Mn0.5O2,材料的2种状态的边界也由外向里推进,使得能够容纳离子嵌入面积也在缩小,在选取的单位面积上,锂离子嵌入速度大小是不变的.在这一过程中,当可容纳锂离子进行嵌入的总面积缩小到无法承受锂离子进行嵌入时,也就是放电停止时,此时的剩余能够容纳锂离子嵌入的面积称之为临界面积.当放电电流增大时,锂离子能够嵌入的数量就减小了,因为临界面积也随放电电流的增大而增大了,由于锂离子嵌入数量少了,放电容量自然也就下降了,可以根据这种特性,探索出材料的最佳放电倍率.
在放电过程中,因为2种状态的边界向内部推进时,脱出锂离子的界面面积在不断地增大,它给予锂离子的脱出的阻碍作用也就愈加明显,为了保证放电电流不变,只有增大电压,从而导致了放电电压略微降低,可见,放电电压降低,与放电容量降低都是与材料可以脱嵌锂离子面积的改变有关.
4 结 论
用共沉淀法合成正极材料LiNi0.5Mn0.5O2,同时对材料进行了表征和测试.锂盐在配比时稍微过量,配比为n(Li)∶n(Ni)∶n(Mn)=1.05∶0.5∶0.5较为合适.通过共沉淀法所得的正极材料,晶型结构完整,结晶性好,镍主要以正二价存在,锰主要以正四价存在,LiNi0.5Mn0.5O2结构稳定.合成的LiNi0.5Mn0.5O2得到了50次的循环,但比容量有待提高.充放电循环性能比较研究表明,经过40次循环后,0.3,0.6,1.5 C的比容量分别是65.88,61.56,52.23 mA·h·g-1.
[1] 陈军,陶占良.能源化学[M].北京:化学工业出版社,2004:239.
[2] 王双才,李元坤,刘述平.锂离子电池正极材料研究动态[J].中国锰业,2004,22(3):31-34.
[3] Ohzuku T,Makimura Y.Lithium insertion material of LiNi0.5Mn0.5O2for advanced lithium-ion batteries [J].J.Power Sources,2003,119-121:156-160.
[4] Gopukumar S,Chung K Y,Kim K B.Novel synthesis of layered LiNi0.5Mn0.5O2as cathode material for lithium rechargeable cells[J].Electrochimica Acta,2004,49(5):803-810.
[5] Ohzuku T,Makimura Y.Layered lithium insertion material of LiNi1/2Mn1/2O2:a possible alternative to LiCoO2for advanced lithium-ion batteries[J]. Chem.Lett.,2001,(8):744-745.
[6] Lu Z,Beaulieu L Y,Donaberger R A,et al.Synthesis structure,and electrochemical behavior of Li [NixLi1/3-2x/3Mn2/3-x/3]O2[J].J.Electrochem. Soc.,2002,149:A778-A791.
[7] Croguennec L,Deniard P,Brec R,et al.Electrochemical behavior of orthorhombic LiMnO2:influence of the grain size and cationic disorder[J].Solid State Ionics,1996,89:127-137.
[8] Wu Mengqiang,Chen Ai,Xu Rongqing,et al.Low temperature hydrothermally synthesized nanocrystalline orthorhombic LiMnO2cathode material for lithium-ion cells[J].Microelectronic Engineering, 2003,66:180-185.
[9] Padhi A K,Naanjundaswamy K S,Masquelier C, et al.Effect of structure on the Fe3+/Fe2+redox couple in iron phosphates[J].J.Electrochemical Soc.,1997,144(5):1 609-1 613.
Preparation and characterization of LiNi0.5Mn0.5O2
LANG Feng-rao1,ZHAO Li-zhu2
(1.Institute of Machinery Architecture,Jilin Agricultural Science and Technology College,Jilin 132101,China; 2.School of Physics,Northeast Normal University,Changchun 130024,China)
LiNi0.5Mn0.5O2samples are prepared by co-precipitation method.XRD and Raman tests show that the LiNi0.5Mn0.5O2samples have hexagonal structure.XPS test shows that manganese and nickel are mainly divalent and quadrivalence.The LiNi0.5Mn0.5O2synthesized can be charged up to 50 times,but the capacity is low.The charge-discharge cycle performance study shows that after 40 cycles,the 0.3 C,0.6 C and 1.5 C discharge capacities are 65.88 mA·h·g-1,61.56 mA·h·g-1and 52.23 mAh·g-1.
Li-ion battery;cathode;LiNi0.5Mn0.5O2;co-precipitation method
TM911
A
1005-4642(2010)09-0011-04
[责任编辑:任德香]
2010-06-07;修改日期:2010-07-27
郎丰饶(1982-),男,吉林省吉林市人,吉林农业科技学院机械建筑学院助教,硕士,研究方向为功能材料.
赵立竹(1962-),女,吉林省吉林市人,东北师范大学物理学院副教授,博士,研究方向为功能材料.
