喷雾干燥-碳热还原法制备的Sn2Sb/C复合材料
2010-09-18闫润宝任建国赵海雷何向明
闫润宝,任建国,赵海雷,何向明
(1.北京科技大学材料科学与工程学院,北京 100083; 2.清华大学核能与新能源技术研究院,北京 100084)
目前,石墨类负极材料已经得到商业化应用,但理论比容量仅为372 mAh/g[1]。金属Sn可与Li生成 Li4.4Sn,理论比容量可达994 mAh/g[2],但在Li嵌脱时的体积变化较大,导致电极材料粉化、活性物质丧失电接触,造成电池性能的恶化[3]。
解决此问题的方法有:①制备纳米尺寸的合金体系,减少体积的变化[4];②与活性或非活性物质复合,主要包括形成金属间化合物,依靠活性物质之间的电化学电位的不同,或非活性组分作为基体,来缓解体积膨胀[5-6]。
本文作者采用喷雾干燥法制备了核壳结构的SnO2/Sb2O3/酚醛树脂(PF)前驱体,通过碳热还原制备Sn2Sb/C复合材料。核壳结构的Sn2Sb/C微球复合材料主要利用碳类材料富有弹性的结构,缓解合金材料的体积膨胀,防止纳米合金颗粒的团聚,减少纳米合金表面SEI膜的生成;碳类材料本身具有一定的容量,有望得到较好的循环性能。
1 实验
1.1 材料的制备
按化学计量比称取纳米SnO2(洛阳产,99.9%,粒度为50 nm)、纳米Sb2O3(长沙产,99.6%,粒度为 100 nm)和水溶性PF(天津产,99.5%),加入去离子水,配成总浓度为30%的悬浊液,并在磁力搅拌和超声波的作用下分散均匀。将混合液进行喷雾干燥,合成SnO2/Sb2O3/PF前驱体,控制进料速度为10 ml/min,喷雾压力为0.4 MPa,空气进口温度为220℃,出口温度为110℃。所得前驱体以高纯氮气保护、在900℃下处理1 h,制备Sn2Sb/C复合材料。PF碳化成炭气凝胶,同时,部分炭气凝胶将氧化物碳热还原成合金。
1.2 材料分析
用D/Max-rB型X射线衍射仪(日本产)进行物相结构分析,Cukα,λ=0.154 18 nm,管压 45 kV、管流 40 mA,扫描速度为 5(°)/min,步长为 0.02°;
用JSM-6301F型场发射扫描电子显微镜(日本产)观察颗粒的形貌;
用100 kV H800型透射电子显微镜(日本产)观察合金在碳微球中的分布。
1.3 电池的组装
将活性材料粉末、导电剂乙炔黑(上海产,99%)、粘结剂聚四氟乙烯(广州产,99.9%)乳液按质量比8∶1∶1混匀,并滚压成薄片(约为0.1 mm厚),裁取直径为6 mm的圆片,以6 MPa的压力压在直径为8 mm的泡沫镍片(深圳产)上,在120℃下真空(-0.1 MPa)干燥24 h以上。每片正极中,活性物质的质量约为2.6 mg。
负极为金属锂片(北京产,99.9%),隔膜为Celgard 2400膜(美国产),电解液为1 mol/L LiPF6/EC+DMC+EMC(体积比 1∶1∶1,张家港产,99.99%)。
2032型扣式电池的组装在充满氩气的手套箱中进行。
1.4 充放电测试
在室温下,用LAND测试系统(武汉产)进行电池的充放电测试,电流为50 mA/g,电压为0.02~1.50 V。
2 结果与讨论
2.1 Sn2Sb/C微球的结构和形貌
SnO2/Sb2O3/PF前驱体和Sn2Sb/C复合材料的XRD图见图1。
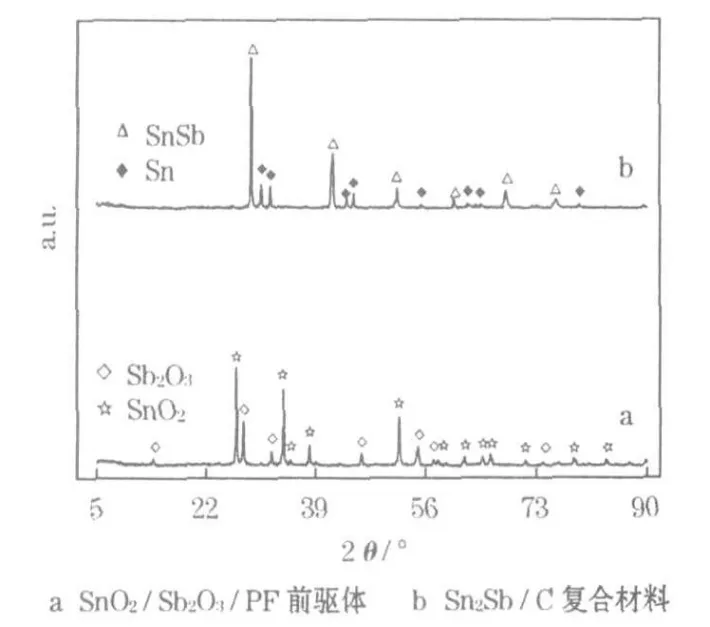
图1 SnO2/Sb2O3/PF前驱体和Sn2Sb/C复合材料的XRD图Fig.1 XRD patterns of SnO2/Sb2O3/PF precursor and Sn2Sb/C composite
从图1可知,SnO2/Sb2O3/PF前驱体的衍射峰主要为SnO2和Sb2O3的衍射峰;在 Sn2Sb/C复合材料中,可看到Sn和SnSb的衍射峰,并无残余氧化物和其他杂质的衍射峰,说明纳米SnO2和Sb2O3完全生成了合金Sn-SnSb,且晶型良好。Sn2Sb/C复合材料中没有观察到碳材料的结晶峰,可能是因为PF热解的炭气凝胶为硬碳类材料,呈现无定形结构[7]。
Sn2Sb/C复合材料中,PF碳化成炭气凝胶,与氧化物发生式(1)所示的反应。
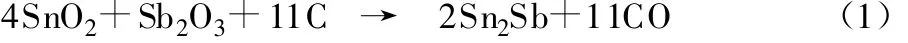
Sn2Sb/C复合材料的SEM和TEM图见图2。

图2 Sn2Sb/C复合材料的SEM和TEM图Fig.2 SEM and TEM photographs of Sn2Sb/C composite
从图2a可知,颗粒呈规则的球形形貌,粒径分布均匀,大约为6~15μ m;球形颗粒周围并无其他氧化物与合金存在,说明还原生成的纳米合金颗粒完全包覆于炭气凝胶微球中。
从图2b可知,黑色合金颗粒包覆于球形的炭气凝胶微球中,可以进一步证明球形颗粒实际上是炭气凝胶包覆纳米合金微粒的核壳结构的复合体,合金尺寸为纳米级,且均匀分布于炭气凝胶载体中,并无团聚现象。
2.2 Sn2Sb/C复合材料的充放电性能
Sn2Sb/C复合材料的充放电曲线见图3。
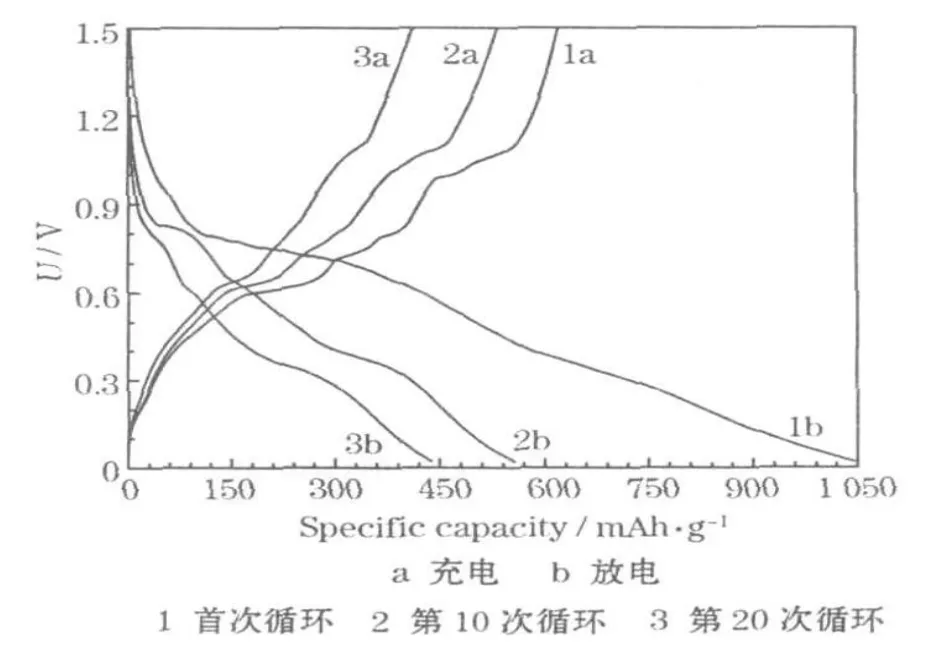
图3 Sn2Sb/C复合材料的充放电曲线Fig.3 Charge-discharge curves of Sn2Sb/C composite
从图3可知,Sn2Sb/C复合材料的充放电曲线具有典型的Sn2Sb合金的电化学嵌脱锂特性。
Sn2Sb合金电极的充放电曲线中,不同的电位分别对应不同的电化学嵌锂反应。锂与合金中SnSb相的反应可分为两步,见式(2)、式(3)[8]。
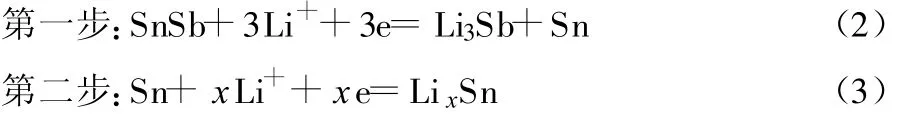
锂嵌入时,首先与Sb生成Li3Sb。此时的Sn处于相对惰性状态,对应的电位大约为0.75 V。Li3Sb完全生成后,Li与Sn开始形成不同的合金相LixSn,对应的电位在0.40 V以下。对应于不同电位范围,单相SnSb可分离为独立的纳米尺寸的Li3Sb和Sn区域,在不同的电位下,总处于活性/惰性的复合状态下,由此降低了嵌脱锂带来的体积效应。
首次嵌锂过程中,在碳微球表面生成固体电解质相界面(SEI)膜,反应电位为0.75 V,此反应为不可逆反应[9]。此电位与生成Li3Sb的电位相近,因此Sn2Sb/C复合电极从0.75 V开始出现一个缓慢下降的电位平台,对应碳微球表面的SEI膜成膜反应和锂嵌入SnSb相生成Li3Sb和Sn相的反应。随着Li的继续嵌入,Li与Sn开始形成一系列的合金相LixSn,对应的电位在0.40 V以下为较倾斜的一段电位平台。在充电的曲线中,电极在0.60~0.80 V具有明显的阶梯状电位平台,对应Li从不同的 LixSn合金相中脱出,在1.00 V左右的平台对应Li从Li3Sb中脱出的电化学反应。
Sn2Sb/C复合材料的首次放电比容量为1 044 mAh/g,充电容量仅为618 mAh/g,库仑效率为59%。
导致首次不可逆容量较大的原因主要有:
①首次嵌锂生成SEI膜为不可逆反应,消耗了部分Li;
②PF碳化不完全,可能残留部分氧原子与Li发生不可逆反应[10];
③合金首次嵌锂过程中发生膨胀,导致电极部分电接触丧失,发生死锂现象。
Sn2Sb/C复合材料的循环性能和库仑效率见图4。
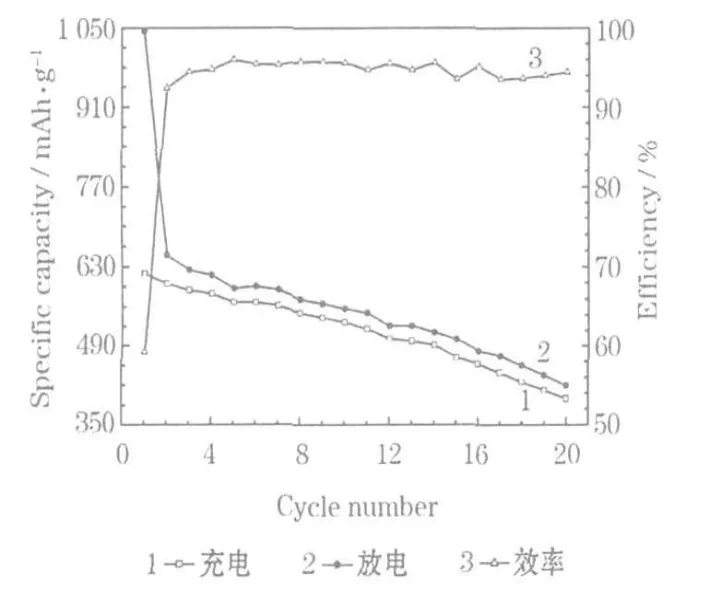
图4 Sn2Sb/C复合材料的循环性能和库仑效率Fig.4 Cycle performance and Coulombic efficiency of Sn2Sb/C composite
从图4可知,第20次循环时Sn2Sb/C复合材料的充电比容量为411.3 mAh/g,容量保持率为66.6%。可以看出,核壳结构的Sn2Sb/C复合材料具有较高的可逆比容量和较好的循环性能,这主要归因于:
①纳米尺寸的Sn2Sb合金的绝对膨胀体积较小;
②富有弹性的碳壳层,可缓解体积膨胀,防止纳米合金颗粒的团聚,提高纳米颗粒间的导电性。
3 结论
以纳米 SnO2、Sb2O3和 PF为原料,采用喷雾干燥-碳热还原法制备了核壳结构的Sn2Sb/C复合材料。
XRD、SEM 和 TEM 分析表明:纳米尺寸的 Sn2Sb合金均匀分布于碳微球体中。
电化学测试表明:材料具有较高的可逆比容量和较好的循环性能,首次充电比容量为618 mAh/g,第20次循环的容量保持率为66.6%。
碳微球对纳米合金颗粒的分散包覆,抑制了纳米合金颗粒的团聚,提高了合金电极的循环性能。该材料的首次不可逆容量较大,循环性能须进一步提高。
[1]LU Mi(路密),YIN Ge-ping(尹鸽平),SHI Peng-fei(史鹏飞).锂离子电池负极石墨材料的修饰与改性[J].Battery Bimonthly(电池),2001,31(4):195-197.
[2]Zhao L Z,Hu S J,Ru Q,et al.Effects of graphite on electrochemical performance of Sn/C composite thin film anodes[J].J Power Sources,2008,184(2):481-484.
[3]Denis B,Catarina N,Cédric M,et al.Electrochemical lithium insertion in graphite containing dispersed tin-antimony alloys[J].Energy Conversion and Management,2008,49(9):2 447-2 454.
[4]Wang F,Zhao M S,Song X P.The improved electrochemical performance of SnSb-based alloy anode materials for Li-ion batteries[J].J.Alloys Compd,2009,472(1-2):55-58.
[5]Jusef H,Gaelle D,Stefania P,et al.A SnSb-C nanocomposite as high performance electrode for lithium ion batteries[J].Electrochim Acta,2009,54(19):4 441-4 444.
[6]SUN Qing(孙庆),SHI Peng-fei(史鹏飞),JIAO Yun-chao(矫云超),et al.高可逆比容量锡基负极的性能[J].Battery Bimonthly(电池),2007,37(5):345-347.
[7]Wang K,He X M,Ren J G,et al.Preparation of Sn2Sb alloy encapsulated carbon microsphere anode materials for Li-ion batteries by carbothermal reduction of the oxides[J].Electrochim Acta,2006,52(3):1 221-1 225.
[8]Yang J,Wachtler M,WinterM,et al.Sub-microcrystalline Sn and Sn-SnSb powders as lithium storage materials for lithium-ion batteries[J].Electrochem Solid-State Lett,1999,2(4):161-163.
[9]Matsumura Y,Wang S,Mondori J.Mechanism leading to irreversible capacity loss in Li ion rechargeable batteries[J].J Electrochem Soc,1995,142(9):2 914-2 918.
[10]Flandrois S,Simon B.Carbon materials for lithium-ion rechargeable batteries[J].Carbon,1999,37(2):165-180.
