工业循环水浓缩倍数的检测方法——离子色谱的应用
2010-09-07房树芹
房树芹
(淮安清江石油化工有限责任公司,江苏 淮安 223002)
1 循环水浓缩倍数
循环水浓缩倍数是指循环冷却水系统在运行过程中,由于水分蒸发、风吹损失等情况使循环水不断浓缩的倍率 (以补充水作基准进行比较),它是衡量水质控制好坏的一个重要综合指标。
1.1 浓缩倍数的工业意义
随着经济的发展,工业用水量日益增长,而循环冷却水占工业水总量的70%左右,循环冷却水大有潜力可挖。浓缩倍数是判定循环冷却水利用率的一个重要指标,一般浓缩倍数低,耗水量、排污量均大且水处理药剂的效能得不到充分发挥;该数越高,说明循环水被利用的次数越多.提高循环水浓缩倍数不仅可以降低补充水量、节约水资源、降低排污水量、减少对环境的污染和废水处理量,还可以减少水处理剂及杀生剂的消耗量、降低水处理成本。可是浓缩倍数过高,水的结垢倾向会增大,结垢控制及腐蚀控制的难度会增加,水处理药剂会失效,不利于微生物的控制,故循环水的浓缩倍数要有一个合理的控制指标。
提高浓缩倍数运行是目前公认的有效方法,浓缩倍数从1.5 提高到2 节水50%,从2 提高到3 节水30%,从3 提高到4 节水15%,从4提高到5 节水6%,浓缩倍数在5 以上再提高已失去了节水意义,反而会带来一些列问题:水中盐含量增加,会使循环冷却水中的硬度、碱度和浊度升得太快太高,加大了水的结垢倾向,加剧了冷换设备的腐蚀和结垢;细菌藻类滋生繁殖加剧;对药剂使用提出更高要求,主要是药剂加入的精度要提高;有害物质对药剂的容忍度产生变化。所以,一般浓缩倍数提高到5 比较适宜。但随着浓缩倍数的提高,循环水系统结垢和腐蚀因子也随之成倍上升,所以高浓缩倍数下水处理技术的开发应用是节水减排技术的关键。
提高浓缩倍数是趋势,但要结合企业的实际情况去处理。这就是说浓缩倍数不是越大越好,要把浓缩倍数控制在一定范围内.目前我厂把浓缩倍数控制在3-5 之间.为了能够正确地反映浓缩倍数的运行情况,我们需要选择一种合适的检测方法。
1.2 目前监测方法的不足
浓缩倍数的测定和控制一般选用水中较稳定的离子来进行。目前我厂采用循环冷却水与补充水中氯离子浓度的比值来测定和控制浓缩倍数N。即
N=循环冷却水氯离子浓度/补充水氯离子浓度
由表1 可以看出,当系统中不加含氯杀菌剂或补充水水质较稳定时,采用此方法简单快捷。但由于河水中氯离子浓度总有一定变化,而且一般都采用聚氯化铝作净水剂,使得补充水中氯离子浓度难以稳定,测定的循环水浓缩倍数也就有一定误差。同时,循环水系统还常常采用Cl2或NaClO 等含氯药剂来控制循环水中的微生物及粘泥,用氯离子浓度来测定和控制浓缩倍数也难以真实反映循环水浓缩状况。这就需要选择一个合适的监测方法。

?

1.3 浓缩倍数监测方法比较
目前用于监测浓缩倍数N 的特性物质一般为氯离子、钙离子、钾离子、二氧化硅和电导率。这些物质浓度或特性在冷却水系统运行中一般不受加热、曝气、投加药剂、沉积或结垢等因素干扰,且随N 的增加而成比例增加。
氯离子性质稳定,不易产生沉淀,测定简单、快捷。补充水质不稳定或是冷却水以氯气等含氯试剂作杀菌剂时不宜采用。
钙离子稳定性好,干扰少,测定简单、快捷.当体系浓缩倍数高或结垢时,产生钙盐沉积物,测定结果偏低。
钾离子稳定性好,干扰少,循环水系统中K+来源较少,K+的溶解度较大,运行过程中也不会从水中析出,故用K+法检测循环水浓缩倍数K 时,受到的干扰相对较少,但分析过程较为繁琐,要求高,费用也高。
二氧化硅性质较稳定,干扰少,但是当硅酸盐与镁离子浓度都高时,生成硅酸镁沉淀,使二氧化硅浓度偏低,测定精度较差。对分析条件要求苛刻,费用较高。
电导率测定迅速,仪器操作简单,受补水水质及水处理工艺影响,适合现场监测。
综观以上几种方法,由于钾离子性质稳定、溶解度大,循环水中又无此来源,基本无影响因素,钾离子测定精密度和准确度都高。因此选用钾离子作为我厂监测浓缩倍数的特性物质是最合适的。
2 钾离子测定方法及离子色谱的应用
目前钾离子测定方法主要有:原子吸收分光光度法;火焰光度法;离子色谱法;钾度计法。测定钾离子的目的,在于确定循环冷却水浓缩倍数时,可将循环冷却水按运行状况进行稀释,使其含盐量接近补充水状况,再进行测定,这样可相对消除干扰。由于我们只是对钾离子进行定量分析,选择离子色谱法测定钾离子是比较合适的.离子色谱法测定钾离子具有下列优点:快速、方便、灵敏度高、选择性好、结果可靠。但对有机物浓度要求太高是其主要缺点。
?
2.1 离子色谱法测定钾离子
离子色谱工作原理及应用前景。离子色谱是高效液相色谱(HPLC)的一种,是分析阴阳离子的一种液相色谱方法。通常情况下,离子色谱可以分为三种类型,高效离子交换色谱(HPIC)、离子排斥色谱(HPIEC)、离子对色谱(MPIC)。
下面我们以离子交换色谱为例,简单介绍一下离子色谱的工作原理。离子色谱的工作原理主要是离子交换平衡。离子色谱中使用的固定相是离子交换树脂。离子交换树脂上分布有固定的带电荷的基团和能游动的配位离子。当样品加入离子交换色谱往后,如果用适当的溶液洗脱,样品离子即与树脂上能游动的离子进行交换,并且连续进行可逆交换吸附和解吸,最后达到吸附平衡。由于各离子与树脂亲和力不同,各离子将按次序先后被洗脱出来,经电导检测器检测出各离子的峰,绘出谱图。
离子色谱主要用于环境样品的分析,包括地面水、饮用水、雨水、生活污水和工业废水、酸沉降物和大气颗粒物等样品中的阴、阳离子,与微电子工业有关的水和试剂中痕量杂质的分析。
离子色谱法测定工业循环水中钾离子(参照GB/T15454-95)
方法提要。离子在固定相和流动相有不同的分配系数,当流动相将样品带到分离柱时,由于各种离子对离子交换树脂的相对亲和力不同,样品中的各种离子被分离,再流经电导池,由电导池检测器检测,并绘出各种离子的色谱图,以保留时间定性,以峰面积或峰高定量测出离子含量。
水样的预处理。水样中常含有大量的细菌,经常会因在色谱柱上形成菌膜而将其损坏。为保护色谱柱,可将经前处理后的样品经0.45um的微孔滤膜过滤,可将细菌阻挡于膜上而仅让水分子和各种离子通过[3]。
仪器。离子色谱仪主机、电导检测器、往复式平流泵、台式记录仪等组成。原理图如图1。
适用范围。本标准适用于测定工业循环冷却水中 Na+、NH4+、Li+、Mg2+和Ca2+含量的测定。检测范围:Na+含量1.00~50.0mg/L、NH4+含量 1.00~30.0mg/L、K+含 量 1.00~50.0mg/L、Mg2+含 量1.00~50.0mg/L 和Ca2+1.00~50.0mg/L 范围的测定,如果超出此范围,可稀释在此范围内测定。
分析步骤
淋洗液的的配制:选用68%的浓硝酸配制1mol/LHNO3作为贮备液,然后根据不同的分离柱而移取不同量的上述贮备液,用去离子水蒸馏水稀释至1000mL 作为淋洗液,使用前应将淋洗液经烧结玻璃漏斗过滤,并真空脱气。
插上阳离子电导池板。将平流泵过滤器放人淋洗液贮液瓶,开启平流泵,流量选择0.5ml/min,通淋洗液20 分钟后,选择色谱柱所规定的流量,转换开关打到“输出”档,调节调零电位器,使数字表显示为零。
选择记录仪档位(根据样品浓度的高低,选择合适的量程)以及基线在记录线上的位置,即可进行分析,根据色谱图的峰高,调节记录仪量程。
进样用注射器吸取1mL 样品(必须排除气泡)由阳离子进样口进样,将进样阀快速扳回分析位置,完成一次进样。
关闭仪器:分析完毕后,先通10 分钟蒸馏去离子水,再依次关闭记录仪、主机和泵电源。
分析结果的表述
以mg/L 表示的待测离子含量x 按下式计算:
X=L/L0*C0*V0/V
式中:L—水样中被测离子峰高,mm;
L0—标准工作溶液中被测离子峰高,mm;
C0—标准工作溶液中被测离子浓度,mg/L;
V—所取水样体积,mL;
V0—水样被稀释后体积。
或由色谱微处理机按峰面积或峰高直接计算出结果。
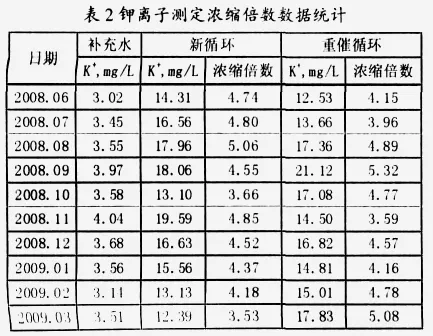
2.2 结果分析(见表2)
与表1 相比,可明显看出补充水中钾离子浓度比较稳定,循环水中又无此来源,选择钾离子作为测定参数可行。
3 总结
目前,离子色谱法已经在能源、环境、冶金、电镀、半导体、水文地质等方面广泛应用,并且开始进入了与生命科学有关的分析领域。我国从80年代初期引进离子色谱仪,开始了离子色谱的应用研究工作,同时也开始了仪器的研制和生产。随着离子色谱技术的发展,离子色谱仪在我国的应用已日益普及。
我厂选用江苏江分电分析仪器厂的型号为WIC-Ⅱ的离子色谱仪,于2008年6月开始使用,为工业循环水浓缩倍数提供更加准确可靠的数据指导。循环水浓缩倍数不仅是反映水质的一个综合性指标,同时也是衡量一个部门甚至一个企业综合管理能力及技术发展水平的重要指标。
[1]杜林琳.循环冷却水浓缩倍数关键是看水质是否结垢型水网论坛2006.8
[2]何世梅.循环水浓缩倍数的检测方法及控制指标中国论文下载中心2006.3
[3]《中华人民共和国国家标准工业循环冷却水中钠、铵、钾、镁和钙离子的测定离子色谱法》GB/T15454-95
