缺血性脑白质疏松症危险因素的临床研究
2010-08-25林志坚张海鸥
张 帅, 林志坚, 吴 军, 张海鸥
脑小血管病(small vessel disease,SVD)会造成相应脑组织持续性和进展性损伤,逐渐导致认知功能障碍和抑郁症状,其影像学表现为腔隙性脑梗死、脑白质疏松症和脑微出血。2008年国际卒中会议和欧洲卒中会议都提出了“小血管病引起大问题”的论点。Hachinski教授指出,痴呆为疾病分子生物学的一种终末状态,是经过 20年的分子生物学改变,从轻度认知障碍到严重认知障碍,最终发展成痴呆。脑血管病可以干预,但对终末阶段却无能为力,因此早期发现和处理血管危险因素是将来研究的重点,特别是 SVD[1]。我们基于 MRI检查,对我科住院病房中伴发和不伴发脑白质疏松症(Leukoaraiosis,LA)的腔隙性脑梗死患者的临床资料仔细进行回顾性分析,以探讨临床常见的血管危险因素在 LA发病机制中的作用。
1 对象与方法
1.1 入组与排除标准 北京大学深圳医院神经内科 2008年 7月 1日 ~2009年 6月 30日入院诊断为腔隙性脑梗死患者 386例,其中男性 214例(55.4%),女性 172例(44.6%),所有患者均行头部 1.5T MRI诊断,入选者单个梗死灶直径均 <2cm。根据 T2加权像上是否伴发脑白质疏松症,分为单纯的腔隙性脑梗死组(Isolated lacunar infarction,LI组)和伴发脑白质疏松症组(Lacunar infarction with leukoaraiosis,LA组)。LA定义为 MRI图像上侧脑室旁及半卵圆中心 T1等或低信号、T2高信号的双侧大致对称的斑点状、斑片状或融合状病灶。
排除标准:除外直径 >2cm脑梗死及脑出血患者,除外非梗死性腔隙病变患者,除外多发性硬化及感染性、代谢性、中毒性、自身免疫性、肿瘤转移性等因素引起脑白质病变者。
1.2 研究方法 详细记录两组的年龄、性别,有无高血压、2型糖尿病、冠心病、心房颤动、颈动脉粥样硬化、脑动脉硬化、高甘油三酯血症、高胆固醇血症、高尿酸血症和贫血等病史。
1.3 统计方法 所有数据均经 SPSS 13.0统计软件包进行分析处理,计量资料以±s表示 ,组间单因素分析采用独立样本 t检验,计数资料采用χ2检验,多因素分析采用 Binary Logistic回归分析,P<0.05有统计学意义。
2 结 果
2.1 LA可能的危险因素单因素分析 见表1。LI组 212例(54.9%),年龄 32~ 91岁,≥60岁 123例(58%),平均 61.05±11.95岁;LA组 174例,年龄 38~98岁,≥60岁 143例(82.2%),平均 68.52±9.59岁。两组间年龄行独立样本 t检验,具有高度显著性差异(P<0.01),说明随着年龄增长 LA发生增多。对性别及高血压、2型糖尿病、冠心病、心房颤动、颈动脉粥样硬化、脑动脉硬化、高甘油三酯血症、高胆固醇血症、高尿酸血症和贫血等病史行 χ2检验,结果显示脑动脉硬化、高血压病、2型糖尿病 3个因素在两组间具有高度显著性差异(P<0.01),≥60岁患者中性别亦无显著性差异(P>0.05)。见表1(按 P值大小排列)及图1。
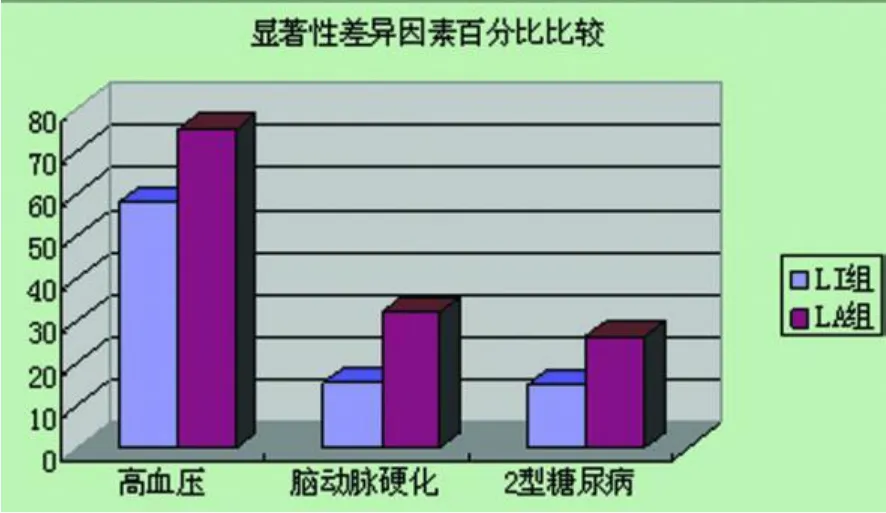
图1 显著性差异因素百分比比较

表1 LA有关的危险因素单变量分析
2.2 LA相关危险因素的 Logistic回归分析采用 Binary Logistic回归分析,因变量为是否伴发LA,自变量包括年龄、性别及高血压、2型糖尿病、冠心病、心房颤动、颈动脉粥样硬化、脑动脉硬化、高甘油三酯血症、高胆固醇血症、高尿酸血症和贫血病史,采用 Backward Stepwise方法,各自变量的 OR值及 P值见表2(按 OR值大小排列,显著性差异放前面)。
结果表明,脑动脉硬化、高血压、高龄在 Binary Logistic回归分析中仍有显著性意义。其中脑动脉硬化(OR=2.029,95%CI:1.194-3.450,P=0.009),高血压(OR=1.664,95%CI:1.032-2.684,P=0.037),年龄 (OR=1.059,95%CI:1.037-1.082,P=0.000),为 LA的独立危险因素。而 2型糖尿病(OR=1.67,95%CI:0.97-2.89,P=0.066),尚不能认为是 LA的独立危险因素。

表2 各危险因素的Binary Logistic回归分析
3 讨 论
3.1 LA及临床意义 LA定义为弥漫性、融合性白质异常(CT为低密度,MRI T2加权像或 FLAIR成像为高信号),经常伴有不规则边缘。因为是一纯粹的放射学概念,这一术语同样可以应用于脑白质营养不良和一些代谢性和感染性疾病,但最常见的病因是由于血管危险因素导致的脑白质区域慢性缺血。本研究在研究对象入组时选取腔隙性脑梗死患者,同时设置了排除标准。
许多学者一度认为 LA是一良性的影像学表现,没有严重的后果,但是现在清楚地知道 LA与信息处理速度和执行功能的缺陷有关联[2,3]。LADIS(leukoaraiosis and disability,LADIS)研究[4]通过对 633例程度不同的 LA患者接近 3年的随访发现重度 LA发生残疾或死亡的风险是轻度 LA两倍多。其他特征如步态障碍[5]、膀胱不稳定(如尿急)[6]和情绪障碍都与之独立性关联。另外,对于脑血栓患者应用抗凝或抗血小板聚集治疗时,LA是发生脑出血并发症的独立危险因素,OR值达 9.2[7]。关于 LA发病机制及临床意义的研究有一定临床价值。
3.2 LA与 LI 病理学研究提示 LA是脑小血管疾病的一种。其与 LI之间密切的病理和临床关联可以支持这种观点[8]。虽然 LA与 LI经常同时共存,但是具体的一位患者可能以其中的一种影像表现占优势,从而有了弥漫性小血管疾病不同亚型的概念。其一为缺血性脑白质疏松症(脑白质疏松症伴有临床腔隙综合征),其二为单纯的腔隙性脑梗死(影像上没有脑白质疏松症)。Khan等[9]的研究表明这两种影像表现的危险因素不同。年龄和高血压与缺血性脑白质疏松症有着更强的关联,而高胆固醇血症、糖尿病和心肌梗死与单纯的腔隙性脑梗死有着更多关联。这些发现提示在发病机制上两者可能有些不同。LA与 LI对比,可能病理上反映的是更小口径血管的非动脉粥样硬化性狭窄或阻塞。
基于上述的研究背景,我们以 386例 LI患者为研究对象,对两种亚型之间的临床危险因素进行单变量的 t检验、χ2检验及多变量的 Logistic回归分析,结果确有差异。
3.3 LA与年龄、高血压、脑动脉硬化及 2型糖尿病的关系 本研究结果表明,年龄(OR=1.059,95%CI:1.037-1.082,P=0.000)、高血压 (OR=1.664,95%CI:1.032-2.684,P=0.037),是 LA的独立危险因素,与 Khan等[9,10]许多临床研究结论一致。年龄与 LA的关系独立于血管危险因素而存在,提示 LA可能与老年化过程本身有关。Brown等[11]认为,凋亡可能参与了 LA的发病机制,病变白质区DNA碎裂的少突胶质细胞数量是临近白质的 2.5倍,是附近皮质的 25倍。慢性高血压导致颅内小动脉及深穿支动脉内壁增厚和玻璃样变性,而深部细穿支动脉很少或完全没有侧支循环,这种改变足以引起深部细穿支动脉血液学障碍,造成其供血的大脑半球白质出现缺血,继发大脑白质损伤。另外,本研究结果提示脑动脉硬化(OR=2.029,95%CI:1.194-3.450,P=0.009),为 LA独立危险因素,且OR值最高,提示 LA与脑动脉硬化之间有着最密切的联系。我科曾回顾性分析了 133例行头部 MRI与MRA的急性脑梗死患者,同样发现随着脑白质疏松症程度加重,颅内动脉硬化条数有增多趋势[12]。脑动脉硬化可以引起白质区血液灌注量下降和血流动力学改变,可以引起微栓子形成,造成穿支动脉闭塞,均可能引起 LA发生。因此,无症状 LA像其他症状性脑梗死一样进行 TCD或头部 MRA检查,完善颅内动脉状态评估,以明确有无脑动脉硬化及狭窄可能,具有重要的临床意义,有利于脑血管疾病的早期防治。
大多数关于糖尿病与 LA相关性的研究提供了支持的证据[13],也有一部分临床研究得到了相反的结果,如 Kim等[14]认为糖尿病仅可增加大血管病的发生率而无明显增加颅内小血管病变危险性的作用的结论。本研究中,单变量分析,2型糖尿病在两组间具有显著性差异(P<0.01),而在多因素 Logistic回归分析中(OR=1.67,95%CI:0.97-2.89,P=0.066),说明 2型糖尿病与 LA可能相关,但尚不能认为其为 LA的独立危险因素,2型糖尿病可能与其他危险因素一起在 LA的发病机制中发挥作用。
3.4 LA与其它因素 由于研究对象及研究方法的不同,关于性别与 LA的临床研究结果不尽统一,其中有些观点认为女性比男性更易发生 LA,对此的可能解释是女性绝经后雌激素水平下降,提高了脑对缺氧的敏感性.而缺血缺氧通常被认为在脑白质损害的发病机制中起中介作用,同时雌激素对脑部有保护作用,包括提高脑血流、抗氧化作用、防止神经元凋亡等,绝经后雌激素下降使脑血流减少和神经元修复机制受阻。本研究中在所有年龄段中未见显著性差异,为此特意分析了年龄≥60岁患者中性别与 LA有无关联性,结果同样无显著性差异(P>0.05),考虑性别因素在 LA发病机制中作用不大,确切关系有待于进一步深入研究。
冠心病、房颤病史、颈动脉粥样硬化与 LA无显著性差异(P>0.05),考虑动脉粥样斑块栓子栓塞可能不是 LA主要的发病机制。颈动脉粥样硬化可以引起颅内血管血流动力学改变,但在本研究中无显著性差异,考虑 Willis环及颅内侧支循环的血流代偿起了关键性作用。有研究[13]表明,高甘油三酯血症与脑白质疏松症的出现相关,而与进展无关,在本研究未被证实。其他高胆固醇血症、高尿酸血症等动脉粥样硬化发展的危险因素均未发现有显著性意义(P>0.05),提示 LA的动脉硬化不同于大血管疾病的动脉粥样硬化,而是穿支动脉玻璃样变性。贫血容易造成组织缺氧,故将其列为研究因素,仅有9例患者符合,其与 LA的关联性有待于进一步研究。
总之,LI与 LA同为脑小血管疾病,临床危险因素相似,但各危险因素的倾向性并不一致。脑动脉硬化、高血压、高龄与 LA的发病机制有着更多的关联,2型糖尿病可能与其他因素一起在 LA的发生中发挥作用,对待伴发 LA的患者有必要行 TCD或头部 MRA对颅内动脉状况进行评估,同时积极控制血压与血糖。
[1] 张微微.脑小血管病的新进展[J].中华脑血管病杂志,2008,2(4):210-213.
[2] Prins ND,van Dijk EJ,den Heijer T,et al.Cerebral small-vessel disease and decline in information processing speed,executive function and memory[J].Brain,2005,128:2034-2041.
[3] O'Sullivan M,Morris RG,Huckstep B,et al.Diffusion tensor MRI correlates with executive dysfunction in patients with ischaemic leukoaraiosis[J].Neurol Neurosurg Psychiatry,2004,75:441-447.
[4] Inzitari D,Pracucci G,Poggesi A,et al.Changes in white matter as determinant of global functional decline in older independent outpatients:three year follow-up of LADIS(leukoaraiosis and disability)study cohort[J].BMJ,2009,339:2477.
[5] Franch O,Calandre L,Alvarez-Linera J,et al.Gait disorders of unknown cause in the elderly:Clinical and MRI findings[J].Neurological sciences,2009,280:84-86.
[6] Poggesi A,Pracucci G,Chabriat H,et al.Urinary complaints in nondisabled elderly people with age-related white matter changes:the leukoaraiosis and disability(LADIS)Study[J].Am Geriatr Soc,2008,56:1638-1643.
[7] Gorter JW.Major bleeding during anticoagulation after cerebral ischemia:patterns and risk factors.Stroke Prevention In Reversible Ischemia Trial(SPIRIT).European Atrial Fibrillation Trial(EAFT)study groups[J].Neurology,1999,53:1319-1327.
[8] Wiszniewska M,Devuyst G,Bogousslavsky J,et al.What is the significance of leukoaraiosis in patients with acute ischemic stroke[J].Arch Neurol,2000,57:967-973.
[9] Khan U,Porteous L,Hassan A,et al.Risk factor profile of cerebral small vessel disease and its subtypes[J].Neurol Neurosurg Psychiatry,2007,78:702-706.
[10] Longstreth WT Jr,Manolio TA,Arnold A,et al.Clinical correlates of white matter findings on cranial magnetic resonance imaging of 3301 elderly people.The Cardiovascular Health Study.The Cardiovascular Health Study[J].Stroke,1996,27:1274-1282.
[11] Brown WR,Moody DM,Thore CR,et al.Apoptosis in leukoaraiosis[J].AJNR Am J Neuroradiol,2000,21,79-82.
[12] 周芬莉,吴 军,江锦赵,等.脑白质病变与颅内动脉硬化的相关性研究[J].罕少疾病杂志,2009,16(3):1-6
[13] Park K,Yasuda N,Toyonaga S,et al.Significant association between leukoaraiosis and metabolic syndrome in healthy subjects[J].Neurology,2007,69:974-978.
[14] Kim BJ,Lee SH,Kang BS,et al.Diabetes increases large artery diseases,but not small artery diseases in the brain[J].Neurology,2008,225:1176-1181.
