炎琥宁肠溶微丸的制备工艺研究
2010-07-21王凤燕黄桂华
徐 淼,李 岩,盛 蕾,王凤燕,石 洋,黄桂华
(山东大学 药学院,山东 济南 250012)
炎琥宁(C28H34KNaO10◦H2O)是穿心莲内酯经人工半合成所得的穿心莲内酯琥珀酸半酯钾钠盐,为目前临床常用的抗菌抗病毒药物之一。注射用炎琥宁主要成分为爵床科植物穿心莲叶中所提取的穿心莲内酯,与琥酸酐反应生成脱水穿心莲内酯琥酸半酯后,再生产单钾盐制成的注射用粉针,具有抗菌,抗病毒,消炎等作用[1],但是临床统计数据表明,注射用炎琥宁对皮肤系统、呼吸系统、血液系统都有一定的不良反应[2]。
微丸在药剂学领域中的应用已十分广泛,作为药物载体,它既可以进一步压制成片剂,又可以装入胶囊中使用,不仅提高了药物稳定性,而且能够有效地调节药物释放速率;作为药物释放系统(drug delivery system,DDS),微丸具有治疗学上的优势,如较少胃肠道刺激性及降低了药物突释造成的风险,提高了用药安全性,且血药浓度重现性好;微丸还具有流动性好、脆碎度小、易装填等工艺学优点[3]。
炎琥宁在 pH值6~8时稳定 ,在酸中不稳定[4]。为避免炎琥宁在胃中酸性环境下被破坏,可将炎琥宁制成肠溶微丸,用于病毒性肠炎的治疗。因此,笔者尝试采用水分散体Eudragit L为包衣材料,内加吸水溶胀层,制备了一种新型炎琥宁肠溶微丸,并进行了体外释放实验。
1 材 料
1.1 药品与试剂
炎琥宁(纯度>98%,批号080101),陕西太康生物科技有限公司;微晶纤维素PH101(MCC)、乙基纤维素(EC),山东聊城阿华制药有限公司;二氧化硅(SiO2)、无水乙醇,天津试剂厂;Eudragit L,上海罗姆药业公司。
1.2 仪器
球形微丸造粒机(华东理工大学化工机械设备研究开发中心);UV-2102PCS紫外分光光度计(上海尤尼柯仪器有限公司);D-800LS智能药物溶出仪(天津大学无线电仪器厂);CX-250超声波清洗器(北京医疗设备二厂);AL104-IC型电子天平(美国托普乐-梅赛德上海公司);JHQ-100型流化沸腾颗粒包衣机(沈阳医联新药研究所制造);投影仪(郑州照相机厂);82-5B型磁力加热搅拌器 (德国 Irka○R,广州);BTQ-100M蠕动泵(保定兰格恒流泵有限公司)。
2 方法与结果
2.1 微丸的制备方法与含量测定方法
2.1.1 标准曲线的制备 精密称取炎琥宁对照品适量,加水制备浓度分别为20,25,30,35,40,45,50 μ g/mL的系列标准溶液,照紫外分光光度法于253 nm波长处测定吸光度(A),以浓度C为横坐标,A为纵坐标,按最小二乘法计算回归方程,得标准曲线方程:A=0.014 3 C+0.002 1,r=0.999 8。表明炎琥宁水溶液在20~50 μ g/mL浓度范围内线性良好。
2.1.2 载药丸芯的制备 将炎琥宁和MCC按处方比例混匀,加适量黏合剂制成具有一定弹性、塑性和黏性的软材,将软材经挤出筛板(孔径0.8 mm)挤成直径相同,光滑致密的条状物,移至高速旋转的滚圆机内,直至颗粒滚成球形微丸,取出,于30℃恒温箱中干燥即得。挤出-滚圆参数:挤出速度为1 080 r/min,滚圆速度为960 r/min,滚圆时间为5 min。
2.1.3 包衣微丸的制备 采用流化床包衣机包衣。取微丸适量,置于气流包衣装置中,将EC,EudragitL30D,PEG6000,无水乙醇,水按处方比例混合搅拌,制得肠溶层包衣液,包衣参数:鼓风机频率为(40±2)Hz;流化温度为(38±1)℃;包衣液流速为0.2~0.3 mL/min;雾化压力为0.15 MPa。
2.1.4 微丸含量测定 精密称取含药微丸适量,加pH 6.8的磷酸盐缓冲液,超声5 min,过滤,于253 nm波长处测定 A值,代入标准曲线方程计算药物含量。在253 nm波长处,辅料对测定无干扰。
2.1.5 体外释放度测定[9]依据标准曲线的线性范围及漏槽条件,精密称取微丸1g(约含炎琥宁320 mg)于释放介质1 000 mL中,转速为100 r/min,温度为(37±0.5)℃。模拟微丸在胃肠道中的释药情况,首先以pH 1.0的盐酸溶液为溶出介质,2 h后将溶出介质换为pH 6.8的磷酸盐缓冲液,于5,10,15,20,30,45,80,120 min取样,过滤,测定含量,并计算累积释放百分率。
2.2 处方因素对丸芯成型性的影响
2.2.1 填充剂种类的影响 固定炎琥宁与各种填充剂的比例,分别采用MCC、淀粉、淀粉与糊精混合物、淀粉与乳糖混合物等为填充剂,以外观形态、粒径分布、圆整度和收率等作为考察指标进行考察。结果如表1所示,最终确定选择MCC为填充剂。

表1 填充剂种类考察Tab.1 The investigation of the types of filler agent
2.2.2 黏合剂种类的影响 为增加软材的可塑性,增强丸芯的硬度,制备微丸过程中需加入一定黏合剂 。分别以水、20%乙醇、40%乙醇、硅油、HPMC 、淀粉浆为黏合剂制备微丸,以是否能够成丸作为考察指标,经考察,以40%乙醇作为黏合剂成丸性良好。
2.2.3 抗黏剂种类的影响 炎琥宁遇水产生较大黏性,需加入一定抗黏剂降低其黏度。分别选择滑石粉、SiO2、CaCl2作为抗黏剂,通过考察是否能够成丸以确定抗黏剂。经考察使用滑石粉和CaCl2时,无法成丸。当以SiO2作为抗黏剂时,调整湿度后,能够顺利成丸。所以选用SiO2作为抗黏剂。
2.3 工艺因素对丸芯成型性的影响
2.3.1 挤出速度的影响 固定滚圆速度为1 200 r/min,滚圆时间为3 min,分别以960,1 080,1 200 r/min的挤出速度制备微丸,综合考察多项指标,结果如表2~3。
从粒径分布(表2)来看,3批次微丸的粒径都主要集中在0.71~0.9 mm。但当挤出速度为960 r/min时,0.71~0.9 mm范围内微丸达到90.3%,明显高于挤出速度为1 080 r/min时的72.4%和1 200 r/min时的75.4%。由圆整度(表3)可知,根据短长径之比反映出的微丸圆整程度,随着挤出速度的增大,微丸的圆整度逐渐降低。
2.3.2 滚圆速度的考察 固定挤出速度为960 r/min,滚圆时间为3 min,分别以960,1200,1 320 r/min的滚圆速度制备微丸,结果如表2~3。
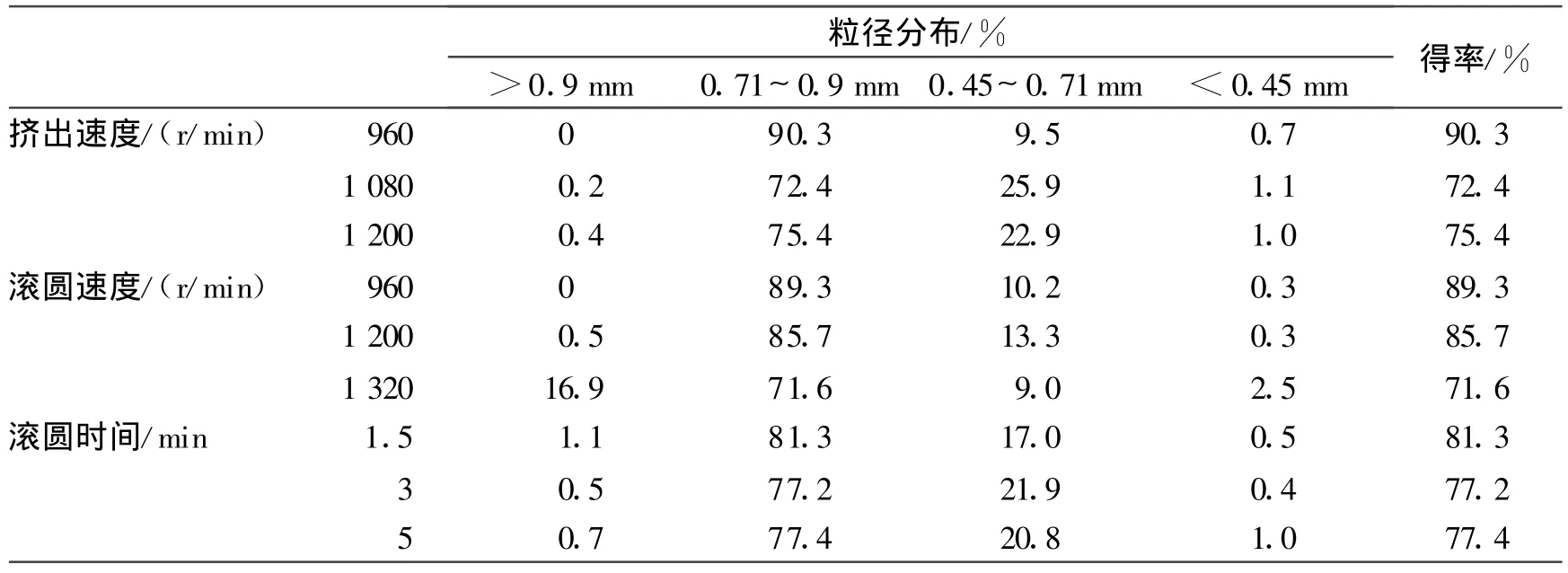
表2 制备工艺对粒径分布的影响Tab.2 The influence of processing on the size distribution
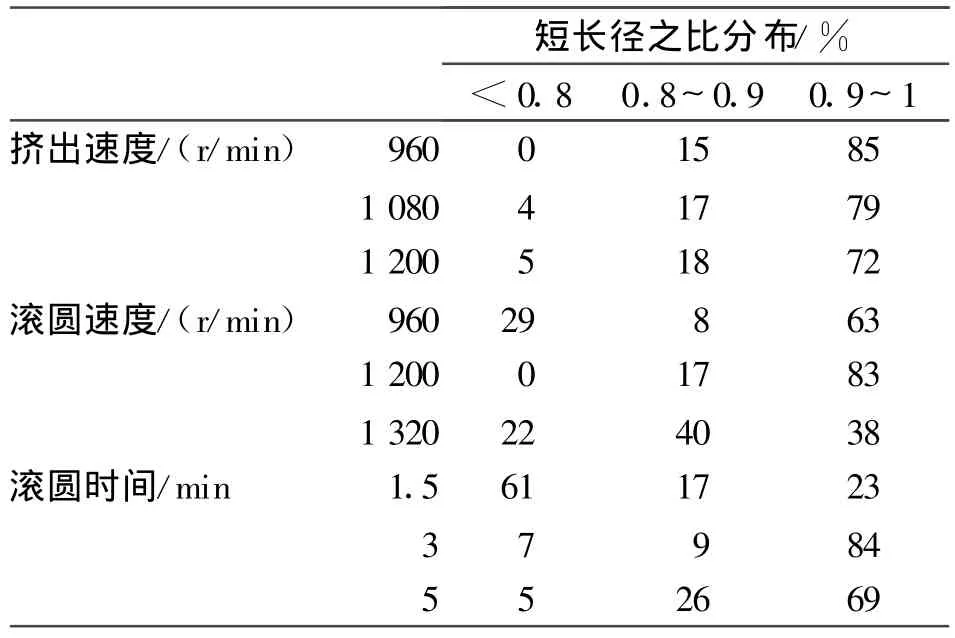
表3 制备工艺对圆整度的影响Tab.3 The influence of processing on the spherical degree
从表2可知,随着滚圆速度的增加,粒径的分布更加分散,微丸的得率逐渐降低。因为滚圆速度越大,滚圆时切割的速度就越大,粒径的分布就越不均匀。由表3可知,在滚圆速度1 200 r/min时,80%以上微丸的长短径之比都在0.9~1之间,960和1 320 r/min时在此范围分别为63%和38%,说明滚圆速度对微丸的圆整度有较大影响。
2.3.3 滚圆时间的考察 固定挤出速度为960 r/min,滚圆速度为1 200 r/min,分别以滚圆时间为1.5,3,5 min制备微丸。从表2可知,滚圆时间为1.5,3,5 min时,粒径分布较为相似,说明滚圆时间的长短对微丸粒径分布影响不大。而由表3可知,1.5 min时微丸短长径之比大部分分布于0.8以下,而3和5min主要分布于0.9~1,分别为84%和 69%,说明滚圆时间过短和过长均降低微丸的圆整度。
2.3.4 正交试验优化制备工艺 选择MCC作为填充剂,40%乙醇作为黏合剂,SiO2作为抗黏剂,选择对微丸质量影响较显坐的3个工艺因素作为考察对象,即挤出速度(A)、滚圆速度(B)、滚圆时间(C),每个因素选振3个水平,按正交试验表L9(34)安排实验,以圆整度和得率为评价指标,采用综合评分法对考察结果进行方差分析,筛选最佳工艺参数。综合得分f=得率评分×0.6+圆整度得分×0.4,评分越高越符合微丸质量控制要求。结果见表4。
3个因素R值排列顺序为B>C>A,对微丸质量影响最明显的是B,即滚圆速度。对于因素A而言,K2值最大,即最佳挤出速度为1 080 r/min,同理可知最佳滚圆速度为960 r/min,最佳滚圆时间为5 min。
2.4 包衣处方墩微丸释放行为影响的考察
2.4.1 隔离层对微丸溶出的影响 以1.5%的HPMC K4M25 mL与水25mL的混合溶液为隔离层,先包隔离层,再包肠溶层,考察隔离层对微丸溶出的影响。结果见图1。
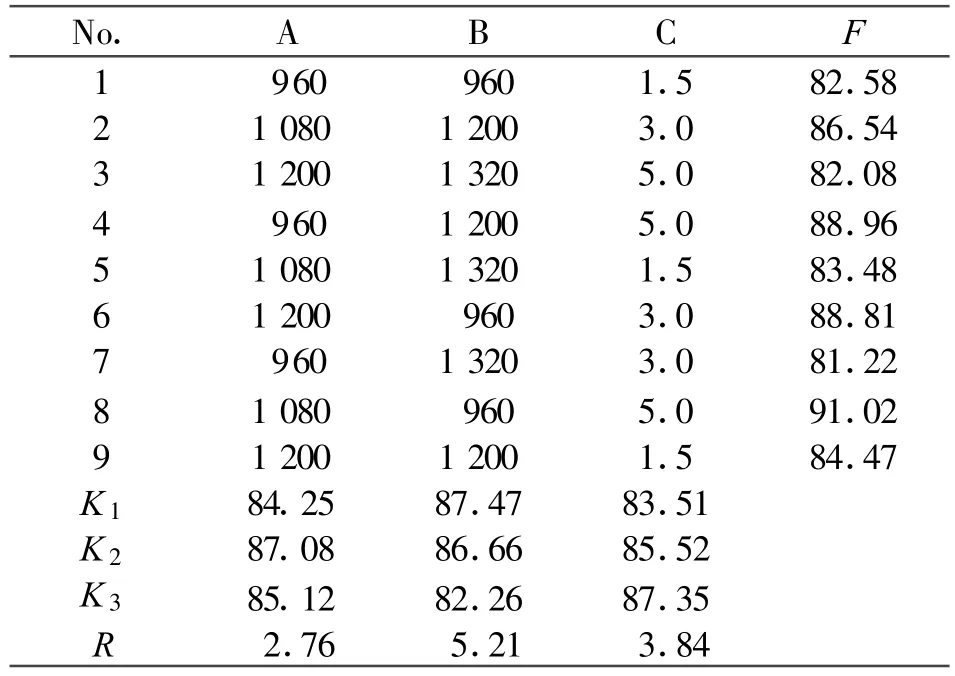
表4 正交试验考察结果Tab.4 The result of orthogonal experiment
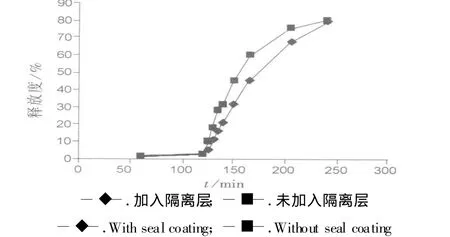
图1 隔离层对微丸溶出的影响Fig.1 The influence on the pellets release of isolation layer
以累积释放百分率(Mt/M∞)对时间t作释药曲线,计算相似系数。使用隔离层与不使用隔离层的f2>50,两条曲线之间没有明显差别。但不使用隔离层在制作工艺上要简便很多,因此采用不加入隔离层的方法制备包衣微丸。
2.4.2 骨架材料与致孔剂比例对微丸溶出的影响
以EC作为骨架材料,Eudragit L作为致孔剂。固定增塑剂用量、包衣增重不变,考察了EC∶Eudragit L的比值分别为为25∶75,35∶65,45∶55三个水平对释药行为的影响,结果见图2。
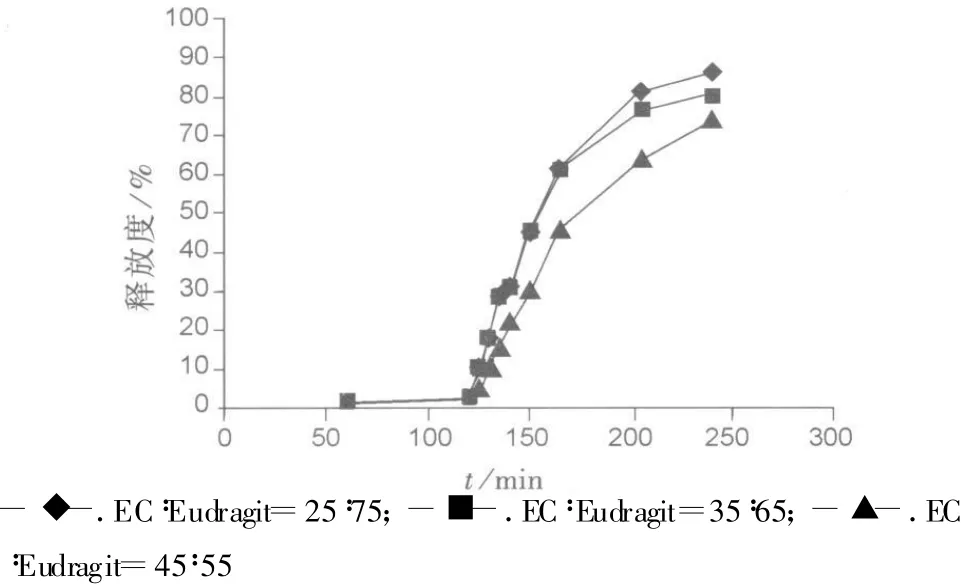
图2 骨架材料与致孔剂用量对微丸影响Fig.2 The influence of ratio of skeletal material to pore-forming agent
计算曲线间f2值分别为75.2,48,46.6。在固定增塑剂用量不变的情况下,随着EC含量增加,致孔剂含量减少,药物释放速率变慢,随着致孔剂含量增大,药物释放速度加快。曲线EC∶Eudragit L=45∶55与另外两条曲线有明显差别,药物释放速度明显变慢,2 h后未达到最大释放。曲线EC∶Eudragit L=35∶65与曲线 EC∶Eudragit L=25∶75相似(f2>50),因Eudragit价格较高,最终两者比例选择为35∶65。
2.4.3 增塑剂用量对微丸溶出的影响 以聚乙二醇为增塑剂,保持EC∶Eudragit L的比值及包衣增重不变,考察增塑剂用量(分别为0%,0.86%,1.71%)对微丸溶出的影响。结果见图3。
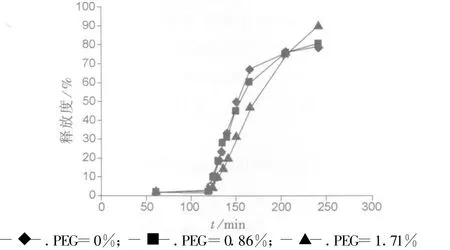
图3 增塑剂用量对微丸溶出的影响Fig.3 The influence on the release of plasticizing agent
增塑剂可以提高薄膜的柔韧性,有助于喷雾液滴在微丸表面铺展和相互结合,有利于完整薄膜的形成。对于水分散体而言,增塑剂的作用更加突出,它能降低聚合物的最低成膜温度,使聚合物中的乳胶粒在包衣操作温度下或包衣后热处理过程中融合成致密的薄膜。依据上述公式,当增塑剂为0%和0.86%时,两条曲线的 f2=68.7,两曲线基本重合,并且释放速度较快,说明在PEG≤0.86%时,还不足以将聚合物的最低成膜温度降到操作温度(40℃)以下,难以形成致密而又均一的衣膜;当将增塑剂的用量升至1.71%时,释放曲线比较平缓,并且在2 h内最大释药量达到90%。因此最终选择增塑剂用量为1.71%。
3 讨 论
本实验用挤出滚圆法制备了含药丸芯,利用流化床包衣技术进行了肠溶包衣,制备了炎琥宁肠溶微丸。经过工艺的单因素考察和正交试验,发现挤出速度1 080r/min,滚圆速度960 r/min,滚圆时间5 min,可以制得圆整度较好,得率较高的含药微丸。由微丸释放行为的考察结果可知,无需加入隔离层,EC∶EudragitL=35∶65,增塑剂含量为1.71%时 ,炎琥宁肠溶微丸的释放符合预期的释放特征。
[1]王宝灿,岳彩连.炎琥宁治疗病毒性肺炎38例疗效观察[J].山东医药,2004,44(31):48.
[2]吴斌.98例注射用炎琥宁不良反应分析[J].安徽医药,2007,11(5):473-474.
[3]王文刚,崔光华.挤出-滚圆制微丸工艺的进展[J].中国新药杂志,2001,10(9):661-664.
[4]张汉利,魏友霞,罗俊,等.炎琥宁注射液在不同输液中的稳定性[J].医药导报,2004,23(9):692.
[5]刘军田,陈修毅.缓控释骨架片药物体外释放行为的评价方法[J].齐鲁药事,2005,24(3):178-179.
[6]刘自远,刘成福.综合评价中指标权重系数确定方法探讨[J].中国卫生质量管理,2006.13(2):44-46.
[7]张娜,黄桂华.肺靶向炎琥宁明胶微球的制备[J].中国药学杂志,2006,41(6):438-441.
[8]Möschwitzer J,Müller R H.Spray coated pellets as carrier system for mucoadhesive drug nanocrystals[J].Eur J Pharm Biopharm,2006,62(3):282-287.
[9]中国药典[S].二部.2005:附录73-附录75.
[10]卢远东,曹国富.炎琥宁的稳定性研究[J].时珍国医国药,2006,17(3),374-375.
[11]Wang Y C,Hu G H.Efficacy of natrikalite dehydrographolid succinates pro injection in the treatment of children acute upper respiratory infection[J].J Pediatr Pharm,2003,9(5):392-401.
