“溶解度曲线”中考题赏析
2010-07-19张大臣
张大臣
(山东省滕州市教学研究室 山东 滕州 277500)
以溶解度曲线为载体,考查对化学图像的识别和分析,是每年中考必考的题目。如何理解溶解度曲线的意义以及运用曲线的相关规律解题呢?
一、溶解度曲线的意义
1.点的意义
(1)同一物质在不同温度时溶解度的数值大小。
(2)不同物质在同一温度下溶解度数值的大小。
(3)若两种物质的溶解度曲线相交,则表明在某温度下这两种物质的溶解度相等,进而可以知道该温度下两物质的饱和溶液的溶质质量分数相同。
2.线的意义
(1)线即溶解度曲线,表明物质的溶解度随温度变化的趋势。
(2)常见的溶解度曲线随温度变化的趋势有三种类型,我们分别称之为“陡升型”、“缓升型”和“下降型”,表明物质的溶解度受温度变化的影响大小的不同。代表物质分别有KNO3、NaCl、Ca(OH)2。
(3)可以根据变化趋势来确定混合物分离的方法。
3.面的意义
曲线下面的各点表示溶液为不饱和溶液;曲线上面(含曲线本身)的各点表示溶液为饱和溶液。
还可以通过溶解度曲线来确定饱和溶液与不饱和溶液相互转化的措施。
二、中考题目赏析
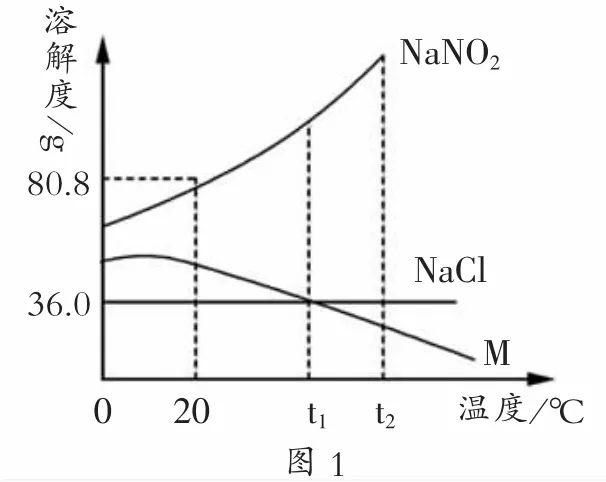
例:(2009 年连云港)NaNO2(亚硝酸钠)、NaCl和物质M(不含结晶水)的溶解度曲线如图1所示,请根据图像和有关信息回答下列问题:
(1)t2℃时,NaNO2、NaCl和 M 的溶解度由大到小的顺序是___。
(2)如图2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊 (不考虑水分蒸发)。请判断:该饱和溶液中的溶质是 NaNO2、NaCl和M中的____。
(3) 分 别 将NaNO2、NaCl 和 M的饱和溶液从 t2℃降温到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是____。
(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故。为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息:NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃。
①小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10mL水 (水的密度近似看作1g/cm3),用玻璃棒充分搅拌后观察。你认为此方案是否可行 ________(填“可行”或“不可行”)。
②该小组其他同学又设计出与小明不同的实验方案,并获得成功。你认为该方案可能是_______________(只填写一种方案并简单叙述)。
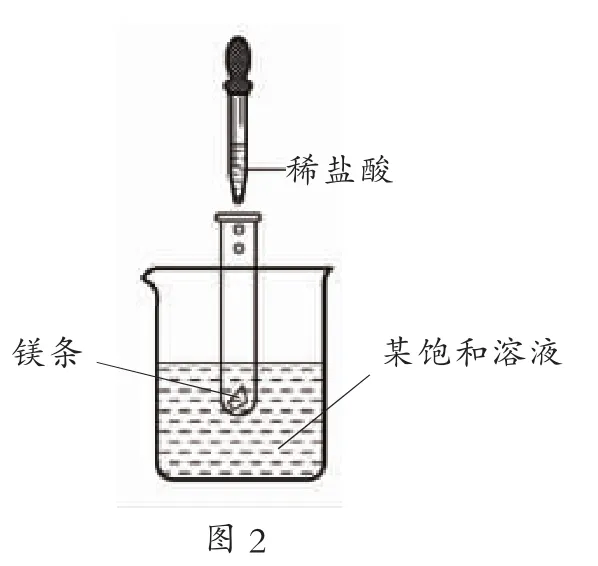
解析:(1)比较不同物质的溶解度大小必须在同一温度下。通过对比t2℃时三种物质纵坐标的数值大小即可。(2)溶解度曲线,本身就是表明物质的溶解度受温度影响变化的趋势。图2实验现象说明该饱和溶液的溶质的溶解度随温度的升高而降低,当温度升高时,就会有溶质析出使溶液变浑浊。
(3)对于某一温度下的饱和溶液,设其溶质的溶解度为Sg,则该饱和溶液的溶质的质量分数w=S/(100+S)×100%=1/(100/S+1)×100%。 当比较不同溶质在同一温度下所形成的饱和溶液的溶质的质量分数时,由上式可知,质量分数随溶解度增大而增大,随溶解度减小而减小。在t2℃时溶解度NaNO2>NaCl>M,所形成的饱和溶液的溶质的质量分数 NaNO2>NaCl>M。将 NaNO2、NaCl和M的饱和溶液从 t2℃降温到t1℃时,NaNO2和NaCl的溶液仍是饱和溶液,且t1℃时溶解度NaNO2>NaCl,则质量分数 NaNO2>NaCl。 而对于 M,从 t2℃降温到t1℃时,其溶解度随温度降低而升高,那么溶液就由饱和溶液变为不饱和溶液,但溶质和溶剂的质量没有变化,所以溶质的质量分数保持不变。在t1℃时,由于NaNO2和NaCl的溶解度仍大于t2℃时M的溶解度,所以溶质的质量分数NaNO2>NaCl>M。
(4)可以根据NaNO2和NaCl的不同性质进行鉴别。①由图1的溶解度曲线可知,在20℃时NaNO2的溶解度为 80.8 g,10 g 水足可以溶解8.08 g 的 NaNO2(饱和溶液);在 20℃时 NaCl的溶解度为 36.0g, 10 g 水最多能溶解 3.60 g 的 NaCl(饱和溶液)。所以在20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10 g水,用玻璃棒充分搅拌后可观察到NaNO2完全溶解而NaCl部分溶解,从而将二者区分开。②还可以利用二者的熔点或者水溶液酸碱性的不同进行鉴别。
答 案 :(1)NaNO2>NaCl>M (2)M (3)NaNO2>NaCl>M (4)① 可行 ②分别取少量的NaNO2、NaCl固体于两支试管中,用酒精灯加热,熔化者为NaNO2,不熔者为NaCl(或分别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl)(或其他合理答案)
