微波消解在茶叶和土壤稀土元素与重金属元素分析中的应用
2010-07-14谭和平张玉兰陈能武王晓玲
谭和平,吕 昊,高 杨,张玉兰,陈能武,王晓玲,唐 宇
(中国测试技术研究院,四川 成都 610021)
1 引 言
微波消解技术自从应用到样品的前处理过程中就受到广泛的关注,不少国家都将其作为样品前处理的首选方法写入到各种检测标准中。这些标准根据分析物性质、待测元素的差异以及后续分析测定方法的不同而对前处理方法做了相应修正。这些标准涉及到水[1-7]、食品[8-13]、土壤[14-21]等方面。微波消解具有三个完全不同于传统电炉加热方式的优势:①体加热(即从物质内部加热而具有极高的热转化效率);②过热现象(即物质内部热量来不及散失而使温度可能高于其沸点的现象);③搅拌作用(由于极性分子的快速方向变换,加剧了分子间的相互作用,使得反应速度显著加快)。
重金属对人体健康具有很大的危害性,与此同时Chen Z Y[22]研究发现了稀土元素的骨积蓄性、毒性以及对人体健康的危害。因此该文运用微波消解技术,辅以ICP-MS对茶叶及土壤中稀土元素和重金属元素以及部分尚未受到重视的有害元素进行了测定试验。
2 试验与方法
2.1 主要试剂
超纯水(电阻率≥18MΩ·cm),HNO3,HCl,H2O2,HF(优级纯,并经酸纯化仪纯化);土壤标准物质(GBW 07405),茶叶标准物质(GBW10016),0.5%TMAH,稀土元素及 In,Rh,Re,Ag,Te,I,As,Hg,V,Cr,Co,Se,Cd,Ni,Rb,Tl,Ba,Pb,Sr标准储备液(国家钢铁研究总院)。Ag以 2%HNO3配制单标曲线,I以0.5%TMAH配制单标曲线[23],其余待测元素以2%HNO3配制混标曲线。
2.2 主要仪器
ICP-MS(X Series,ThermofisherScientific,USA),微波消解仪(Mars X,CEM,USA),电子天平(BP211D,Satorius,Germany),超纯水发生器(Milli-Q Synthesis,MILLIPORE,USA),试剂纯化系统(Analab,France)。
2.3 仪器条件
ICP-MS经预热、调谐后,以表1所示条件测定样品,每次测定重复3次。内标选择的依据为:质量数51~89以 103Rh为内标;107~137以 115In为内标;139~208以180Re为内标。内标从旁路进样。

表1 ICP-MS工作条件
2.4 样品处理
对于土壤样品,称取约0.25 g样品,加入9 mL HNO3,1mL HCl及 3mL H2O2,按照表 2 工作条件进行微波消解,采用6个平行样品,同时做试剂空白。消解完成后,将样品转移至三角瓶中,在160℃条件下赶酸40min。完全冷却后,以超纯水定容至25mL。作为方法对照,同样称取约0.25g样品,9mL HNO3,1mL HCl及3mL H2O2,于240℃电热板消解6h。期间补加 6mL HNO3,1mL HCl及 2mL H2O2,并做试剂空白。消解完成后,于160℃赶酸50min。冷却后,以超纯水定容至25mL。

表2 微波消解工作条件(土壤)
对于茶叶样品,称取约0.5 g样品,加入6mL HNO3及2mL H2O2,按照表3工作条件进行微波消解,采用6个平行样品,同时做试剂空白。消解完成后,将样品转移至三角瓶中,在160℃条件下赶酸40min。完全冷却后,以超纯水定容至25mL。作为方法对照,同样称取约0.5 g样品,先加入6 mL HNO3,1 mL HCl浸泡2h后再加入3mL H2O2,于240℃电热板消解3h。期间补加2mL HNO3,0.5mL HCl及1mL H2O2,同时做试剂空白。消解完成后,于160℃赶酸50min。冷却后,以超纯水定容至25mL。

表3 微波消解工作条件(茶叶)
3 结果与讨论
3.1 检出限
对试剂空白连续测定11次,取其3倍样本标准偏差值作为相应方法的检出限。见表4、表5,As,Se,V,Cr,Co 分别受 75ArCl,16O+66Zn,51ClO,1H+51V和1H+58Ni较为严重的干扰而致检出限较高。其余元素的检出限都达到了pg·g-1水平。

表4 微波消解法在土壤和茶叶样品中的应用1)
3.2 准确度实验
将测定值与标称值相比较,见表4、表5。微波消解和电热板消解都能达到样品处理的要求,说明测定方法是可靠的。但敞开体系的电热板法因为难于克服元素在加热时的挥发,对一些热稳定性差且含量极低的元素处理结果不理想。如茶叶中干物质含量为3.8ng·g-1的 Hg,电热板消解法所得结果为 2.5ng·g-1,为标称值的65.8%;茶叶中的As测定为0.07μg·g-1,为标称值0.09μg·g-1的77.8%。

表5 电热板消解法在土壤和茶叶样品中的应用1)
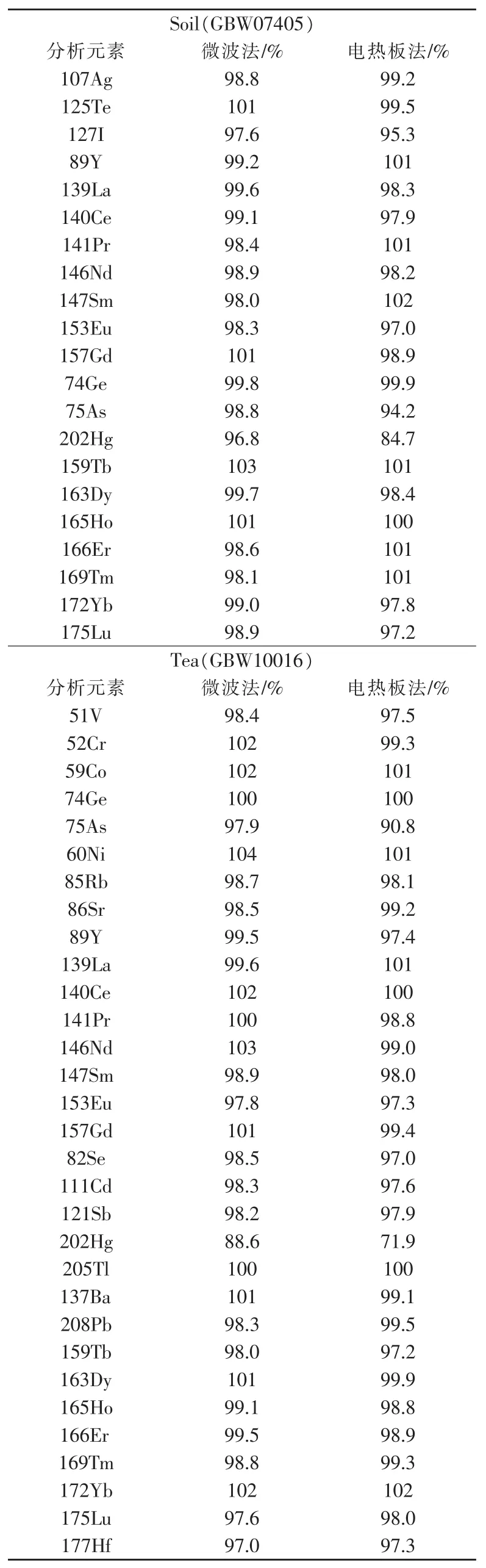
表6 回收率实验结果
3.3 精密度实验
将各样品的6次测定值求算RSD%,检验测定结果的精密度水平,见表4、表5。精密度实验的结果表明测定方法是稳定的,也进一步说明消解方法是基本稳定的,且微波消解法的精密度好于电热板消解法,可能是因为微波消解法是密闭系统,受热均匀,几乎不受外界环境因素干扰。
3.4 回收率实验
为了进一步对微波消解方法进行考察,取茶叶和土壤样品进行回收率实验。同样用电热板消解法与其对比,结果见表6。
由表6可以看出,不论是微波消解法还是电热板消解法,都适用于性质稳定的稀土元素的前处理(回收率在97.0%~104%之间);对于Hg,电热板法对茶叶样品处理结果准确度达不到要求,其回收率已经没有意义。对于另外两个容易受到挥发影响的元素As和I,在电热板法的结果中回收率也明显降低。
4 结果与讨论
微波消解和电热板消解是目前应用最为广泛的两种样品前处理方法,通过该实验可以看出微波消解和电热板法都能满足土壤和茶叶中重金属与稀土元素消解的要求,但在消解含量极低且热不稳定的元素如As,I,Hg时,电热板消解存在一定的不稳定性。同时电热板法还具有高耗能、高耗时、高试剂消耗量、环境污染大、人工成本高等缺点。
微波消解法具有性能可靠、操作简便、处理过程快捷、高度自动化、低人力成本、低试剂消耗量、低能耗等显著优势,除了能满足目前所有已测定元素的消解要求外,其高压环境还为一些难于在常压下分解的物质消解提供了可能。
[1]ASTM D 4309-2002,Standard practice for sample digestion using closed vessel microwave heating technique for the determination of total metals in water[S].
[2]ASTM D 5513-1999,Standard practice for microwave digestion of industrial furnace feedstreams and waste for trace element analysis[S].
[3]EPA Method 3005A,Acid digestion of waters for total recoverable or dissolved metals for analysis by FLAA or ICP spectroscopy[S].
[4]EPA Method 3010A,Acid digestion of aqueous samples and extracts or dissolved metals for analysis by FLAA or ICP spectroscopy[S].
[5]EPA Method 3015,Microwave assisted acid digestion of aqueous samples and extracts[S].
[6]EPA Method 3020A,Acid digestion of aqueous samples and extractsfortotalmetalsforanalysisby GFFA spectroscopy[S].
[7]EPA Method 2002,Sample preparation procedure for spectrochemical determination of total recoverable elements[S].
[8]GB/T 23870-2009,蜂胶中铅的测定微波消解-石墨炉原子吸收分光光度法[S].
[9]SN/T 2208-2008,水产品中钠、镁、铝、钙、铬、铁、镍、铜、锌、砷、锶、钼、镉、铅、汞、硒的测定 微波消解-电感耦合等离子体-质谱法[S].
[10]BS EN 15505:2008,Foodstuffs-determination of trace elements-determination of sodium and magnesium by flame atomic absorption spectrometry (AAS) after microwave digestion[S].
[11]DIN EN 14084:2003,Foodstuffs-determination of trace elements-determination of lead,cadmium,zinc,copper and iron by atomic absorption spectrometry(AAS) after microwave digestion[S].
[12]NF EN 14332:2004,Foodstuffs-determination of trace elements-determination of arsenic in seafood by graphite furnace atomic absorption spectrometry(GFAAS) after microwave digestion[S].
[13]AOAC Official Method 999.10,Lead,Cadmium,Zinc,Copper, and iron in foods.Atomic absorption spectrophotometry after microwave digestion[S].
[14]DB 37/T 1305-2009,土壤中重金属微波消解快速测定方法[S].
[15]ASTM D 5258-2002,Standard practice for acidextraction ofelements from sediments using closed vessel microwave heating[S].
[16]EPA Method 3050B,Acid digestion ofsediments,sludges,and soils[S].
[17]EPA Method 3052,Microwave assisted acid digestion of siliceous and organically based matrices[S].
[18]EPA Method 3546,Microwave extraction[S].
[19]EPA Method 3200,Mercury species fractionation and quantification by microwave assisted extraction,selective extraction and/or solid phase extraction[S].
[20]EPA Method 3051A,Microwave assisted acid digestion of sediments,sludges,soils,and oils[S].
[21]EN 13656:2002,Characterization of waste-microwave assisted digestion with hydrofluoric (HF),nitric(HNO3),and hydrochloric (HCl) acid mixture forsubsequent determination of elements[S].
[22]Chen Z Y,Zhu X D.Accumulation of rare earth elements in bone and its toxi city and potential hazard to health[J].Journal of Ecology and Rual Environment,2008,24(1):88-91.
[23]BS EN 15111:2007,Foodstuffs-determination of trace elements-determination of iodine by ICP-MS(inductively coupled plasma mass spectrometry)[S].
