抗乙肝病毒相关疾病的药物研究概况
2010-04-24姜俊
姜 俊
乙型肝炎是当今国际公认的治疗难题,全世界大约有20亿乙型肝炎病毒(hepatitis B virus,HBV)感染者,其中3.5亿~4亿为HBV慢性感染者[1,2]。而我国就有1.3亿HBV携带者,占全球三分之一[3]。HBV慢性感染可引起慢性乙型肝炎(chronic hepatitis B,CHB)、肝硬化(liver cirrhosis,LC)和原发性肝细胞癌(hepatocellular carcinoma,HCC)等相关疾病,全球每年死于乙肝病毒相关疾病者约为50万~120万人[4]。乙型肝炎病毒感染严重危害着人类健康,乙型肝炎的治疗已成为世界各国共同关心的问题。
1 乙型肝炎病毒
1.1 乙型肝炎病毒的形态和结构 1970年,Dane发现了乙型肝炎完整的病毒颗粒,称Dane(丹氏)颗粒,是目前所发现的最小的具有复制功能的DNA病毒。完整的乙肝病毒颗粒(Dane颗粒)是由双层外壳和一个核心组成的,核心直径为27 nm,是由240个核心抗原分子装配而成的正20面体结构,包装有病毒基因组DNA和DNA聚合酶。核心颗粒外包厚度为7 nm的外壳,外壳是由脂质双层和蛋白质组成的囊膜。脂质双层内含有S抗原、前S1和前S2抗原,它们一起又构成了外壳上大、中、小三种蛋白形式,统称为乙肝表面抗原(HBsAg)。其结构见乙型肝炎病毒结构示意图1。
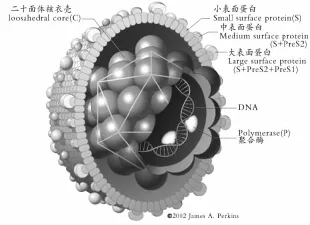
图1 乙型肝炎病毒结构示意图
1.2 乙肝病毒的复制[5-7]乙型肝炎病毒侵入机体后,在肝细胞内进行复制繁殖。乙型肝炎病毒基因组DNA在肝细胞核内进行复制,转录,在合成核心颗粒后,被转运到肝细胞浆内,再包上外衣壳成为病毒体,并以发芽的形式释放出肝细胞。在复制过程中,外壳的数量总比核心为多,过剩的病毒外壳就释入血中,以小球形或管形颗粒的形式存在于血液循环中。此即在血清中查到的表面抗原。
在乙型肝炎病毒基因组的复制过程中,有两个很重要的因素:一个是“催化剂”,另一个是“模板”。乙型肝炎病毒的基因组(DNA)是由两条螺旋的DNA链围成的一个环形结构。其中一条较长负链已经形成完整的环状;另一条长度较短的正链,呈半环状。在感染肝细胞之后,这条半环状的DNA链就会以负链为模板,在催化剂—乙肝病毒DNA聚合酶的作用下延长,最终形成完整的环状。这时的乙肝病毒基因组就形成了一个完全环状的双股DNA,即共价闭合环状DNA(cccDNA),可以把它看作是病毒复制的原始模板。模板形成后,病毒基因会以其中的一条cccDNA为模板,利用肝细胞基因中的酶和DNA聚合酶的催化,一段基因又一段基因地复制,形成负链和正链。最后再装配到一起形成新的乙肝病毒DNA颗粒。
2 抗HBV药物的作用靶点[8]
抗HBV药物的作用靶点大体可分为以下两种。
2.1 特异性的干扰病毒蛋白质的功能 高效低毒的抗病毒药物应当选择性的抑制病毒复制,而不干扰宿主细胞和机体的正常功能。从这个角度来讲,特异性的干扰病毒蛋白质的功能是抗病毒药物研究的一个重要方向。研究内容主要包括:①HBV DNA聚合酶:目前,临床应用和正在开发阶段的抗HBV药物多以HBV DNA聚合酶为靶点;②病毒核心颗粒的装配:这是一个由多种病毒和细胞蛋白及病毒前基因组RNA参与的极其复杂的多分子相互作用过程,因此也是一个很受关注的靶点。
在抗HBV药物的实验研究和临床研究中发现,HBV DNA聚合酶抑制剂尽管可显著抑制病毒DNA复制,但对改变病毒感染细胞中cccDNA水平无明显作用,因此当停药后病毒复制反跳。这表明cccDNA要么非常稳定,要么是由于目前的DNA聚合酶抑制剂效能较差,并不能完全阻断病毒DNA复制,而极少量DNA复制则足以维持细胞核内cccDNA库稳定。这就要求一方面研发更为高效的DNA聚合酶抑制剂,另一方面应当深入研究cccDNA合成的生物化学机制,寻找新的可供药物作用的分子靶点。
2.2 激活和重建抗病毒免疫应答 近年来对HBV感染的免疫病理机制的研究表明,强且多特异性的CD4+和CD8+T淋巴细胞免疫反应可清除HBV感染,而HBV慢性持续性感染是机体病毒特异性细胞免疫功能低下或发生免疫耐受所致。因此,如何激活和重建慢性乙型肝炎患者的抗病毒免疫应答系统,调动机体内部因素以清除病毒感染应当是一种重要的治疗手段。
3 乙型肝炎的预防与治疗
3.1 乙型肝炎疫苗 简称“乙肝疫苗”。分为血源性乙肝疫苗和基因工程乙肝疫苗。由于基因工程疫苗可工业化生产,成本低廉,得到推广和应用。它既可用于阻断母婴传播,又可用于HBsAg阴性的不同年龄的HBV易感者的预防。但上述疫苗也存在不完善之处,如注射期较长,影响疫苗的覆盖率;约有10%的健康人群,尤其是老年人对疫苗应答情况欠佳等,而且一旦HBV发生变异,即可逃过现有疫苗的保护[9,10]。
目前国内外正致力于研制新一代疫苗,临床应用证实它能诱导更高的血清阴转率和机体应答。新型乙肝核酸疫苗、乙肝-丙肝、乙肝-流感等多价联合疫苗、多肽疫苗、口服乙肝疫苗等也在研制中。
3.2 抗HBV药物 当前用于治疗乙肝病毒的药物主要分为核苷类药物、非核苷类药物、中草药和免疫调节剂等。
3.2.1 临床中应用的抗HBV药物 虽然乙型肝炎病毒的发现距今已有30多年,但对慢性肝炎的治疗仍然没有取得令人满意的进展。目前经FDA批准用于慢性乙型肝炎治疗的抗病毒药物仅有干扰素、拉米夫定、阿德福韦和恩替卡韦4种。这4种药物的疗效均有一定局限性。
干扰素(IFN)。α干扰素(IFN-α)是被FDA最早批准的用于治疗慢性乙型肝炎的药物,迄今在临床上已经使用了20多年。IFN-α具有抗病毒、免疫调节及抗增殖作用。其抗HBV作用的机制,不是直接作用于病毒而是通过与同种靶细胞膜上的特异性受体结合后产生的。受体与IFN-α结合后,发生构型变化,通过一系列酶促反应,向细胞核内传递信息,使细胞的IFN激活基因(ISGs)被激活,在细胞内合成数种“抗病毒蛋白”,建立起抗病毒状态。同时,IFN-α还具有较强的免疫调节作用,使患者免疫系统对HBV感染细胞的识别和清除能力增强。长效IFN(Peg-IFN)是第二代IFN,系IFN-α与聚乙二醇的结合物。Peg-IFN半衰期较长,可在体内较长期维持有效的血药浓度,每周只需注射1次,用药方便[11]。
拉米夫定(lamivudine,3TC)。 拉米夫定化学名2′3′-二脱氧-3′-硫代胞嘧啶,是治疗艾滋病的核苷类HIV逆转录酶抑制剂。1998年,在美国、加拿大等10多个国家和地区相继批准用于治疗慢性乙型肝炎。其主要作用机制是抑制HBV聚合酶,从而抑制HBV的增殖。是目前对慢性乙型肝炎治疗最有效的一线药物[12]。临床研究显示,尽管拉米夫定治疗可很快使患者血清HBV DNA水平降低,但由于该药不能清除细胞内HBVcccDNA的复制,如果在血清HBeAg转阴之前停药,病毒复制则会很快反跳,因此必须进行长期治疗,期望在长期抑制病毒复制的基础上,宿主能清除cccDNA[13]。而长期应用会诱导HBV产生耐药性,研究发现,耐药性的产生与病毒多聚酶编码区变异相关,变异导致YMDD(酪氨酸-甲硫氨酸-天冬氨酸-天冬氨酸)基序中甲硫氨酸(M)被缬氨酸(V)或异亮氨酸(I)替代,该部位正是拉米夫定干扰HBV复制的结合位点,YMDD变异导致拉米夫定无法与之结合,丧失了抗病毒活性[14,15]。 阿德福韦酯(adefovir dipivoxil,ADV),恩替卡韦(entecavir,ETV)也是这一类的代表性药物。
核苷类抗病毒药物是竞争性抑制剂,提高药效、降低毒性和抗耐药性是新型核苷类药物的研究方向。依据作用机制、药物靶点和代谢途径设计新类似物或对已知活性物的碱基和糖环进行修饰是该类药物研究的主要策略[16]。
3.2.2 中草药有效成分及单味中草药 我国治疗慢性乙型肝炎的长期实践中,发现一些天然药物及天然药物提取物具有抗HBV作用,如叶下珠、甘草酸、苦参素或氧化苦参素、猪苓多糖、云芝多糖等[17-19]。但其作用机制仍缺乏深入系统的研究,抗HBV疗效也需进一步严格的双盲随机对照临床试验证实。
3.2.3 免疫调节剂 在慢性乙型肝炎发生的过程中,自身免疫作用不可忽视。目前已知,HBV持续感染与机体免疫功能尤其是细胞免疫功能不全有关。近年来,国内外研究较多的免疫调节药物包括细胞因子、胸腺衍生物和疫苗 (重组抗-HBV疫苗、基于脂多肽的T细胞疫苗、遗传性疫苗)等。免疫调节治疗在理论上具有意义,但其临床疗效有待进一步提高[20]。
综上所述,虽然抗HBV药物近年来取得了很大进展,但由于cccDNA不能彻底地被清除、病毒变异,如HBV的DNA聚合酶YMDD的突变、Pre-S基因的突变及患者的免疫耐受等原因,造成目前抗病毒治疗仅对一小部分患者有效,且复发率高,因此如何抑制病毒复制、减少基因突变、提高机体抗病毒的特异免疫功能、加强各种肝细胞抗病毒能力,防止复发以及开发作用于不同靶点的新型抗病毒药物是今后发展的方向[21]。
[1]Mohamadnejad M,Malekzadeh R.Hepatitis B[J].N Engl J Med,2004,350(26):2719.
[2]McMahon BJ.Selecting appropriate management strategies for chronic hepatitis B:who to treat[J].AmJ Gastroenterol,2006,101(5):7.
[3]刘胜洋,华维一,徐云根,等.抗乙肝病毒感染的核苷类药物研究现状[J].药学进展,2005,29(5):212-218.
[4]Lavanchy D.Hepatitis B virus epidemiology,disease burden,treatment,and current and emerging prevention and control measures[J].Viral Hepat,2004,11(1):97-107.
[5]陈鸿珊,张兴权.抗病毒药物及其研究方法.第1版.北京:化学工业出版社,2006.387.
[6]Man-Fung Yuen,Cling-Lung Lai.Treatment of chronic hepatitis B[J].The Lancet.Infectious Diseases,2001,1:232-241.
[7]Fabien Zoulim.Mechanism of viral persistence and resistance to nucleotide analogs in chronic Hepatitis B virus infection[J].Antiviral Research,2004,64:1-15.
[8]陈鸿珊,张兴权.抗病毒药物及其研究方法.化学工业出版社,2006,(6):388.
[9]戴泉力,张茂金.浅谈乙肝的预防与基因工程疫苗[J].中国药业,2003,12(2):44.
[10]吴 军,林 薇.马铃薯乙肝疫苗的研究新进展.国外医学免疫学分册,2001,24(6):33.
[11]邓 洪.慢性乙型肝炎抗病毒治疗的研究进展.国外医学内科学分册,2002,29(10):422.
[12]潘玉卿.慢性乙型肝炎治疗进展[J].世界临床药物,2004,25(11):668-673.
[13]陈鸿珊,张兴权.抗病毒药物及其研究方法.北京:化学工业出版社,2006,(6):390.
[14]Dienstag JL,Schiff ER,Wright TL,et a1.Lamivudine as intial treatment for chronic hepatitis B in the United States[J].N Engl J Med,1999,341(17):1256.
[15]Sokal EM,Robert EA,Mieli-Vergani G,et al.A dose ranging study of the pharmacokineties,safety,and preliminary efficacy of lamivudine in children and adolescent with chronic hepatitis B[J].Antimicrob Agents Chemiother,2000,44(2):590.
[16]刘 琨,谢 蓝.新型核苷类抗病毒药物的研究进展[J].药学学报,2006,41(8):689-693.
[17]张大志,郭树华,张定风,等.叶下珠制剂抑制乙型肝炎病毒作用的实验研究[J].现代医药卫生,2001,17(7):512-513.
[18]刘天灯,朱 琳,丁霞秋.苦参素联合阿昔洛韦治疗慢性乙型肝炎28例[J].中西医结合肝病杂志,2001,11(1):38-39.
[19]高耀华.猪苓多糖及基因乙肝疫苗抗乙肝病毒疗效观察[J].实用中医药杂志,2003,19(2):66.
[20]Sprengers D,Janssen HL.Immunomodulatory therapy for chronic hepatitis B virus infection[J].Fundam Clin Pharmacol,2005,19(1):17.
[21]吴剑涓.抗乙型肝炎病毒药物研究进展[J].天津药学,2006,18(2):49-52.
