Eu3+标抗原盐酸克伦特罗的时间分辨荧光免疫检测
2010-03-22樊晓博杨金易高秀杰吴英松孙远明雷红涛
樊晓博,杨金易,高秀杰,吴英松,孙远明,雷红涛,*
(1.西北农林科技大学食品科学与工程学院,陕西 杨凌 712100;2.广东省食品质量安全重点实验室,华南农业大学食品学院,广东 广州 510642)
Eu3+标抗原盐酸克伦特罗的时间分辨荧光免疫检测
樊晓博1,2,杨金易2,高秀杰2,吴英松2,孙远明2,雷红涛2,*
(1.西北农林科技大学食品科学与工程学院,陕西 杨凌 712100;2.广东省食品质量安全重点实验室,华南农业大学食品学院,广东 广州 510642)
采用时间分辨荧光免疫分析(time-resolved fluoroimmunoassay,TRFIA)建立简便、快速、灵敏的盐酸克伦特罗(clenbuterol hydrochloride,CBL)检测方法。以自制盐酸克伦特罗单克隆抗体包被96孔微孔板作为固相抗体,Eu3+标记抗原与样品中的CBL竞争结合抗体,建立直接竞争荧光免疫分析体系。猪尿、组织样品添加回收率实验表明:方法灵敏度为0.02μg/L,样品回收率为91%~101%,与沙丁胺醇、莱克多巴胺等结构类似物的交叉反应率均小于1%。建立盐酸克伦特罗铕标抗原直接竞争时间分辨免疫检测方法,方法灵敏度高、特异性强,且操作简单,完全可以满足现有实际检测需求。
盐酸克伦特罗;时间分辨;标记抗原;检测
盐酸克伦特罗(clenbuterol hydrochloride,CBL),俗称“瘦肉精”,是β-兴奋剂的一种[1],过量使用可提高畜类瘦肉率,而在可食用组织中CBL的残留对人体有相当大的毒性[2],尤其是残留于肝脏,并通过食物链危害人类健康[3],我国政府明令禁止其作为饲料添加剂使用[4],但受经济利益驱使,仍有一些不法商贩非法使用克伦特罗,致使克伦特罗中毒事件时有发生。因此,建立一种高效、简便、快速、灵敏的克伦特罗残留检测方法十分必要。
目前,针对动物组织和尿液中盐酸克伦特罗的检测方法主要有酶联免疫吸附法(ELISA)[5-6]、气相色谱-质谱法(GC-MS)[7-9]、高效液相色谱法(HPLC)[10]及高效液相色谱-质谱联用法[11]等。仪器法检测虽然检测精度高,但其检测过程繁琐、检测时间长、仪器昂贵等特点导致其不能进行高通量的筛查检测,通常用于阳性样品的确证。而免疫检测法灵敏度高、价格低、操作简单、样品通量高的特点使得其非常适合大规模的筛查检测[12]。时间分辨免疫技术(time-resolved fluoroimmunoassay,TRFIA)是基于抗原抗体的特异性反应,以稀土元素为信号放大标记物,结合抗原抗体反应的特异性和Eu3+标记信号的高灵敏度,可以实现违禁药物的痕量检测,应用前景十分广阔。与传统的酶免疫法(EIA)、发射免疫分析法(RIA)相比,它具有很多优点:灵敏度10-19mol/L,稳定性好,克服了酶和放射性荧光物质的不稳定性、动态范围宽、试剂货架期长、无放射性危害等缺点,时间分辨荧光分析目前被公认为是灵敏度最高的分析方法之一。
通过Eu3+标记抗体,其灵敏度为0.03μg/L[13],而本研究以稀土元素铕直接标记抗原,通过固相包被抗体,研究目的是建立Eu3+标抗原直接竞争TRFIA。通过Eu3+标记抗原,一方面减少铕标记抗体对抗体识别性能的下降,另一方面降低抗原与抗体的亲和力,从而进一步提高检测灵敏度。采用一步法竞争反应模式,建立具有快速、灵敏、特异、准确的盐酸克伦特罗违禁药物残留检测方法。
1 材料与方法
1.1 材料与试剂
盐酸克伦特罗、沙丁胺醇、莱克多巴胺、特布他林、卡布特罗、塞曼特罗和马不特罗(纯度大于99%)华南农业大学动物科学院;CBL-OVA(Ovalbumin)、抗CBL单克隆抗体 本实验室自制; 96孔微量反应板 雷博公司;Eu3+标记试剂盒(1244-302) 美国PE-Wallac 公司;CBL-ELISA试剂盒 德国拜发公司;阴性猪尿样广州市兽药监督所;其他试剂均为国产分析纯。
1.2 仪器与设备
恒温振荡器 上海智城分析仪器制造有限公司;1-13型快速离心机 Sigma公司;1575型洗板机 Bio-RAD公司;P200微量可调移液枪 吉尔森公司;KJ-201C型微量振荡器 江苏康健医疗用品有限公司;1235型TRFIA全自动分析仪 Wallac公司。
1.3 方法
1.3.1 CBL标准液的配制
CBL以标准品稀释液配制成质量浓度20mg/L的溶液,稀释到500μg/L作为标准贮备液。使用前配成质量浓度梯度0、0.1、0.3、0.9、2.7、8.1μg/L的CBL标准工作液。
1.3.2 Eu3+-CBL-OVA标记物的制备[14]
将0.5mg CBL-OVA加入到纯化离心柱中,8000r/min离心5~6min,加入200μL标记缓冲液,8000r/min离心,弃滤液,再加入200μL标记缓冲液,按上述方法离心重复5次。将离心管取出,弃滤液,把离心柱反转,2000~3000r/min离心1min,收集滤液,即为待标记物。标记物完成浓缩去杂质后,按10:1质量比将标记物和铕标记试剂充分混匀进行标记。按标记试剂盒说明,置4℃冰箱过夜,次日经过凝胶层析柱SephadexTMG25纯化,每管收集产物1mL,各管取50μL于96孔反应板中,加入荧光增强液200μL,室温振荡5min后测荧光值,以荧光值为纵坐标,管号为横坐标,绘制曲线。
1.3.3 固相包被抗体制备[15]
将CBL单克隆抗体用PBS缓冲液(pH7.2)稀释至1mg/L,96孔微孔板中各孔加入200μL,37℃放置过夜,弃去包被液,加入封闭液,每孔220μL,封闭3h。弃去封闭液,烘干,备用。
1.3.4 反应条件优化
以CBL单克隆抗体1:500、1:1000、1:2000、1:4000这4种稀释度包被,加入100μL标准品和100μL稀释度为1:2000的Eu3+-CBL-OVA标记物,确定最佳包被稀释度。用最佳的包被稀释度包板,加入100μL标准品和质量浓度分别为0.2、0.5、1.0、2.0mg/L的Eu3+-CBLOVA标记物,确定最佳铕标抗原的质量浓度。
1.3.5 一步法直接竞争TRFIA操作步骤
取包被好的板条,加入100μL CBL的标准品(或处理好的样品) 到相应的微孔中,加分析缓冲液稀释的Eu3+-CBL-OVA标记物100μL,室温振荡1h,用洗涤液洗6次,加200μL 增强液振荡5min 后测定荧光值。标准曲线计算样品中CBL的含量。
1.3.6 样品处理
将组织样品绞碎,取绞碎样品1g于离心管,加入5mL水,振荡5min,于沸水浴中加热至组织样品变色,5000r/min离心10min,取上清检测。尿样直接检测即可。
1.3.7 考察指标
灵敏度:计算标准曲线零质量浓度点8次重复的荧光值,CBL标准溶液质量浓度(0、0.1、0.3、0.9、2.7、8.1μg/L)的对数值为横坐标以抑制率为纵坐标绘制标准曲线,测定灵敏度。

式中:F为各质量浓度的荧光值;F0为零浓度的荧光值。
特异性:将CBL的结构类似物沙丁胺醇、莱克多巴胺、特步他林和卡布特罗配成不同质量浓度的溶液作为待测样品,采用直接竞争TRFIA检测,计算交叉反应率。

回收率:向阴性样品中分别加入添加不同质量浓度的CBL标准品,处理后用直接竞争TRFIA 进行浓度测定,每个质量浓度做3个平行测定。
1.3.8 与德国拜发ELISA试剂盒进行比较
分别用两种方法测定5份尿样样品,对结果进行比较。
2 结果与分析
2.1 Eu3+-CBL-OVA标记物的收集
Eu3+-CBL-OVA标记物经过凝胶层析柱SephadexTMG25纯化,收集纯化的标记物,由于Eu3+标记的抗原为大分子物质,先出峰,且比较集中,所以第一个荧光峰即为成功进行标记的抗体产物;后出峰的为游离Eu3+及其螯合物质。故收集第一洗脱峰(图1)。

图1 SephadexTMG25洗脱图Fig.1 Elution profile of europium labeled CBL-ovalbumin on SephadexTMG25 column
2.2 反应条件优化
抗原和抗体的质量浓度对免疫学检测方法的灵敏度和特异性有重要影响,因此有必要对合适的抗原和抗体质量浓度进行探索。
2.2.1 最佳抗体包被稀释度确定

图2 包被抗体稀释度曲线Fig.2 Dilution curve of the coating antibody obtained by direct competitive TRFIA
以最高荧光值(Fmax)、IC50和IC50/Fmax为综合参考指标,由图2可知,最高荧光值与抗体质量浓度成正比,抗体质量浓度过高时,抗体结合的铕标抗原过多,影响方法的灵敏度。包被抗体稀释度为1:2000时,IC50/ Fmax达到最低,这时检测方法灵敏度最高。当抗体稀释度为1:4000时,尽管IC50差别不大,但其Fmax太低,使表示灵敏度的IC50/Fmax也升高,因此选择稀释度1:2000为最佳包被抗体质量浓度。
2.2.2 最佳铕标抗原质量浓度确定
选择包被抗体稀释度为1:2000,选择不同质量浓度的铕标抗原做直接竞争TRFIA实验,结果如图3所示,随着铕标抗原质量浓度的降低,荧光值逐渐减小,IC50也相应降低,当铕标记物质量浓度为1mg/L时,IC50和IC50/Fmax均为最低,Fmax与其他铕标抗原浓度相比也处在最适宜的范围内,说明此质量浓度下反应体系的灵敏度最高,故选择1mg/L为最佳铕标抗原质量浓度。

图3 CBL-TRFIA铕标抗原质量浓度曲线Fig.3 Concentration curve of Eu3+labeled CBL-OVA obtained by direct competitive TRFIA
2.3 TRFIA方法的考核
2.3.1 方法灵敏度

图4 CBL-TRFIA标准曲线Fig.4 Standard curve for the TRFIA determination of CBL
在优化的反应条件下绘制标准曲线,如图4所示。以零剂量荧光值(F0)均值减2s后的计数率在标准曲线上得到的相应质量浓度为检测的灵敏度,灵敏度为0.02μg/L,IC50为0.29μg/L ,曲线的相关系数为0.995,说明方法线性关系良好。
2.3.2 方法的特异性
将CBL的结构类似物配成不同质量浓度的溶液作为被测样品,采用TRFIA方法进行测定,沙丁胺醇、莱克多巴胺、特步他林、卡布特罗、塞曼特罗、马不特罗的交叉反应率分别为0.12%、0.62%、0.34%、0.50%、0.29%、0.43%,抗体与几种药物交叉反应率很小,说明抗体特异性较高。
2.3.3 方法回收率
直接CBL-TRFIA的批内和批间变异系数(CV)分别为4.4%和8.1%,都符合批内CV<5%,批间CV<10%的要求。加标回收实验是评价ELISA、TRFIA等检测方法准确度的一个重要指标。由表1可见,添加量0.1、1.0、3.0、5.0μg/L的回收率都达到90%以上,变异系数在合适的范围内,说明该方法重复性好,用于样品分析较为准确。
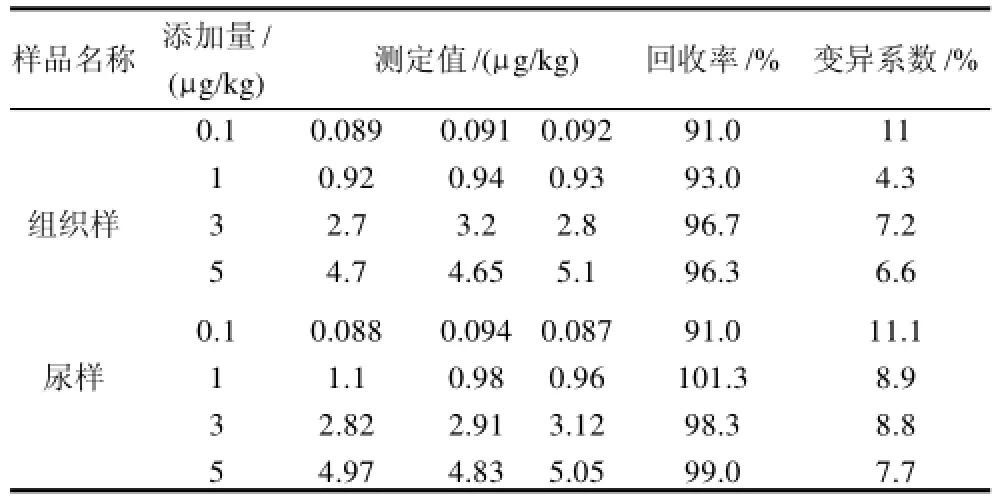
表1 回收率实验结果Table1 Spike recoveries of the developed TRFIA method for CBL in different matrix samples
2.4 方法的准确度
采用克伦特罗ELISA检测试剂盒,通过运用两种方法分别对5份已知质量浓度的尿样进行测定,结果见表2。由表2可知,两种方法对同一种样品的测定值接近,与样品实际浓度符合程度较高,说明实验建立的直接竞争TRFIA方法准确度较高,可以满足实际样品的检测需求。

表2 TRFIA与ELISA试剂盒测定样品结果比较(x±s,n=5)Table2 Results of TRFIA and ELISA determinations of known porcine urine samples (x±s,n=5)
3 结 论
成功建立铕标记抗原、包被抗体的直接竞争盐酸克伦特罗时间分辨荧光免疫分析法。该方法操作简单,稳定性高,灵敏性好,标准曲线显示该方法检测限为灵敏度为0.02μg/L,IC50为0.29μg/L,回收率在91%~101%,同时对实际样品检测结果与进口试剂盒所检测结果接近,与已有时间分辨方法相比,本方法检测速度快、灵敏度高、特异性强,且操作简单,完全可以满足现有实际检测需求,具有良好的应用前景。
[1]MERSMAN H J. Evidence of classicβ-adrenergic receptors inporcine adipocytes[J]. Jamin Sci , 2005, 74: 984-992.
[2]ANDREJ P, ALES O, SLAVKO P. Abuse of clenbuterol and its detection [J]. Curr Med Chem, 2003, 10(4): 281-290.
[3]CHURCHWEELL M I, HOLDER C L. Solid phase extraction of clenbuterol from plasma using immunoaffinity follow by HPLC[J]. J Pharm Biomed. Anal, 1999, 21(3): 635-639.
[4]中华人民共和国农业部. 关于发布《动物性食品中兽药最高残留限量》的通知农牧发[1997]17号[S]. 1997-09-04.
[5]HAASNOOT W, STREPPEL L, CAZEMIER G, et al. Development of a tube enzyme immunoassay for on-site screening of urine samples in the presence of beta-agonists[J]. Analyst, 1996, 121: 1111-1114.
[6]BACIGALUPO M A, LUS A, MERONI G, et al. Comparison of time resolved fluoroimmunoassay and immunoenzymometric assay for clenbuterol[J]. Analyst, 1996, 120: 2269-2271.
[7]谢孟峡, 刘媛, 蒋敏. 固相萃取-气相色谱-质谱分析肉样中盐酸克伦特罗的残留量[J]. 分析化学, 2002, 30(11): 1308-1311.
[8]LEYSSEN L, DRIESSEN C, JACOBS A. Determination of 2-receptoragonists in bovine urine and liver by gas chromatography mass spectrometry[J]. J Chromatogr, 1991, 564: 515-519.
[9]LEE X, WHAITES E, MURBY J. Determination of clenbuterol in bovine urine using gaschromatography-mass spectrometry following cleanup on an ion-exchange resin[J]. J Chromatogr B, 1999, 728: 67-73.
[10]张雪竹, 甘一如, 赵福年. 液相色谱电化学法检测猪肉及肝中残留的盐酸克伦特罗[J]. 药学学报, 2004, 39(4): 276-280.
[11]GUY P A, SSAVOY M C, STADLER R H. Quantitative analysis of clenbuterol in meat products using liquid chromatography-electrospray ionization tandem mass spectrometry[J]. J Chromatogr B, 1999, 736: 209-219.
[12]赵利霞, 李甲振, 魏彦林, 等. 化学发光免疫分析[J]. 世界科技研究与发展, 2004, 26(4): 24-33.
[13]雷红涛, 高秀洁, 潘科, 等. 盐酸克伦罗特时间分辨免疫检测方法建立[J]. 中国食品学报, 2006, 6(1): 6-10.
[14]HUANG Biao, TAO Weiyi, ZHANG Lianfen, et al. Ultrasensitive timeresolved xuoroimmunoassay of ochratoxin A[J]. Prog Biochem Biophys, 2005, 32(7): 662-666.
[15]蒋艺勤, 汤永平, 丁岚, 等. 游离雌三醇时间分辨免疫荧光分析法的建立[J]. 热带医学杂志, 2007, 7(3): 212-214.
Time-resolved Fluoroimmunoassay of Clenbuterol Hydrochloride using Europium Labeled Antigen
FAN Xiao-bo1,2,YANG Jin-yi2,GAO Xiu-jie2,WU Ying-song2,SUN Yuan-ming2,LEI Hong-tao2,*
(1. College of Food Science and Engineering, Northwest A & F University, Yangling 712100, China;2. Key Laboratory of Food Quality and Safety of Guangdong Province, College of Food Science, South China Agricultural University, Guangzhou 510642, China)
A convenient, rapid and sensitive method has been presented for the determination of clenbuterol hydrochloride (CBL) using the direct competitive time-resolved fluoroimmunoassay (TRFIA). In the direct competitive assay, the anti-CBL monoclonal antibody was bound on the surface of a 96-cell microplate, and samples containing CBL or the standards competed for the antibody binding sites with Eu3+labeled antigen in the wells of microplate. The determinations of CBL in porcine urine and tissue samples showed that the limit of detection was 0.02μg/L, with spike recoveries ranging from 91% to 101%. The cross-reaction rates with other six drugs were less than 1%. The proposed TRFIA method is sensitive and specific, and can be used for the determination of CBL residue in food samples.
cenbuterol hydrochloride (CBL);time-resolved fluoroimmunoassay (TRFIA);antigen;detection
X792
A
1002-6630(2010)20-0307-04
2009-12-24
樊晓博(1984—),女,硕士研究生,研究方向为食品质量与安全。E-mail:fxb307@yahoo.com.cn
*通信作者:雷红涛(1973—),男,副教授,博士,研究方向为食品质量与安全。E-mail:hongtao@scau.edu.cn
