肝癌微波热疗手术规划系统的设计与实现
2010-03-12高宏建杨春兰艾海明吴水才程志刚
高宏建,杨春兰,赵 磊,艾海明,吴水才,程志刚,梁 萍
(1.北京工业大学生命科学与生物工程学院,北京 100124;2.解放军总医院超声科,北京 100853)
肝癌已成为人类生命安全的最大威胁,据统计全世界每年死于肝癌的人数超过 25万.我国是肝癌的高发区,每年有 10万人死于此病.目前对肝癌的治疗可以使用手术、放疗和化疗,但肝癌的 5 a生存率仅为 5%左右,而且仅有 10%~20%的病人其肝癌能被切除.近年来,微波热疗技术成为治疗人体肿瘤行之有效的方法,它通过微波加热来消灭肿瘤细胞.北京 301医院(解放军总医院)超声科利用微波临床治疗肝癌近千例,取得突出疗效,局部热凝固消融治疗已达到国际领先水平.
但目前在临床微波热疗手术过程中完全依靠医生对二维图像(CT、MRI、超声等)的理解,医生的主观经验起到决定性的作用[1].医生通过医学图像上显示出的肿瘤形状、大小及位置等信息决定穿刺部位、穿刺深度、加热参数,带有很大的主观性.另外考虑到患者的身体条件,介入性治疗不能进行过多的穿刺,对肿瘤的杀灭也必须达到一次性完成,以防止其复发或转移[2].针对上述临床应用中存在的问题,研制一套肝癌微波热疗手术规划系统迫在眉睫,该系统的引入可对微波加热参数及方式进行优化,从而能较好地完成肝脏肿瘤的三维适形治疗,避免对正常肝组织的损害.这对于提高外科手术的科学性和可靠性、减少手术创伤具有非常重要的意义.
计算机图像处理技术、医学成像技术以及工程技术的发展使得计算机辅助手术成为可能[3].通过肝脏微波热疗手术规划系统可以确定肝脏、肿瘤及其管道系统的三维解剖关系,同时通过该系统可以制定合理的手术规划方案,确定穿刺点的位置、穿刺针的方向和加热参数(加热时间和功率等).因此,肝脏微波手术规划系统的研制能科学地引导临床手术,提高临床手术的可预见性,这将极大地促进微波热疗在临床中的应用.
1 设计与实现
肝癌微波热疗手术规划系统的最终目的是辅助医生寻找最佳的热疗参数,制定合理的手术计划.
1.1 系统设计
1.1.1 系统设计环境
由于医学图像数据量非常大,所以选用运行效率比较高的 Microsoft Visual C++作为系统开发平台.另外,为了加快软件开发速度和避免重复劳动,把重点放在算法研究和具体功能实现上,系统采用图像处理工具包 MITK(Medical Imaging ToolKit)作为开发框架.MITK是建立在 VTK(visualization ToolKit)和ITK(insight segmentation and registration ToolKit)的基础上,在统一的框架下实现了医学影像的分割、配准和三维可视化等算法.
1.1.2 系统软件结构
基于系统功能要求,系统软件主要由三维可视化模块、有限元仿真模块和手术规划及预测模块组成.通过系统软件主界面(如图 1)对各功能模块进行调用,完成微波热疗手术规划.

图 1 系统主界面Fig.1 Main interface of the system
1)三维可视化模块 该模块的主要功能是对肝脏二维 CT扫描图像进行三维可视化,得到肝脏及其肿瘤的三维模型,并输出模型数据.该模块主要由 2部分组成:一部分是利用 MITK的数据流模型作为框架对医学断层图像进行处理,实现图像分割、图像配准、图像滤波、三维可视化、网格化简和图像测量[4];另一部分是可调用商业化的三维可视化软件 Amira 3.1对医学图像进行处理,以便对图像三维可视化结果进行分析比较和对比验证.
2)有限元仿真模块 该模块的主要功能是模拟微波热疗温度场的分布,通过不断调整加热参数,获得不同的温度场三维模型,从而建立温度场分布数据库.该模块由 2部分组成:一部分在VC++开发平台下对温度场进行模拟仿真计算;另一部分是可调用商业化的有限元分析软件 ANSYS,以便对模拟的三维温度场进行分析比较和对比验证.
3)手术规划与预测模块 该模块的主要功能是制定最终的肝癌微波热疗手术规划方案,用于指导临床手术.该模块主要由模型匹配和最佳手术方案制定 2部分组成.模型匹配是对肝脏三维可视化模型和温度场三维模型进行比较和匹配,判断微波热疗温度场是否适形覆盖了肝肿瘤.最佳手术方案制定是通过模型匹配获得最佳的微波热疗参数(加热功率、分时比、加热持续时间等),获得合理手术方案,并以规范文本形式输出供医生治疗参考.
1.1.3 系统工作流程
手术前,首先使用 CT或 MR对病人肝脏部位进行扫描,将所得二维扫描图像读入计算机进行预处理(分割、配准、滤波等),然后对感兴趣区域(肝癌)进行三维可视化并进行测量分析,提取所需三维参数(大小、长径、横径等).接下来,利用有限元分析得到设定微波热疗参数下温度场的大小并建立相应模型.最后将温度场模型的参数和肝癌三维可视化模型参数进行匹配,不断调整热疗参数,得到最佳手术方案.肝脏微波热疗手术规划系统基本工作流程如图 2所示.
1.2 系统实现
本文在手术规划系统设计框架的基础上,利用 MITK和现有的三维可视化工具 Amira以及有限元分析软件 Ansys,对该系统进行了实现.
1.2.1 肝脏及肿瘤的三维可视化模型的建立
本次实验数据来源于解放军总医院 2例肝癌病人的 CT数据.每例数据为 60张断层图像,层间距为2.5mm,每张 CT图像由 512×512个像素组成,像素大小为0.703125mm×0.703125mm.实验中首先利用 Amira进行图像剪切、分割、表面重建、网格化简、表面光滑等步骤[5],最终完成肝脏及肿瘤的三维重建,重建结果如图 3和图 4所示,图 3中肝脏表面由9 000个三角形面片组成,肿瘤表面由 1 869个三角形面片组成.图 4中肝脏表面由 7 944个三角形面片组成,肿瘤表面由 7 040个三角形面片组成.通过肝脏及肿瘤的三维可视化模型可以了解肿瘤的大小以及相互解剖位置关系,进而可提取相应的特征参数.
1.2.2 仿真温度场模型的建立
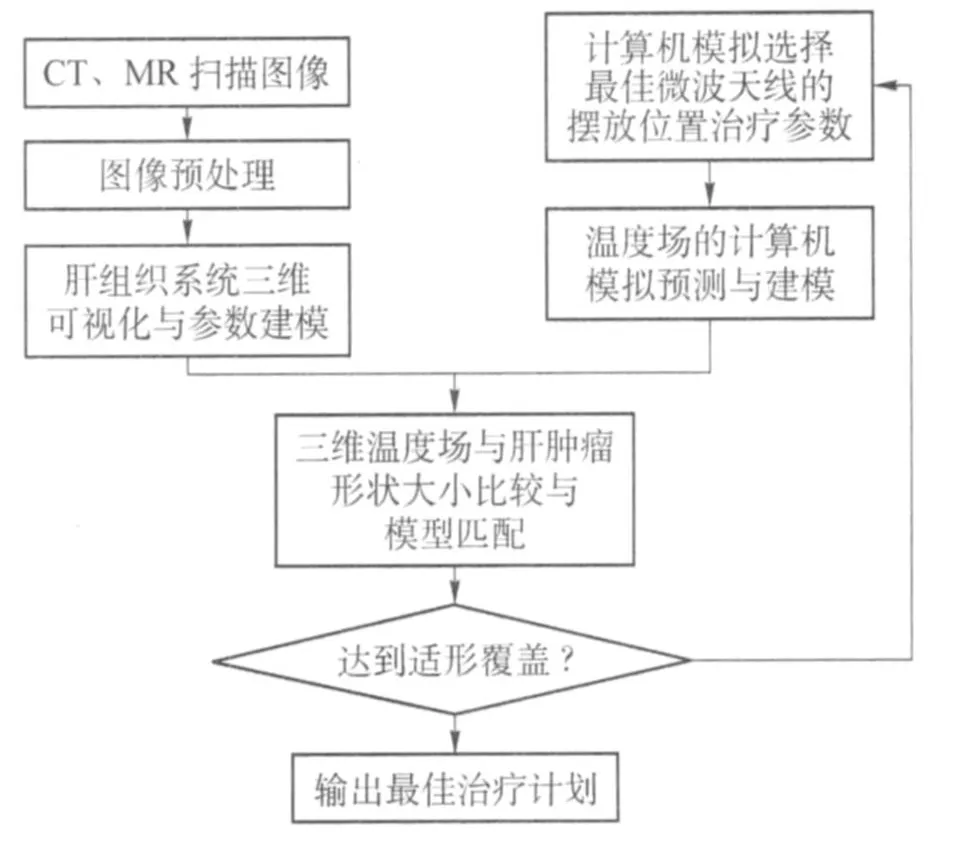
图 2 计算机辅助肝脏微波热疗手术规划系统工作流程图Fig.2 Data flow diagram of liver hyperthermia treatment planning system

图 3 第 1例肝脏及肿瘤的三维可视化模型Fig.3 3-D visualization model of the 1st liver and tumor

图 4 第 2例肝脏及肿瘤的三维可视化模型Fig.4 3-D visualization model of the 2nd liver and tumor
临床上将(54±0.5)℃作为热凝固区的外边界[6],目前微波热疗单极连续加热时凝固区的范围已被成功扩展到(4±0.5)cm×(5±0.5)cm×(5±0.5)cm[7].热疗的实际应用中几乎都是通过实验数据的拟合得到比吸收率 SAR(specific absorption rate)的分布函数[8].因此通过体模实验得到恒功率 50W在组织内的 SAR分布,拟合出空间的分布函数:正向函数为 1.07×3.7×1.567 7×1.805 5×2.718 28-2.15×r×(-0.1z3+0.37z2-0.529z+0.796 3);负向函数为 1.07×3.7×1.034 9×1.805 5×2.71828-2.15×r×(-0.1z3-0.59z2-0.493z+0.629 4).利用 Ansys和SAR分布函数对 50W、2 450MHz单极植入式微波天线温度场的分布进行了模拟,三维温度场仿真结果(外边界 54℃)如图 5所示.
1.2.3 参数提取和模型匹配
图 6所示为肝脏肿瘤和模拟温度场的三维模型图.首先对图 6(a)中的肿瘤三维可视化模型进行数据测量和参数提取,第 1例肿瘤测量结果为:长径 3.290 1 cm;横径 2.438 2 cm;肿瘤长径与 X轴夹角为78°、与 Y轴夹角为 10.4°、与 Z轴夹角为 75°(X、Y、Z分别为冠状位、矢状位、轴状位方向).第 2例测量结果为:长径 2.8965 cm;横径 2.4645 cm;肿瘤长径与 X轴夹角为 78.8°、与 Y轴夹角为 155.7°、与 Z轴夹角为 161.9°.将长径和横径的交点作为坐标原点,测得肝肿瘤表面数据如表 1和表 2所示.
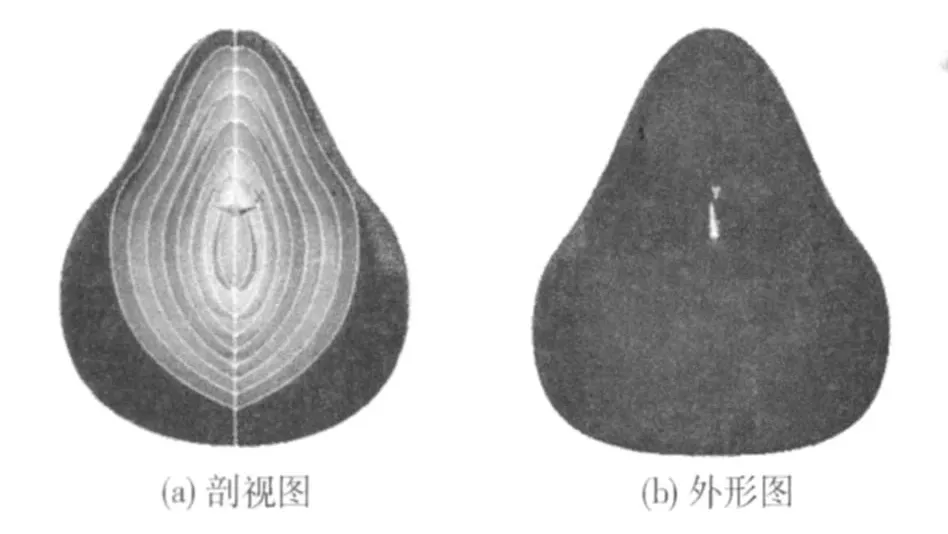
图 5 50W,2450MHZ单极植入式微波天线三维温度场分布Fig.5 The simulation models of temperature field of 50W,2450MHZ

图 6 肝肿瘤与温度场的三维模型比较Fig.6 Comparison results of 3-Dmodels between the liver tumor and temperature field
通过有限元模拟仿真得到 50W、2450MHz微波热疗天线的三维温度场如图 6(b)所示,通过不断调整加热时间来改变模拟温度场的大小以期完全覆盖肝脏肿瘤.当调整微波加热时间为 465 s时的温度场数据如表 1所示,中心温度为 83.182℃;当调整加热时间为 480 s时的温度场数据如表 2所示,中心温度为 84.238℃;通过与肝肿瘤三维可视化模型数据对比,能够满足肝脏肿瘤热疗的要求.
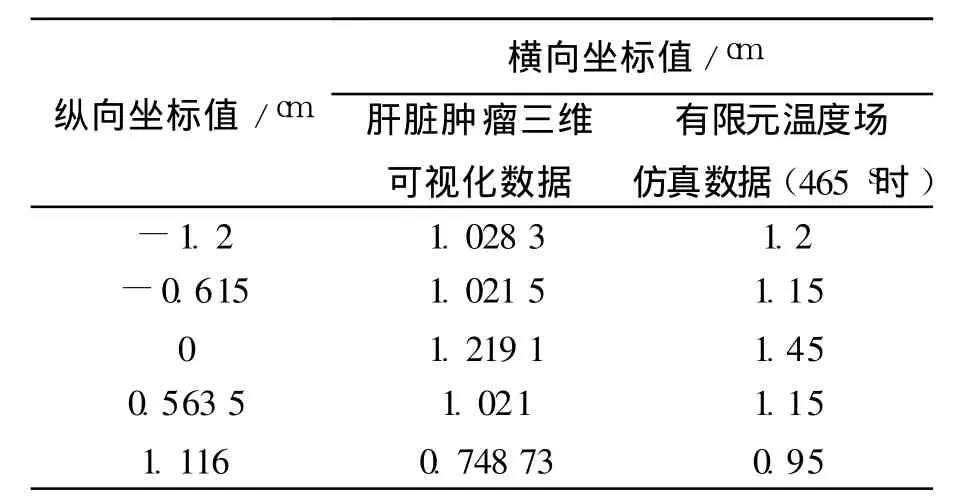
表 1 第 1例肝脏肿瘤三维模型的测量数据Table 1 M easuring data o f the 1st model of liver and tumor
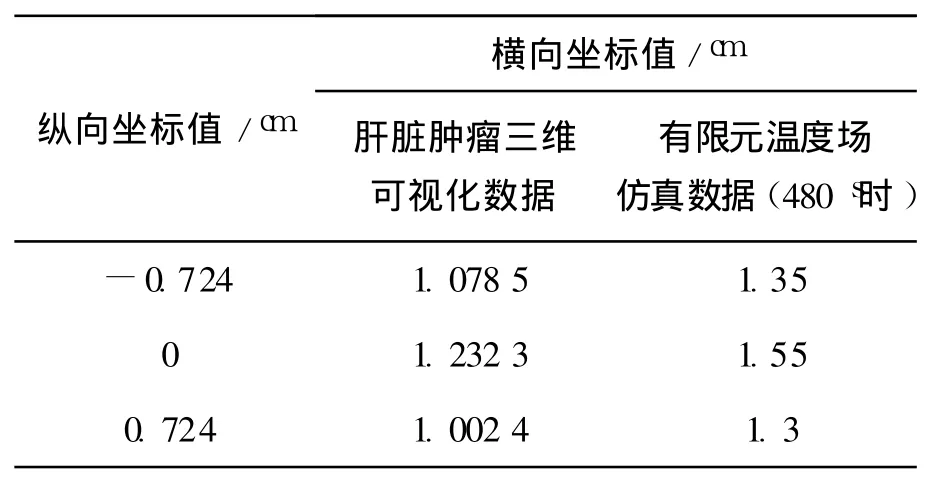
表 2 第 2例肝脏肿瘤三维模型的测量数据Table 2 Measuring data o f the 2nd model of liver and tumor
1.2.4 肝癌微波热疗手术方案的制定
通过以上肝肿瘤和温度场三维模型数据的对比,最终通过计算机辅助制定的第 1例肝癌手术规划方案为加热功率:50W;微波频率:2 450MHz;加热时间:465 s;天线的方向:与 X轴夹角为 78°,与 Y轴夹角为 10.4°,与 Z轴夹角为 75°.
第 2例肝癌手术规划方案为加热功率:50W;微波频率:2450MHz;加热时间:480s;天线的方向:与 X轴夹角为 78.8°,与 Y轴夹角为 155.7°,与 Z轴夹角为 161.9°.
2 结束语
本文利用 VC++和 MITK并结合 Amira和 Ansys研制了计算机辅助肝癌微波热疗手术规划系统.通过对 2例肝癌病人 CT扫描图像的处理和温度场的模拟匹配,制定出合理的微波热疗手术计划,实验结果表明了系统的可行性;但该系统还是初步的,下一步的工作中应建立多种微波热疗温度场模拟数据库,提取更加准确的肿瘤模型参数并且寻找优化的模型匹配算法.该系统经过进一步的完善,有望应用于肝癌微波热疗的临床手术中.
[1]王子罡,唐泽圣.基于虚拟现实的计算机辅助立体定向神经外科手术规划系统[J].计算机学报,2000,23(9):932-937.WANG Zi-gang,TANG Ze-sheng.VR based computer assisted stereotatic neurosurgery system[J].Chinese Journal of Computers,2000,23(9):932-937.(in Chinese)
[2]李娜.肝癌微波热疗中热物性参数与血液灌注率测量及温度场模拟[D].北京:北京工业大学环境与能源工程学院,2000.LINa.Measurements of thermal properties and blood perfusion and simulation of temperature field in microwave hyper thermia for liver cancer[D].Beijing:College of Environmental and Energy Engineering,Beijing University of Technology,2000.(in Chinese)
[3]赵英俊,陶青林,裴君.脑微创手术规划系统的设计与实现[J].中国医学影像技术,2004,20(9):1443-1447.ZHAO Ying-jun,TAO Qing-lin,PEI Jun.Design and implementation of computer aided m inimally invasive neurosurgery planning system[J].Chin JMed Imaging Technol,2004,20(9):1443-1447.(in Chinese)
[4]GAO H J,WU S C,REN X Y,et al.3-D reconstruction of liver slice images based on MITK framework[C]∥The 1st International Con ference on Bioinformatics and Biomedical Engineering(ICBBE2007),Wuhan:IEEE,2007:952-955.
[5]高宏建,吴水才,任新颖,等.利用Amira进行肝脏及其管道系统的三维重建[J].北京生物医学工程,2006,25(5):534-537.GAO Hong-jian,WU Shui-cai,REN Xin-ying,et al.The three-dimensional reconstruction of liver and its vessel system by amira[J].Beijing Biomedical Engineering,2006,25(5):534-537.(in Chinese)
[6]陈新,南群,彭见曙.肝癌恒功率介入微波热凝固术的有限元模拟[J].中国科学,2002,32(5):636-643.CHEN Xin,NAN Qun,PENG Jian-shu.Finite element analysis of constant-power invasive microwave coagulation of liver tumors[J].Science in China,2002,32(5):636-643.(in Chinese)
[7]DONG B W,PING L,XIAO L Y,et al.Sonographically guided microwave coagulation treatment of liver cancer:an experimental and clinical study[J].American Journal of Roentgenology,1998,171(2):449-454.
[8]南群,夏雅琴,刘有军,等.微波消融治疗肝癌中的若干热学问题[J].北京工业大学学报,2008,34(5):551-555.NAN Qun,XIA Ya-qin,LI U You-jun,et al.Some thermal problems in microwave ablation therapy for hepatocellular carcinoma[J].Journal of Beijing University of Technology,2008,34(5):551-555.(in Chinese)