蓝色荧光粉Ca2B 5O 9C l∶Eu2+的甘氨酸燃烧法合成及其发光性能
2010-02-07陈栋华郑映丽刘文庆
陈栋华,郑映丽,刘文庆
(中南民族大学化学与材料科学学院催化材料科学湖北省暨国家民委-教育部共建重点实验室,武汉430074)
由于发光二极管(W LED)在照明领域的潜在市场,W LED用荧光粉成为当前国内外的研究热点.采用近紫外LED芯片涂敷蓝、绿、红三基色荧光粉制备W L ED具有显色性好的优点,因此研究可被近紫外有效激发的LED用荧光材料很有必要[1].碱土金属中Eu2+的荧光性能早有研究,发现Eu2+离子的发光是由4f7→4f65d宽带和4f7→4f7线性跃迁引起的[2].自报道了Ca2B 5O 9C l的结构[3,4]以来,以Ca2B 5O 9C l为基质,掺杂不同稀土离子或掺杂同种稀土离子而采用不同制备方法均可获得具有不同光谱特性的发光材料[5,6].近年来,采用燃烧法[7]、溶胶-凝胶法[8]、喷雾热解法[9]、共沉淀法[10]等软化学合成荧光材料得到迅速发展,其中燃烧法是近年来提出的一种新的合成方法.该法利用氨基酸、柠檬酸或尿素等燃料燃烧反应所放出的热量,从而产生化学反应.较其它法,燃烧法反应迅速,合成产物疏松,易粉碎,生产过程简便,节约能源等.目前,采用燃烧法合成Ca2B 5O 9C l∶Eu2+荧光粉还没见报道.
本文采用甘氨酸燃烧法合成Ca2B 5O 9C l∶Eu2+,研究了铕离子的浓度,初始炉温,以及甘氨酸与硝酸根中铕离子的配比对荧光材料发光性能的影响.
1 实验部分
1.1 试剂
实验所用试剂:CaCO3(A.R)、H 3BO3(A.R)、NH 4C l(A.R)、甘氨酸(A.R)、硝酸(A.R),Eu2O 3为99.99% 的高纯试剂.
1.2 样品制备
(1)取1.7596 g Eu2O3于20m L浓硝酸溶解后移至100m L容量瓶中定容.
(2)按化学计量比于坩埚中称取所需CaCO3、H3BO3、NH 4C l(其中NH 4C l过量30% 以补偿蒸发的损失),从(1)中移取所需的Eu2O3硝酸溶液,碾磨至胶体状.将坩埚迅速置于预热至550~850℃的马弗炉中.随着反应的进行,溶液迅速燃烧,并伴随大量氨气和一氧化碳放出,30m in燃烧至完全.冷却即得最终产物.
1.3 仪器
所得产物性能表征:使用德国B ruker D 8型X射线衍射仪(CuK<alpha>射线,λ=0.15406 nm,石墨单色器,工作电压为40 kV,工作电流为40m A,步长0.02°,扫描速度4(°)/m in,扫描范围10°≤2θ≤50°)对合成产物进行了物相分析;Pek inE lm er LS555型荧光光谱仪(PE,美国)测量产品的激发和发射光谱.
2 结果与讨论
2.1 物相分析
Ca2B5O9C l为正交晶系,其晶格常数a=112.6 nm,b=111.3 nm,c=63.0 nm. 图1为550~850℃燃烧30m in后的Ca1.994B5O9C l∶E(x为摩尔分数)荧光材料的XRD图谱.由图1知,该荧光粉在550℃时XRD图谱相似于Ca2BO3C l(JCPDS 29-0302),晶相开始形成,说明550℃时,该荧光粉的晶格为Ca2BO3C l;650℃时,开始形成Ca2B5O9C l晶格,但此时衍射峰较弱,说明晶格还未完全形成;750℃时衍射峰强度达到最大,与Ca2B5O9C l标准图谱JCPDS 23-0859很好吻合,说明此时晶型形成较完全.因此,确定750℃为最佳初始燃烧温度.850℃时谱图中出现新的晶型,此衍射峰与Ca(BO2)2的标准图谱JCPDS 78-1277较好吻合,说明850℃时发生了晶型转变生成了Ca(BO2)2的晶型.另外,由图1知,稀土Eu2+离子的加入并未影响Ca2B5O9C l的晶型.

图1 不同初始炉温的XRD图谱Fig.1 XRD pattern of the pow dersob tained at different tem peratu res
2.2 Ca2B 5O 9C l∶Eu2+ 发光性能
图2为Ca1.994B5O9C l∶E荧光粉的激发和发射光谱.由图2知,该荧光粉的激发图谱由260~420 nm 的宽激发带组成,最大吸收强度位于340 nm,该激发为激发离子Eu2+的4f-5d跃迁产生,最大发射峰值位于434 nm,峰型单一.此激发和发射波长均不同于文献[5,6]报道.由此进一步说明不同的合成方法对发光性能有着一定影响.
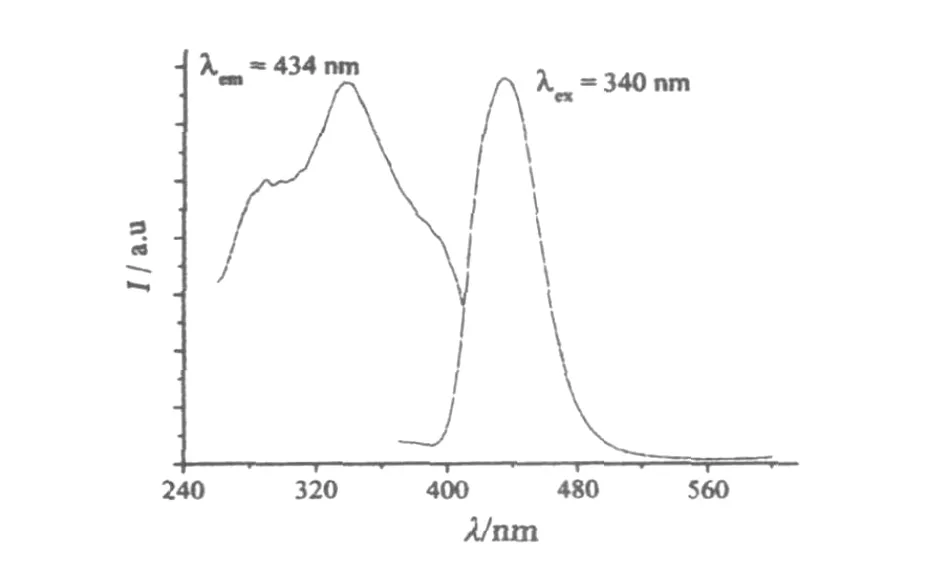
图2 Ca2B 5O 9C l∶Eu2+荧光粉的激发和发射光谱Fig.2 Excitation and em ission spectra of Ca2B 5O 9C l∶Eu2+pho spho r
图3为掺杂不同摩尔分数x的Eu2+的Ca2(1-x)B5O9C l∶E(x=0.003,0.006,0.01,0.013,0.016,0.02)材料的发射光谱.由图3知,x=0.006时,Ca2B5O9C l∶Eu2+材料具有最大吸收,发射峰最强,所以Eu2+最佳掺杂摩尔分数为0.006;x≤0.006时,随着Eu2+掺杂摩尔分数的增大,样品发射峰的强度逐渐增强;x≥0.006时,随着Eu2+掺杂浓度的增大,样品发射峰的强度逐渐减弱,因为随着激活离子掺杂浓度的增大,激活离子间距变短,其相互作用增强,产生了激活离子到基质的非辐射能量传递,使得激活离子的发光效率降低.

图3 不同摩尔分数Eu2+的发射光谱(λex= 340 nm)Fig.3 Em ission spectra of sam p lesw ith different ratios o f Eu2+(λex=340 nm)
2.3 不同初始炉温对荧光粉发光性能影响
图4为Ca1.994B5O9C l∶E荧光粉在不同的初始炉温下的发射光谱.由图4可见,初始炉温为550℃时,发光强度较弱;初始炉温为750℃时得到最强发射强度,发光性能较好;初始炉温高至850℃,发光性能又降低.对应于图1,可知550~850℃时样品晶型形成与其发光性能较一致.说明发光性能与基质晶型有关;基质晶型的形成受温度的影响,不同的温度可生成不同晶型;而不同的晶型则发光性能又不同.

图4 不同初始温度样品的发射光谱(λex=340 nm)Fig.4 Em ission spectraso f sam p les p repared at different in itiating com bustion tem peratu re(λex=340 nm)
2.4 甘氨酸用量对发光性能影响
取一定量含Eu2+(x=0.006)硝酸根溶液,分别加入0,1,2,3,4倍于铕离子的甘氨酸,反应完全所得产物的发射光谱见图5.由图5知,甘氨酸浓度3倍于Eu2+时,反应条件最佳,发光强度最强.此步可能为甘氨酸与Eu2+溶液中硝酸根反应,从而因生成大量CO,N2,NH3等还原气氛将Eu3+还原为Eu2+所至;甘氨酸用量为0时,反应原料中的NH 4C l可使部分Eu3+还原为Eu2+,发光强度不理想;甘氨酸用量过高时,可使反应温度升高,晶体易聚结,影响发光性能.
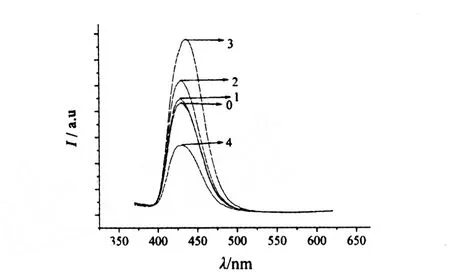
图5 甘氨酸与Eu2+的摩尔分数比(n∶1)对产物发射光谱的影响Fig.5 Em ission spectra o f sam p lesw ith d ifferen t am oun to f G lycine and Eu(n∶1)
图6为甘氨酸用量对Ca2B5O9C l∶Eu2+荧光粉激发光谱的影响.由图6知,当甘氨酸用量3倍于Eu2+时吸收最强,与发射光谱的强度一一对应.
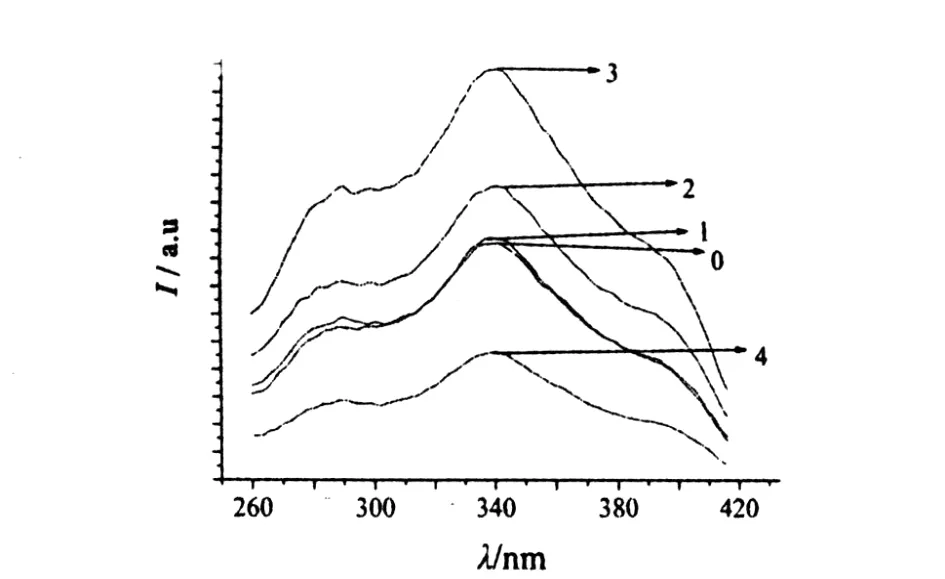
图6 甘氨酸与Eu(n∶1)的摩尔分数比对产物的激发光谱的影响Fig.6 Excitation spectra o f sam p lesw ith different am oun to f G lycine and Eu(n∶1)
3 结语
(1)采用甘氨酸燃烧法合成Ca2B 5O 9C l∶Eu2+蓝色荧光粉.确定了最佳的合成温度为750℃,低于文献报道的固相法温度[11].得到了甘氨酸与硝酸根中Eu2+离子的最佳摩尔分数比为3∶1.当甘氨酸用量少则Eu2+还原不彻底,而用量过多则易使燃烧温度过高且易碳化而使粉体颜色发灰.
(2)掺杂Eu2+的最佳摩尔分数x= 0.006,此荧光粉的激发范围在260~420 nm,最大激发峰为340 nm,该荧光粉能被InGaN 芯片(发光区域350~420 nm)有效激发,发射单一的蓝光,可用于白光发光二极管.
(3)合成方法的不同对发光性能有一定影响.
(4)与其他合成方法相比,燃烧法具有设备简单、操作简便,反应迅速,节省能源等优点,是一种较有前途的制备发光材料的方法,具有广阔的应用前景.
[1]Sheu J K,Chang S J,Kuo C H,et al.W h ite-ligh t em ission from near UV InGaN-GaN LED chip percoated w ith b lue/g reen/red phospho rs[J].IEEE Pho tou ics Techno lL ett,2003,15:140-145.
[2]B lasse G,W anm akerW L,Terv rugt JW,et al.F luo rescence of Eu2+activated silicates[J].Jou rnal o f E lectrochem ical Society,1968,23:189-220.
[3]L loydM D J,L evasseu r A,Fouassier C.Structu re cristalline du b rom obo rate Ca2B 5O 9B r[J].J So lid State Chem,1973(6):179.
[4]Q ing Z,N at han K,M ark R,et al.L um inescence p roperties of Sm-activatedbarium ch lo robo rates[J].Jou rnalo f L um inescence,2003,104(1/2):65.
[5]N akam u ra S,Inabe K,TakeuchiN.L um inescenceo f Sin tered Ca2B 5O 9C l∶Eu2+excited by UV-L igh to r X-rays[J].Jpn JA pp l Phys,1992,31(6A):1823.
[6]董红军,常树岚.水热法与固相法制备Ca2B5O9C l∶Eu光谱特性的研究[J],光谱学与光谱分析,2007,27(11):2167-2270.
[7]Saradh iM P,V aradaraju U V.Pho to lum inescence stud ies on Eu2+-activated L i2SrSiO4-a po ten tial o range-yellow phospho r fo r so lid-state ligh ting[J].Chem istry o fM aterials,2006,18(22):5267-5272.
[8]Cannas C,M ainasM,M usinu A,et al.Structu ral investigations and lum inescence p roperties o f nanocrystalline eu rop ium-doped yttrium silicates p repared by a so l-gel techn ique [J]. Op tical M aterials,2007,29:585-592.
[9]Jung K Y,L ee H W,Jung H K.L um inescen t p roperties o f(Sr,Zn)A l2O4∶Eu2+,B3+particles as a po ten tialg reen phospho r fo rUV L ED s[J].Chem M ater 2006,18:2249-2255.
[10]Zhou Y,L in J,YuM,et al.Syn thesis depend ing lum inescence p ropertieso f Y 3A l5O12∶Re3+(Re=Ce,Sm,Tb)phospho rs[J].M ater L ett,2002,56:628.
[11]Zhang XM,Chen H,D ingW J,et al.Ca2B 5O 9C l∶Eu2+,a su itab le b lue-em itting pho spho r fo r n-UV excited so lid-state ligh ting[J].J Am cceram Soc,2009,92(2):429-432.
