正交实验联用星点设计-效应面法优化紫草素脂质体处方
2010-01-25邢建国王新春张永军袁勇蒲宇红
邢建国,王新春,张永军,袁勇,蒲宇红
(1.新疆维吾尔自治区药物研究所,新疆乌鲁木齐830004;2.新疆石河子大学一附院,新疆石河子832008;3.新疆石河子大学药学院,新疆石河子832008)
新疆软紫草为紫草科多年生草本植物,具有多种生物学作用[1-2]。紫草素为紫草中脂溶性很强的萘醌类色素,具有逆转肿瘤细胞多药耐药[3]和广泛的抗肿瘤作用[4],但紫草素水溶性差的性质影响了其在医药领域的广泛应用。脂质体作为难溶于水的药物输送载体具有许多优越性,其所具有的生物膜特性可将难溶药物包埋于脂质体双分子层所形成疏水腔内,使得药物粒子溶解度增大,促进被包裹的难吸收性的药物在肠道的传递,提高其生物利用度。
在脂质体处方优化中,常需考察多个因素的多个水平,因此,寻找一种实验次数少、而实验结果接近全面实验优化出的结果的实验设计方法是每位研究者十分关心的问题。正交设计[5]、均匀设计[6]和星点设计-效应面优化法[7]是常采用的试验设计方法。其中正交实验设计安排的实验具有均衡搭配的特点,但其所建立的指标和因素之间关系的数学模型是一种线性模型,因此模型的精度不够、预测性较差。星点设计-效应面优化法是一种多元非线性拟合的实验设计方法,所建立的非线性数学模型精度高、预测性较好。但若需考察的因素较多时,则存在实验次数偏高的不足,如五因素则需52次试验。因此,基于正交设计和均匀设计联用的研究[8]结合正交设计与星点设计两种设计方法的各自特点,在进行紫草素脂质体处方优化过程中,首先采用正交实验设计试验次数较少的特点,进行多因素的初步筛选,再将所确定的主要影响因素采用预测精度较高的星点设计非线性数学模型进行优化,旨在达到利用较少的试验次数得到具有较高预测精度的数学模型的研究目的,进而保证紫草素脂质体的处方优化的准确性。
1 药物、试剂和仪器
紫草素(青岛市海大化工有限公司);大豆磷脂(上海太伟药业有限公司,批号070614,含量90%);胆固醇(上海生物化学试剂公司,批号051023);乙醇、曲拉通等试剂为分析纯。
SPD-10ATVP液相色谱仪(日本岛津);85-2A数显式磁力加热搅拌器(江苏省金坛市荣华实验仪器厂);电子分析天平(德国赛多利斯Sartorius);BP211D台式离心机TGL-16G(上海安亭科学仪器厂);KQ-250B型超声清洗器(昆山市超声仪器有限公司);90plus激光粒度分析仪(美国Brookhaven);SAS统计软件(Release 8.20,SAS Institute Inc.);Origin6.0绘图软件(Microcal Software Inc.)。
2 方法与结果
2.1 紫草素脂质体的制备[8]
结合实验室条件及预试验研究结果,采用乙醇注入法制备紫草素脂质体。分别取处方量的大豆磷脂、胆固醇、紫草素于棕色瓶中,精密称定。加入适量无水乙醇,超声使完全溶解。在600 r/min机械搅拌条件下,将所得的乙醇混合物溶液注入到含甘露醇的水性溶液中,室温搅拌5 min,得到脂质体胶体分散液。
2.2 载药量和包封率的测定
紫草素脂质体中紫草素的含量用高效液相色谱法测定。色谱柱:AgilentXDB C18色谱柱(250 mm×4.6 mm,5 μm),流动相:甲醇-0.025 mol/L磷酸(78∶22);柱温:25℃;流速:1.0 mL/min;测定波长:516 nm,进样量20 μL。载药脂质体和游离药物采反相透析法分离。含药脂质体0.5%曲拉通乙醇溶液超声10 min进行消解。高效液相色谱法检测,每批样品测定3次计算药物包封率和载药量。
2.3 纳米粒粒径及分布的测定方法[9]
待测样品的平均粒径及粒度分布用90plus激光粒度分析仪测定。
2.4 实验设计
按L8(27)安排实验,依据文献及预实验结果初步考察药物与脂质比(X1)、大豆磷脂浓度(X2)、有机相和水相体积比(X3)、大豆磷脂与胆固醇比(X4)、甘露醇浓度(X5)5种影响因素,以包封率(EE%)、载药量(DL%)及归一化值为指标,对数据进行直观分析及方差分析,确定主要影响因素。因素-水平表见表1。

表1 L8(27)正交实验因素-水平表
依据正交实验设计筛选结果,按三因素五水平星点设计安排实验,进一步考察影响处方配比的主要因素X1、X3及X4对包封率、载药量及归一化值(OD)三个评价指标的影响,依据三次多项式非线性回归方程及效应面法确定紫草素脂质体处方的最佳配比。因素-水平表,见表2。

表2 星点实验设计因素水平表
2.5 数据处理与结果分析
2.5.1 正交实验结果处理
采用正交设计助手v3.1软件,综合考虑各因素对包封率、载药量及归一值的影响,确定主要影响因素为大豆磷脂浓度、药脂比和有机相-水相体积比。次要因素进一步确定为甘露醇浓度2%、大豆磷脂与胆固醇比4∶1。试验结果见表3。
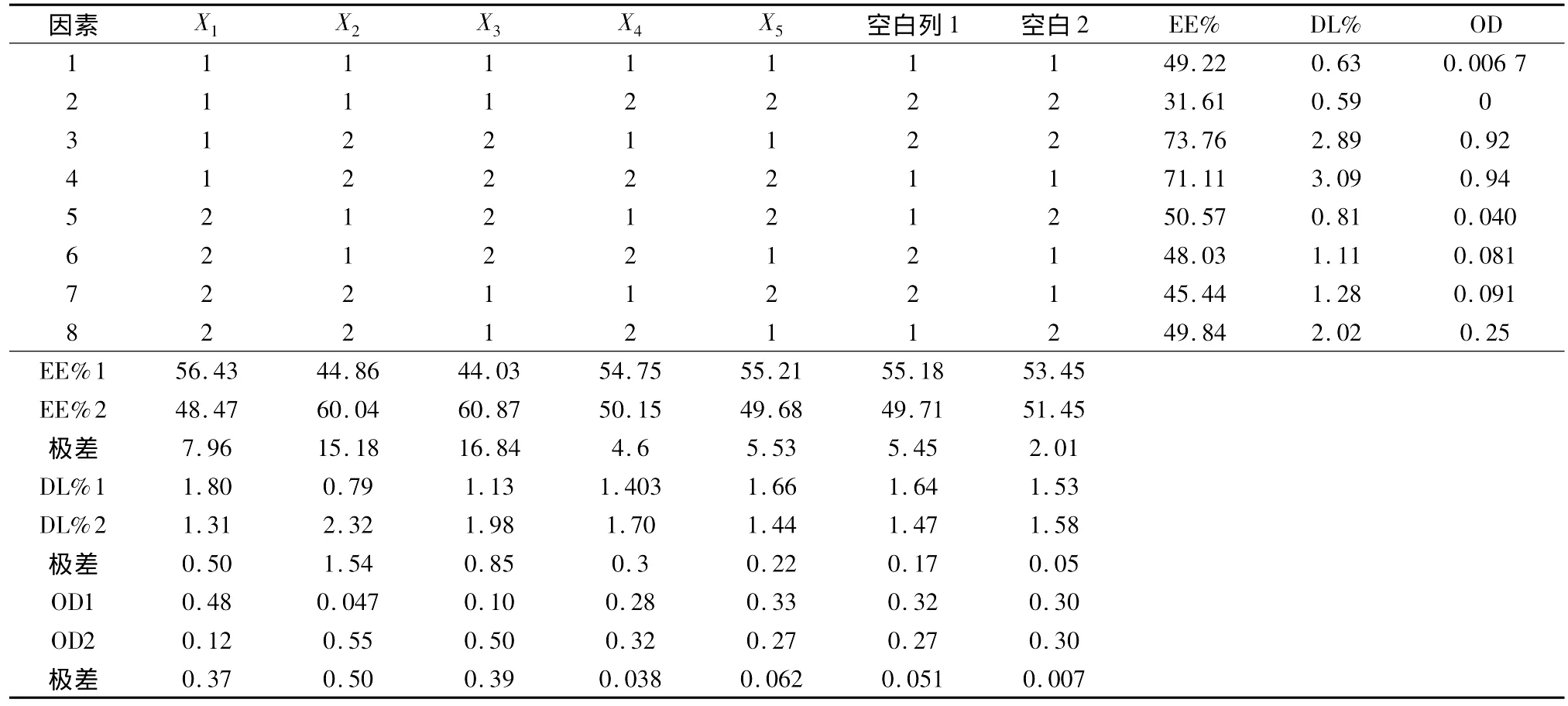
表3 正交试验结果
2.5.2星点设计模型拟合
用SAS8.0统计软件,以各评价指标(因变量)分别对各因素(自变量)选择3种数学模型进行曲线拟合。模型如下:
多元线性方程:D=b0+b1x1+b2x2+b3x3
二次多项式:D=b0+b1x1+b2x2+b3x3+b4x1x2+b5x1x3+b6+b7x2x3+b8+b9
三次多项式:
D=b0+b1x1+b2x2+b3x3+b4x1x2+b5x1x3+b6+b7x2x3+b8x22+b9x23+b10+b11x1+b133+b14x2
三个指标的多元线性回归方程结果显示,尽管模型可以通过检验,但模型拟合的相关度不佳,因此应采用多元高次的数学模型。三个指标二次多项式回归方程的拟合结果是,各项系数的估计值多数不能通过P<0.2的检验,一定程度的简化后仍不能通过P<0.1的检验;三次多项式方程的拟合结果则各项系数在删除P>0.2的项后,进行t检验,三个指标的方程均通过P<0.005的检验,模型拟合优度好。
三个指标的三次多项式方程如下:
y1=172.193+25.881X1-533.374X2-25.586X3-196.211X1X2-0.254X1X3+139.156X2X3+0.489X3X3+367.979X1X2X2-135.832X2X2X3-1.585X2X3X3R=0.991 0
y2=-1.643+3.247X1-0.792X3-17.069X1X2-0.107X1X1+6.087X2X3+0.285X1X1X2+25.296X1X2X2-9.875X2X2X3R=0.974 5
y3=-0.163+0.767X1-0.216X3-3.965X1X2-0.035 0X1X1+1.274X2X3+0.001 54X3X3+0.100X1X1X2+5.447X1X2X2-2.010X2X2X3R=0.987 6
上述结果显示,包封率、载药量和归一化值三指标的三项式拟合均比线性模型相关系数高。
2.6 优化工艺
固定3个自变量中影响较弱者,设为中值,代入原方程,应用Origin6.0软件分别绘制各指标与影响较显著的2个自变量的三维效应面和二维等高图。从三维效应面图和等高图中,选取包封率和载药量较高及综合指标较理想的区域,求其相应的自变量范围,得较优处方为X1=8%,X2=0.45%,X3=20。根据优化处方平行制备3份样品,所得脂质体的包封率、载药量分别为85.4%,载药量为5.16%,偏差的绝对值均小于5%,平均粒径为98.1 nm、多分散指数为0 203,说明模型预测性好。
3 讨论
3.1 用线性数学模型进行拟合的正交实验方法是一种实验次数少、预测性精度不高的方法;星点设计是一种非线性数学模型拟合的实验设计方法,是根据模型所建立的效应面的区域进行筛选,具有预测精度高的特点,但考察因素多时,实验次数也较多。本实验将两者有机地结合,采用正交实验,通过较少的实验次数确定主要影响因素,在此基础上采用星点设计进一步优化,对实验数据进行模型预测。验证实验结果表明,两个方法的联用不仅提高了实验效率,而且使预测结果具有较高的准确性。因此,是一种简便、可行及可靠的实验设计方法,尤其更适用于影响因素较多的实验。
3.2 目前微粒给药系统中用于药物包封率测定的方法有超速离心法、离心超滤法、柱分离法等。本实验依据文献[10]建立了反相透析法测定药物包封率的方法,同时对各方法进行比较研究,结果表明,该方法与上述方法相比,具有经济、简便和准确的特点,是一种用于处方和工艺筛较为理想、可靠的方法。
[1]孙培杰.紫草的药理作用与临床应用研究进展[J].中医药信息,2002,19(4):19.
[2]Xin Chen,Lu Yang,Joost J,et al.Cellular harmacology Studies of Shikonin Derivatives[J].Phytother Res,2002,(16):199.
[3]方建平.肿瘤多药耐药逆转制剂的筛选和紫草素抗MDR肿瘤活性的研究[D].浙江大学,2004,(2):55.
[4]徐坤山,孟松树.紫草素及其衍生物抗肿瘤作用研究综述[J].泰州职业技术学院学报,2007,7(6):40.
[5]Wang YM,Sato H,Adachi I,et al.Optimization of the formulation design of chitosan microspheres containing cisplatin[J].J Pharm Sci,1996,85(11):1204.
[6]黄虹,唐琦文.均匀设计和模式识别法优化鱼腥草口服液制备工艺[J].中成药,2000,22(10):684.
[7]Molpeceres J,Guzman M,Aberturas MR,et al.Application of central composite designs to the preparation of polycaprolactone nanoparticles by solvent displacement[J].J Pharm Sci,1996,85(2):206.
[8]杨轲,彭桂,刘宣麟,异甘草素纳米脂质体色封率测定方法的研究[J].新疆中医药,2009,27(4):45-46.
[9]王新春,侯世祥,李文.均匀设计联用星点设计优化白藜芦醇固体脂质纳米粒制备处方[J].中成药,2007,29(8):1139-1142.
[10]熊非,朱家壁,王维,等.灯盏花素纳米脂质体包封率测定方法研究[J].药学学报,2004,39(9):755.
