纳米Au/TiO2薄膜真空紫外光催化降解甲醛
2010-01-07傅平丰张彭义清华大学环境科学与工程系环境模拟与污染控制国家重点联合实验室北京100084
李 佳,傅平丰,张彭义 (清华大学环境科学与工程系,环境模拟与污染控制国家重点联合实验室,北京 100084)
甲醛是室内空气中主要污染物之一.TiO2光催化能有效去除包括甲醛在内的可挥发性有机污染物[1-2].近年来,为提高 TiO2光催化效率的研究非常多[3-6].其中,真空紫外光催化技术采用真空紫外光(波长<200nm 的紫外线, VUV)照射光催化剂,条件温和、适用范围广、去除效率高而具有较大应用前景[7-9].值得注意的是,真空紫外光系统的副产物臭氧可以作为一种强氧化剂与254nm 紫外光激发的光催化过程协同作用,具有分解有机污染物、灭菌和除臭等高效率的净化作用[10].然而,当臭氧浓度达到0.1~0.14mg/m3以上时,就会对人体产生危害[11].所以减少真空紫外光催化过程中臭氧的产生是非常必要的.金属氧化物如MnO2、NiO、TiO2、Ag2O和CuO等对臭氧有催化分解作用[12].已有不少研究金、铂、钌、铑、钯、银等贵金属沉积到二氧化钛等光催化剂表面以增强光催化活性[13-15].其中氧化钛载金(Au/TiO2)纳米复合材料具有优良的光化学与光催化性能[16-18].但是在真空紫外光催化系统中同步降解气相中有机污染物和分解臭氧的研究未见报道.本研究选择接近室内真实浓度的甲醛作为研究对象,采用低温吸附法制备纳米 Au/TiO2复合薄膜,研究其在真空紫外光条件下同时去除甲醛和臭氧的效果.
1 材料与方法
1.1 Au/TiO2光催化剂的制备
采用改性溶胶-凝胶法制备以钛网(40目,10cm×10cm)为载体的TiO2薄膜[19].Au/TiO2复合薄膜采用低温吸附法制备[20],主要步骤如下.先向一定浓度聚乙烯醇(PVA)溶液中滴加0.048mol/L的HAuCl4以配制[AuCl4]-浓度为3×10-4mol/L 的溶液,暗处放置 1h.按 NaBH4与[AuCl4]-物质的量比(5~10):1将 0.07mol/L 的NaBH4溶液快速滴加到氯金酸溶液中(保持0℃),超声搅拌.调节其pH值到4~6,将负载TiO2的钛网浸于0℃下的Au溶胶中30min,取出后自然干燥,热水洗氯2~3次,再置于空气中350℃焙烧1h,即制得Au/TiO2光催化剂.
1.2 试验装置与材料
试验空气经过干燥、稳流装置后分流,分别通入增湿瓶、甲醛气体发生瓶(瓶中装有一定溶度的甲醛水溶液,)进行配气,使空气流中含有一定浓度的甲醛,空气流进入真空紫外光催化反应器.甲醛气体发生瓶放置在恒温槽(0℃)中,用质量流量计 (S49-32B/MT,北京汇博隆仪器有限公司)调节通入甲醛气体发生瓶的空气流量.真空紫外光降解反应器材质为不锈钢,中间为圆柱型,两端加锥形帽,圆柱部分内径10cm,长9cm,总长14cm,反应器内放置2支3W紫外灯(广东雪莱特光电科技有限公司).普通光催化实验用UV紫外灯,波长254nm,光强3.1W/m2;真空紫外光催化实验用VUV紫外灯,主波长254nm,发射少量185nm真空紫外线, 总光强3.2W/cm2,185nm紫外线约占总光强 5%.灯管两侧分别放置等量催化剂片.进入真空紫外光降解反应器的气体流量固定为1.8L/min,甲醛入口浓度为0.50±0.05mg/m3.
1.3 采样与分析方法
甲醛采用酚试剂分光光度法[21]分析.用一个内装5mL酚试剂吸收液的大型气泡吸收管,采样管入口接强化光催化反应器的尾气排放装置,出口接大气采样器(QC-2型,北京市劳动保护科学研究所),以1L/min流量,采气20min.为避免臭氧对甲醛测定的干扰,吸收管前设置臭氧洗涤器.臭氧洗涤器制作方法参考Waters SEP-PAK DNPHSILICA Cartridge使用手册附录C,即将饱和KI溶液用去离子水1:1稀释,注入长1m、内径0.46cm的铜管中,并用高纯氮气吹干而得到.
臭氧浓度用在线臭氧分析仪(Model ZX-01,Instrument of Lab. Institute)测定.
2 结果与讨论
2.1 Au/TiO2复合薄膜电镜表征

图1 Au-TiO2/Ti复合薄膜的SEM和TEM照片Fig.1 SEM and TEM images of Au/TiO2 nanocomposite film
图1(a)为Au/TiO2复合薄膜的高倍SEM照片,图中白色圆点为Au颗粒,灰色部分为TiO2薄膜.图1(b) 为Au/TiO2复合薄膜的TEM照片,图中黑色圆点为Au颗粒.制备的TiO2薄膜颗粒尺寸为10~30nm.由于干燥和焙烧过程中TiO2薄膜局部收缩和开裂,TiO2表面并不平整致密,呈现多孔与褶皱.Au颗粒主要分布于TiO2薄膜的表面及孔道口,基本呈圆形、单分散、均匀分布,表面粒密度达5.07×1011个/cm2,平均粒径为(4.3± 1.4)nm.
2.2 不同光化学方法降解甲醛的效果比较
由图2可见,TiO2/UV、VUV、TiO2/VUV等3种方法对甲醛均有显著的降解作用,在35h的试验期内对甲醛的去除率保持稳定,分别为65.1%、72.9%,91.3%.TiO2/VUV对甲醛的去除率明显高于TiO2/UV、VUV.这是由于在气相光催化过程中,电子和空穴存在表面复合,光催化效率很低,而真空紫外光催化可以通过以下多种途径降解气相污染物: VUV直接光解有机污染物;VUV产生羟基自由基(HO·)及臭氧,氧化降解有机污染物;臭氧/UV光催化.

图2 3种方法对甲醛去除效果的比较Fig.2 Comparison of three methods for formaldehyde degradation
2.3 真空紫外光下不同催化剂降解甲醛和臭氧的比较及机理分析
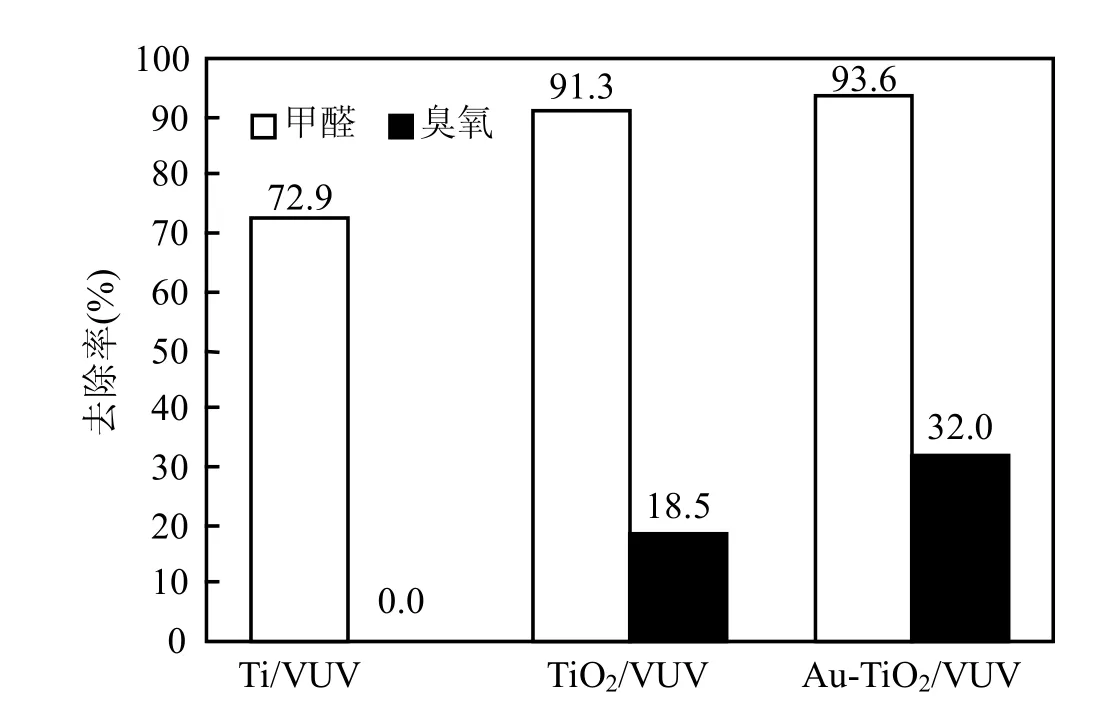
图3 不同催化剂对甲醛及臭氧的去除率Fig.3 Removal ratio of formaldehyde and ozone under different catalysts
在VUV条件下比较了Ti网、TiO2和Au/TiO2对甲醛的降解效果,同时检测这 3种情况下尾气中的臭氧浓度.从图3可见,与纯 TiO2相比,Au/TiO2对甲醛的去除率稍有提高,从91.3%增加到93.6%.单纯Ti网时VUV尾气中臭氧浓度为22.2mg/m3,当在Ti网上负载TiO2时,臭氧下降为18.1mg/m3,去除率达到18.5%;当采用Au/TiO2时,臭氧去除率达到32.0%.这表明,在TiO2表面负载纳米 Au不仅能够提高有机物降解效率,而且显著降低真空紫外光产生的臭氧.
由图4(a)可见,反应前 Au4f7/2的结合能为83.44eV,比标准谱图中金属态Au4f7/2的结合能84.10eV有0.66eV的负偏差.这表明Au/TiO2表面的Au有一定程度的负电荷.除了Au的量子尺寸效应外[22],可能是因为Au/TiO2中的TiO2表面存在少量的Ti3+缺陷,此缺陷位上电子的逸出功小于纳米Au的逸出功,因此电子可以从Ti3+迁移到Au原子簇上,致使 Au/TiO2表面 Au4f7/2的结合能向低结合能方向移动[23].Au-TiO2催化剂在VUV下反应35h后,Au4f7/2的结合能没有变化,说明TiO2表面的Au仍然以金属态存在,催化剂性能在35h试验期内保持稳定.由图4(b)可见,VUV下反应 35h后的O1s与反应前相比,529.93eV和531.27eV两处峰强都有不同程度的增加,而且531.27eV处的小峰在反应后向高结合能方向移动了0.54eV.位于 529.93eV的O1s主峰接近于Ti-O键中O1s电子结合能(530.3eV).较大的电子结合能(531.27eV)来源于薄膜表面较松散结合的O,如 OH(O1s结合能为531.5eV)以及吸附的O2(533.3eV)[24].反应后529.93eV的峰增强,是由于TiO2表面晶格发生了重构而造成的[25].同时由于催化剂表面吸附了更多的H2O(O1s结合能为533eV)以及含氧的反应产物,531.27eV 处的峰移至较大结合能处(531.81eV),且强度也有所增加.由图4(c)可见,VUV下反应35h后的C1s在284.87eV处的峰强增加,同时C1s在 282.50、286.23、288.26eV分别出现了新的峰.结合O1s和C1s谱反应前后的变化可推断有甲醛分解产物在催化剂表面吸附.
综合以上实验结果,可认为Au/TiO2促进真空紫外光催化体系中臭氧分解的原因有以下2点:

图4 Au/TiO2在VUV反应35h前后的XPS谱Fig.4 XPS spectra of Au/TiO2 before and after 35h reaction under VUV irradiation
(1)Au纳米粒子促进臭氧的热催化分解.Oyama等[12]的研究表明,O3很容易被Mn2O3、TiO2等吸附并在其表面形成负氧离子.对于TiO2来说,其表面的Ti3+就是 O3分解的活性位,Ti4+是电子捕获中心[26].O3在 TiO2上只有一种活性吸附位,而在Au/TiO2催化剂上,Au也是臭氧分解的活性位.当纳米 Au颗粒分散在 TiO2表面时,Au簇和TiO2周界处是主要活性位[27],与电中性的Au相比,负载在TiO2表面带负电的纳米Au显然更容易成为吸附及催化分解臭氧的活性中心.
(2)Au纳米粒子促进臭氧在光催化下的分解.Lin等[15]和Ohtani等[28]研究发现,Ag/TiO2在室温暗态下分解O3时,Ag逐渐被氧化成AgO而使得臭氧分解效率降低;但在紫外光下Ag/TiO2的活性不变.他们提出,在光照条件下,光生电子把被臭氧氧化成的高价 Ag(AgO)还原为单质 Ag,从而使得Ag/TiO2保持长久的臭氧分解活性.对于Au/TiO2,负载在TiO2表面的Au是光生电子的捕获中心,Au的存在不仅使光生电子和空穴能够有效地分离,而且由于Au又是臭氧分解的活性中心,因此在Au捕获的光生电子正好与臭氧反应,所以氧化钛上的Au纳米粒子促进了臭氧的光催化分解.
3 结论
3.1 采用低温吸附法负载在TiO2薄膜的Au纳米颗粒分布均匀,呈单分散,平均粒径为(4.3±1.4)nm.
3.2 与TiO2/UV和VUV相比,TiO2/VUV能够显著提高甲醛降解效率,对甲醛的去除率达90%以上.在真空紫外光催化体系中,与TiO2相比,Au/TiO2对甲醛的去除率从91.3%增加到93.6%.
3.3 在真空紫外光照射下,TiO2表面负载纳米Au后,纳米Au颗粒成为吸附及催化分解臭氧的活性中心,在提高甲醛降解率的同时,还能显著降低VUV系统中的臭氧浓度,臭氧去除率达32%,催化剂性能在测试的35h内保持稳定.XPS测试也表明,Au4f7/2的结合能在反应前后没有变化.
[1]Yu H, Zhang K, Rossi C. Experimental study of the photocatalytic degradation of formaldehyde in indoor air using a nano-particulate titanium dioxide photocatalyst [J]. Indoor and Built Environment, 2007,16(6):529-537.
[2]Yang L P, Liu Z Y, Shi J W. Degradation of indoor gaseous formaldehyde by hybrid VUV and TiO2/UV processes [J].Separation and Purification Technology, 2007,54(2):204-211
[3]Huang X, Yuan J, Shi J W, et al. Ozone-assisted photocatalytic oxidation of gaseous acetaldehyde on TiO2/H-ZSM-5 catalysts [J].Journal of Hazardous Materrials, 2009,171(1-3):827-832.
[4]Li R H, Chen W X, Wang W. Magnetoswitchable controlled photocatalytic system using ferromagnetic Fe-0-doped titania nanorods photocatalysts with enhanced photoactivity [J].Separation and Purification Technology, 2009,66(1):171-176.
[5]Riassetto D, Holtzinger C, Langlet M. Influence of platinum nano-particles on the photocatalytic activity of sol-gel derived TiO2films [J]. Journal of Materials Science, 2009,44(10):2637-2646.
[6]孙梦君,柳丽芬,杨凤林.β-环糊精/Ce/TiO2光催化氧化气相甲苯[J]. 中国环境科学, 2008,28(7):593-598.
[7]Juyoung J, Kazuhiko S. Photodegradation of gaseus volatile organic compounds (VOCs) using TiO2photoirradiated by an ozone-producing UV lamp: decomposition characteristics,identification of by-products and water-soluble organic intermediates [J]. Journal of Photochemistry and Photobiology A:Chemistry, 2004,169(3):277-285.
[8]Zhang P Y, Liu J, Zhang Z L. VUV photocatalytic degradation of toluene in the gase phase [J]. Chemistry Letters, 2004,33(10):1242-1243.
[9]Zhao J, Yang X D. Photocatalytic oxidation for indoor air purification: a literature review [J]. Building Environment,2003,38(5):645-654.
[10]刘 栋,张彭义,王军伟.真空紫外光催化降解甲烷 [J]. 中国环境科学, 2006,26(6):653-656.
[11]孔琴心,刘广仁,李桂忱.近地面臭氧浓度变化及其对人体健康的可能影响 [J]. 气候与环境研究, 1999,4(1):61-66.
[12]Dhandapani B, Oyama S T. Gas phase ozone decomposition catalysts [J]. Applied Catalysis B-Environmental, 1997,11(2):129-166.
[13]Kubo W, Tatsuma T. Photocatalytic remote oxidation with various photocatalysts and enhancement of its activity [J]. Journal of Materials Chemistry, 2005,15(30):3104-3108.
[14]Seery M K, George R, Floris P. Silver doped titanium dioxide nanomaterials for enhanced visible light photocatalysis [J].Journal of Photochemistry and Photobiology A-Chemistry,2007,189(2/3):258-263.
[15]Lin Y C, Lin C H. Catalytic and photocatalytic degradation of ozone via utilization of controllable nano-Ag modified on TiO2[J]. Environmental Progress, 2008,27(4):496-502.
[16]Anandan S, Ashokkumar M. Sonochemical synthesis of Au-TiO2nanoparticles for the sonophotocatalytic degradation of organic pollutants in aqueous environment [J]. Ultrasonics Sonochemistry,2009,16(3):316-320.
[17]Kumar P S S, Sivakumar R, Anandan S. Photocatalytic degradation of Acid Red 88 using Au-TiO2nanoparticles in aqueous solutions [J]. Water Research, 2008,42(19):4878-4884.
[18]Dai W X, Chen X, Wang X X. CO Preferential oxidation promoted by UV irradiation in the presence of H2over Au/TiO2[J]. Physical Chemistry Chemical Physics, 2008,10(22):3256-3262.
[19]Zhang L, Zhang P Y, Chen S Z. Influence of pretreatment of titanium substrate on long-term stability of TiO2film [J]. Chinese Journal of Catalysis. 2007,28(4):299-306.
[20]傅平丰,张彭义.低温吸附制备Au-TiO2复合薄膜及其光电化学性质 [J]. 无机化学学报, 2009,25(11):2026-2030.
[21]室内环境空气质量监测技术规范 [M]. 北京:中国环境科学出版社, 2005:51-52.
[22]毛立群,冯彩霞,金振声.Au/TiO2的制备及其光催化氧化丙烯的研究 [J]. 感光科学与光化学, 2005,23(1):61.
[23]Arrii S, Morfin F, Renouprez A J, et al. Oxidation of CO on gold supported catalysts prepared by laser vaporization: Direct evidence of support contribution [J]. Journal of the American Chemical Society, 2004,126(4):1199-1205.
[24]Chan M H, Lu F H. Characterization of N-doped TiO2films prepared by reactive sputtering using air/Ar mixtures [J]. Thin Solid Films, 2009,518(5):1369-1372.
[25]Yang D M, He P K, Dong F, et al. Effect of water vapor at room temperature on photocatalytic decomposition of gaseous ozone over Au/TiO2[J]. Chinese Journal of Catalysis, 2006,27(12):1122-1126.
[26]贺攀科,杨建军,杨冬梅,等.Au/ TiO2光催化分解臭氧 [J]. 催化学报, 2006,27(1):71-74.
[27]He P K, Zhang M, Yang D M. Preparation of Au-loaded TiO2by photochemical deposition and ozonepHotocatalytic decomposition [J]. Surface Review and Letters, 2006,13(1):51-55.
[28]Ohtani B, Zhang S W, Ogita T, et al. Photoactivation of silver loaded on titanium (IV) oxide for room-temperature decomposition of ozone [J]. Journal of Photochemistry and Photobiology A-Chemistry, 1993,71(2):195-198.
