Al70−xSi30Mnx(x=0,3,7)过饱和固溶体的时效分解及其对电化学性能的影响
2010-01-04孙占波李雪鹏
李 倩,胡 青,孙占波,李雪鹏
(1. 西安交通大学 金属材料强度国家重点实验室,西安 710049;2. 西安交通大学 物质非平衡合成与调控教育部重点实验室,西安 710049)
在商用锂离子电池中,石墨由于其具有优异的充放电循环性能而被广泛使用,但由于其质量比容量很低,限制了电池容量的提高[1]。研究表明,Si、Sn、Sb等金属或类金属可得到比石墨高得多的比容量[2−5]。如果这些材料可代替石墨使用在锂离子电池中,容量将期望得到一个飞跃,这些金属因此被定义成对于锂的活性金属。但研究发现,这些材料在充锂过程中会与Li形成金属间化合物,材料的原始结构被改变;放锂时化合物分解,材料的结构又一次改变。但这些金属因不具备室温再结晶能力使其原始状态不能回复,导致材料的非晶化和粉化,充放电循环寿命远低于石墨的。因此,近20年关于锂离子电池负极材料的研究大多集中在如何提高这些金属的循环寿命上[5−8]。其中,在将纯金属制备成由活性金属和非活性金属组成的金属间化合物,降低材料的容量和减小体积膨胀方面进行了大量的研究[9−10],使得合金的循环性能有所改善,这些材料也因此定义成合金负极材料。
Al可与 Li形成 AlLi、Al2Li3和 Al4Li9化合物[11]。SURESH等[12]和卢普涛等[13]的研究显示,Li可嵌入纯Al,因此可视 Al为锂离子电池负极材料。其中,Al基合金薄膜负极材料表现出极高的质量比容量和优异的循环特性[14]。但研究显示,纯 Al充锂时也伴随有含锂化合物的形成[12−14],其晶体结构的演变依然是不可避免的。
熔体快淬可有效提高合金的过饱和度、细化微观组织[15]。最近,本文作者所在课题组采用熔体快淬法制备含30%和40%Si、不同含Mn量的Al-Si-Mn合金。结果表明,采用熔体快淬法制备的Al-Si-Mn合金,根据成分的不同其组成物可以为fcc-Al与α-Si、fcc-Al、α-Si和金属间化合物共存,并预测fcc-Al是Si和Mn在Al中的过饱和固溶体[16−17]。电化学测试结果显示,熔体快淬Al-Si合金表现出比Al和Si更好的电化学循环性能,而三元Al-Si-Mn则表现出比二元Al-Si优异得多的循环性 能[16−17]。上述工作为采用快淬法制备锂离子电池材料进一步提高熔体的性能打下了良好的基础。
为了研究熔体快淬 Al-Si-Mn合金的状态与电化学性能间的关系,分析充放锂机理和为进一步提高合金的电化学性能提供参考,本文作者首先对加热过程中快淬样品的相变进行实验分析。并在此基础上,选取Al67Si30Mn3和Al63Si30Mn7进行时效,分析合金状态对其电化学性能的影响。
1 实验
用纯度为 99.95%的铝、99.99%的硅和 99.95%的锰配制Al-Si-Mn合金。按比例精确称量以上原料,放入真空炉的坩埚中,抽真空至3×10−3Pa,在Ar气气氛下采用非消耗电极电弧熔炼法制备合金铸锭。将电弧熔炼后的合金铸锭放入底部带有直径为1 mm左右的小孔的石英管内。当高频感应加热将铸锭熔化并过热到要求的温度后,用5 μPa的Ar气将合金熔体从石英管底部小孔吹至冷却辊上制成薄带,薄带的宽度约为3 mm,厚度为30~50 µm。
采用NETZSCH STA449C综合热分析仪对样品进行示差扫描量热法(DSC)分析,加热速度为10 K/min,氩气保护,利用曲线相减法确定相变过程中的热效应;根据DSC分析结果确定时效温度,在真空热处理炉中对样品进行时效;采用Bruker D8 Advance X射线衍射仪(XRD)进行相分析;采用 Oxford INCA型能谱仪(EDS)分析相的元素组成;将不同状态的样品装配成模拟电池,采用Arbin BT2000电池测试仪对模拟电池进行电化学性能测试,其组装和测试方法在文献[16−17]中有详细描述。测试完成后,采用JEOL JSM−7000F型扫描电子显微镜(SEM)观察电极的形貌。
2 结果与分析
图 1所示为熔体快淬 Al70Si30、Al67Si30Mn3和Al63Si30Mn7合金的DSC曲线。由图1可看出,对于Al70Si30合金,DSC曲线上出现了2个放热峰,而对于Al67Si30Mn3和Al63Si30Mn7合金,则检测到3个放热峰,各合金加热过程中总放热量见表1。由表1可看出,随着Mn含量的增加,总放热量增加。
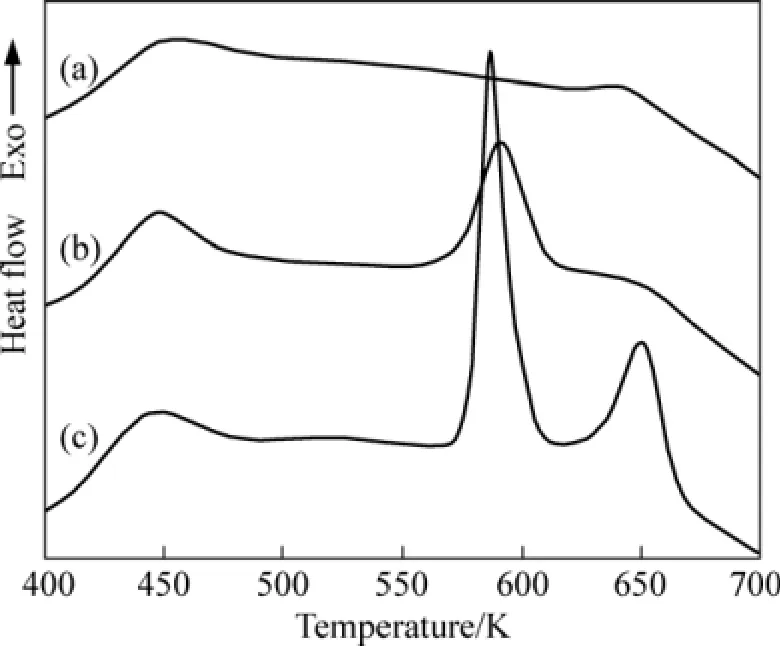
图1 快淬态Al70Si30、Al67Si30Mn3和Al63Si30Mn7合金的DSC曲线Fig.1 DSC curves of as-quenched Al70Si30 (a), Al67Si30Mn3 (b)and Al63Si30Mn7 (c) alloys

表1 熔体快淬Al-Si-Mn合金加热过程中的热效应Table 1 Heat releases of melt-spun Al-Si-Mn alloys during heating
为了判定上述放热过程所对应的相变以及相变过程是否可逆,将样品首先加热到一定温度后自由冷却至室温,再重新加热,为讨论方便问题,将首次加热到的最高温度标识为 TF。图 2所示为不同 TF的Al67Si30Mn3合金二次升温过程中的DSC曲线。快淬态的DSC曲线重新列于其中以便于比较。当TF=523 K时,DSC曲线上出现了2个放热峰(见图2(b)),低于500 K时,放热峰消失;当TF=593 K时,重新加热的样品仅在630~670 K出现1个放热峰(见图2(c)),而当TF=723 K的样品所有的放热峰均消失(见图2(d))。
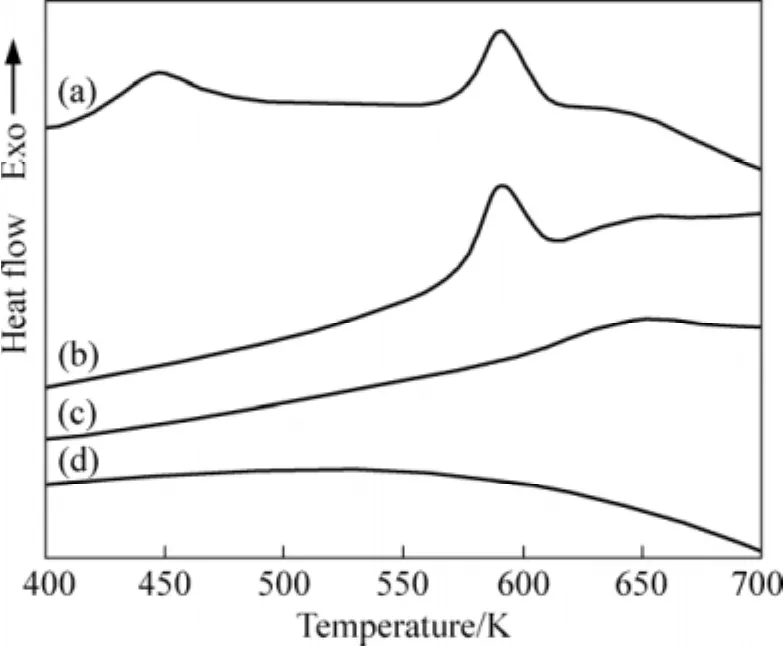
图2 Al67Si30Mn3合金的DSC曲线Fig.2 DSC curves of Al67Si30Mn3 alloy: (a) As-quenched; (b)TF=523 K; (c) TF=593 K; (d) TF =723 K
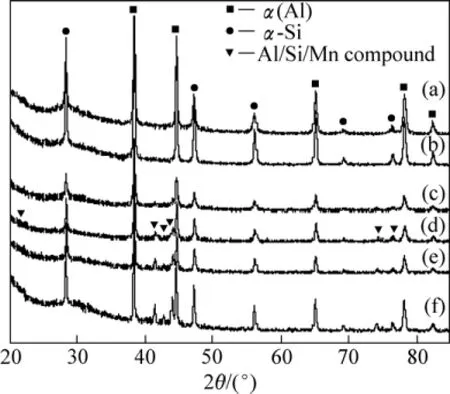
图 3 不同状态的熔体快淬 Al70Si30和 Al67Si30Mn3合金的XRD谱Fig.3 XRD patterns of Al70Si30 and Al67Si30Mn3 alloys at different states: (a) Al70Si30, TF=523 K; (b) Al70Si30, TF=673 K;(c) Al67Si30Mn3, TF=523 K; (d) Al67Si30Mn3, TF=573 K;(e) Al67Si30Mn3, TF=673 K; (f) Al67Si30Mn3, annealed at 673 K for 4 h
不同加热过程的样品X射线衍射分析结果如图3所示。对于Al70Si30合金,当TF分别为523 K和673 K时,样品的衍射特征与快淬态相比仅α-Si的相对衍射强度增大(见图3(a)和(b)),表明α-Si在这一温度段内析出。对于熔体快淬Al67Si30Mn3合金,当TF=523 K时,相变产物与Al70Si30区别不大(见图3(c)),表明低温放热主要为α-Si的析出。当TF=593 K时,可清晰地探测到图 3(d)中 Al/Si/Mn复合物的衍射峰。当TF=673 K时,其衍射特征与TF=593 K的样品无明显区别(见图3(e))。根据文献[18]的结果,Al-Si-Mn系可形成多个金属间化合物,因此上述特征可以确认,温度高于523 K的2个放热(见图2)主要对应于金属间化合物析出,且由于2个温度段的分解产物没有明显区别,表明化合物的析出也可分为2个阶段。
上述结果充分证明文献[16−17]的预测,快淬态的Al70−xSi30Mnx(x=0,3,7)为过饱和固溶体,加热过程中的相变对应于过饱和固溶体的分解。当 Si含量为30%时,Mn含量越高,放热量越多,合金偏离平衡态越远。
图4所示为不同状态的Al63Si30Mn7合金的XRD谱。由图 4可看出,除 α(Al)、α-Si之外,快淬态的Al63Si30Mn7合金中存在少量金属间化合物的衍射峰。快淬态样品在673 K时效4 h后,金属间化合物的衍射峰大幅度增强。结果还显示,熔体快淬Al63Si30Mn7合金加热分解后,含3%Mn和7%Mn的Al-Si-Mn合金在加热或时效过程中的相变类型和产物相近,只是Al63Si30Mn7中含有更多的金属间化合物。
根据2008年ASTM卡片,可以排除相变产物中包含 Al-Mn和 Si-Mn二元化合物的可能性。根据文献[18]报道的结果,550 ℃时,Al67Si30Mn3和Al63Si30Mn7平衡态下为 α(Al)、α-Si 和(τ9) (化学式Al14Mn4(Al,Si)5) 三相平衡,但 ASTM 中没有 τ9的标准衍射谱。能谱分析显示,该化合物的成分为67.29%Al、14.74%Si和 17.97%Mn(摩尔分数)。大致符合τ9的成分范围。这个结果可以确定其为Al-Si-Mn三元金属间化合物,但结构类型需要进一步分析。
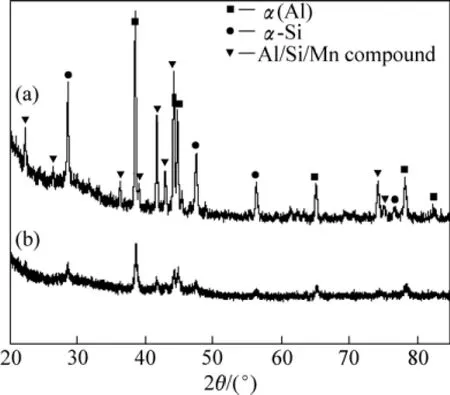
图4 不同状态的Al67Si30Mn7的XRD谱Fig.4 XRD patterns of Al67Si30Mn7 alloys at different states:(a) Annealed at 673 K for 4 h; (b) As-quenched[17]
图 5所示为时效对熔体快淬 Al70−xSi30Mnx(x=3,7)合金电化学循环性能的影响。由图5可看出,熔体快淬Al67Si30Mn3合金经673 K时效4 h后再经过10次循环后,放电比容量衰减到167 mA·h/g,但仍优于Al70Si30的;Al63Si30Mn7合金经673 K时效后再经过2次循环后,放电比容量即降为 124 mA·h/g。而Al67Si30Mn3和 Al63Si30Mn7快淬态样品[17]循环性能远优于时效样品的。经673 K时效的Al67Si30Mn3样品经历15次电化学循环和Al63Si30Mn7样品经历5次循环后,在SEM下均可观察到粉化现象(见图6)。而对于快淬态 Al-Si-Mn样品,经过多次循环也不会出现粉化[16−17]。
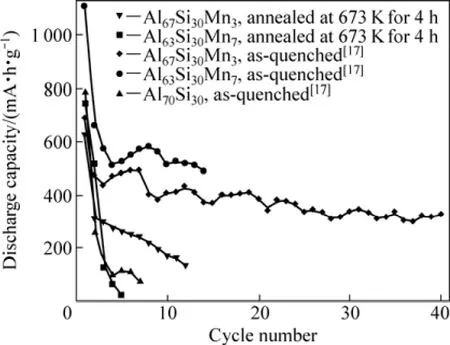
图 5 不同状态的熔体快淬 Al70Si30、Al67Si30Mn3和Al67Si30Mn7合金的循环性能曲线Fig.5 Cycle property curves of annealed and as-quenched[17]Al70Si30, Al67Si30Mn3 and Al67Si30Mn7 alloys
3 讨论
根据Al-Si二元相图[11],在平衡态下,Si在fcc-Al中的饱和溶解度不超过2%。熔体快淬Al70Si30合金在加热过程中出现了 2个放热峰,表明熔体快淬使 Si在Al中的溶解度明显增加。对于Al-Si-Mn三元系,823 K时,fcc-Al的饱和溶解度不大于 0.4%Si和0.07%Mn(摩尔分数)[18]。经过熔体快淬,合金加热过程中系统的放热量较Al70Si30二元合金明显增加(见图1),表明Si和Mn的协同作用可大幅度提高各自在Al基过饱和固溶体中的过饱和度,使体系偏离平衡态更远。这些结果符合合金组元相互作用以及熔体快淬制备样品的一般规律。

图6 经673 K时效4 h后Al67Si30Mn3和Al63Si30Mn7合金负极的SEM像Fig.6 SEM images of Al67Si30Mn3 and Al63Si30Mn7 alloy anodes annealed at 673 K for 4 h: (a) Al67Si30Mn3, 15 cycles; (b)Al63Si30Mn7, 5 cycles
图 1所示的结果显示,熔体快淬 Al70Si30和Al67Si30Mn3中α-Si的析出开始温度基本相同,表明加入Mn没有对α-Si的起始析出温度产生明显影响。尽管在低温时有一部分Si原子从过饱和固溶体中析出,但由于Mn的作用,依然有大量的Si原子固溶于Al基过饱和固溶体,使合金的高过饱和度可保持在更高的温度,即Mn有效地稳定了Al-Si-Mn过饱和固溶体。
实验结果显示,随着温度的升高,熔体快淬二元Al70Si30合金中α-Si的析出分为2个阶段。对于熔体快淬Al67Si30Mn3和Al63Si30Mn7合金,化合物的析出也分为2个阶段。尽管其机制有待进一步分析,但根据上述现象可以推测,当Al-Si二元系和Al-Si-Mn三元系过饱和固溶体的过饱和度达到一定值时,过饱和固溶体的分解对过饱和度有强烈的依赖关系,过饱和度下降到一定值后,分解趋缓。只有当温度足够高时,热激活促使其状态进一步快速向平衡态接近。
时效后,形成α(Al)、α-Si和Al/Si/Mn三元化合物,系统接近平衡态,此时,充放电循环过程中合金极片发生粉化(见图6),合金放电比容量随循环次数的增加快速衰减(见图5)。根据已有的研究结果[13−14]可推测,熔体快淬Al67Si30Mn3和Al63Si30Mn7合金时效分解产物中的一个相或几个相在充放锂过程中发生结构演变。
上述分析表明,熔体快淬Al-Si-Mn合金的电化学性能强烈地依赖于合金的状态。当合金为热力学非平衡态的过饱和固溶体时,具有良好的充放电循环性能;当合金时效后过饱和固溶体分解,粉化现象发生,电化学性能严重劣化。
4 结论
1) 熔体快淬得到的Si、Mn在fcc-Al中的过饱和固溶体,在加热过程中过饱和固溶体发生分解,析出α-Si 和Al/Si/Mn三元化合物。
2) 将Mn加入熔体快淬Al-Si合金中,会大幅度提高Al基固溶体的过饱和度,同时过饱和固溶体更稳定。
3) 熔体快淬 Al-Si-Mn合金的电化学性能强烈地依赖于合金的状态,过饱和固溶体分解后,电池极片在充放锂过程中会发生粉化,合金的电化学循环性能下降。
[1] MENACHEM C, PELED E, BURSTEIN L, ROSENBERG Y.Characterization of modified NG7 graphite as an improved anode for lithium-ion batteries[J]. J Power Sources, 1997, 68:277−282.
[2] 赵吉诗, 何向明, 万春荣, 姜长印. 锂离子电池硅基负极材料研究进展[J]. 稀有金属材料与工程, 2007, 36(8): 1490−1494.
ZHAO Ji-shi, HE Xiang-ming, WAN Chun-rong, JIANG Chang-yin. Research progress in silicon based anode materials for lithium-ion batteries[J]. Rare Metal Materials and Engineering, 2007, 36(8): 1490−1494.
[3] TAMURA N, OHSHITA R, FUJIMOTO M, FUJITANI S,KAMINO M, YONEZU I. Study on the anode behavior of Sn and Sn-Cu alloy thin-film electrodes[J]. J Power Sources, 2002,107: 48−55.
[4] WANG Y, LEE J Y, DEIVARAI T. Tin nanoparticle loaded graphite anodes for Li-ion battery applications[J]. J Electrochem Soc, 2004, 151(11): A1804−A1809.
[5] DONG H, AI X P, YANG H X. Carbon/Ba-Fe-Si alloy composite as high capacity anode materials for Li-ion batteries[J].Electrochem Commun, 2003, 5: 952−957.
[6] 樊小勇, 庄全超, 江宏宏, 黄 令, 董全峰, 孙世刚. 锂离子电池三维多孔Cu6Sn5合金负极材料的制备及其性能[J]. 物理化学学报, 2007, 23(7): 973−977.
FAN Xiao-yong, ZHUANG Quan-chao, JIANG Hong-hong,HUANG Ling, DONG Quan-feng, SUN Shi-gang. Threedimensional porous Cu6Sn5alloy anodes for lithium-ion batteries[J]. Acta Phys-Chim Sin, 2007, 23(7): 973−977.
[7] 曹高劭, 李 涛, 朱铁军, 吕春萍, 赵新兵. Zn4Sb3的电化学吸放锂特性[J]. 有色金属, 1999, 51(4): 68−70.
CAO Gao-shao, LI Tao, ZHU Tie-jun, LÜ Chun-ping, ZHAO Xin-bing. Electrochemical lithiuate/delithiuate properties of Zn4Sb3[J]. Nonferrous Metals, 1999, 51(4): 68−70.
[8] 文钟晟, 谢晓华, 王 可, 杨 军, 解晶莹. 锂离子电池中高容量硅铝/碳复合负极材料的制备与性能研究[J]. 无机材料学报, 2005, 20(1): 139−143.
WEN Zhong-sheng, XIE Xiao-hua, WANG Ke, YANG Jun, XIE Jing-ying. High capacity SiAl/C anode material for lithium-ion batteries[J]. J Inorganic Materials, 2005, 20(1): 139−143.
[9] KEPLER K D, VAUGHEY J T, THACKERAY M M. LixCu6Sn5(0<x<13): An intermetallic insertion electrode for rechargeable lithium batteries[J]. Electrochem Solid-State Letter, 1999, 2:307−309.
[10] HATCHARD T D, OBROVAC M N, DAHN J R.Electrochemical reaction of the Si1−xZnxbinary system with Li[J].J Electrochem Soc A, 2005, 152(12): 2335−2344.
[11] OKAMOTO H. Phase diagrams for binary alloys[M]. Detroit:ASM International, 2000: 35.
[12] SURESH P, SHUKLA A K, SHIVASHANKAR S A,MUNICHANHRAIAH N. Electrochemical behaviour of aluminium in non-aqueous electrolytes over a wide potential range[J]. J Power Sources, 2002, 110: 11−18.
[13] 卢普涛, 谢 维, 苏玉长. 金属 Al作为锂离子二次电池负极材料的制备和机理研究[J]. 矿业工程, 2005, 25(6): 90−92.
LU Pu-tao, XIE Wei, SU Yu-chang. Mechanism and preparation of aluminum anode material for lithium ion secondary batteries[J]. Mining and Metallurgical Engineering, 2005, 25(6):90−92.
[14] HAMON Y, BROUSSE T, JOOUSSE F, TOPART P, BUVAT P,SCHLEICH D M. Aluminum negative electrode in lithium ion batteries[J]. J Power Sources, 2001, 97/98: 185−187.
[15] 周 轩, 孙占波, 王宥宏, 宋晓平, 朱蕊花. 熔体快淬Cu100−XCrX合金过饱和固溶体的时效分解及对电阻率的影响[J]. 中国有色金属学报, 2005, 15(6): 935−939.
ZHOU Xuan, SUN Zhan-bo, WANG You-hong, SONG Xiao-ping,ZHU Rui-hua. Separation of supersaturation solid solution and effects on resistivity in melt-spun Cu100−XCrXribbons[J]. The Chinese Journal of Nonferrous Metals, 2005,15(6): 935−939.
[16] SUN Z B, WANG X D, LI X P, ZHAO M S, LI Y, ZHU Y M,SONG X P. Electrochemical properties of melt-spun Al-Si-Mn alloy anodes for lithium-ion batteries[J]. J Power Sources, 2008,182: 353−358.
[17] SUN Z B, LI X P. Melt-spun Al70−XSi30MnX(X=0, 3, 5, 7, 10)anode in lithium ion batteries[J]. Science in China E, 2009, 52(8):2288−2294.
[18] DU Y, SCHUSTER J C, WEITZER F, KRENDELSBERGER N,HUANG B, JIN Z, GONG W, YUAN Z, XU H. A thermodynamic description of the Al-Mn-Si system over the entire composition and temperature ranges[J]. Metall Mater Trans A, 2004, 35: 1613−1628.
