热休克蛋白70在赛来昔布联合热疗治疗胰腺癌中的作用
2009-11-28刘丽燕王兴鹏姜立新吴恺杨佳芳
刘丽燕 王兴鹏 姜立新 吴恺 杨佳芳
热休克蛋白70在赛来昔布联合热疗治疗胰腺癌中的作用
刘丽燕 王兴鹏 姜立新 吴恺 杨佳芳
热休克蛋白(HSP) 又被称为是“伴侣蛋白”,它在细胞生长、发育、分化、基因转录等功能方面发挥重要作用,在多种肿瘤细胞表面都有它过度表达的现象[1]。近年来的研究发现,HSP参与机体特异的抗肿瘤免疫反应[1],且HSP表达量与肿瘤免疫原性强弱密切相关[2],与肿瘤的恶性程度及患者的预后密切相关[3]。
我们前期的研究证实,热疗联合赛来昔布可抑制胰腺癌细胞增殖,抑制移植瘤的生长[4]。本文报道HSP70在热疗联合赛来昔布治疗胰腺癌中所起的作用。
一、材料与方法
1.HSP70蛋白检测:人胰腺癌细胞株SW1990细胞常规培养后分为4组:对照组、热疗组、赛来昔布组及热疗联合赛来昔布组(联合组)。处理方法同我们以前报道[4]。热疗为细胞置44℃ 1 h,赛来昔布终浓度为100 μmol/L。培养24 h后胰酶消化,离心收集各组细胞,提取总蛋白,行Werstern blotting。以β-actin作为内参。小鼠抗人HSP70单抗1∶200稀释,小鼠抗人β-actin单抗1∶200稀释。
2.HSP70 mRNA检测:收集上述各组细胞,常规提取总RNA。按逆转录聚合酶链式反应试剂盒说明书操作。引物序列:HSP70上游5′-CAGGTGATCAACGACGGAGACA-3′,下游5′-GTCGATCGTCAGGATGGACACG-3′,扩增片段365 bp;内参GAPDH上游5′-GTGAAGGTCGGAGTCAACG-3′,下游5′-GGTGAAGACGCCAGTGGACTC-3′,扩增片段223 bp。先逆转录获得cDNA,后行PCR反应。PCR参数:94℃预变性3 min,95℃变性30 s,55℃(HSP70)或58℃(GAPDH)30 s,72℃延伸1 min。25个循环后,72℃延伸5 min。PCR反应产物置1.5%琼脂糖凝胶电泳。采用美国GeneGenius凝胶电泳成像系统观测,实验重复3次。
3.移植瘤组织HSP70蛋白表达的检测:裸鼠胰腺癌移植瘤制备及分组同我们以前报道[4]。实验结束后处死裸鼠取移植瘤组织,常规固定、包埋、切片、免疫组化染色,光镜下观察。
4.移植瘤组织HSP70 mRNA 检测:收集上述各组移植瘤组织,常规抽提总mRNA,同上述RT-PCR方法检测HSP70 mRNA表达,以GAPDH为内参。
二、结果
1.SW1990细胞HSP70 mRNA和蛋白的表达:各组均有HSP70mRNA和蛋白的表达,但热疗组和联合组较赛来昔布组及对照组增强(图1、2)。
2.裸鼠移植瘤组织HSP70 mRNA和蛋白的表达:各组肿瘤组织均见HSP70 mRNA和蛋白的阳性表达,其中热疗组和联合组的表达明显强于对照组和赛来昔布组(图3、4)。

图1对照组(1)、赛来昔布组(2)、热疗组(3)和联合组(4)SW1990细胞HSP70 mRNA的表达

图2对照组(A)、赛来昔布组(B)、热疗组(C)和联合组(D)SW1990细胞HSP70蛋白的表达

图3对照组(1)、赛来昔布组(2)、热疗组(3)和联合组(4)裸鼠移植瘤HSP70 mRNA的表达
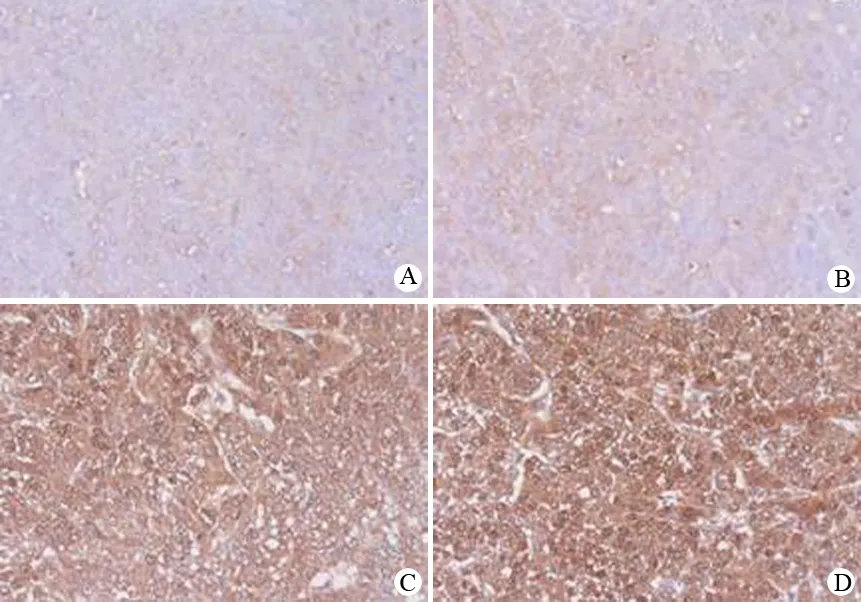
图4对照组(A)、赛来昔布组(B)、热疗组(C)和联合组(D)移植瘤组织HSP70蛋白表达(免疫组化 ×400)
讨论近年来的研究显示,HSP70与抗肿瘤活性密切相关,其免疫机制表现为[5]:(1)HSP70与肿瘤细胞内的特异性抗原肽结合形成多肽复合物,通过抗原提呈细胞 (树突状细胞、巨噬细胞)表面的特异性高亲和受体,介导抗原肽进入抗原提呈细胞,与胞内MHC分子形成复合物,并在抗原提呈细胞表面呈现,被α、βT细胞识别,激发抗肿瘤细胞特异性反应。HSP70还可以促进Th细胞向Thl细胞转化,调整肿瘤患者机体的免疫状态;(2)通过激活CTL(CD8+)细胞杀伤肿瘤细胞;(3)NK细胞无需致敏、补体激活和抗原诱导,可以通过识别MHC类样分子(如HSP70家族蛋白)而发挥作用,还可以通过细胞毒性作用杀伤一些肿瘤细胞[6];(4)HSP70可作为抗原递呈分子,将肿瘤抗原呈递到细胞表面,使γ、δT细胞活化,从而发挥杀伤细胞效应;(5)通过诱导PBMCs和γ、δT细胞产生多种细胞因子(如TNF-α、IL-1β、IL-2、IL-8、IFN-γ)达到抑制肿瘤细胞生长及杀伤肿瘤细胞的目的[7];(6)HSP70还可以活化补体系统,发挥抗肿瘤的作用。
本研究结果显示,热疗组和热疗联合赛来昔布组HSP70mRNA和蛋白的表达较赛来昔布组及对照组明显上调。因HSP表达量多少与肿瘤免疫源性强弱密切相关[2],HSP表达越多,其免疫源性越强,则其诱导的机体免疫反应相应越明显,提示在热疗组和联合组中HSP70的高表达通过上述机制诱导的机体免疫反应也相对更强,这可能是赛来昔布对胰腺癌热疗协同杀伤作用的一个机制。
[1] Kramer G,Steiner GE,Grobl M,et al.Response to sublethal heat treatment of prostatic tumor cells and of prostatic tumor infiltrating T-cells.Prostate,2004,58:109-120.
[2] Melcher A,Todryk A,Hardwick N,et al.Tumor immumogenicity is determined by the mechanism of cell death via induction heat shock protein expression.Nat Med,1998,4:581-587.
[3] 王群伟,杨竹林,李永国,等.胰腺癌细胞中HSP70和HSP60表达及意义.中华中西医杂志,2003,4:10-11.
[4] 刘丽燕,王兴鹏,姜立新,等.赛来昔布联合热疗治疗胰腺癌的研究.中华胰腺病杂志,2008,8:31-34.
[5] Ciupitu AM,Petersson M,Kono K,et al.Immunization with heat shock protein 70 from methlcholanthrene-induced sarcomas induces tumor protection correlating with in vitro T cell response.Cancer Immunol Immunother,2002,51:163-170.
[6] Casey DG,Lysaght J,James T,et al.Heat shock protein derived from a non-autologous tumour can be used as an anti-tumour vaccine.Immunology,2003,110:105-111.
[7] 王笑虹,苗迎秋,宋光.热休克蛋白70生物学功能研究的新进展.大连大学学报,2003,24:103-105.
2008-08-29)
(本文编辑:屠振兴)
10.3760/cma.j.issn.1674-1935.2009.02.017
200080 上海,上海交通大学附属第一人民医院消化科(刘丽燕、吴恺、杨佳芳);同济大学医学院附属第十人民医院消化科(王兴鹏);上海交通大学附属第六人民医院B超室(姜立新)
王兴鹏,Email:xpwcn@public7.sta.net.cn
