含氟芳香查尔酮衍生物的合成与三阶非线性光学性质
2025-02-14王桂林郝建峰石玉芳王迎进赵明根
摘要 合成4种查尔酮衍生物: 1-(2,3-二氟苯基)-3-(3-氯噻吩-2-基)-2-丙烯-1-酮(0208#)、1-(2,4-二氟苯基)-3-(5-苯基噻吩-2-基)-2-丙烯-1-酮(0809#)、1-(2,3-二氟苯基)-3-(5-苯基噻吩-2-基)-2-丙烯-1-酮(0808#)和1-(2,6-二氟苯基)-3-(5-苯基噻吩-2-基)-2-丙烯-1-酮(0812#)。 通过核磁共振氢谱(1H NMR)和碳谱(13C NMR)、液相色谱-质谱联用质谱(LC-MS)、紫外-可见吸收光谱(UV-Vis)、荧光发射(EM)光谱和Z-扫描技术对化合物的结构和性质进行了表征。 采用密度泛函理论方法计算获得了该4种化合物的最高占据分子轨道与最低空分子轨道能量和极化率,从轨道电子云图发现存在显著的分子内电荷转移现象。 大π共轭和电荷转移的结构效应使这4种芳香基查尔酮衍生物表现出良好的三阶非线性光学性质。 它们可作为非线性吸收(NLA)和激光防护候选材料,具有潜在应用前景。
关键词 查尔酮衍生物;理论计算;光学性质
中图分类号:O625. 4 文献标识码:A 文章编号:1000-0518(2025)01-0086-09
山西省忻州市科学技术局项目(No. 20230511)资助
随着超快激光器的快速发展和广泛应用,超短脉冲激光的有效衰减对脆弱探测器的激光保护至关重要,这给新型激光吸收材料的研究带来了新的挑战[1]。 有机非线性吸收(NLA)材料由于其独特的π共轭结构产生极大的非线性吸收而得到了广泛的研究,如酰胺基衍生物、乙烯链化合物和四苯基衍生物等[2-5]。 有机材料线性透过率高,非线性吸收系数大; 同时,该类材料能够在分子水平上改变光学性质,不同的科研人员以不同的思路和策略,利用不同结构的有机材料如供体(D)-π-受体(A)、D-π-D和A-π-A等,来增强材料的非线性吸收光学效应[6-7]。 在几种类型的有机化合物中,查尔酮衍生物因其高损伤阈值、高非线性光学系数和高合成柔韧性而备受关注[8-9]。 此外,由于推-拉构型,从D/A取代查尔酮衍生物结构能够预期提高NLA活性[10-11],并可通过更换不同的D/A基团以增加共轭桥长度来增强查尔酮的NLA行为[12-15]。 Nayak等[16]报告了3种基于多环芳烃 (PAH) 的苯并[e]芘衍生物的非线性吸收光学特性的结果,3种分子均表现出强烈的反饱和吸收。 Vinaya等[17]采用溶剂蒸发法制备了查尔酮衍生物4-[(1E)-3-(4-甲氧基苯基)-3-氧丙基-1-烯-1-基]-4-甲基苯-1-磺酸盐(4MPMS),发现非线性光学吸收系数和三阶非线性光磁化率值均大于其他查尔酮衍生物晶体的相应值。
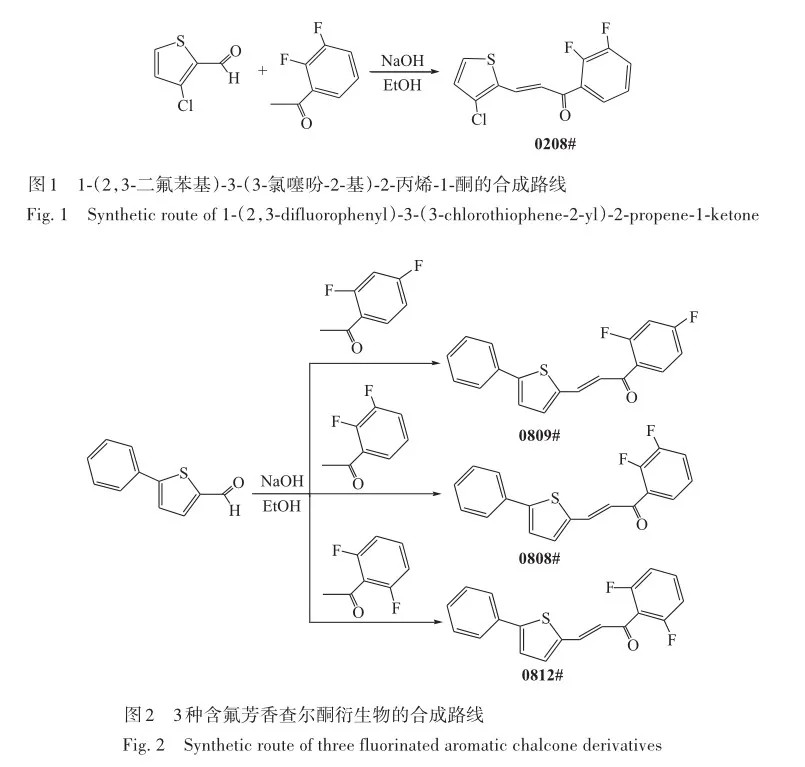
国内也有较多的专家学者进行非线性光学材料方面的研究,如Shen等[18]报道了2个双查尔酮分子1,4-二[3(-2,4-二甲氧基苯基)-2-丙烯基]苯和4,4′-二[3-(2,4-二甲氧基苯基)-2-丙烯基]联苯,分别采用飞秒开孔Z-扫描和光强相关透射率测量研究了其宽带非线性吸收特性和光限响应,结果表明可以通过分子内电荷转移来增强双查尔酮化合物的非线性光学响应和激发态动力学。 Yang等[19]通过Z-扫描方法研究了2个双查尔酮分子的三阶光学非线性,进一步拓展查尔酮衍生物在非线性光学中的应用潜力,并提供了一种调整此类材料光学非线性的方法。 Wang等[20]报道了2种新的供体(D)/受体(A)交替体系芳香查尔酮衍生物,Z-扫描实验表明,2种化合物均有从饱和吸收到反饱和吸收的转变和自散焦效应。 Sun等报道[21]了4种新型芘基查尔酮衍生物,在4 ns、460 nm时表现出较好的三阶非线性吸收和折射,并有较大的分子极化率。 Shi等[22]报道了2种芘基查尔酮衍生物,研究表明典型的分子内电荷转移(ICT)对超快非线性光学(NLO)吸收有明显影响,飞秒Z-扫描实验表明这些芘衍生物具有显著的超快NLO吸收性能; 其光物理机制为单光子吸收(OPA)。 此外,石玉芳课题组还研究了芘基、噻吩基等芳香双查尔酮衍生物,它们的非线性吸收性能优于许多由苯单元组成的类衍生物和双查尔酮衍生物[23-25]; 实验和理论计算结果均表明,改变有机分子的D-A交替可以有效地调节三阶非线性光学行为,这可能为未来的分子设计提供指导。 本课题组新近合成了4种不同位置供体芳香查尔酮衍生物,合成方案如图1和图2所示。 4种化合物均具有有利的离域π电子,扩大了分子结构的π共轭体系,并提供了更多的离域电子,期望在非线性吸收性能和激光防护应用方面能有新的突破。
1 实验部分
1. 1 仪器和试剂
WRS-1B型数字熔点仪(中国上海精密科学仪器有限公司,温度未校正);Advanced Ⅲ型核磁共振仪(NMR,瑞士Bruker Biospin公司);LC-MS8030型液相色谱-质谱联用仪(LC-MS,ESI离子源,日本岛津公司);UV-2550型紫外-分光光度计(UV-Vis,日本岛津公司);F-4600型荧光光谱仪(日本日立公司);Nd∶YAG[NT 342B]型可调谐激光器(立陶宛EKSPLA公司)。
5-苯基噻吩-2-甲醛、2,3-二氟苯乙酮、2,4-二氟苯乙酮和2,6-二氟苯乙酮均购自JK Chemical试剂公司,纯度均为分析纯。 无水乙醇、氢氧化钠(NaOH)、乙酸乙酯和石油醚(60~90 ℃),均为分析纯试剂,购自天津永大化学试剂厂。
1. 2 4种含氟芳香查尔酮衍生物的合成通法
将3. 0 mmol 5-苯基噻吩-2-甲醛/3-氯噻吩-2-甲醛和3. 0 mmol的二氟苯乙酮加入到100 mL三颈烧瓶中,再加入50 mL无水乙醇并搅拌溶解,然后向反应混合液中滴加2 mL质量分数5%的NaOH水溶液,在室温下继续搅拌,反应液中逐渐出现黄色沉淀。 薄层色谱(TLC)跟踪反应进程(V(乙酸乙酯)∶V(石油醚)=1∶5~1∶15),在室温下继续搅拌反应1. 5~3. 0 h,大量黄色固体析出。 减压抽滤,用无水乙醇洗涤滤饼3次,得纯品。
0208#: 0. 66 g,产率78%; mp: 88. 5~88. 8 ℃。 1H NMR(600 MHz,DMSO-d6),δ: 7. 955(s,1H),7. 772~7. 745(d,1H,J=16. 2 Hz,alkene-H),7. 717~7. 703(d,1H,J=8. 4 Hz),7. 622(s,1H),7. 379(s,1H),7. 269(s,1H),7. 261~7. 234(d,1H,J=16. 2 Hz,alkene-H); 13C NMR(150 MHz,DMSO-d6),δ: 187. 04;151. 31,151. 23;149. 78,149. 68,149. 59;148. 10,148. 01;133. 59;132. 38;131. 36;130. 07;129. 74;128. 87,128. 81;126. 00,125. 98,125. 83,125. 80,125. 79,125. 76,125. 27,125. 24;121. 82;121. 71。LC-MS(ESI),m/z: C13H8ClF2OS([M+H]+)实测值: 285. 00; 理论值284. 98。 绝对误差: 0. 02; 相对误差:0. 07‰。
0809#: 0. 79 g,产率81%,mp: 114. 9~115. 3 ℃。 1H NMR(600 MHz,DMSO-d6),δ: 7. 914~7. 900(d,1H,J=8. 4 Hz),7. 889~7. 875(d,1H,J=8. 4 Hz),7. 866~7. 841(d,1H,J=15. 0 Hz,alkene-H),7. 754~ 7. 741(d,1H,J=7. 8 Hz),7. 693~7. 687(d,1H,J=3. 6 Hz),7. 637~7. 631(d,1H,J=3. 6 Hz),7. 482~7. 469(d,1H,J=7. 8 Hz),7. 453~7. 438(d,1H,J=9. 0 Hz),7. 435~7. 405(d,1H,J=18. 0 Hz),7. 392~7. 380(d,1H,J=7. 2 Hz),7. 281~7. 253(t,1H,J=8. 4 Hz),7. 146~7. 121(d,1H,J=15. 0 Hz,alkene-H); 13C NMR(150 MHz,DMSO-d6),δ: 186. 95;148. 01;139. 01;137. 93;135. 78;133. 32;133. 09,133. 02;129. 77;129. 28;126. 24;125. 85;123. 85;112. 91;112. 79;105. 75;105. 57;105. 39。 LC-MS(ESI),m/z:C19H13F2OS([M+H]+)实测值: 327. 00; 理论值: 327. 07。 绝对误差: 0. 07; 相对误差: 0. 21‰。
0808#: 0. 78 g,产率79. 6%,mp: 84. 7~85. 2 ℃。 1H NMR(600 MHz,DMSO-d6),δ: 7. 873~7. 847(d,1H,J=15. 6 Hz,alkene-H),7. 756~7. 742(d,1H,J=8. 4 Hz),7. 742~7. 714(d,1H,J=16. 8 Hz,alkene-H),7. 707~7. 690(d,1H,J=10. 2 Hz),7. 646~7. 639(d,1H,J=4. 2 Hz),7. 598~7. 581(d,1H,J=10. 2 Hz),7. 579~7. 569(d,1H,J=6. 0 Hz),7. 486~7. 473(d,1H,J=7. 8 Hz),7. 473~7. 460(d,1H,J=7. 8 Hz),7. 409~ 7. 385(t,1H,J=7. 2 Hz),7. 377~7. 363(t,1H,J=4. 2 Hz),7. 130~7. 101(q,1H,J=5. 8 Hz); 13C NMR(150 MHz,CDCl3),δ: 187. 11;148. 76;139. 11;138. 08;134. 23;133. 43;129. 12;128. 72;126. 09;125. 41;124. 48;124. 45;124. 38;123. 39;123. 34;120. 71;120. 59。 LC-MS(ESI),m/z: C19H13F2OS([M+H]+)实测值:327. 05; 理论值: 327. 07。 绝对误差: 0. 02; 相对误差: 0. 06‰。
0812#: 0. 76 g,产率77. 6%,mp: 130. 7~131. 1 ℃。 1H NMR(600 MHz,DMSO-d6),δ: 7. 743~7. 729(t,1H,J=2. 4 Hz),7. 720~7. 694(d,1H,J=15. 6 Hz,alkene-H),7. 659~7. 657(d,1H,J=1. 2 Hz),7. 646~ 7. 632(d,1H,J=8. 4 Hz),7. 630~7. 626(d,1H,J=2. 4 Hz),7. 626~7. 623(d,1H,J=1. 8 Hz),7. 480~7. 455(t,2H,J=7. 5 Hz),7. 408~7. 383(m,1H,),7. 287~7. 274(d,1H,J=7. 8 Hz),7. 274~7. 260(d,1H,J=8. 4 Hz),6. 889~6. 863(d,1H,J=15. 6 Hz,alkene-H); 13C NMR(150 MHz,DMSO-d6),δ: 187. 10;160. 32,160. 25;158. 65,158. 60;149. 03;140. 30;138. 38;136. 27;133. 41,133. 34,133. 27,133. 23;129. 78;129. 40;126. 28;125. 97;125. 62;117. 43;112. 95,112. 92,112. 81,112. 78。 LC-MS(ESI),m/z: C19H13F2OS([M+H]+)实测值: 327. 10; 理论值: 327. 07。 绝对误差: 0. 03; 相对误差: 0. 09‰。
2 结果与讨论
2. 1 结构表征
化合物0208#、0809#、0808#和0812#的结构由1H NMR(600 MHz,DMSO-d6)、13C NMR(150 MHz,DMSO-d6)和LC-MS(ESI)m/z表征。 质子种类及个数与设计分子吻合; 由于分子中均含有2个F原子,对碳谱的测定产生干扰,使之出现碳峰的裂分而出现多重谱峰[26]; 0808#样品因溶解性较差导致碳峰种类缺少3个,更换氘代氯仿作溶剂重新测得碳谱,碳峰数与样品分子所含碳原子种类数一致; LC-MS显示,误差极小; 综合分析可认定合成的化合物与设计的目标化合物一致。 其核磁共振氢谱、碳谱和液-质联用质谱参见辅助材料图S1-S12。
2. 2 紫外-可见吸收光谱和荧光发射光谱
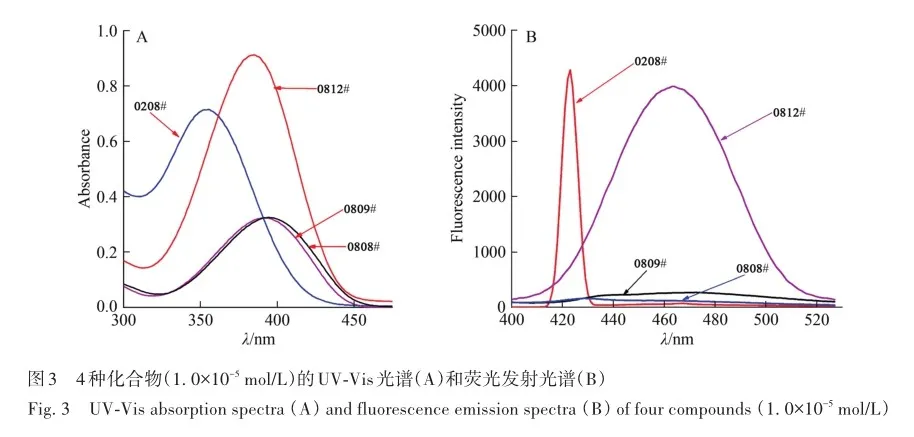
室温条件下,4种化合物样品浓度为1. 0×10-5 mol/L的二氯甲烷(DCM)溶液的UV-Vis光谱和荧光发射光谱如图3所示。
由图3A可知,4种化合物最大吸收波长(λmax)分别为355 nm(0208#)、391 nm(0808#)、394 nm(0809#)和385 nm(0812#); 相应的摩尔消光系数分别为7. 15×104、3. 24×104、3. 25×104和9. 13×104 L/(mol·cm)。
电子跃迁的难易取决于前线分子轨道间的能隙大小。 能隙越小,电子越容易跃迁,相应的紫外吸收波长也越长。 4种化合物紫外最大吸收波长由大到小依次是394 nm(0809#)、391 nm(0808#)、385 nm(0812#)和355 nm(0208#),反映或预示着它们前线分子轨道间能隙(ΔELUMO - HOMO)的大小及变化情况,这可由理论计算结果获得印证。 从分子结构来看,0809#分子中苯环上的2个F原子处于查尔酮基(—C== C—C== O)的邻、对位,显示了最强的拉电子效应,分子极化程度较大,使得电子跃迁变得更为容易,因而在4种化合物中它的紫外吸收波长最长(394 nm)。 而在0208#分子中,噻吩环上的氯原子由于主要显示拉电子的诱导效应,反而减弱了分子的极化,电子跃迁变难,它的紫外吸收波长在4种化合物中是最短(355 nm)。 另外,分子的共平面性越好,紫外吸收越长。 0208#、0812#的共平面性较差导致吸收波长较短。 4种化合物的紫外最大吸收峰波长范围均低于450 nm,表明它们在可见光区具有良好的透明度。 此外,紫外吸收范围小于532 nm,不影响Z-扫描测定。
由图3B可明显看出,4种化合物的荧光强度差别较大,0808#、0809#两化合物几乎无荧光,0208#、0812#的相对荧光强度较强,分别为4285和3987,对应的最大发射波长分别为364和464 nm。 影响荧光及强度的主要因素有跃迁类型、共轭效应、分子的刚性结构和取代基效应,具有π-π*及n-π*跃迁结构的分子才会产生荧光,而且π-π*跃迁的量子效率比n-π*跃迁的要大得多。 上述4种化合物分子在跃迁类型、共轭效应和取代基效应3方面基本一样,唯有分子的刚性差异较大。 理论计算表明:0208#、0812#分子非共平面,具有较强的刚性。 而分子刚性越强,分子振动越少,与其他分子碰撞失活的机率下降,荧光量子效率提高[28]。 这可能是造成荧光强度差异较大的原因所在。
2. 4 量子化学计算
物质分子结构决定着物质性质的表现。 0809#、0808#和0812#中2个F原子因连接位置的差异,将影响它们的化学性质与光物理性质; 0208#与0809#、0808#和0812#在噻吩环上取代基的较大差异,也影响着它们之间的化学性质和光学性质表现。 为了进一步研究它们的分子结构与非线性光学性质之间的关系,运用Gaussian 09量子化学程序包[27],在B3LYP/6-311+G(d,p)[29-30]理论水平上对上述4种化合物分子结构优化计算,从而获得它们的分子轨道能量、能隙和极化率,同时给出了他们相应的几何结构(Geometry)、最高占据分子轨道(HOMO)、最低空分子轨道(LUMO)以及附近其他Kohn-Sham轨道等电子云图(辅助材料图S13和图S14)、轨道能量和分子的极化率(表1)。
辅助材料图S15和图S16显示了0208#、0809#、0808#和0812#的分子轨道、电子云分布情况,在 HOMO中电子云主要分布在左端的噻吩环或5-苯基噻吩环和查尔酮基(—C== C—C== O)上,而在HOMO-1中则主要分布在右端的苯环和查尔酮基上。 分子内电子可从一端跃迁转移到另一端,说明π电子体系的共振较强、极化程度较大,存在显著的分子内电荷转移现象,有利于表现非线性光学性质。 由表1可知,0809#、0808#和0812#的LUMO与HOMO之间的能隙(ΔE)差异较小,π电子云易于被极化,较大的极化率意味着易发生分子内电荷转移; 其中,因F原子连接位置的不同,0812#存在分子内F与H之间的非键张力而导致苯环出现一定角度的扭曲,表现出一定刚性,且分子极化率数值较小(295. 17 a.u.),但荧光性质较好; 0809#中2个F原子处于拉电子能力最强的邻、对位,整体上构成D-π-A型分子,相应的极化率最大(325. 85 a.u.),说明最容易发生分子内电荷转移。 0208#与0809#、0808#、0812#相比,从组成结构看主要是噻吩环上的取代基差异,0208#中噻吩环3-位上连有体积较大的氯原子,几何结构显示出噻吩环及查尔酮基与右端的苯环之间存在较大扭曲,整个分子共平面性较差,在4种分子中LUMO与HOMO之间的ΔE最大、极化率最小(199. 14 a.u.)。 上述分析表明,取代基种类及位置影响分子结构的共平面程度,因取代基大小而产生的非键张力亦影响分子结构的共平面程度; 分子的共平面性直接影响分子内电荷转移的难易和极化率的大小。 对于有机共轭芳香化合物分子,共平面性好,共轭效应强,共轭电子离域化程度大,分子内电荷转移容易发生。 计算结果显示,ΔE较小,则极化率较大。 当取代基处于推/拉电子最强效应的位置时,共轭体系分子的极化率最大。
2. 5 非线性光学性质
利用脉冲激光技术,采用Nd∶YAG[NT 342B型]可调谐激光器在532 nm、1. 2 μJ、2 mg/mL和10 ps条件下研究了0208#、0809#、0808#和0812#的三阶非线性光学吸收与折射。 对纯DMSO溶剂进行了相同的Z-扫描测量,没有观察到峰谷信号,排除了溶剂对样品非线性吸收与折射的影响。 实验测得样品0208#、0809#、0808#和0812#的反饱和吸收曲线和折射曲线(图5,小圆圈或三角符号表示样品吸收/折射实验测定数据),即归一化透过率随着入射到样品上的光强增大而减小,并经拟合获得三阶非线性吸收系数(β)和折射系数(γ),数据详见表2。


图4显示,开孔Z-扫描曲线为下行曲线,反饱和吸收特征(β>0),闭孔Z-扫描曲线先谷后峰,表现出自聚焦性质(γ>0)。 表2中显示,4种化合物三阶非线性吸收与折射由大(强)到小(弱)变化顺序是0809#>0808#>0812#>0208#,这反映了共轭体系分子结构与非线性光学性质之间的内在关联,也即分子的共平面性越好,非线性光学性质表现就越好。 反饱和吸收源于第一激发态至更高激发态的能级跃迁所伴随的非线性吸收过程,可用作吸收型光开关或吸收型双稳器件候选材料,具有响应快、损耗低等优点[31]。

3 结 论
比较研究了4种含F芳香基查尔酮衍生物(0208#、0809#、0808#和0812#)的光学性质,线性光谱表明化合物在可见光区具有良好的透明度; 量子化学计算结果分析表明,化合物的分子轨道间能隙较小,极化率较大,易于激发,存在明显的分子内电荷转移现象; 在20 ps、532 nm激光能量条件下非线性光学研究表明,4种化合物均表现出三阶非线性光学吸收和折射,是一类较好的非线性光学材料,预计可用于吸收型光开关或吸收型双稳器件以及激光防护等潜在候选材料。
辅助材料(Supporting Information)[0208#、0809#、0808#和0812#的核磁、质谱、理论计算结果]均可从本刊网站(http:// yyhx.ciac.jl.cn/)下载。
致谢 本工作中核磁共振谱由山西大学测试,非线性光学吸收由苏州大学-微纳非线性光学研发中心测定,作者在此一并致谢。
参考文献
[1]WANG M Y, HAN Y B, WU X Z, et al. Enhancement of ultrafast nonlinear absorption by different substituted positions in pyrene-containing twistacenes isomers[J]. Opt Laser Technol, 2022, 156: 108563.
[2]GAO L J, LI B Y, LI H Y, et al. Nonlinear optical, optical limiting and structural properties of tetrastyryl derivatives with pyrene and bithiophene[J]. Opt Mater, 2023, 137: 113531.
[3]PERRY J W, MANSOUR K, LEE I Y S, et al. Organic optical limiter with a strong nonlinear absorptive response[J]. Science, 1996, 273: 1533-1536.
[4]PELOSI A G, SILVEIRA-ALVES E, COCCAL H Z, et al. Two-photon absorption and multiphoton excited fluorescence of acetamide-chalcone derivatives: the role of dimethylamine group on the nonlinear optical and photophysical properties[J]. Molecules, 2023, 28(4): 1572.
[5]沃彤, 高爽, 张涵, 等. 查尔酮衍生物分子非线性光学性质的理论研究[J]. 化学研究与应用, 2023, 35(6): 1136-1141. WO T, GAO S, ZHANG H, et al. Theoretical study on nonlinear optical properties of chalcone derivatives[J]. Chem Res Appl, 2023, 35(6): 1136-1141.
[6]PATIL P S, BHUMANNAVAR V M, BANNUR M S, et al. Second harmonic generation in some donor-acceptor substituted chalcone derivatives[J]. J Cryst Process Technol, 2013, 3(3): 108-117.
[7]TERKIA-DEDDRA N, ANDREU R, SALLE M, et al. π Conjugation across the tetrathiafulvalene core: synthesis of extended tetrathiafulvalene derivatives and theoretical analysis of their unusual electrochemical properties[J]. Chem Eur J,2000, 6(7): 1199-1213.
[8]SHETTY T C S, RAGHVENDRA S, CHIDAN KUMAR C S, et al. Nonlinear absorption, optical limiting behavior and structural study of a new chalcone derivative 1-(3,4-dimethylphenyl)-3-[4-(methylsulfanyl)phenyl] prop-2-en-1-one[J]. Opt Laser Technol, 2016, 77: 23-30.
[9]ALEN S, SAJAN D, JOSEPH L, et al. Synthesis, growth, vibrational spectral investigations and structure-property relationship of an organic NLO crystal: 3,4-dimethoxy chalcone[J]. Chem Phys Lett, 2015, 636(7): 208-215.
[10]MUHAMMDA S, AL-SEHEMI A G, IRFAN A, et al. Tuning the push-pull configuration for efficient second-order nonlinear optical properties in some chalcone derivatives[J]. J Mol Graph Model, 2016, 68: 95-105.
[11]PATIL P S, SHKIR M, MAIDUR S R, et al. Key functions analysis of a novel nonlinear optical D-π-A bridge type (2E)-3-(4-methylphenyl)-1-(3-nitrophenyl) prop-2-en-1-one chalcone: an experimental and theoretical approach[J]. Opt Mater, 2017, 72: 427-435.
[12]RAVINDRA H J, KIRAN A J, CHADDRASEKHARAN K, et al. Third order nonlinear optical properties and optical limiting in donor/acceptor substituted 4′-methoxy chalcone derivatives[J]. Appl Phys B, 2007, 88(1):105-110.
[13]SHKIR M, PATIL P S, ARORA M, et al. An experimental and theoretical study on a novel donor-π-acceptor bridge type 2,4,5-trimethoxy-4′-chlorochalcone for optoelectronic applications: a dual approach[J]. Spectrochim Acta Mol Biomol Spectrosc, 2017, 173: 445-456.
[14]TEJKIRAN P J, TEJA M S B, KUMAR P S S, et al. D-A-π-D synthetic approach for thienyl chalcones-NLO-a structure activity study[J]. J Photochem Photobiol A: Chem, 2016, 324: 33-39.
[15]ASEJAO L M G, FONSECA R D, SANTOS F A, et al. Second- and third-order nonlinear optical properties of unsubstituted and mono-substituted chalcones[J]. Chem Phys Lett, 2016, 648: 91-96.
[16]NAYAK S K, AHMED M S, RAAVI S S K, et al. Femtosecond nonlinear optical properties of polycyclic aromatic hydrocarbon-based benzo[e] pyrene derivatives [J]. Opt Mater, 2023, 137: 113603.
[17]VINAYA P P, PRASHU A N, SUBRAHMANYA BHAT K, et al. Synthesis, growth and characterization of a long-chainπ-conjugation based methoxy chalcone derivative single crystal: a third order nonlinear optical material for optical limiting applications[J]. Opt Mater, 2019, 89: 419-429.
[18]SHEN L, LI Z, WU X, et al. Ultrafast broadband nonlinear optical properties and excited-state dynamics of two bischalcone derivatives[J]. RSC Adv, 2020, 10: 15199-15205.
[19]YANG Y, WU X, JIA J, et al. Investigation of ultrafast optical nonlinearities in novel bis-chalcone derivatives[J]. Opt Laser Technol, 2020, 123: 105903.
[20]WANG M, ZHOU W, WUAN Y, et al. Investigation of third-order nonlinear optical properties in two novel ethyne-linked chromophores: effect of donor-acceptor alternation[J]. Opt Mater, 2023, 136: 113511.
[21]SUN J, WANG G, LIU C, et al. Synthesis of four pyrene-containing chalcone derivatives: achieving excellent third-order nonlinear optical properties by optimizing halopyridines[J]. Opt Laser Technol, 2019, 109: 600-607.
[22]SHI Y F, JIA J D, SUN J Y, et al. Study of ultrafast nonlinear optical response and transient dynamics of pyrene derivatives with intramolecular charge transfer characteristics[J]. Opt Mater, 2022, 128: 112378.
[23]石玉芳, 孙金鱼, 尹爱萍, 等. 含噻吩基双查尔酮衍生物的合成及光学性质研究[J]. 分子科学学报, 2022, 38(6):521-528. SHI Y F, SUN J Y, YIN A P, et al. Synthesis and study on optical properties of thiophenyl bis-chalcone derivatives[J]. Chin J Mol Sci, 2022, 38(6): 521-528.
[24]石玉芳, 王迎进, 孙金鱼, 等. 含多甲氧基芳香基双查尔酮的合成、表征及光热性能[J]. 应用化学, 2022, 39(2):235-240. SHI Y F, WANG Y J, SUN J Y, et al. Synthesis,characterization,photothermal properties of dichalcone containing polymethoxy aromatic group[J]. Chin J Appl Chem, 2022, 39(2): 235-240.
[25]孙金鱼, 王桂林, 石玉芳, 等. 2-(芘-1-基) -1,8-萘啶的合成、理论计算及超快三阶非线性光学响应[J]. 应用化学,2019, 36(10): 1172-1178. SUN J Y, WANG G L, SHI Y F, et al. Synthesis, theoretical investigation and ultrafast third-order nonlinear optical response of 2-(pyren-1-yl)-1,8-naphthyridine[J]. Chin J Appl Chem, 2019, 36(10): 1172-1178.
[26]梁向晖, 毛秋平, 钟伟强. 浅谈一维核磁共振谱图的解析方法[J]. 分析仪器, 2017, 48(4): 102-106. LIANG X H, MAO Q P, ZHONG W Q. Discussion on analytical method of one-dimensionalnuclear magnetic resonant spectra[J]. Chin Anal Instrum, 2017, 48(4): 102-106.
[27]FRISCH M J, TRUCKS G W, SCHLEGEL H B, et al. Gaussian 09, revision B. 01, gaussian, Inc, wallingford CT, 2010.
[28]丙研, 姚旭森, 毛兵, 等. 基于改性苯环的有机多功能发光材料研究进展[J]. 化学进展, 2024, 36(10): 1490-1519. BING Y, YAO X S, MAO B, et al. Organic multifunctional luminescent materials based on modified phenyl derivatives[J]. Prog Chem, 2024, 36(10): 1490-1519.
[29]BECKE A D. Density-functional thermochemistry.Ⅲ. the role of exact exchange[J]. J Chem Phys, 1993, 98(7): 5648-5652.
[30]LEE C, YANG W, PARR R G. Development of the colle-salvetti correlation energy formula into a functional of the electron density[J]. Phys Rev B, 1988, 37(2): 785-789.
[31]石玉芳, 白杨, 孙金鱼, 等. 新型同分异构芘基查尔酮的理论研究和超快三阶非线性光学响应[J]. 应用化学,2019, 36(9): 1035-1043. SHI Y F, BAI Y, SUN J Y, et al. Theoretical investigation and ultrafast third order nonlinear optical response of novel isomeric pyrenyl chalcones[J]. Chin J Appl Chem, 2019, 36(9): 1035-1043.
Synthesis and Third-Order Nonlinear Optical Properties of Fluorinated Aromatic Chalcone Derivatives
WANG Gui-Lin1, HAO Jian-Feng2, SHI Yu-Fang1*, WANG Ying-Jin1, ZHAO Ming-Gen1
1(Key Laboratory of Materials and Computational Chemistry, Department of Chemistry,Xinzhou Normal University, Xinzhou 034000, China)2(Road Traffic Safety Education Center, Xinzhou City Public Security Bureau, Xinzhou 034000, China)
Abstract Four novel chalcone derivatives were synthesized: 1-(2,3-difluorophenyl)-3-(3-chloro thiophene-2-yl)-2-propene-1-ketone (0208#), 1-(2,4-difluorophenyl)-3-(5-phenylthiophene-2-yl)-2-propene-1-ketone(0809#), 1-(2,3-difluorophenyl)-3-(5-phenylthiophene-2-yl)-2-propene-1-ketone (0808#), 1-(2,6-difluorophenyl)-3-(5-phenylthiophene-2-yl)-2-propene-1-ketone (0812#). The structures and properties of the compounds were characterized by 1H NMR, 13C NMR, liquid chromatography-mass spectrometry, ultravioletvisible spectrum (UV-Vis) absorption spectrum, fluorescence emission (EM) spectrum and Z-scanning technique. The energy and polarizability of the highest occupied molecular orbitals (HOMO) and the lowest unoccupied molecular orbital (LUMO) of the four compounds were obtained by density functional theory, and significant intramolecular charge transfer was found from orbital electron cloud images. The combination of large π-conjugation and charge transfer makes the four aryl chalcone derivatives exhibit good nonlinear optical properties. They can be used as useful candidates for nonlinear absorption (NLA) and have potential applications.
Keywords Chalcone derivatives; Theoretical calculation; Optical properties
Received 2024?07?11; Accepted 2024?10?31
Supported by the Project of Science and Technology Bureau of Xinzhou City, Shanxi Province( No. 20230511)