基于标准汤剂的石榴皮配方颗粒质量评价研究
2025-01-16秦金淼宁波刘羽康张京华张风超刘兴村张玉伟曹桂云孟兆青


摘要:
基于标准汤剂建立石榴皮配方颗粒的质量评价方法。 制备15批石榴皮标准汤剂和3批配方颗粒, 测定出膏率, 基于高效液相色谱法(HPLC)建立特征图谱, 并进行相似度评价, 采用化学计量学方法包括无监督的聚类分析(HCA)、 主成分分析(PCA)和有监督的偏最小二乘判别分析(PLS-DA)对特征图谱数据进行分析, 针对指标成分进行HPLC含量测定, 计算石榴皮标准汤剂和配方颗粒中指标成分的转移率。 结果表明: 石榴皮配方颗粒与标准汤剂特征图谱的相似度均大于0.9。 15批石榴皮标准汤剂出膏率为27.95%~41.32%, 标准汤剂中石榴皮鞣素、 安石榴苷、 鞣花酸的转移率分别为21.49%~39.00%、 18.99%~33.62%、 53.37%~95.45%。 按照标准汤剂数据制定石榴皮配方颗粒中上述指标成分的含量限度应为10.58~19.64 mg/g、 29.91~55.55 mg/g、 10.51~19.52 mg/g。 石榴皮配方颗粒出膏率为41.9%~43.1%, 配方颗粒中指标成分的转移率与标准汤剂接近, 指标成分的含量在根据标准汤剂所制定含量限度范围内。 本研究基于标准汤剂建立了石榴皮配方颗粒的质量控制标准, 为石榴皮配方颗粒的质量控制以及后续的工艺研究提供参考。
关" 键" 词:
石榴皮; 标准汤剂; 配方颗粒; 特征图谱; 高效液相色谱法
中图分类号:
R283; S665.4
文献标志码:A
文章编号:16739868(2025)02019510
收稿日期:20240424
基金项目:
山东省重点研发计划(2021CXGC010511)。
作者简介:
秦金淼, 硕士, 工程师, 主要从事中药研发工作。
通信作者: 曹桂云, 博士, 正高级工程师。
DOI: 10.13718/j.cnki.xdzk.2025.02.017
秦金淼, 宁波, 刘羽康, 等. 基于标准汤剂的石榴皮配方颗粒质量评价研究 [J]. 西南大学学报(自然科学版), 2025, 47(2): 195-204.
Quality Evaluation of Granati Pericarpium Dispensing
Granules Based on Standard Decoctions
QIN Jinmiao," NING Bo," LIU Yukang," ZHANG Jinghua,
ZHANG Fengchao," LIU Xingcun," ZHANG Yuwei,
CAO Guiyun," MENG Zhaoqing
Shandong Hongjitang Pharmaceutical Group Co. Ltd., Jinan 250103, China
Abstract:
To establish a quality evaluation method for Granati Pericarpium formula granules based on standard decoctions, 15 batches of Granati Pericarpium standard decoctions and 3 batches of dispensing granules were prepared, the extraction rates were determined. The specific chromatogram was established based on high performance liquid chromatography (HPLC), and the similarity was evaluated. The chemometric methods including unsupervised cluster analysis (HCA), principal component analysis (PCA) and supervised partial least squares discriminant (PLS-DA) were also used for analysis of the characteristic chromatogram data. The content of the index components were detected with HPLC, and the transfer rates of these components in standard decoctions and dispensing granules were calculated. The results showed that similarity of the specific chromatograms between standard decoctions and dispensing granules were all above 0.9. Extraction rates of 15 batches of Granati Pericarpium standard decoctions were 27.95%-41.32%. The transfer rates of punicalin, punicalagin and ellagic acid in standard decoctions were 21.49%-39.00%, 18.99%-33.62%, 53.37%-95.45%, respectively. The allowable concentration ranges of those components in dispensing granules were 10.58-19.64 mg/g, 29.91-55.55 mg/g, 10.51-19.52 mg/g, respectively. Extraction rates of dispensing granules were 41.9%-43.1%. The transfer rates of index compounds in dispensing granules were close to these in standard decoctions, and the contents of these compounds in dispensing granules was within the scope of the quality standard. In this study, the quality control standard of Granati Pericarpium formula granules was established based on the standard decoction, which provided a reference for the quality control and process research of Granati Pericarpium formula granules.
Key words:
Granati Pericarpium; standard decoction; dispensing granule; specific chromatogram; high performance liquid chromatography (HPLC)
石榴皮为石榴科植物石榴(Punica granatum L.)的干燥果皮, 用于治疗久泄、 久痢、 便血、 脱肛、 崩漏、 带下、 虫积腹痛等症[1-2]。 研究表明, 安石榴苷、 石榴皮鞣素、 鞣花酸等多酚类成分, 具有抗癌、 抗菌、 抗病毒等多种药理活性, 为石榴皮主要有效成分[3-7]。 据方书记载, 石榴皮在方剂中与其他药物配伍均能发挥止泻作用。 如《圣济总录》石榴皮汤方中, 与干姜、 黄柏、 阿胶配伍; 华佗治赤白痢神方中, 与鹿茸、 干姜、 枣仁配伍; 《圣济总录》黄连当归汤方中, 与黄连、 当归、 甘草配伍等[8]。 另外, 石榴皮含量最高的抑菌活性成分是鞣质, 与黄连、 香薷、 苏木按适当比例配伍可达到相互补充且协同抗菌作用[9-10]。 石榴皮与白鲜皮、 蛇床子、 土茯苓、 酒黄精、 熟地黄、 当归配伍, 在改善银屑病皮损症状和减轻瘙痒方面临床疗效确切[11]。 基于石榴皮广泛的应用前景, 为更好地控制和评价产品质量, 目前多位学者建立了石榴皮药材及饮片有效成分含量测定方法[12-14]。
石榴皮配方颗粒是传统中药汤剂的新剂型, 便于配方及服用, 更适应现代人的生活习惯, 已成为石榴皮临床用药的重要形式。 因此建立完善的石榴皮配方颗粒质量评价方法, 规范质量标准并明确其与标准汤剂一致性对于临床应用具有重要意义。 然而目前尚无石榴皮配方颗粒相关文献报道, 不利于其质量控制及临床应用。
本研究根据国家药品监督管理局发布的《中药配方颗粒质量控制与标准制定技术要求》[15](下称《技术要求》)等规定, 制备15批标准汤剂, 基于标准汤剂建立石榴皮配方颗粒质量评价标准, 并基于高效液相色谱(HPLC)建立特征图谱、 多成分含量测定法、 化学计量学方法考察配方颗粒与标准汤剂的一致性, 为石榴皮配方颗粒的质量控制、 后续的工艺研究及临床应用提供参考。
1" 材料与方法
1.1" 材料与仪器
1.1.1" 主要药品与试剂
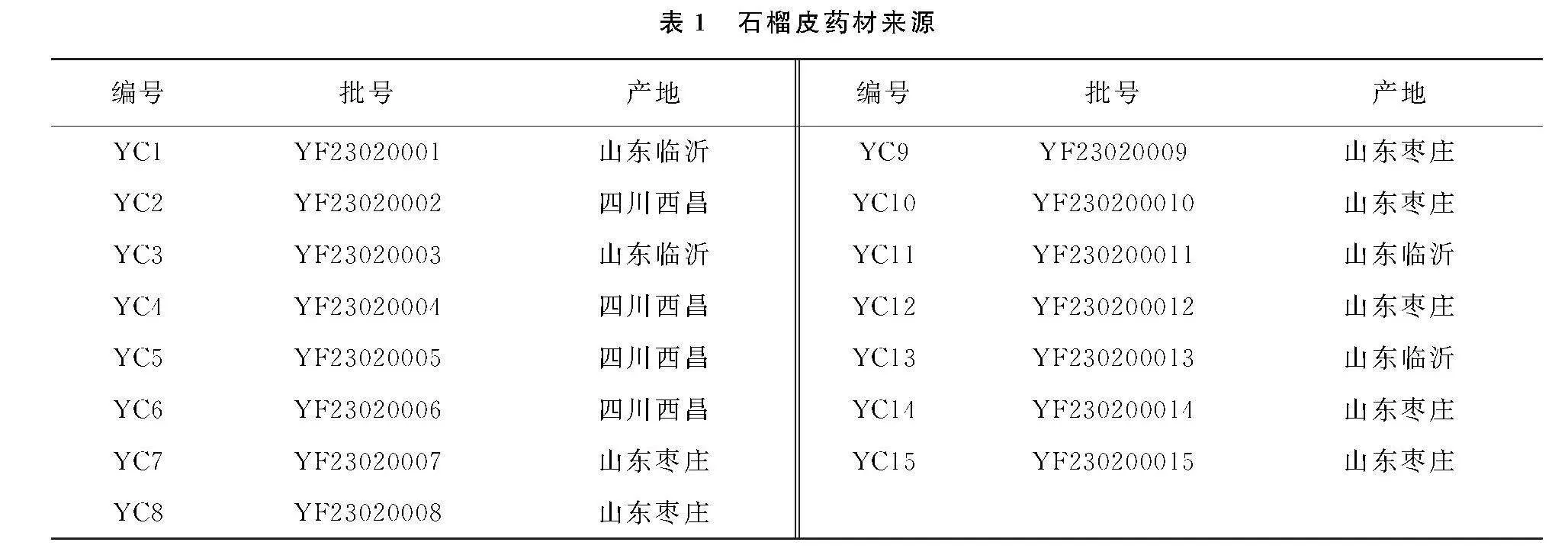
石榴皮鞣素和安石榴苷对照品(上海鸿永生物科技有限公司, 批号分别为010026-202112、 010004-202104, 纯度均为98.0%), 鞣花酸对照品(上海诗丹德标准技术服务有限公司, 批号为ST04700120, 纯度为98.0%), 石榴皮配方颗粒(山东宏济堂制药基团股份有限公司, 每1 g配方颗粒相当于2.2 g饮片, 批号为230301、 230302、 230303, 由批号为YF23020003的石榴皮饮片制备)。 15批石榴皮药材来源详见表1, 经山东省食品药品检验研究院林永强主任药师鉴定为石榴科植物石榴(Punica granatum L.)的干燥果皮。 糊精(曲阜圣城医药销售有限公司, 批号2008001)。 乙腈(上海月旭科技股份有限公司, 批号为AHJ010100204)、 磷酸(天津科密欧精细化工有限公司, 批号为20210710)为色谱纯, 水为超纯水。
1.1.2" 仪器
1260型高效液相色谱仪(美国Agilent科技有限公司), XS105型1/10万电子天平(梅特勒-托利多), BSA224S-CW型1/1万电子天平(赛多利斯科学仪器(北京)有限公司), SCIENTZ-10N型冷冻干燥机(宁波新芝生物科技股份有限公司), KQ-800VSW双频静音型超声波清洗器(昆山市超声仪器有限公司)。
1.2" 方法
1.2.1" 石榴皮标准汤剂冻干粉的制备
将15批石榴皮药材按照《中华人民共和国药典: 2020年版: 一部》(以下简称《中国药典》)石榴皮饮片项下的方法进行炮制, 得到15批饮片(批号同药材)。 按照下述方法制备标准汤剂: 称取15批石榴皮饮片(不少于100 g), 置于砂锅中, 煎煮2次。 煎煮前加水浸泡30 min。 2次煎煮加水量分别为8倍、 6倍; 煎煮时间分别为武火煮沸后采用文火保持微沸30 min, 武火煮沸后采用文火保持微沸20 min。 合并2次滤液, 减压浓缩, 冷冻后干燥, 即得15批标准汤剂的冻干粉(编号S1~S15)。
1.2.2" 色谱条件
色谱柱: Agilent Eclipse Plus Phenyl-Hexyl(4.6 mm×250 mm, 5 μm)。 流动相: 以乙腈(A)-0.1%磷酸溶液(B)。 梯度洗脱: 0~8 min, 3% A; 8~23 min, 3%~8% A; 23~43 min, 8%~13% A; 43~57 min, 13%~18% A。 57~60 min, 18% A; 检测波长: 254 nm; 流速: 1 mL/min; 进样量: 5 μL。 理论板数按鞣花酸峰计算应不低于5 000。
1.2.3" 样品溶液的制备
1) 参照物溶液的制备。 取石榴皮对照药材0.2 g, 加水25 mL, 回流提取30 min, 放冷, 滤过, 取续滤液, 即得。
2) 对照品溶液的制备。 精密称取石榴皮鞣素、 安石榴苷、 鞣花酸对照品适量, 用50%甲醇溶液制成浓度为1.035 8 mg/mL、 1.272 0 mg/mL、 1.000 6 mg/mL的对照品储备液。 上述储备液用50%甲醇稀释制成含石榴皮鞣素、 安石榴苷、 鞣花酸浓度分别为207.18 μg/mL、 254.41 μg/mL、 500.29 μg/mL的混合对照品溶液。
3) 供试品溶液的制备。 取石榴皮配方颗粒或标准汤剂冻干粉0.1 g, 精密称定, 置具塞锥形瓶中, 精密加入50%甲醇50 mL, 密塞, 称定质量, 回流提取15 min, 放冷后再次称定质量, 用50%甲醇补充质量, 摇匀, 滤过, 取续滤液, 即得。
4) 阴性样品溶液的制备。 取0.1 g糊精(配方颗粒所用辅料), 按照“1.2.3”项下供试品溶液的制备方法制备阴性对照溶液。
2" 结果与分析
2.1" 特征图谱研究
2.1.1" 方法学考察
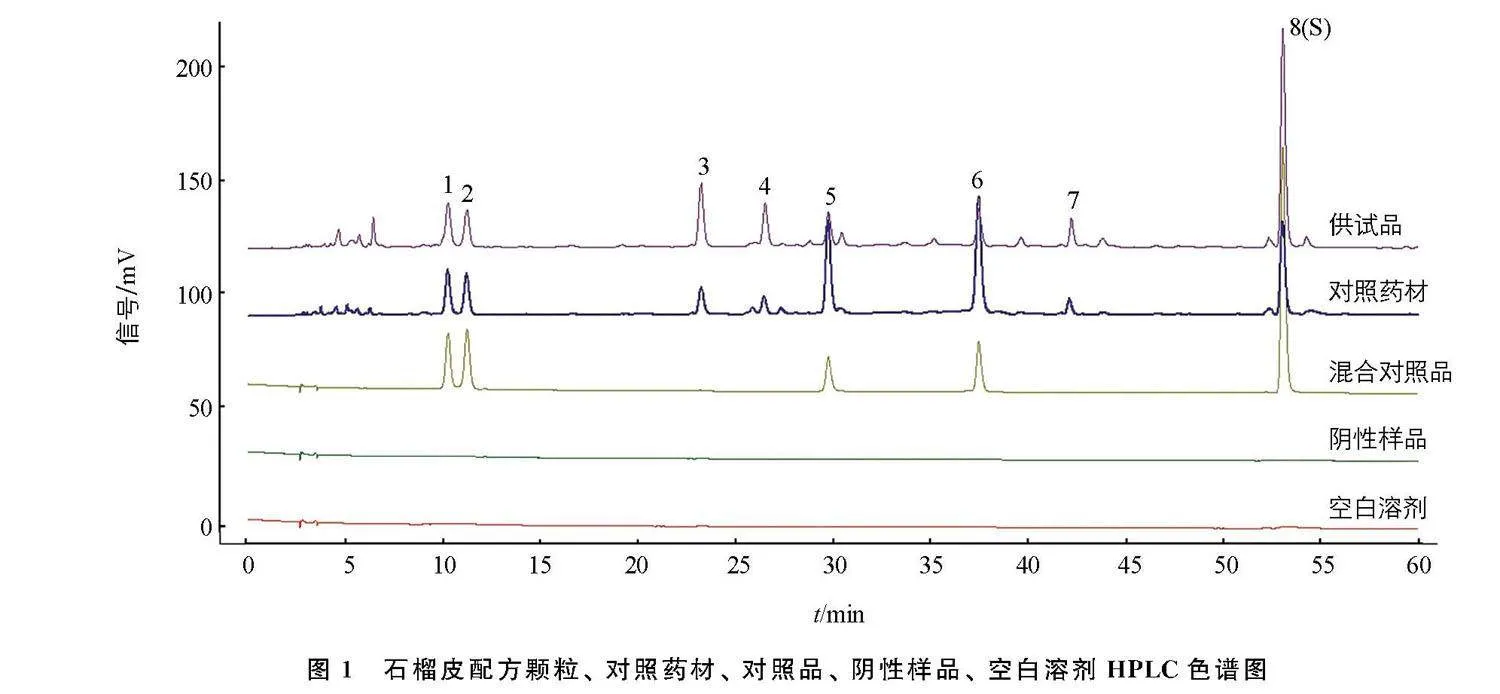
制备的石榴皮配方颗粒供试品溶液、 石榴皮对照药材参照物溶液、 混合对照品溶液、 阴性对照溶液、 空白溶剂(即50%甲醇溶液)按拟定方法检测, 结果见图1, 阴性对照无干扰, 该方法的专属性良好。 取上述石榴皮配方颗粒供试品溶液, 按照设定的进样时间点(0 h、 2 h、 4 h、 8 h、 12 h、 24 h)进样检测, 以第8个色谱峰为参照峰(S), 峰1~峰7与S峰相对保留时间、 相对峰面积的相对标准偏差(RSD)在0.12%~1.94%、 0.59%~3.66%范围内, 供试品溶液在24 h内稳定性良好。 取同一批次石榴皮配方颗粒6份, 按照拟定方法平行制备供试品溶液后进行进样检测, 各特征峰与S峰相对保留时间、 相对峰面积的RSD分别在0.00%~0.62%、 1.46%~3.87%范围内, 表明该方法的重复性较好。 由2个分析人员按拟定方法用同一批石榴皮配方颗粒各平行制备供试品溶液6份, 利用序列号分别为DEAE203284、 DEAEW06793的2台安捷伦高效液相色谱仪进行检测, 各特征峰与S峰的相对保留时间、 相对峰面积RSD分别在0.00%~2.45%、 2.21%~3.15%范围内, 该方法的中间精密度良好。
2.1.2" 特征图谱的建立
取15批石榴皮标准汤剂和3批石榴皮配方颗粒样品, 按拟定方法制备供试品溶液并进行测定。 将18批数据导入“中药色谱指纹图谱相似度评价系统”(2012版), 得到其叠加色谱图(图2)。 以S1样品图谱为参照, 以8个共有峰作为Mark峰进行匹配, 生成石榴皮标准汤剂对照特征图谱(图3)。 采用对照品比对, 指认峰1为α-石榴皮鞣素、 峰2为β-石榴皮鞣素、 峰5为α-安石榴苷、 峰6为β-安石榴苷、 峰8为鞣花酸。
2.1.3" 石榴皮配方颗粒与标准汤剂特征图谱比较
采用“中药色谱指纹图谱相似度评价系统”(2012版), 进行相似度评价, 3批配方颗粒与标准汤剂对照特征图谱及15批标准汤剂特征图谱之间相似度均大于0.9, 与相应标准汤剂(S3)的各共有峰相对峰面积差别不大, 表明石榴皮配方颗粒与标准汤剂样品之间相似度较好, 目前的生产制造工艺能够稳定传递石榴皮饮片中的主要成分。 此外, 15批石榴皮标准汤剂与对照特征图谱的相似度均大于0.9, 说明不同批次石榴皮饮片所制备的标准汤剂相似度较好。
2.2" 聚类分析
将15批石榴皮标准汤剂特征图谱中8个特征色谱峰的峰面积按制成量折算配方颗粒理论峰面积(配方颗粒特征峰理论峰面积=标准汤剂特征峰峰面积×出膏率÷制成量), 通过SPSS 20.0软件导入折算后的峰面积和3批配方颗粒的峰面积进行聚类分析, 结果如图4所示。 当刻度距离为15时, 可分为3类, 3批配方颗粒(S16、 S17、 S18)与S3、 S13批标准汤剂聚为一类, S5、 S12批标准汤剂聚为一类, S1、 S2、 S4、 S6-S11、 S14、 S15批标准汤剂聚为一类。 3批配方颗粒与对应标准汤剂S3聚为一类, 说明配方颗粒生产工艺较稳定且与标准汤剂成分较为一致。
2.3" 主成分分析
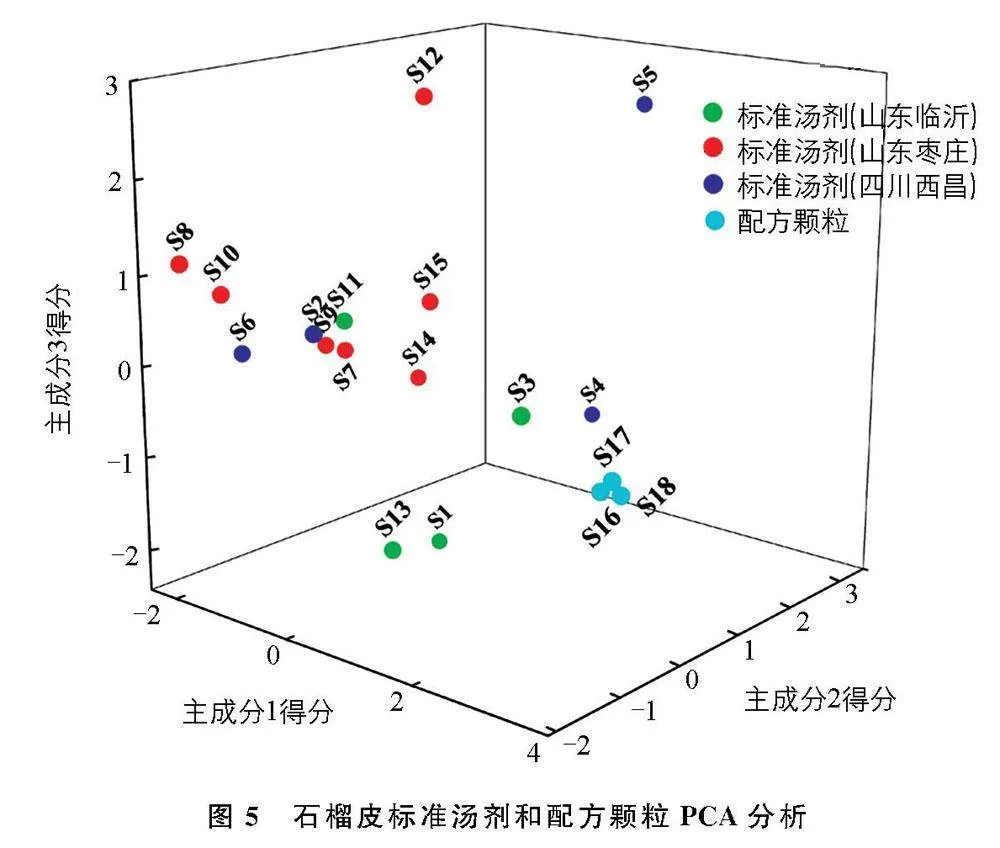
将“2.2”项下折算后的峰面积和配方颗粒的峰面积导入SPSS 20.0软件进行主成分分析(PCA), 3个主成分的方差贡献率分别为46.515%、 24.292%、 20.915%, 累计91.722%, 3个主成分能够反应样品的主要色谱信息, 得分图见图5。 3批配方颗粒与其对应标准汤剂S3分布距离较近, 与聚类分析结果相似, 说明配方颗粒与其对应标准汤剂成分一致性较好。
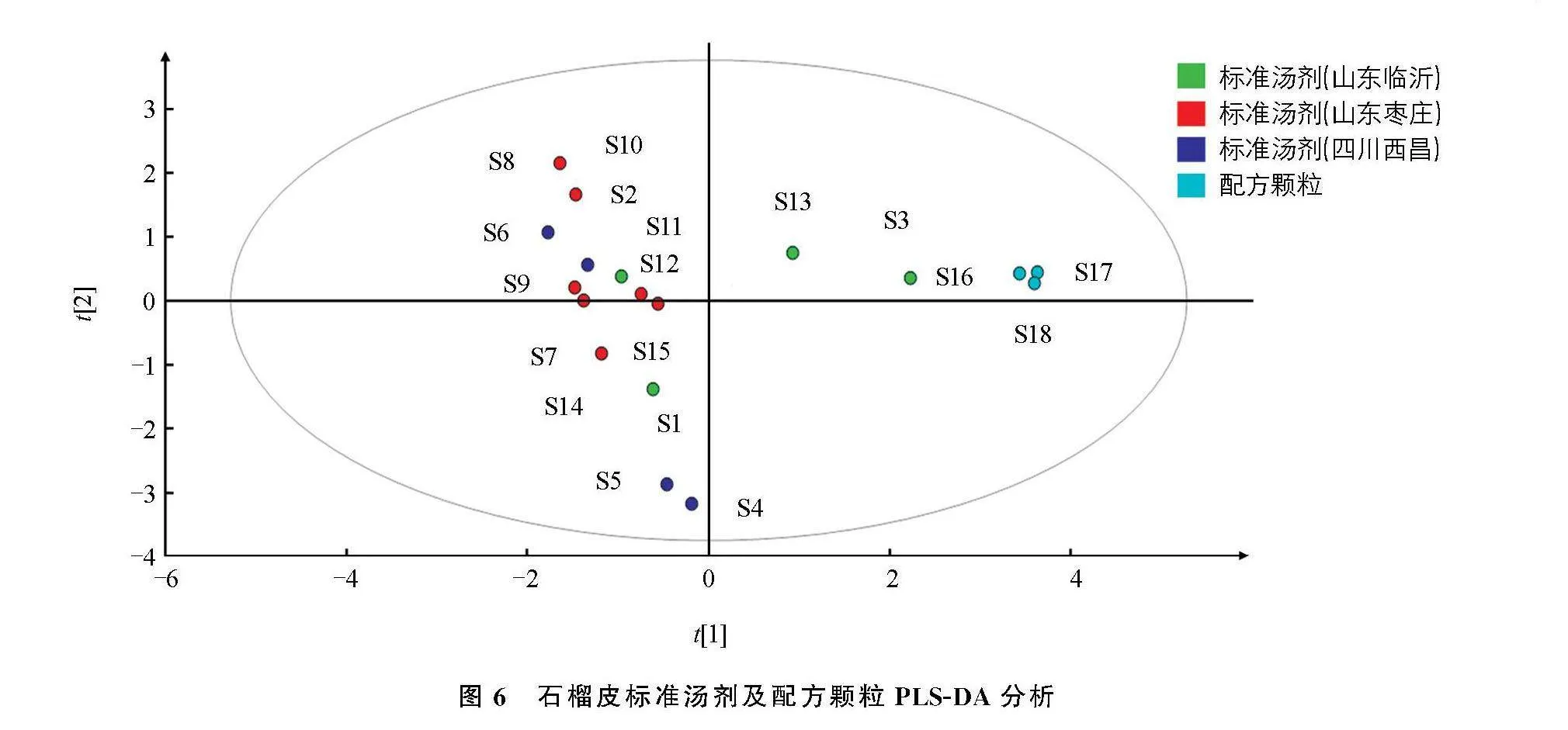
2.4" 偏最小二乘法判别分析
利用SIMCA14.1软件, 以“2.2”项下折算后的峰面积和配方颗粒的峰面积为变量进行有监督的偏最小二乘法判别分析(PLS-DA), 结果见图6。 3批配方颗粒与其对应标准汤剂S3分布距离接近, 说明配方颗粒生产工艺稳定且与其对应批次标准汤剂成分较为一致。
2.5" 多成分定量研究
2.5.1" 方法学考察
1) 专属性考察。 制备石榴皮配方颗粒供试品溶液, 并取“1.2.3”项下对照品溶液和阴性样品溶液以及空白溶剂(50%甲醇溶液)按拟定方法测定, 结果表明阴性对照无干扰, 该方法专属性良好。
2) 稳定性考察。 取所准备石榴皮配方颗粒供试品溶液, 按照设定的进样时间点(0 h、 2 h、 4 h、 8 h、 12 h、 24 h)进样检测, 石榴皮鞣素、 安石榴苷、 鞣花酸含量的RSD分别为2.29%、 1.82%、 0.91%, 所制备供试品溶液在24 h内稳定性良好。
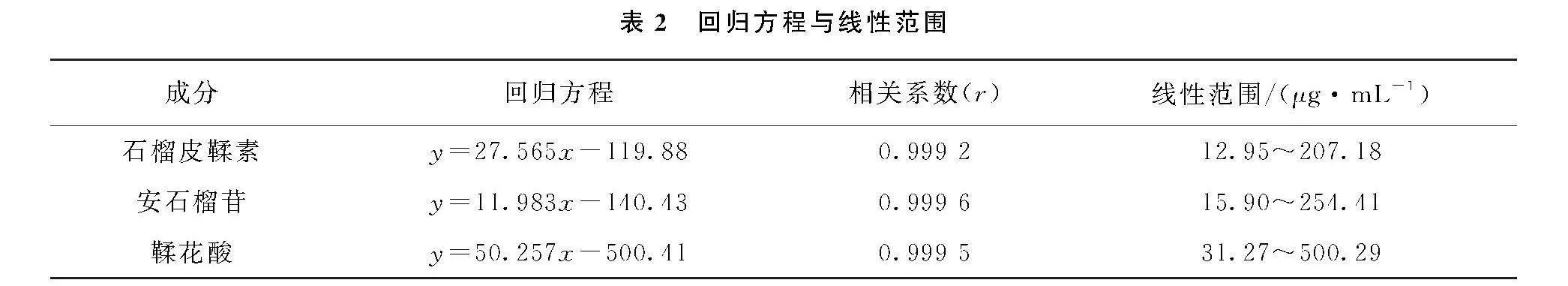
3) 线性关系考察。 精密吸取“1.2.3”项下对照品溶液, 用50%的甲醇水溶液倍比稀释, 精密吸取所得系列混合对照品溶液5 μL进样分析, 记录色谱峰面积。 以浓度为横坐标(x), 色谱峰面积为纵坐标(y)进行线性回归, 得各指标成分的相关系数在0.999 2~0.999 6范围内线性关系良好, 结果见表2。
4) 重复性考察。 按“1.2.3”项下供试品溶液的制备方法制备石榴皮配方颗粒供试品溶液6份, 分别吸取5 μL进样分析, 石榴皮鞣素、 安石榴苷、 鞣花酸含量的RSD分别为2.54%、 2.83%、 1.74%, 该方法重复性较好。
5) 中间精密度考察。 由2个分析人员在不同日期采用同一批次石榴皮配方颗粒样品按照拟定方法分别平行制备供试品溶液6份, 利用序列号分别为DEAE203284、 DEAEW06793的2台高效液相色谱仪进样检测, 结果显示, 石榴皮鞣素、 安石榴苷、 鞣花酸含量的RSD分别为2.95%、 2.68%、 1.80%, 该方法中间精密度良好。
6) 加样回收考察。 取石榴皮配方颗粒6份, 每份0.05 g, 置于锥形瓶中, 分别加入石榴皮鞣素、 安石榴苷、 鞣花酸对照品储备液适量(对照品加入量与供试品中指标成分含量之比为1∶1), 按照拟定方法制备供试品溶液进样分析, 计算得石榴皮鞣素、 安石榴苷、 鞣花酸的加样回收率为95.83%~97.38%、 96.87%~101.05%、 100.69%~101.63%, 符合分析要求。
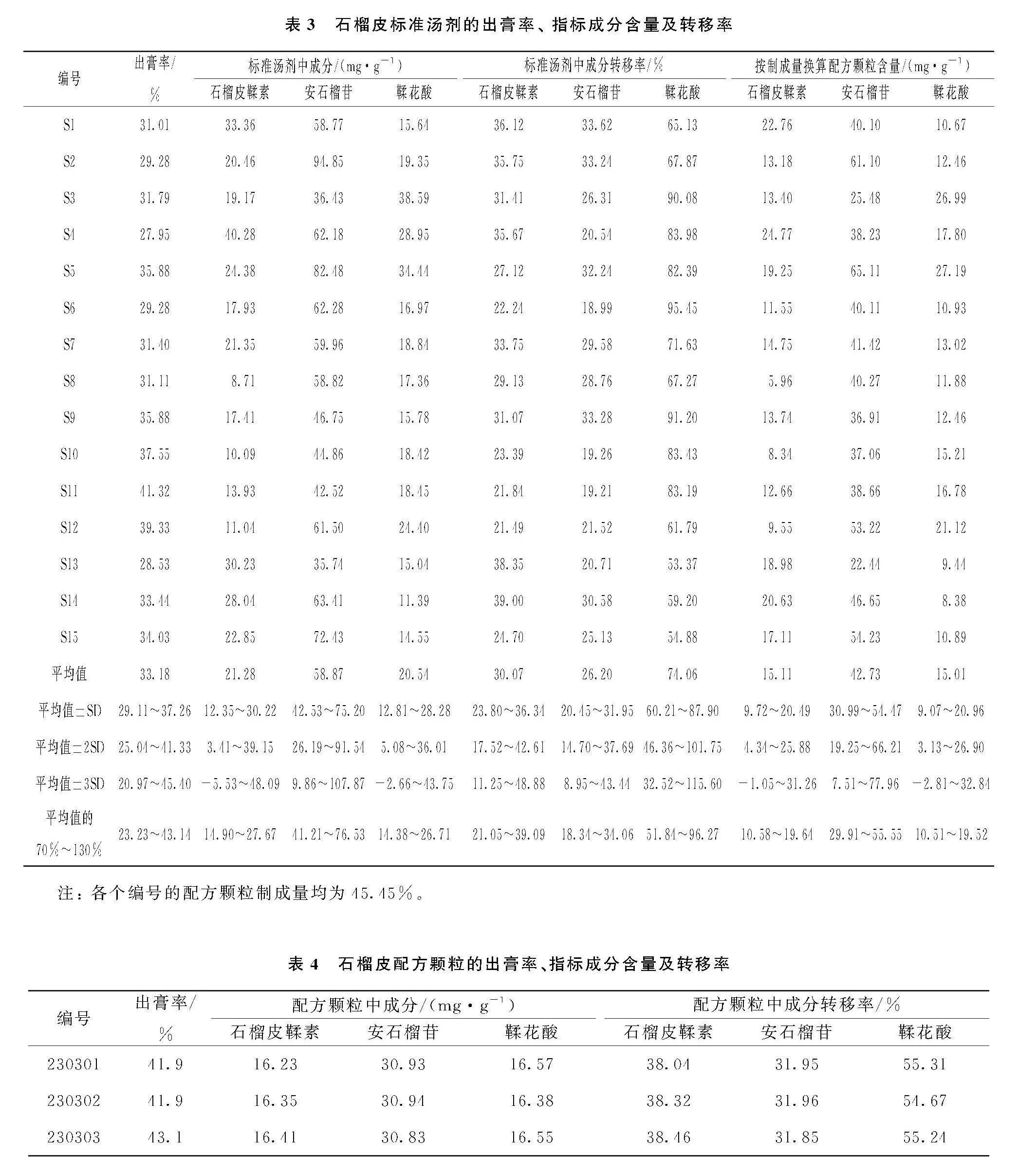
2.5.2" 石榴皮配方颗粒与标准汤剂出膏率、 有效成分含量及转移率比较
对石榴皮标准汤剂和配方颗粒的出膏率、 石榴皮鞣素、 安石榴苷、 鞣花酸含量进行测定, 数据详见表3、 表4。 由表可知3批石榴皮配方颗粒的出膏率为41.9%~43.1%, 符合标准汤剂出膏率平均值±30%范围(23.23%~43.14%)。 根据《技术要求》采用标准汤剂中指标成分的含量、 标准汤剂出膏率、 配方颗粒制成量(45.45%), 换算配方颗粒中3种成分的理论含量(理论含量=标准汤剂指标成分含量×出膏率÷制成量), 并分别计算换算后指标成分含量平均值、 平均值±SD、 平均值±2SD、 平均值±3SD以及平均值的70%~130%范围。 为严格控制配方颗粒的质量, 取上述平均值的70%~130%范围作为配方颗粒指标成分含量限度范围, 即石榴皮鞣素、 安石榴苷、 鞣花酸含量限度分别为10.58~19.64 mg/g、 29.91~55.55 mg/g、 10.51~19.52 mg/g。 经检测, 3批配方颗粒石榴皮鞣素、 安石榴苷、 鞣花酸的含量符合所上述限度要求(表4)。
对3种指标成分在饮片中的含量进行测定。 经过提取方式、 提取溶剂、 提取时间、 称样量等因素考察, 以及方法学验证确定测定方法。 方法为: 石榴皮饮片粉末(过3号筛)约0.2 g, 按“1.2.3”项下参照物溶液的制备方法制备供试品溶液, 按照“1.2.2”项下色谱条件测定, 计算15批石榴皮饮片中指标成分的含量。 计算得到指标成分从饮片到标准汤剂的转移率, 由结果可知15批标准汤剂中指标成分的转移率均在转移率平均值的70%~130%范围内(石榴皮鞣素: 21.05%~39.09%; 安石榴苷: 18.34%~34.06%; 鞣花酸: 51.84%~96.27%), 标准汤剂中指标成分转移率较稳定。 配方颗粒中3种指标成分的转移率也在15批标准汤剂指标成分转移率平均值的70%~130%范围内。 以上结果表明石榴皮配方颗粒制备工艺合理, 可使指标成分稳定地转移, 与石榴皮饮片临床汤剂一致性较好。
3" 结论与讨论
3.1" 供试品溶液的制备
预试验采用单因素试验对供试品溶液的制备方式进行了优化。 对提取方式进行了考察: 分别以超声、 回流制备供试品溶液, 结果表明回流提取效果较好。 对提取溶剂进行了考察: 分别以30%甲醇水、 50%甲醇水、 70%甲醇水、 甲醇为提取溶剂, 制备供试品溶液, 结果表明甲醇提取存在溶剂效应, 色谱峰峰型较差, 50%甲醇水提取效率较好。 对提取时间进行了考察: 分别考察回流时间15 min、 30 min、 45 min对待测成分的提取效率, 结果表明回流15 min以上均能提取完全, 故选择回流时间为15 min。 根据以上研究最终确定供试品溶液制备方式。
3.2" 指标性成分的选择
石榴皮的化学成分较为丰富, 其中的主要活性成分为多酚类。 对石榴皮配方颗粒进行成分分析, 石榴皮鞣素、 安石榴苷、 鞣花酸是其主要成分。 石榴皮鞣素和安石榴苷具有抗氧化、 抗肝损伤、 抗炎、 抗病毒等药理作用[16-19]。 鞣花酸具有抗炎、 抗氧化、 抗衰老、 抗肿瘤等多种药理作用[20-24], 是石榴皮发挥药效的物质基础。 另外, 鞣花酸也是《中国药典》2020年版石榴皮药材质量控制的指标成分。 本研究以石榴皮鞣素、 安石榴苷、 鞣花酸作为配方颗粒质控的指标成分, 其在饮片和配方颗粒中具有高含量, 且与石榴皮药理作用相一致, 保证了测定成分的代表性和方法的适用性。
目前石榴皮鞣素和安石榴苷均仅可购得同分异构体(α-石榴皮鞣素和β-石榴皮鞣素; α-安石榴苷和β-安石榴苷)的混合物[13-14], 2个同分异构体结构相似, 仅端基碳的立体构型不同, 因此紫外吸收基本相同, 利用混合对照品进行定量可达到含量测定相关方法学要求。 对照品与样品中2个同分异构体的比例未知, 且二者之间会相互转化[24], 所以未将2个同分异构体绘制成2条标准曲线, 分别计算其含量, 而是用总峰面积, 做一条标准曲线计算其总含量。
3.3" 配方颗粒质量评价标准的建立及与标准汤剂对比分析
本研究根据《技术要求》收集了不同产地的15批石榴皮药材, 炮制成饮片并制备标准汤剂, 采用高效液相色谱法建立了石榴皮标准汤剂和配方颗粒的特征图谱, 建立石榴皮标准汤剂和配方颗粒中石榴皮鞣素、 安石榴苷、 鞣花酸含量的测定方法。 以出膏率、 特征图谱、 3种指标成分含量及转移率为指标, 并结合化学模式识别分析, 多维度衡量了石榴皮配方颗粒与标准汤剂的一致性, 为石榴皮配方颗粒生产工艺的研究提供依据。 配方颗粒出膏率在标准汤剂出膏率平均值±30%范围内; 3批配方颗粒与其对应标准汤剂的特征图谱相似度均>0.9; 聚类分析显示3批配方颗粒可与其对应标准汤剂聚成一类; 主成分分析与偏最小二乘法判别分析显示3批配方颗粒与其对应标准汤剂S3分布距离较近; 配方颗粒中3种指标成分的含量符合要求, 转移率与标准汤剂基本一致。 以上结果说明石榴皮配方颗粒制备工艺合理, 与石榴皮饮片临床汤剂物质基础基本一致。 以上研究能够比较全面地反映石榴皮配方颗粒的内在质量, 可为石榴皮配方颗粒在临床中的应用提供研究基础, 并为其他配方颗粒研究提供思路。
参考文献:
[1]
国家药典委员会. 中华人民共和国药典: 2020年版: 一部 [M]. 北京: 中国医药科技出版社, 2020.
[2]" ABEDI M, SALMANI M H, MOZAFFARI S A. Adsorption of Cd Ions from Aqueous Solutions by Iron Modified Pomegranate Peel Carbons: Kinetic and Thermodynamic Studies [J]. International Journal of Environmental Science and Technology, 2016, 13(8): 2045-2056.
[3]" TAKTAK F, ILBAY Z,瘙塁AHIN S. Evaluation of 2, 4-D Removal via Activated Carbon from Pomegranate Husk/Polymer Composite Hydrogel: Optimization of Process Parameters through Face Centered Composite Design [J]. Korean Journal of Chemical Engineering, 2015, 32: 1879-1888.
[4]" 张骞文, 殷田田, 刘帅坤, 等. 石榴的化学成分及药理活性研究 [J]. 科学咨询(科技·管理), 2022(10): 104-107.
[5]" 闫恒, 张辉. 石榴化学成分及其药理作用研究进展 [J]. 中国处方药, 2016, 14(2): 18-19.
[6]" 陈伟, 刘瑞, 韩振斌, 等. 石榴皮的化学成分及药理作用 [J]. 北京农业, 2015(17): 97.
[7]" 胡正梅, 马清河. 石榴的化学成分及药理活性研究进展 [J]. 新疆中医药, 2015, 33(1): 74-77.
[8]" 曾祥法. 部分常用中药功效规范化表述的初步研究 [D]. 成都: 成都中医药大学, 2008.
[9]" 周梦宇, 周本宏, 郭咸希. 石榴皮鞣质作为天然抑菌剂的研究进展 [J]. 中国药师, 2018, 21(11): 2037-2040, 2044.
[10]李华, 李强, 付雷. 几种中草药对海水养殖中常见病原菌的抗菌作用 [J]. 大连海洋大学学报, 2011, 26(1): 6-11.
[11]王俊月. 基于数据挖掘的卢传坚教授治疗寻常型银屑病外洗方药物配伍规律研究 [D]. 广州: 广州中医药大学, 2019.
[12]范高福, 韦梦强, 吴丹, 等. RP-HPLC法同时检测石榴皮3种多酚类提取物含量研究 [J]. 长春师范大学学报, 2023, 42(6): 133-138.
[13]刘振平, 陈祥贵, 彭海燕, 等. RP-HPLC法同时测定石榴皮中4种多酚类成分的含量 [J]. 中国药房, 2013, 24(3): 238-240.
[14]邓佩欣, 周文财, 高雅媛, 等. HPLC法同时测定石榴皮中4种多酚类成分的含量 [J]. 广州化工, 2017, 45(2): 107-109.
[15]国家药品监督管理局. 国家药监局关于发布《中药配方颗粒质量控制与标准制定技术要求》的通告(2021年第16号) [EB/OL]. (2021-02-10) [2023-12-23]. http: //www.gov.cn/zhengce/zhengceku/2021-02/11/content_5586817.htm.
[16]WANG Y, ZHANG H C, LIANG H, et al. Purification, Antioxidant Activity and Protein-Precipitating Capacity of Punicalin from Pomegranate Husk [J]. Food Chemistry, 2013, 138(1): 437-443.
[17]LIN C C, HSU Y F, LIN T C, et al. Antioxidant and Hepatoprotective Effects of Punicalagin and Punicalin on Acetaminophen-Induced Liver Damage in Rats [J]. Phytotherapy Research, 2001, 15(3): 206-212.
[18]左风. Punicalagin和Punicalin抗氧化和对扑热息痛诱导大鼠肝损伤的保护作用 [J]. 国外医学(中医中药分册), 2002, 24(2): 105-106.
[19]LIU C L, CAI D W, ZHANG L, et al. Identification of Hydrolyzable Tannins (Punicalagin, Punicalin and Geraniin) as Novel Inhibitors of Hepatitis B Virus Covalently Closed Circular DNA [J]. Antiviral Research, 2016, 134: 97-107.
[20]李小萍. 红树莓果中鞣花酸的提取、 纯化及抗氧化性和抑菌活性的初步研究 [D]. 兰州: 甘肃农业大学, 2010.
[21]ASLAN A, BEYAZ S, GOK O, et al. The Effect of Ellagic Acid on Caspase-3/Bcl-2/Nrf-2/NF-kB/TNF-α /COX-2 Gene Expression Product Apoptosis Pathway: A New Approach for Muscle Damage Therapy [J]. Molecular Biology Reports, 2020, 47(4): 2573-2582.
[22]邢晓平, 杨笑笑, 卢婕, 等. 石榴皮中鞣花酸的抗衰老性能及机理研究 [J]. 食品与生物技术学报, 2015, 34(4): 436-442.
[23]于娅, 李利民, 潘嘉, 等. 鞣花酸抗S180, H22肿瘤及其抑制新生血管机制探讨 [J]. 中国实验方剂学杂志, 2015, 21(8): 145-150.
[24]张杰, 崔艳娜, 刘绣华. 安石榴苷的研究进展 [J]. 化学研究, 2014, 25(6): 551-562.
责任编辑" 王新娟
