伊维菌素浇泼溶液在牛组织中的残留和消除规律
2024-12-31徐先达李帅鹏李荣顺原振清袁慧平王学恩



摘要:为研究伊维菌素浇泼溶液在牛组织中的残留消除规律,500 μg/kg·bw,单次给药,由背中线浇注伊维菌素浇泼溶液,分别于用药后7、14、28、48 d用高效液相色谱荧光检测法(HPLC-FLD)检测牛肌肉、肝脏、肾脏、皮下脂肪以及给药部位肌肉中伊维菌素的残留量。HPLC-FLD方法的检测限(LOD)为2 μg/kg,定量限(LOQ)为5 μg/kg。结果表明,以500 μg/kg背部浇淋后,伊维菌素在牛体内代谢缓慢,在肝脏组织中的残留量远高于其他组织。伊维菌素在组织中的残留量:肝脏>脂肪>给药部位>肾脏>肌肉。肝脏在给药后7 d达到最大浓度306 μg/kg,除肝脏外,肌肉、肾脏、皮脂以及给药部位肌肉均在给药后28 d,组织浓度低于最高残留限量;肝脏在第48天时,其浓度才低于最高残留限量;根据WT1.4软件分析,参照农业部235公告和欧盟关于IVM在牛组织中规定的MRL,测得各组织的休药期分别为:肌肉21.2 d、肝脏42.1 d、肾脏21.5 d、皮脂39.9 d、给药部位肌肉31 d。因此伊维菌素浇泼溶液的休药期为43 d。
关键词:伊维菌素浇泼溶液;透皮;高效液相色谱;荧光检测器;残留消除规律;休药期
伊维菌素(ivermectin,IVM)是目前公认的具有广谱、高效、低毒、低残留的大环内酯类抗寄生虫药物,对家畜的胃肠道线虫、外寄生虫(蜱、虱、螨、蝇蛆等)有特殊的疗效,在临床上被广泛使用。已有的研究表明,不同畜种、不同药物剂型、不同给药途径使IVM的药代动力学有明显差异。IVM通过皮肤涂抹的渗透性极低,渗透是涂抹量的0.17%~0.55%[1];通过口服或皮下注射,效果显著,机体吸收很快,血液浓度在给药后2 d基本达到峰值。给药后7 d药物清除率达到90%以上,给药后28 d药物在体内基本代谢完毕。IVM在犬体内排泄较快(半衰期为1.6~1.8 d)。牛、羊体内半衰期约为2.7 d;猪的半衰期长达4 d[2-3]。吸收后IVM广泛分布于全身组织,其中肝脏浓度最高,其次为脂肪,最低为脑[4]。国内外许多文献报道了口服、注射给药在牛羊、猪组织中的残留消除规律,对于伊维菌素浇泼透皮剂在牛组织中的残留消除规律未见系统的报道。本研究采用“农业部1025号公告-5-2008高效液相色谱法”对牛组织中伊维菌素进行检测[5],得出肉牛背部浇泼伊维菌素透皮溶液后组织中伊维菌素浓度的变化规律,为伊维菌素浇泼溶液的临床使用和食品药物残留检测提供参考。
1 材料与方法
1.1 设备与仪器
超高液相色谱仪(ACQUITY UPLC,配备二元并联泵、色谱工作站、荧光检测器、自动进样器等,美国WATERS公司);Avanti J-26高速冷冻离心机(美国BECKMAN COULTER公司); XW-80A旋涡混合仪(上海青浦沪西仪器厂); KS501digital轨道式摇床(德国IKA公司);高速组织匀浆器;氮气吹干浓缩仪;电子分析天平等。
1.2 试剂药品与试剂
供试药品:0.5%伊维菌素浇泼溶液,以伊维菌素(H2B1a+H2B1b)计算,批号201205001,内蒙古金河动物药业有限公司,试验前测定药物的有效含量(以伊维菌素计)为0.5%。
伊维菌素对照品:伊维菌素(H2B1a+H2B1b),纯度91.2%,批号K0191106,中国兽医药品监察所。
甲醇、乙腈为色谱纯。三乙胺、冰醋酸、异辛烷等均为分析纯。水为符合GB/T 6682规定的二级水。
1.3 试验动物
选择18头健康的黄牛,公母各半,按常规饲养,自由饮水和采食,饲料为全价日粮,不含任何抗菌药物。临床观察两周表现健康。
1.4 给药
将牛分为给药组(16头)与空白对照组(2头),平均体重为411.3 kg(411.3±24.6 kg),试验组随机分为4组进行残留消除试验,每组4头,给药组单次背部浇淋伊维菌素浇泼溶液,给药剂量为500 μg/kg·bw。空白组浇注生理盐水,给药方式同给药组。
1.5 样品采集
给药组在给药后第7、14、28、48天的时间点各宰杀一组牛,分别采集以下组织及部位:①肌肉 腿部肌肉,500 g;②肝脏 最大叶部位,500 g;③肾脏 双肾纵切,各取一半;④给药部位 以背中线为中心划10×10cm方形,采10 cm×10 cm×6 cm(深)的肌肉样本;⑤脂肪 皮下脂肪200 g。各样品采集后立即做好标记、包装,保存于-20 ℃冰箱,待测。
1.6 组织样品中伊维菌素的检测方法
1)样品前处理。①试料制备:取出冷冻试料50 g,切碎、高速均质,匀浆备用。每种组织进行平行双样本测定。②处理:提取:称取试样2.5 g(精确到0.01 g)于50 mL离心管中,加8 mL乙腈,旋涡0.5 min,2 000 r/min离心2 min,取上清液。残渣用8 mL乙腈重复提取一次,合并两次提取液。净化:取碱性氧化铝柱,加2 g无水硫酸钠。加10 mL乙腈预洗,将上清液过柱,收集滤液于鸡心瓶中。接着用5 mL乙腈洗脱,收集于同一鸡心瓶中,50 ℃下减压浓缩至干。用0.5 mL乙腈溶解残余物,旋涡0.5 min,使充分溶解,备用。取C18固相萃取柱,用5 mL乙腈预洗,将备用液过柱,收集流出液于5 mL刻度试管内,继续用3 mL乙腈洗脱,收集于同一鸡心瓶中,50 ℃下氮气吹干,备用。荧光衍生化:加入衍生化试剂A液100 μL,旋涡0.5 min,再加衍生化试剂B液100 μL,旋涡0.5 min,密闭。于96 ℃衍生化反应100 min,加50 μL乙腈,过0.45 μm滤膜,进行HPLC荧光检测。
2)各种溶液配制。伊维菌素标准储备液:准确称取的对照品0.0532 g于100 mL棕色容量瓶中,用甲醇溶解并定容到刻度,摇匀,即成500 μg/mL伊维菌素标准液,4 ℃冰箱保存,临用前用流动相配成系列标准工作液。衍生化试剂:A液:N-甲基咪唑-乙腈(1+1,v/v),现用现配。B液:三氟乙酸酐-乙腈(1+2,v/v),现用现配。
1.7 液相色谱条件
色谱柱:Thermo CigODS(4.6 mm×250 mm,5μm),美国Thermo公司;流动相:甲醇:水(98:2,v/v);流速为1 mL/min,进样量为20 μL;荧光检测器;激发波长为365 nm,发射波长475 nm;柱温:30 ℃。
1.8 检测限与定量限
按信噪比S/N≥3时为检测限(LOD),S/N≥10时为定量限(LOQ)。所得检测限为2 μg/kg,定量限为5 μg/kg,表明方法的灵敏度高,可满足残留检测的要求。
1.9 标准曲线与线性范围
在6个50 mL进口离心管中分别称取1 g空白组织,依次加入工作液,制成含伊维菌素药物浓度分别如下:5、10、20、50、100、200 μg/kg的组织样品。按照组织样品处理方法处理后,进样分析。以测得的伊维菌素的峰面积(A)与药物浓度(C)作线性回归,求得标准曲线的回归方程和相关系数。结果见表1。
1.10 回收率和变异系数测定
在1 g空白组织中加入伊维菌素标准工作液,制成含药浓度为5、10、100 μg/g的肾脏、肝脏、肌肉、脂肪组织样品。按照样品处理方法处理后,进样分析,每批次每个浓度设5个平行样品,共3个批次。以其药物峰面积与外标峰面积之比,求得低、中、高3种浓度的回收率,计算批内,批间变异系数(CV,%)。
2 结果与分析
2.1 伊维菌素浇泼溶液在牛组织残留消除
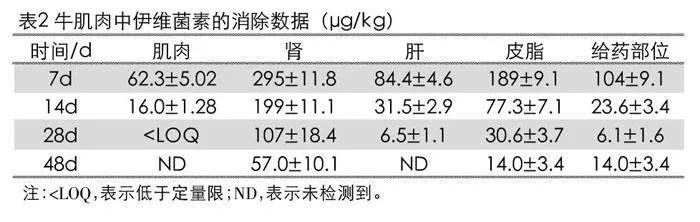
依据上述建立的方法,对试验动物在第7、14、28、48天时间点采集的肌肉、肝脏、肾脏、脂肪、给药部位肌肉5种组织进行了双样本检测,各组织中伊维菌素的测定结果见表2。
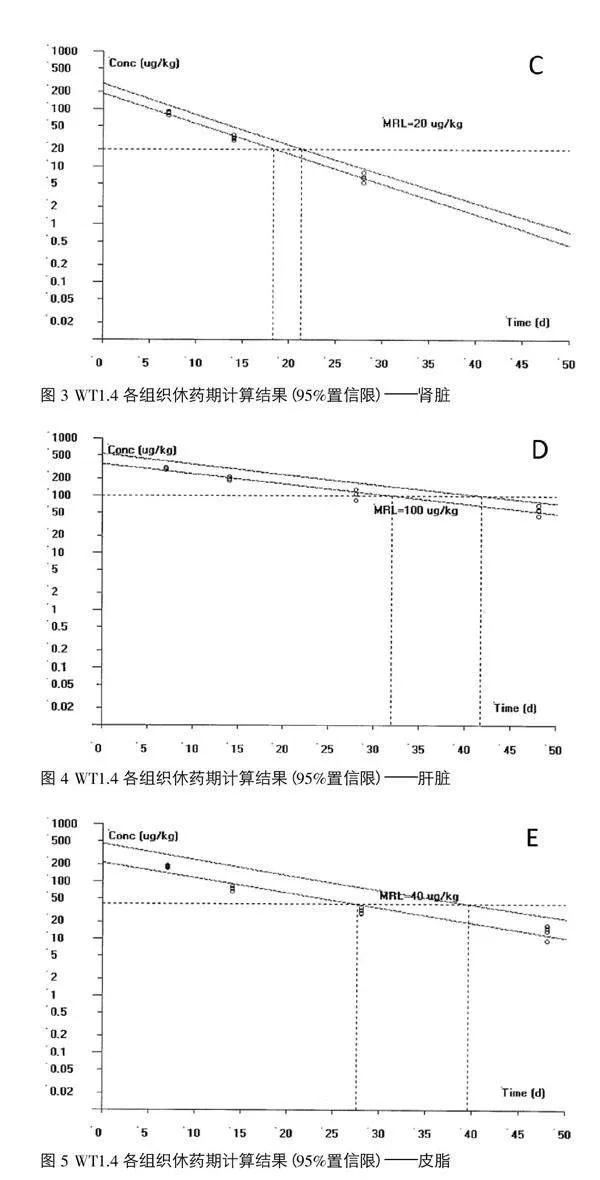
2.2 伊维菌素浇泼溶液在牛组织中的休药期
农业部235公告关于伊维菌素在牛各个组织中的最高残留限量(MRL)规定如下:肌肉为10 μg/kg,脂肪为40 μg/kg,肝为100 μg/kg。肾脏MRL没有具体规定,参照欧盟关于伊维菌素在鹿体内的最高残留限量,暂定为20 μg/kg[6-7]。根据计算机软件WT1.4计算,各种组织的休药期(95%置信限)见图1~图5。
3 讨论
3.1 伊维菌素在牛组织中的分布
从检测的5种组织所得到的最高浓度点为:肝脏306 μg/kg(7 d)、皮脂194 μg/kg(7 d)、给药部位肌肉115 μg/kg(7 d)、肾脏89.3 μg/kg(7 d)、肌肉68.8 μg/kg(7 d)。从上述结果来看伊维菌素在动物组织中以肝脏的浓度最高,残留时间最长,其次是皮脂、给药部位肌肉、肾脏、肌肉。
试验结果表明:以500 μg/kg背部浇淋后,伊维菌素在牛体内代谢缓慢,肝脏在给药后7 d达到最大浓度306 μg/kg,除肝脏外,肌肉、肾脏、皮脂以及给药部位肌肉均在给药后28 d,组织浓度低于最高残留限量;肝脏在第48天时,其浓度才低于最高残留限量。
3.2 关于伊维菌素浇泼溶液在牛体内休药期的评价
农业部235公告关于伊维菌素在牛各个组织中的最高残留限量(MRL)规定如下:肌肉为10 μg/kg,脂肪为40 μg/kg,肝为100 μg/kg;肾脏MRL没有具体规定,参照欧盟关于伊维菌素在鹿体内的MRL,暂定为20 μg/kg[4]。
根据WT1.4软件,参照农业部235公告和欧盟关于伊维菌素在牛组织中规定的MRL,测得伊维菌素浇泼溶液以500 μg/kg背部浇淋给药,给药1次,各组织的休药期分别为:肌肉21.2 d、肝脏42.1 d、肾脏21.5 d、皮脂39.9 d、给药部位肌肉31 d" (表3)。
4 结论
根据表3结果,内蒙古金河动物药业有限公司研制的伊维菌素浇泼溶液(0.5%)的休药期为43 d。
参考文献:
[1] 徐楷,王巧玲.兽用伊维菌素研究进展[J].国外畜牧学(猪与禽),2011,31(1):85-86.
[2] 孙庆申,赵凯.伊维菌素的研究进展[J].畜牧兽医科技信息,2008(4):7-9.
[3] 何继红.阿维菌素类药物多残留分析方法的研究[D].中国农业大学,2005.
[4] LEE CHIU S H, TAUB R, SESTOKAS E, et al. Comparative in Vivoand in Vitro Metabolism of Ivermectin in Steers, Sheep, Swine, and Rat[J]. Drug metabolism reviews, 1987, 18(2-3):289-302.
[5] 农业部1025号公告-5-2008,动物性食品中阿维菌素类药物残留检测 酶联免疫吸附法、高效液相色谱法和液相色谱-串联质谱法[S].
[6] 农业部发布动物性食品中兽药最高残留限量(续)[J].中国兽药杂志,2003 (3):5-11.
[7] COMMISSION REGULATION (EU) No 37/2010 of 22 December 2009 on pharmacologically active substances and their classification regarding maximum residue limits in foodstuffs of animal origin[EB/OL]. https://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=CONSLEG:2010R0037:
20110714:EN:PDF,2010-01-20/2022-05-09.
收稿日期:2023-08-30
作者简介:徐先达(1993— ),内蒙古人,硕士,兽医师,从事兽药技术服务工作。172467548@qq.com。
