贝伐珠单抗联合常规化疗对晚期结肠癌患者的治疗效果及无进展生存期的影响
2024-09-20苏亭亭穆秀君
【摘要】目的 探究晚期结肠癌患者采用贝伐珠单抗联合常规化疗对其治疗效果及无进展生存期的影响,为临床治疗提供参考。方法 选取2020年5月至2022年6月曹县人民医院收治的82例晚期结肠癌患者,参照随机数字表法分为参照组和研究组,每组各41例。参照组患者采用奥沙利铂联合卡培他滨行常规化疗,研究组患者在参照组基础上联合贝伐珠单抗治疗。比较两组患者无进展生存率、临床疗效、肿瘤标志物[糖类抗原(CA)199、CA125、多效蛋白(PTN)、结肠癌特异性抗原-1(CCSA-1)、癌胚抗原(CEA)]水平、T淋巴细胞亚群分布、不良反应发生情况。结果 研究组患者无进展生存率高于参照组(P<0.05)。研究组患者临床疗效优于参照组,客观缓解率(ORR)高于参照组(均P<0.05)。治疗后,两组患者CA199、CA125、PTN、CCSA-1、CEA水平均降低,且研究组均低于参照组(均P<0.05)。治疗后,两组患者CD3+、CD4+T淋巴细胞百分比及CD3+/CD4+比值均降低,但研究组降低幅度均小于参照组(均P<0.05)。两组患者不良反应总发生率比较,差异无统计学意义(P>0.05)。结论 贝伐珠单抗与常规化疗联合应用于晚期结肠癌患者,对病情的控制效果良好,能切实有效降低肿瘤标志物水平,增强患者的免疫功能,并且具有较高的安全性,值得在临床中应用。
【关键词】贝伐珠单抗;晚期结肠癌;无进展生存期;奥沙利铂;卡培他滨
【中图分类号】R735.3+7 【文献标识码】A 【文章编号】2096-2665.2024.16.0058.04
DOI:10.3969/j.issn.2096-2665.2024.16.019
结肠癌是临床常见的消化道恶性肿瘤,早期无明显症状,患者就诊时多数已处于晚期,导致患者治疗效果不佳[1]。早期结肠癌通过手术切除肿瘤组织,可取得较好的治疗效果,但晚期患者病情复杂,需进行辅助化疗,达到延长生存期、提高生活质量的目的[2]。奥沙利铂和卡培他滨是临床治疗胃肠道肿瘤的常用药物。其中,奥沙利铂通过与DNA形成链内和链间交联,抑制DNA的合成和复制,诱导肿瘤细胞凋亡,但其神经毒性不良反应较为明显,患者易出现手脚麻木、感觉异常等症状;卡培他滨可经体内代谢转化为具有细胞毒性的5-氟尿嘧啶,干扰肿瘤细胞的DNA和RNA合成,进而达到治疗目的,但其易引起手足综合征等不良反应[3]。贝伐珠单抗通过抑制血管内皮生长因子(VEGF)的活性,阻断肿瘤血管的生成,进而抑制肿瘤的生长和扩散[4]。基于此,本研究探究晚期结肠癌患者应用贝伐珠单抗联合常规化疗对病情控制及无进展生存期的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2020年5月至2022年6月曹县人民医院收治的82例晚期结肠癌患者,按照随机数字表法分为参照组和研究组,各41例。参照组患者中男性21例,女性20例;年龄38~79岁,平均年龄(58.43±3.59)岁;肿瘤直径3~6 cm,平均肿瘤直径(4.52±0.47)cm;病理分期[5]:Ⅲ期23例,Ⅳ期18例;发病部位:左半结肠25例,右半结肠16例。研究组患者中男性22例,女性19例;年龄37~80岁,平均年龄(58.52±3.61)岁;肿瘤直径3~6 cm,平均肿瘤直径(4.58±0.49)cm;病理分期:Ⅲ期22例,Ⅳ期19例;发病部位:左半结肠24例,右半结肠17例。两组患者一般资料比较,差异无统计学意义(P>0.05),组间具有可比性。本研究经曹县人民医院医学伦理委员会批准,患者及家属均对本研究知情并签署知情同意书。纳入标准:
⑴符合《外科学》[6]中晚期结肠癌的诊断标准,并经临床相关检查确诊;⑵生命体征平稳。排除标准:⑴合并心功能障碍者;⑵合并感染性疾病者;⑶合并凝血功能障碍者;⑷近期存在放疗、化疗史者;⑸合并其他恶性肿瘤者;⑹对本研究所用药物存在禁忌证者。
1.2 治疗方法 参照组患者采取奥沙利铂联合卡培他滨进行常规化疗:在每个疗程的第1天,对患者静脉滴注奥沙利铂注射液[齐鲁制药(海南)有限公司,国药准字H20203216,规格:10 mL∶50 mg]130 mg/m2(单次最大剂量825 mg), 2~6 h内滴注完毕;口服卡培他滨(南京优科制药有限公司,国药准字H20223015,规格:0.5 g)1μg/(m2·d), 2次/d,于早、晚餐后30 min服用,服药2周后停药1周。
研究组患者在参照组基础上联合贝伐珠单抗治疗:于每个疗程第1天、第15天静脉滴注贝伐珠单抗注射液[正大天晴药业集团南京顺欣制药有限公司,国药准字S20233105,规格:100 mg(4 mL)/瓶] 5 mg/kg(单次最大剂量500 mg),首次输注持续90 min,后根据患者耐受程度可逐渐缩减至30~60 min/次。
两组患者均以21 d为1个疗程,持续治疗2个疗程,观察并记录两组患者恢复情况。
1.3 观察指标 ⑴无进展生存率。患者从接受治疗到疾病进展或死亡的时间段为无进展生存期(PFS)[7]。观察并记录两组患者治疗期间肿瘤进展情况,无进展生存率=PFS患者总例数/总例数×100%。⑵临床疗效。完全缓解(CR):肿瘤病灶近乎消失;部分缓解(PR):肿瘤面积缩小达到或超过50%;疾病稳定(SD):肿瘤面积缩小<50%;疾病进展(PD):肿瘤面积增大或者出现新的肿瘤病灶[8]。客观缓解率(ORR)=[(CR+PR)例数/总例数]×100%。⑶肿瘤标志物水平。于治疗前后,采集患者晨起空腹静脉血5 mL,以1 500 r/min的转速(8 cm半径)离心10 min,取上层清液,采用酶联免疫吸附试验(ELISA)检测糖类抗原(CA)199、 CA 125、多效蛋白(PTN)、结肠癌特异性抗原-1(CCSA-1)水平;采用免疫分析法检测癌胚抗原(CEA)水平。⑷T淋巴细胞亚群分布。于治疗前后,采集患者晨起空腹静脉血5 mL,以流式细胞仪[克曼库尔特生物科技(苏州)有限公司,苏械注准20182220262,型号: DxFLEX]检测CD3+、 CD4+T淋巴细胞百分比,并计算CD3+/CD4+比值。⑸不良反应发生情况。不良反应表现为恶心呕吐、腹泻、厌食、便秘。不良反应总发生率=不良反应总发生例数/总例数×100%。
1.4 统计学分析 采用SPSS 20.0统计学软件进行数据分析。计数资料以[例(%)]表示,采用χ2检验,等级比较采用秩和检验;计量资料以(x)表示,采用t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者无进展生存率比较 研究组患者无进展生存率为70.73%(29/41),高于参照组的43.90%(18/41),差异有统计学意义(χ2值=6.032, P=0.014)。
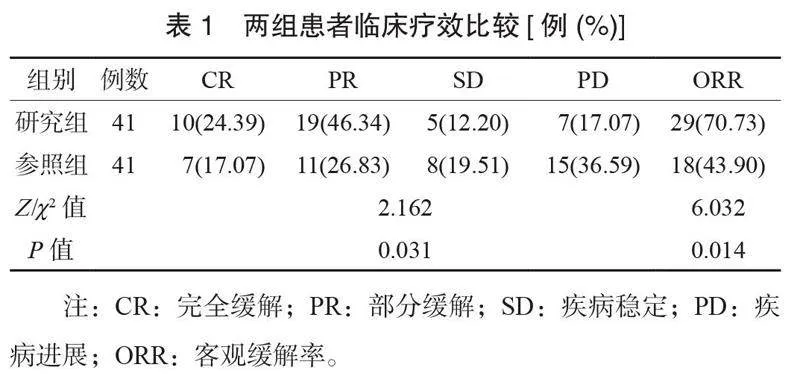
2.2 两组患者临床疗效比较 研究组患者临床疗效优于参照组, ORR高于参照组,差异均有统计学意义(均P<0.05),见表1。
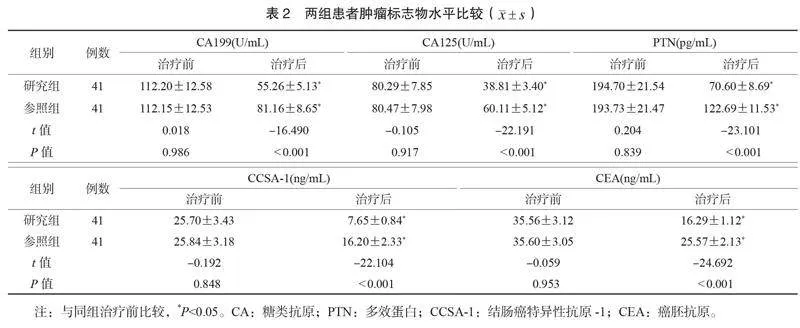
2.3 两组患者肿瘤标志物水平比较 治疗后,两组患者CA199、 CA125、 PTN、 CCSA-1、 CEA水平均降低,且研究组均低于参照组,差异均有统计学意义(均P<0.05),见表2。
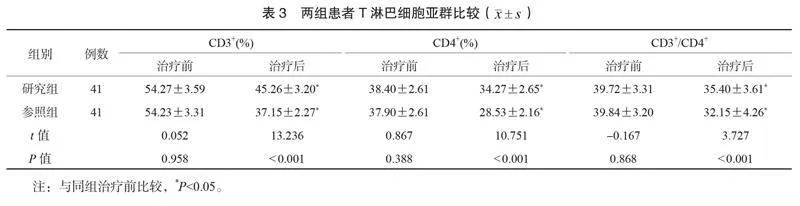
2.4 两组患者T淋巴细胞亚群分布比较 治疗后,两组患者CD3+、 CD4+T淋巴细胞百分比及CD3+/CD4+比值均降低,但研究组降低幅度均小于参照组,差异均有统计学意义(均P<0.05),见表3。
2.5 两组患者不良反应发生情况比较 参照组患者发生恶心呕吐4例、腹泻3例、厌食3例,不良反应总发生率为24.39%(10/41);研究组患者发生恶心呕吐5例、腹泻3例、厌食2例、便秘2例,不良反应总发生率为29.27%(12/41)。两组患者不良反应总发生率比较,差异无统计学意义(χ2值=0.249, P=0.618)。
3 讨论
晚期结肠癌患者的临床症状较为严重,主要表现为持续加重的腹痛、消化系统症状(腹泻、便秘、便血、呕吐、腹胀等)、消瘦和乏力、其他器官受累症状(若转移到肝脏,会出现黄疸、肝区疼痛;若转移到肺部,会出现咳嗽、咳血、呼吸困难等)[9]。针对晚期结肠癌患者,临床常采用化疗、靶向治疗、免疫治疗、姑息性手术等综合治疗方案,以延长其生存期和提高其生活质量为主要目标。奥沙利铂联合卡培他滨是临床常用的化疗方案,奥沙利铂可抑制DNA合成,卡培他滨则可在体内转化为具有细胞毒性的物质,干扰肿瘤细胞的生长。两者联合使用能够发挥协同抗肿瘤的效果,提高治疗的有效性[10]。贝伐珠单抗是一种重组人源化VEGF的单克隆抗体,通过抑制VEGF活性,可阻碍肿瘤新生血管的形成,有效延缓肿瘤的进展,提高患者的生存质量,且该药物靶向性强,能针对特定的靶点发挥作用,对正常细胞的损伤相对较小。
肿瘤生长需借助血管输送氧气、营养物质,肿瘤生长、转移与患者自身血供紧密相关,故化疗期间需联合抗血管生成药物,以抑制肿瘤的生长。本研究结果显示,研究组患者无进展生存率高于参照组,临床疗效优于参照组,ORR高于参照组。这提示贝伐珠单抗联合常规化疗能有效地控制晚期结肠癌疾病进展,延长病情稳定的时间。分析原因为,化疗药物通过直接作用于肿瘤细胞的生长、分裂等过程来杀死癌细胞。而贝伐珠单抗通过抑制肿瘤血管生成,切断肿瘤的营养供应和氧气输送。两种治疗方案联合使用,产生协同效应,从不同途径发挥抗肿瘤作用,对肿瘤生长的抑制作用显著[11]。且贝伐珠单抗可降低肿瘤组织内血管的通透性,减轻组织水肿,改善药物在肿瘤组织内的分布和渗透,提高化疗药物的疗效。
本研究结果显示,治疗后,两组患者CA199、CA125、PTN、CCSA-1、CEA水平均有所降低,且研究组上述指标均低于参照组。这表明贝伐珠单抗联合常规化疗在抑制肿瘤的活性、控制肿瘤细胞的增殖方面效果良好。分析原因为,贝伐珠单抗可降低肿瘤血管的通透性,能使化疗药物有效地渗透到肿瘤组织内部,提高化疗药物在肿瘤部位的浓度,从而增强其对肿瘤细胞的杀灭作用[12]。本研究结果显示,治疗后,两组患者CD3+、CD4+T淋巴细胞百分比及CD3+/CD4+比值均降低,但研究组降低幅度均小于参照组,提示贝伐珠单抗联合常规化疗可有效控制肿瘤的转移。分析原因为,肿瘤的转移依赖新生血管为其提供的通道和营养支持,贝伐珠单抗能减少肿瘤新生血管的形成,降低癌细胞进入血液循环和向远处器官转移的发生概率;化疗药物可直接杀灭可能发生转移的癌细胞,两种治疗方案协同,可有效控制肿瘤的转移。
本研究结果进一步表明,两组患者的不良反应总发生率进行对比,差异不具有统计学意义,这提示贝伐珠单抗联合常规化疗具有较高的安全性。分析原因为,贝伐珠单抗作用靶点明确,对正常细胞的非特异性损伤较小,可减少患者全身性的不良反应[13]。且贝伐珠单抗可改善肿瘤周围组织的微环境,减少周围组织水肿和缺氧,从而降低因肿瘤周围组织微环境异常导致的不良反应风险。贝伐珠单抗常见的不良反应(如高血压、蛋白尿等)通常是可预测和可控的,密切监测患者的血压、肾功能等指标,并及时给予患者相应的治疗干预。
综上所述,贝伐珠单抗联合常规化疗对晚期结肠癌患者病情控制效果较好,可有效降低肿瘤标志物水平,增强免疫功能,且安全性较高,值得临床应用。但本研究仍存在样本容量小、观察时间短等不足,后续需加大样本量、延长观察时间,深入分析贝伐珠单抗联合常规化疗在晚期结肠癌患者中的应用效果,为临床治疗提供更为可靠的数据支持。
参考文献
周磊,李钢.结肠癌靶向治疗研究进展[J].吉林医学, 2024, 45(7): 1709-1712.
易涵,古再丽努尔·如则托合提,姜明燕,等.贝伐珠单抗联合伊立替康与雷替曲塞治疗氟尿嘧啶耐药晚期结直肠癌的疗效和安全性[J].药物评价研究, 2020, 43(2): 293-298.
蒋锐沅,蓝巧玉,李春姗,等.参一胶囊联合贝伐珠单抗+FOLFIRI方案对晚期转移性结肠癌患者的临床疗效及血清血管生成因子、T淋巴细胞亚群影响的观察[J].中药材, 2021, 44(6): 1504-1510.
ZHOU Y W, LONG Y X, CHEN Y, et al. First-line therapy of bevacizumab plus chemotherapy versus cetuximab plus chemotherapy for metastatic colorectal cancer patients with mucinous adenocarcinoma or mucinous component[J]. Cancer Med, 2021, 10(10): 3388-3402.
国家卫生计生委医政医管局,中华医学会肿瘤学分会.中国结直肠癌诊疗规范(2015版)[J].中华胃肠外科杂志, 2015, 18(10): 961-973.
陈孝平,汪建平,赵继宗.外科学[M].9版.北京:人民卫生出版社, 2018: 438-440.
卫生部医政司.结直肠癌诊疗规范(2010年版)[J/CD].中国医学前沿杂志(电子版), 2011, 3(6): 130-146.
张百红,岳红云.实体瘤疗效评价标准简介[J].国际肿瘤学杂志, 2016, 42(11): 845-847.
李佳,马晓捷,王宇翔.射频消融后辅助mFOLFOX6联合贝伐珠单抗方案在结直肠癌肝转移瘤中的疗效和安全性评价[J].国际肿瘤学杂志, 2021, 48(12): 729-734.
邢玉广,孙航,郭得兴,等.贝伐珠单抗联合奥沙利铂+亚叶酸钙+5-氟尿嘧啶化疗方案在晚期结肠癌中的应用效果分析[J].肿瘤基础与临床, 2024, 37(3): 298-300.
曹冉华,石秀换,王薇,等.贝伐单抗联合卡培他滨治疗晚期转移性直肠癌及对血清表皮生长因子受体及人表皮生长因子受体表达的影响[J].药物评价研究, 2019, 42(10): 2016-2020.
谢甲贝,杨帆,付琳韩,等.贝伐珠单抗联合FOLFOX化疗方案治疗转移性结肠癌的疗效及对免疫功能和生活质量的影响[J].癌症进展, 2021, 19(18): 1913-1916.
于静.晚期结肠癌患者应用化疗联合贝伐珠单抗的治疗效果[J].大医生, 2024, 9(10): 14-16.
