高血压与高血压合并干燥综合征患者血清蛋白质差异表达研究
2024-05-28马慧敏蔡昕添阿依古再丽艾合买提夏衣热艾尔肯王梦卉李南方张德莲
马慧敏,蔡昕添,阿依古再丽·艾合买提,朱 晴,吴 婷,夏衣热·艾尔肯,王梦卉,李南方,张德莲
(1.新疆维吾尔自治区人民医院高血压中心,新疆 乌鲁木齐 830001;2.新疆高血压研究所,新疆 乌鲁木齐 830001;3.国家卫生健康委高血压诊疗研究重点实验室,新疆 乌鲁木齐 830001;4.新疆维吾尔自治区重点实验室“新疆高血压病研究实验室,新疆 乌鲁木齐 830001;5.新疆高血压(心脑血管)疾病临床医学研究中心,新疆 乌鲁木齐 830001)
高血压是一种心血管综合征,其特征是全身循环动脉压(收缩压和/或舒张压)升高。它常与其他心血管危险因素并存,可损害心脏、大脑、肾脏等重要器官的结构和功能。目前,高血压仍然是心脑血管疾病最重要的危险因素[1]。
研究表明高血压与自身免疫性疾病密切相关,两者之间可能存在相互影响[2]。自身免疫性疾病是指人体对自身抗原发生免疫反应后导致自身组织自我损害引起的疾病[3]。一些研究表明,自身免疫性疾病与血管炎症和内皮功能障碍相关[4],可能对高血压的发展产生影响。高血压本身也涉及到血管功能和炎症反应的异常,因此,自身免疫性疾病可能进一步加剧了血管的炎症状态,导致血压升高[5,6]。干燥综合征(Sjogren's syndrome,SS)是常见的自身免疫性疾病,其主要表现为外分泌腺(主要是唾液腺和泪腺)的症状和体征功能障碍。SS 患者体内液体分泌减少,这可能导致血管内皮功能障碍,从而加重了高血压的发生风险[7]。研究表明高血压合并SS 时发生心脑血管事件的风险显著增加[8]。研究发现在SS 人群中高血压的患病最高可达37.3%[9]。有研究发现SS 患者的高血压患病率高于年龄和性别匹配的健康对照组[10]。目前大量证 据 表 明 高 血 压 与SS 密 切 相 关[11],但 具 体 发 病 机制尚不明确。
本研究利用基于DIA-MS 蛋白质组学方法,对高 血 压 伴 干 燥 综 合 征(hypertensive with Sjogren's syndrome,SH)患者和不伴干燥综合征的原发性高血压(essential hypertensive,EH)患者的差异蛋白质进行鉴定,以期为SH 的发病机制提供新的认识。
1 资料与方法
1.1 研究对象
选 择2017 年1 月~2018 年12 月 期 间 就 诊 于 新疆维吾尔自治区高血压诊疗中心的患者。
1.2 诊断标准
1.2.1 高血压诊断标准 根据美国心脏学会指南:(1)收缩压≥140 mmHg 和或舒张压≥90 mmHg,三次均未服用降压药物;(2)有抗高血压病史的高血压患者。(3)利用生化指标排除其他继发性高血压,包括原发性醛固酮增多症、库欣综合征、嗜铬细胞瘤、肾实质高血压、肾血管性高血压、阻塞性睡眠呼吸暂停综合征。诊断为EH[12],同时排除罹患自身免疫性疾病如血管炎、狼疮、类风湿关节炎、系统性硬化、自身免疫性肝炎、桥本甲状腺炎、恶性肿瘤、急慢性感染和感染性疾病的患者。对于符合以上标准且临床资料完整的患者均纳入EH 患者组。
1.2.2 原发性SS 诊断标准 根据中华医学会风湿病学分会2023 年发布的原发性SS 的分类标准[13]:入选标准:至少有眼干或口干症状之一的患者,即下列至少一项为阳性:(1)每日感到不能忍受的眼干,持续3 个月以上;(2)眼中反复沙砾感;(3)每日需用人工泪液3 次或3 次以上;(4)每日感到口干,持续3 个月以上;(5)吞咽干性食物需要频繁饮水帮助。排除标准:可能有重叠的临床表现或干扰诊断的试验结果,出现下述疾病,应予排除:(1)头颈部放疗史;(2)活动性丙型肝炎病毒感染;(3)获得性免疫缺陷综合征;(4)结节病;(5)淀粉样变性;(6)移植物抗宿主病;(7)IgG4 相关疾病。满足上述入选标准和排除标准者,且下述五项评分总和≥4 分者诊断为pSS:(1)唇腺灶性淋巴细胞浸润,且灶性指数≥1 个灶/4 mm2,计3 分;(2)血清抗SSA 抗体阳 性,计1 分;(3)至 少 单 眼OSS≥5 分 或Van Bijsterveld 评分≥4 分,计1 分;(4)至少单眼Schirmer试验≤5 mm/5 min,计1 分;(5)未刺激的全唾液流率≤0.1 mL/min,计1 分。当诊断为患者同时诊断为SH 且临床资料完整,排除继发性高血压、感染、肿瘤;排除其他自身免疫性疾病,如系统性红斑狼疮、类风湿关节炎、系统性硬化症、自身免疫性肝炎、桥本甲状腺炎等。排除恶性肿瘤、急慢性感染和感染性疾病后纳入SH 组,SH 患者均进行检测了C 反应蛋白、补体C3、C4 以及相关自身免疫性抗体(包括ANA、抗-SSA、抗-SSB、 RO-52)。
根据上述标准,选择8 例原发性高血压无SS 的患者为EH 组和8 例高血压伴SS 患者为SH 组,收集纳入患者生化指标。
1.3 血液样本采集
收集患者的血清样本,在室温放置凝结,在4 ℃下以3 000 r/min 离心15 min。离心后取出血清,在-80 ℃环境保中存备用,
1.4 DIA 蛋白定量
1.4.1 主要试剂 试剂(盒):SDT 缓冲液:4%十二烷基硫酸钠,100 mmol/L 二硫苏糖醇,150 mmol/L三羟甲基氨基甲烷盐酸盐(Tris-HCl) pH 8.0;尿酸缓 冲 液:8 mol/L 尿 素,150 mmol/L Tris-HCl pH 8.5;BCA 蛋白质测定试剂盒;碘乙酰胺(100 mmol/L 吲哚-3-乙酸在尿酸缓冲液中);缓冲液A (10 mmol/L HCOONH4, 5% ACN, pH 10.0);缓 冲 液B(10 mmol/L HCOONH4,85% ACN,pH 10.0)。
1.4.2 样品制备及蛋白质酶解 取血清样本,加入SDT 缓冲液,14 000g离心20 min,获得上清液,使用BCA 蛋白质分析试剂盒进行蛋白定量。每个样本 取200 μg 逐 步 加 入30 μL SDT 缓 冲 液,100 mmol/L 的碘乙酰胺,UA 缓冲液及TEAB 缓冲液获得蛋白悬液。后加入蛋白酶酶解获得多肽。
1.4.3 反相(RP)色谱法分离多肽 采用Agilent 1260 infinity IIHPLC 进 行RP 色 谱 分 离。用 缓 冲 液A 稀释肽混合物,并上样于液相色谱柱(XBridge peptide BEH C18 Column, 130Å,5 μm, 4.6 mm×100 mm)。多肽以1 mL/min 的流速洗脱,液相梯度:0%~7% B,5 min,7%~40% B,5~40 min,40%~100%B,45~50 min, 100% B,50~65 min。通过测量214 nm 吸光度监测洗脱过程,每1 分钟收集一次,收集的多肽在45 ℃的高速真空中干燥,干燥后的样本在0.1%的甲酸中重新溶解,并合并成12 个组分。
1.4.4 DDA 及DIA 分析 将2 μL 10×iRT 多肽加入6 μL 多肽溶液中。然后将混合物注入Q-Exactive HF-X(Thermo Fisher Scientific)中,并用梯度缓冲液B(80%乙腈和0.1%甲酸)以300 nL/min 的流速分离。
DDA 分析质谱仪参数设置如下:(1)MS:扫描范围(m/z)=350~1 500;分辨率=60 000;AGC 目标=3E6;最大离子注入时间=50 ms;包括电荷状态=2~7;过滤动态排除:排除持续时间=30 s;(2)dd-MS2:隔 离 窗 口=1.6m/z,分 辨 率=15 000;AGC 目标=1E5;最大离子注入时间=45 ms;NCE=28%。
DIA 分析质谱仪参数设置如下:(1)MS:扫描范围(m/z)=350~1 500;分辨率=60 000;AGC 目标=3E6;最大离子注入时间=50 ms;(2)DIA:分辨率=30 000;AGC 目标=1E6;最大离子注入时间=AUTO;NCE=28%。 原 始 数 据 由SpectrAert Pulsar X(版本12,Biognosys AG)处理和分析,参数为BGS 出厂设置,Q-value(FDR)阈值为1%。
1.5 生物信息学分析
采用DIA 蛋白质组学方法对差异表达蛋白质进行鉴定。在SH、EH 组中选择倍数变化(FC)>1.20 或<0.83 且P<0.05 的蛋白质作为差异表达蛋白质(FC>1.2 为上调蛋白)。利用GO 和KEGG 数据库(https://david.ncifcrf.gov/summary.jsp)对差异表达蛋白质进行生信学分析。
FDR 用于评估GO 项或KEGG 途径的差异蛋白富集度的显著水平。使用String 据库构建蛋白质相互作用网络(PPI)。使用Cytoscape 进行模块化分析,得到得分最高的核心模块。最后结合DIA 定量结果和KEGG 通路分析结果,从核心模块包含的蛋白质中筛选出关键蛋白质。
1.6 统计学处理
采用SPSS 软件23.0 进行统计分析,用Origin和Excel 软件建立曲线图。正态分布的数据使用t检验,用(±s)表示。非正态分布的数据使用非参数检验,P<0.05 为差异具有统计学意义。
2 结 果
2.1 基线特征
EH 患者平均年龄(45.9±7.1)岁,SH 患者平均年 龄(53.8±11.7)岁,差 异 无 统 计 学 意 义(P>0.05),两组的基线数据如表1 所示。
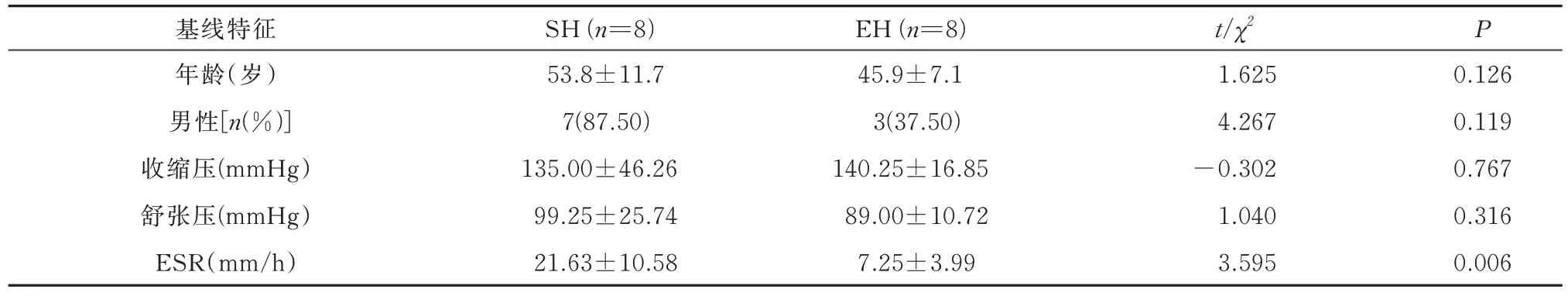
表1 研究对象的基线特征Tab 1 Baseline characteristics of the subjects
2.2 血清中差异表达蛋白质
EH 组与SH 组差异表达的蛋白有35 个,其中32 个蛋白表达上调,3 个蛋白表达下调(P<0.05)(图1、2)。
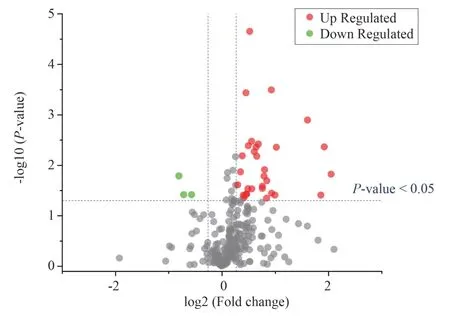
图1 差异表达蛋白的火山图Fig 1 Volcano map of differentially expressed proteins
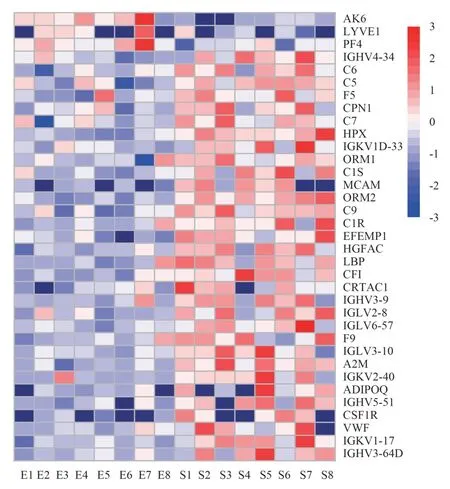
图2 差异表达蛋白热图Fig 2 Heat map of differentially expressed protein
2.3 GO 富集度分析
分析结果提示SH 组与EH 组相比,差异表达蛋白在细胞组分中主要位于细胞外区域,在生物过程集中在血小板减少、免疫应答、信号通路、补体激活(经典途径)、蛋白水解、受体介导的内吞作用、丝氨酸型内肽酶活性和抗原结合等过程中。分子功能中主要集中在抗原结合和丝氨酸型内肽酶活性过程。GO 分析结果如图3 所示。
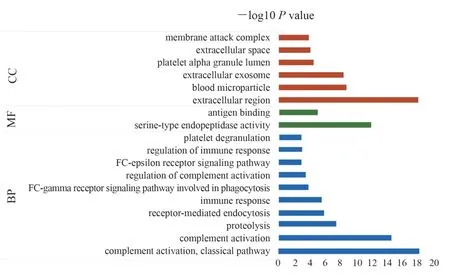
图3 差异蛋白的GO 富集分析Fig 3 GO enrichment analysis of differential proteins
2.4 差异表达蛋白KEGG 途径的富集分析
对上述差异蛋白进行KEGG 信号通路富集分析,相关差异蛋白在以下几个方面显著富集:补体和凝血级联、系统性红斑狼疮和朊病毒病。KEGG分析的结果如图4 所示。

图4 差异表达蛋白KEGG 通路的富集分析Fig 4 Enrichment analysis of differentially expressed protein KEGG pathway
2.5 蛋白质相互作用网络和模块化分析
为了更好地预测蛋白质之间的相互作用,本课题组构建了PPI 网络来识别最重要的蛋白质。使用STRING 数据库,选择蛋白质相互作用得分为≥0.4的蛋白质节点,并删除未连接的节点。PPI 图是用Cytosscape 绘制的。使用MCODE 插件对蛋白质相互作用网络进行分析,并根据MCODE 聚类条件(Score=6.667)选择得分最高的核心模块。如图5所示,红色圆圈代表核心模块中的蛋白质。与其他蛋白质相比,这7 种蛋白质在整个蛋白质相互作用网络中具有更强的相互作用。表2 总结了这七种蛋白质在两组之间的差异倍数。VWF、A2M 和F9 在补体和凝血级联途径中均显著富集,且两组间表达差异显著。结合DIA 定量结果和KEGG 通路分析结果,我们筛选出与高血压合并SS 相关的3 个关键蛋白:血管性血友病因子(Von Willebrand factor,VWF), α-2-巨 球 蛋 白(Alpha-2-Macroglobulin,A2M), 凝血因子Ⅸ(FⅨ,F9)。
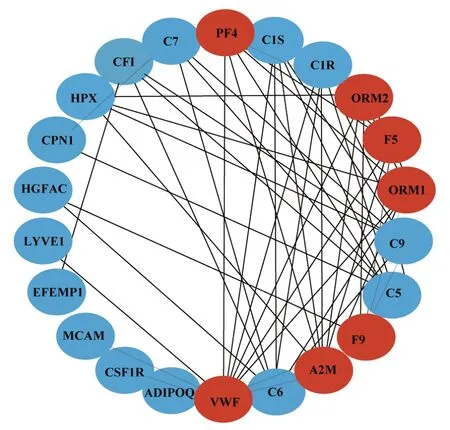
图5 蛋白质相互作用网络和模块化分析Fig 5 Protein interaction networks and modular analysis
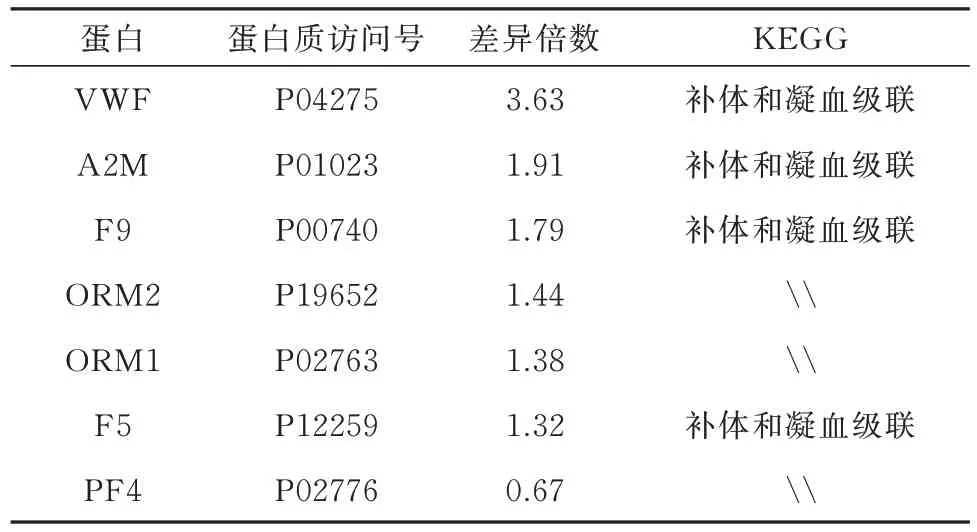
表2 两组中7 种蛋白质差异表达总结Tab 2 Summary of differential expression of 7 fold protein between the two groups
3 讨 论
本研究采用蛋白质组学技术鉴定了SH 患者与EH 患者血清差异表达蛋白。结果发现两组间共检测出35 个差异表达蛋白。其中32 个蛋白上调,3 个蛋白表达下调。 Li 等[14]发现SS 患者泪液中防御素α1、簇蛋白上调、乳转铁蛋白表达下调的表达。Liao等[15]使用蛋白组学分析发现与健康人群相比,SS 患者的差异表达蛋白存在331 个下调蛋白和289 个上调蛋白。发现转化生长因子β-1 和CD40 配体的表达下调,从而丰富了炎症相关途径。信号转导子和转录激活子1-α/β(STAT1)的表达上调并富集Ⅰ型干扰素信号通路和IL-27 介导的信号通路。KEGG富集分析显示,相关差异蛋白在补体和凝血级联、SLE 和朊病毒疾病中显著富集。其中VWF、A2M和F9 的差异表达更为显著。蛋白质(VWF、A2M和F9)和KEGG 途径(补体和凝血级联)在以往的SS 蛋白质组学研究中没有发现,它们可能是高血压人群发生SS 的重要蛋白质和生物通路。
VWF 是一种由内皮细胞和巨核细胞合成和释放的大分子糖蛋白,是一种重要的血浆成分,在血小板聚集和血栓形成中发挥重要作用[16]。此外VWF 是内皮细胞识别的标志物,其在循环中的释放和水平被认为是内皮细胞功能障碍的主要指标[17]。有研究发现老年高血压合并动脉粥样硬化患者血清VWF 水平升高[18]。本研究发现SH 患者的血清VWF 水平显著高于EH 患者,提示SH 患者血管内皮细胞损伤程度更严重。虽然本研究没有证实SH 患者的内皮功能障碍发生在血压升高之前,但笔者认为VWF 相关的内皮功能障碍在SH 患者的发病机制中起着重要作用。如果在降压治疗的基础上检测SH 患者的VWF,并进一步调节血管内皮功能,SH 患者的预后将得到改善。
A2M 是一种细胞外大分子,主要以其作为广谱蛋白酶抑制剂的作用而闻名。同时A2M 可结合多种细胞因子,如白细胞介素-6,血小板衍生生长因子,转化生长因子、神经生长因子,肿瘤坏死因子-α等,并在多种细胞因子相互作用和炎症反应中发挥重要作用[19]。A2M 可以通过中和纤溶酶、纤溶酶原激活剂和活化的蛋白C 来增强促凝血特性[20]。促凝血剂特性和慢性炎症与血管危险因素、动脉粥样硬化和血栓栓塞症有关。
Shimomura 等[21]对102 名有中风病史或任何心血管危险因素的患者进行了横断面分析,发现在有心血管危险因素的患者中,血清A2M 水平与血管内皮功能独立相关,其血清水平可反映慢性卒中患者或有心血管危险因素患者的血流介导扩张对血管内皮功能的影响。本研究数据表明高血压合并SS患者的A2M 水平显著高于EH 患者。A2M 与炎症反应和内皮功能有关,在高血压合并自身免疫性疾病中的作用值得进一步探讨。此外,A2M 的促凝血特性提示应更密切地监测SH 患者的凝血功能,以预防血栓栓塞症的发生,这应有助于改善患者的预后。
凝血因子Ⅸ(FⅨ,F9)是一种依赖维生素K 的凝血蛋白,在内源性凝血途径中起关键作用[22]。FⅨ是蛋白酶FⅨA 的前体,激活的FⅦ(FⅦIa)是其辅因子。与缺乏FⅨ或FⅦ相关的严重出血性疾病(血友病)表明它们在止血中的重要。研究表明,凝血可以被认为是一种内部炎症。高凝状态伴随着凝血因子的增加,纤维蛋白凝块的过量产生是细胞活化的原因,从而导致细胞因子、黏附分子等多种炎症介质的增加[23]。此外,高凝状态引起的血栓形成、补体活化、血小板活化等直接高凝结果也容易导致炎症[24]。已有研究报道,高血浆FⅦ水平与静脉血栓栓塞症、心肌梗死和中风的风险略有增加有关[25,26]。本研究数据表明,FⅦ可能通过凝血途径参与SS 高血压的炎症过程。另一方面,SH 患者发生血栓的风险高于EH 患者,预后较差。
本研究存在一定的局限性。首先,本研究患者数量有限。其次,本研究只是相对定量的初步蛋白质筛选研究,样本量相对较小,还需要进一步扩大样本量进行蛋白质印迹来验证差异蛋白。
综上所述,本课题组通过DIA 对SH 和EH 患者的外周血样本进行了蛋白质表达差异检测。共筛选出35 个差异蛋白。结合生物信息学分析结果,笔者认为VWF、A2M 和F9 蛋白可能在高血压患者发生SS 中发挥作用。然而,仍需要进一步进行蛋白质印迹验证性研究来验证这一结果。
作者贡献度说明:
马慧敏:负责文稿的设计和撰写;阿依古再丽·艾合买提,朱晴,蔡昕添,夏衣热·艾尔肯,吴婷,王梦卉:负责文章相关数据库分析;李南方,张德莲:负责文稿的修改和审校。
所有作者声明不存在利益冲突关系。
